ВЉЮФ
БрМаоИФДэЮѓmRNAСЦЗЈШЁЕУЭЛЦЦ  ОЋбЁ
ОЋбЁ
|
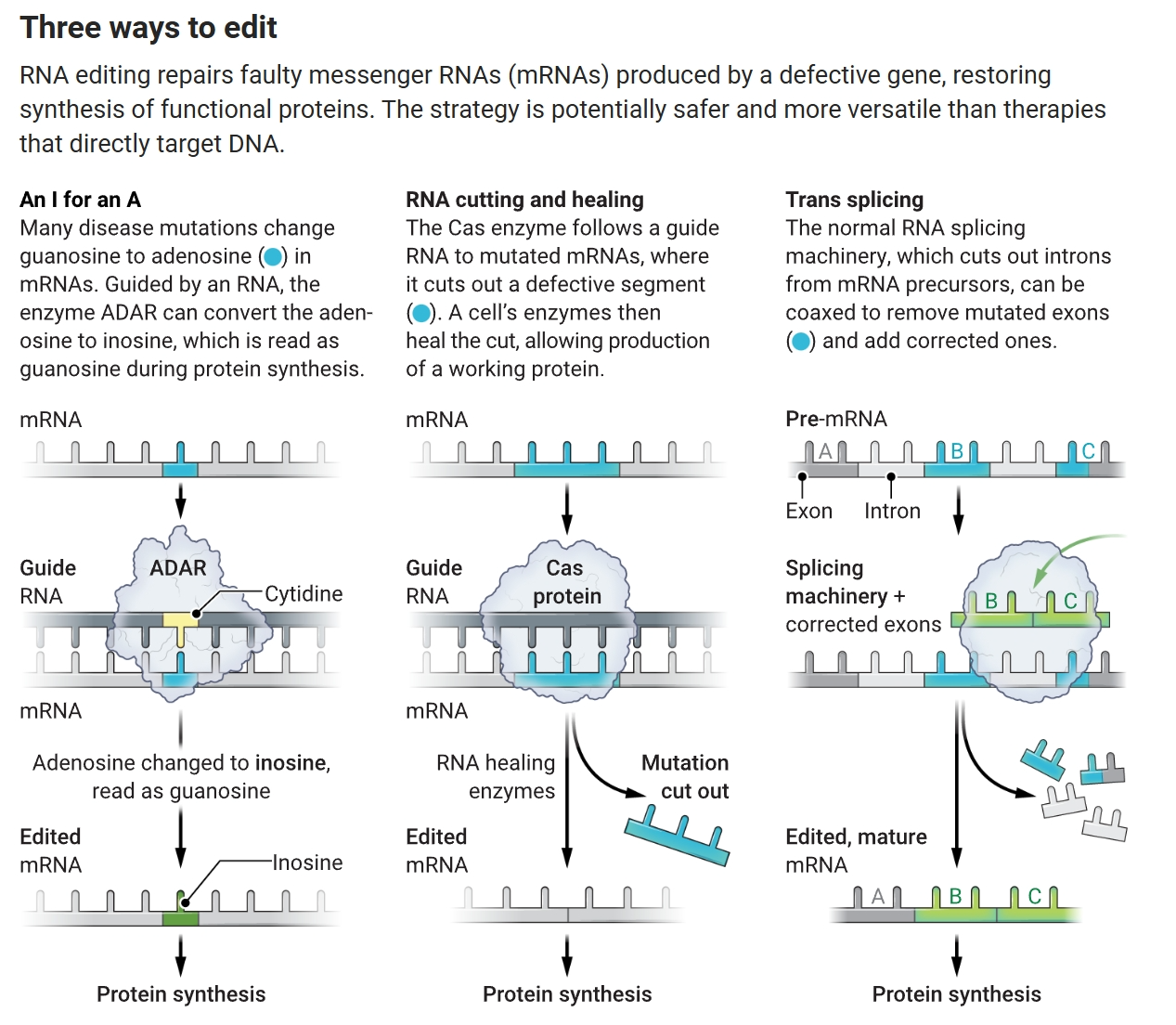
ФЊФнПЈЁЄПЦЖїРЕТГаШЯЃЌзїЮЊвЛИіУЛгаЬЋЖргыКЂзгЯрДІОбщЕФаТЪжМвГЄЃЌЫ§ЖдХЎЖљЧаЖћЮїГіЯжЕФЮЪЬтЗДгІГйЖлЁЃШЛЖјЃЌЕБЧаЖћЮї1ЫъЪБЃЌЫ§ЕФЗЂеЙЯдШЛЭЃжЭЩѕжСПЊЪМЕЙЭЫЁЃЫ§жЛбЇЛсСЫЫЕвЛИіДЪЃЌКмПьОЭВЛдйЫЕЛАСЫЁЃжЛгадкгаШЫЗізХЕФЧщПіЯТЧаЖћЮїВХФмзпТЗЁЃЫ§ЪЇШЅСЫзЅЮеЕФФмСІЃЌЗДЖјПЊЪМЁАгУЪжзіГіжиИДЕФЖЏзїЁБЃЌБШШчХФЪжЃЌПЦЖїРЕТЫЕЃЌЕБЪБЫ§УЧвЛМвзЁдкИЅМЊФсбЧжнЁЃ
ЁАЮвЦШЧаЯЃЭћЕУЕНвЛИіеяЖЯЃЌЁБПЦЖїРЕТЫЕЁЃЕЋЕБЫ§жегкЕУЕНеяЖЯЪБЃЌЧаЖћЮї2ЫъСЫЃЌЁАетЪЧвЛИіЫЋжиДђЛїЁЃЁБВЛНіЧаЖћЮїЛМгаРзЬизлКЯеїЃЌетЪЧвЛжжЮоЗЈжЮгњЕФЩёОЯЕЭГМВВЁЃЌЖјЧвПЦбЇМвУЧЖдетжжВЁжЂЫљжЊЩѕЩйЁЃЫћУЧУїАзЫќжївЊгАЯьХЎКЂЃЌПЩФмЪЧгЩгкЛљвђЭЛБфв§Ц№ЕФЃЌЕЋЫћУЧЛЙУЛгаШЗЖЈвХДЋдЊазЁЃ
ФЧЪЧдк1998ФъЁЃНёЬьЃЌПЦЖїРЕТКЭЫ§ЕФеЩЗђШддкееЙЫзХЯжФъ28ЫъЁЂЮоЗЈЫЕЛАЁЂаазпЛђЪЙгУЫЋЪжЕФЧаЖћЮїЁЃЫ§ашвЊЗўгУвЉЮяРДПижЦёВ№яЗЂзїЁЂМѕЧсНЙТЧВЂАяжњЫЏУпЁЃЯждквбжЊЕФМВВЁБГКѓЕФЛљвђШБЯнЭЈГЃЪЧMECP2ЛљвђЕФЭЛБфЃЌИУЛљвђПижЦАќРЈДѓФддкФкЕФаэЖрЦїЙйжаЕФЛљвђЛюЖЏЁЃЯёЦфЫћРзЬизлКЯеїЖљЭЏЕФИИФИвЛбљЃЌПЦЖїРЕТЯЃЭћПЦбЇМвФмМгПьПЊЗЂжЮСЦЗНЗЈЁЃЕЋзїЮЊРзЬизлКЯеїбаОПаХЭаЛљН№ЛсЕФДДЪМШЫМцCEOЃЌЫ§гаФмСІзіаЉЪВУДЁЃ
Г§СЫзЪжњвЛЯЕСаВпТдРДОРе§ЛђЬцЛЛгаШБЯнЕФDNAЭтЃЌЫ§ЕФзщжЏЛЙдкжЇГжвЛжжЗЧДЋЭГЗНЗЈЁЃИУаХЭаЛљН№вбОЭЖШыСЫ850ЭђУРдЊЁЊЁЊГЌЙ§ЦфЮЊбаОПЗжХфзЪН№ЕФ10%ЁЊЁЊгУгкБрМгЩЭЛБфMECP2БрТыЕФRNAСДЕФЙЄзїЁЃЭЈЙ§етбљзіЃЌЫћУЧе§дкдіЧПжЮСЦМВВЁЕФвЛИіаТаЫЕЋгаЧАОАЕФЗНЗЈЃКБрМЕААзжЪЕФRNAРЖЭМЁЃЁАЮвУЧЕФФПБъЪЧЮЊетИіСьгђзЂШыЛюСІЃЌЁБПЦЖїРЕТЫЕЁЃ
Ы§ВЂВЛЪЧЮЈвЛЖдRNAБрМЧБСІГфТњШШЧщЕФШЫЁЃетжжЬцДњCRISPRКЭЦфЫћDNAаоЪЮСЦЗЈЕФЗНЗЈЁАе§ГЩЮЊНЙЕуЁБЃЌвСРћХЕвСДѓбЇЖђАЭФЩ-ЯущФЗжаЃЕФЩњЮяЙЄГЬЪІЭаТэЫЙЁЄМгНмЫЕЁЃгыЛљгкDNAЕФжЮСЦЯрБШЃЌБрМЙ§ЕФRNAПЩФмИќШнвзБЛЯИАћНгЪмЃЌВЂЧветжжЗНЗЈПЩФмвВИќАВШЋЁЃ
ЕНФПЧАЮЊжЙЃЌЛЙУЛгаеыЖдРзЬизлКЯеїЕФRNAБрМСЦЗЈГіЯжЁЃЕЋдкИУСьгђЕФвЛИіЧБдкРяГЬБЎжаЃЌWave Life SciencesЩЯжмдквЛЗнаТЮХИхжааћВМЃЌЦфRNAБрМЗНЗЈЬсИпСЫвЛжжЩњУќЭўаВадвХДЋМВВЁЛМепЕФе§ГЃЕААзВњСПЃЌетжжМВВЁЛсЫ№КІЫћУЧЕФИЮдрКЭЗЮВПЁЃ
Г§СЫWaveЭтЃЌЛЙгаШ§МвЩњЮяММЪѕЙЋЫОЁЊЁЊAscidian TherapeuticsЁЂRznomicsКЭHuidaGeneЁЊЁЊвбОПЊЪМдкЛМгаблВЁЛђАЉжЂЕФЛМепжаВтЪджЮСЦЗНЗЈЁЃИќЖрЕФЙЋЫОе§дкОКЯрПЊЗЂздМКЕФСЦЗЈЃЌЭЈГЃгыДѓаЭжЦвЉЙЋЫОКЯзїЃЌЖјбЇЪѕЪЕбщЪвдђЩюШыЬНОПБрМЛњжЦЁЃ
RNAБрМЁАВЛЪЧCRISPRЕФЬцДњЦЗЁЃЫќЪЧЖдПЙМВВЁЕФСэвЛжжЮфЦїЃЌЁБЙўЗ№ДѓбЇвНбЇдКЕФЩњЮяЙЄГЬЪІЧЧФЩЩЁЄЙХыјБЄЫЕЃЌЫћЕФЪЕбщЪввбОПЊЗЂГіаоИФRNAЕФаТЗНЗЈЁЃбаОПШЫдБШддкЖрИіЗНУцХЌСІЭъЩЦММЪѕЃКЬсИпЦфаЇТЪКЭОЋШЗадЃЌИФЩЦДЋЕнЫљашЗжзгЕФЗНЪНЃЌвдМАМѕЩйИБзїгУЁЃбЁдёКЯЪЪЕФМВВЁНјааАаЯђвВЪЧжСЙиживЊЕФЃЌЖХПЫДѓбЇвНбЇдКЕФЩњЮяЙЄГЬЪІАЂРЮФЕТЁЄАЂЫїПВЫЕЁЃЁАвЛЧаЖМЙщНсЮЊгІгУЕФНїЩїбЁдёЁЃЁБ
ЖдаэЖрШЫРДЫЕЃЌвРРЕRNAЕФаТаЭCOVID-19впУчЛНЦ№СЫЫћУЧдкИпжаЩњЮяПЮЩЯбЇЕНЕФЙигкЫЋСДDNAНіДцДЂжЦдьЕААзжЪжИСюЕФФЃК§МЧвфЁЃЮЊСЫЪЕМЪзщзАвЛИіЕААзжЪЃЌЯИАћЛсНЋЛљвђзЊТМГЩаХЪЙRNAЃЈmRNAЃЉЃЛЫќНЋЕААзжЪЕФРЖЭМДЋДяИјГЦЮЊКЫЬЧЬхЕФаЁЗжзгЙЄГЇЃЌетаЉЙЄГЇНЋАБЛљЫсСЌНгЦ№РДжЦГЩЕААзжЪЁЃCOVID-19впУчжаЕФКЯГЩmRNAРћгУетвЛЩњЮябЇдРэЃЌгеЦЯИАћжЦдьВЁЖОЕААзвдМЄЗЂУтвпЗДгІЁЃ
жСЩйвбгаЪЎМИжжеыЖдвХДЋадМВВЁЕФЛёХњСЦЗЈЃЌАќРЈвЛжжвРРЕCRISPRИФБфИіШЫDNAЕФжЮСЦЗНЗЈЁЃетаЉжЮСЦеыЖдСзДЯИАћадЦЖбЊЁЂвЛжжРраЭЕФМЁгЊбјВЛСМжЂвдМАЦфЫћМИжжМВВЁЁЃеыЖдаэЖрЦфЫћзДПіЕФDNAаоЪЮСЦЗЈе§дкПЊЗЂжаЁЊЁЊНіЛљгкCRISPRЕФВпТдОЭга40ЖрЯюСйДВЪдбще§дкНјааЁЃШЛЖјЃЌжЅМгИчДѓбЇКЃбѓЩњЮяЪЕбщЪвЕФЗжзгЩњЮябЇМвдМЪщбЧЁЄТоЩЫўЖћЫЕЃКЁАдкRNAЖјВЛЪЧDNAжаНјааЛљвђИФБфгавЛаЉОоДѓЕФгХЪЦЁБЃЌЫћЙВЭЌДДСЂСЫвЛМвRNAБрМЙЋЫОKorro BioЁЃ
ЪзЯШЃЌБрМmRNAВЛЩцМАДэЮѓИФБфвЛИіШЫЛљвђЕФЗчЯеЃЌетжжИФБфПЩФмЪЧгРОУадЕФЁЃЯрБШжЎЯТЃЌвђЮЊаоИФКѓЕФRNAдкЬхФкКмПьЗжНтЃЌБрМЕФНсЙћжЛЪЧднЪБЕФЃЌетЪЙЕУНсЪјжЮСЦКЭМѕЩйИБзїгУБфЕУИќШнвзЁЃетЪЙЕУRNAБрМИќЯёЪЧЦфЫћвЉЮяЁЃЁАДѓЖрЪ§жЮСЦЖМВЛЪЧгРОУадЕФЃЌЁБТоЩЫўЖћЫЕЁЃЁАФуВЛЛсгРОУЕиЗўгУвЛЦЌАЂЫОЦЅСжЁЃЁБ
етЮовЩЪЧRNAБрМСьгђЕФвЛИіРяГЬБЎЁЃ
ЦеРЩаЬиЁЄТэРћ
МгРћИЃФсбЧДѓбЇЪЅЕибЧИчЗжаЃ
ДЫЭтЃЌCRISPRвРРЕгкЯИОњУИЃЌШчCas9ЃЌРДЧаИюDNAЃЌЫќУЧПЩФмЛсв§ЗЂУтвпЯЕЭГЕФЗДгІЁЃЁАФуе§дкНЋвЛИіЭтРДЕААзЗХШыШЫЬхЯИАћжаЃЌЁБМгРћИЃФсбЧДѓбЇЃЈUCЃЉЪЅЕибЧИчЗжаЃЕФЩњЮяЙЄГЬЪІЦеРЩаЬиЁЄТэРћЫЕЁЃвЛаЉбаОПШЫдБе§дкПЊЗЂЕФRNAБрМЗНЗЈЃЈМћЯТЭМЃЉБмУтСЫетжжЗчЯеЁЃ
RNAБрМздШЛЗЂЩњдкЯИАћжаЁЃР§ШчЃЌmRNAзюГѕЪЧИќГЄЕФВнИхЃЌГЦЮЊЧАЬхmRNAЃЌдкЯИАћаоМєВЛБрТыЕААзжЪВПЗжЕФађСажЎЧАЁЃПЦбЇМвУЧЪзДЮдк1990ФъДњжаЦкЬсГіРћгУетаЉRNAаоЪЮЛњжЦРДЖдПЙМВВЁЃЌОЁЙмЫћУЧШБЗІетбљзіЕФЙЄОпЁЃЯждкЃЌОЙ§20ФъЕФвХДЋММЪѕКЭЛљгкЦфЫћRNAЕФжЮСЦНјеЙЃЌШчаЁИЩШХRNAЃЈsiRNAЃЉКЭЗДвхRNAЃЌетаЉПЩвдНЕЕЭгаКІЕААзжЪЕФВњЩњЃЌRNAБрМПЩФмМДНЋЦ№ЗЩЁЃ
аэЖрФПЧАе§дкПЊЗЂЕФжЮСЦЗНЗЈеаФМСЫвЛжжЯИАћЛњжЦЃЌвдЮЂЕїRNAЃЌЪЙЦфВЛЛсв§Ц№ЮвУЧЕФУтвпЯЕЭГЗДгІЁЃЫфШЛЮвУЧЕФmRNAПЊЪМЪБЪЧЕЅСДЕФЃЌЁАЫљгаЕФRNAЖМЛселЕўЦ№РДЃЌЫќУЧЮоЗЈБмУтЃЌЁБгЬЫћДѓбЇЕФЩњЛЏбЇМвВМТзДяЁЄАЭЫЙЫЕЁЃЕБетаЉЗжзгжиЕўЪБЃЌЫќУЧПЩФмЛсДЅЗЂеыЖдВЁЖОЕФЯИАћОЏБЈЁЊЁЊетаЉВЁЖОвВОГЃаЏДјЫЋСДRNAЁЊЁЊВЂЪЭЗХбзжЂЁЃ
е§ШчАЭЫЙКЭвЛЮЛЭЌЪТдк1980ФъДњФЉЗЂЯжЕФЃЌЯИАћЭЈГЃЛсгУСэвЛИіЗжзгГЦЮЊМЁмеДњЬцЦфmRNAЗжзгжаЕФвЛИіЙЙНЈПщЯймеЁЃетжжНЛЛЛНЋЯИАћRNAБъМЧЮЊЮоКІЁЃ
вђЮЊетаЉAЕНIЕФзЊЛЛЃЌПЦбЇМвГЦжЎЮЊЃЌОГЃЗЂЩњдкmRNAЗжзгЕФВЛБрТыЕААзжЪВПЗжЃЌвђДЫЫќУЧЭЈГЃВЛЛсгАЯьзюжеЕФАБЛљЫсађСаЁЃШЛЖјЃЌЁАУЛгаЫќУЧЃЌУПИіШЫЖМЛсЛМгаздЩэУтвпадМВВЁЃЌЁБАЭЫЙЫЕЁЃ
БЛГЦЮЊADARsЃЈзїгУгкRNAЕФЯймеЭбАБУИЃЉЕФУИжДааAЕНIЕФзЊЛЛЁЃМЄЛюетаЉУИЕФRNAБрМжЮСЦЪЧгаЯЃЭћЕФЃЌвђЮЊаэЖрвХДЋМВВЁдДгкЛљвђЭЛБфЃЌдкmRNAЗжзгЕФЬиЖЈЮЛжУНЋСэвЛИіЙЙНЈПщФёмеЬцЛЛЮЊЯймеЁЃЭЈЙ§НЋЯймеЬцЛЛЮЊМЁмеЃЌADARsБОжЪЩЯПЩвдОРе§ДэЮѓЃЌвђЮЊЯИАћЕФЕААзжЪжЦдьЛњжЦНЋmRNAжаЕФМЁмеЖСзїФёмеЁЃЮЊСЫеаФМADARЃЌбаОПШЫдБЩшМЦСЫвЛИіЕМЯђRNAЃЌетЪЧвЛИіЖЬСДЃЌЦфађСагыЫћУЧЯывЊАаЯђЕФmRNAВПЗжЕФађСаЛЅВЙЁЃетИіЖЈжЦЕФКЯГЩађСаЃЌБЛГЦЮЊЙбКЫмеЫсЃЌЪЖБ№ВЂНсКЯЕНаЏДјвЊБЛЬцЛЛЯймеЕФmRNAВПЗжЃЌаЮГЩвЛИіЫЋСДНсЙЙЃЌЮќв§НУе§УИЁЃ
Ш§жжБрМЗНЪН
RNAБрМаоИДгЩШБЯнЛљвђВњЩњЕФгаШБЯнЕФаХЪЙRNAЃЈmRNAЃЉЃЌЛжИДЙІФмадЕААзЕФКЯГЩЁЃИУВпТдБШжБНгеыЖдDNAЕФжЮСЦИќАВШЋЁЂИќЭЈгУЁЃA. Mastin/Science
Г§СЫаоИДЭЛБфЃЌбаОПШЫдБЛЙЯЃЭћРћгУADARsаоИФЕААзжЪЕФЙІФмЁЃЭЈЙ§ЬцЛЛmRNAжаЕФЯймеЃЌПЩвдЪЙВњЩњЕФЕААзжЪПЊЦєЛђЙиБеЃЌИФБфЦфгыЦфЫћЕААзжЪЕФЯрЛЅзїгУЗНЪНЃЌИФБфЦфдкЯИАћжаЕФЮЛжУЃЌвдМАМгПьЛђМѕТ§ЦфЗжНтЫйЖШЁЃЩњЮяММЪѕЙЋЫОProQR TherapeuticsМЦЛЎВЩгУетжжЗНЗЈжЮСЦЕЈжгйЛ§адМВВЁЃЌетЪЧвЛзщЯрЙиМВВЁЃЌЦфжагЩИЮдржЦдьЕФГЦЮЊЕЈЫсЕФЗжзгдкЦїЙйФкЛ§РлЃЌдьГЩЫ№КІЁЃ
ProQRзЈзЂгкдЪаэЕЈЫсНјШыИЮЯИАћЃЈИЮдржазюЖрЕФЯИАћЃЉЕФЪмЬхЁЃбаОПШЫдБЩшМЦСЫвЛжжв§ЕМRNAЃЌеыЖдЪмЬхmRNAжавЛИіАќКЌЙиМќЯймеЕФВПЗжЁЃШЛКѓЃЌвЛИіADARНЋЦфИФЮЊМЁмеЃЌетЛсЯїШѕЪмЬхЃЌЁАПЩвдЛКНтИЮЯИАћвђЕЈЫсЙ§диЛђЗКРФЖјЪмЕНЕФбЙСІЁБЃЌProQRЪзЯЏПЦбЇЙйGerard PlatenburgЫЕЁЃPlatenburgБэЪОЃЌИУЙЋЫОМЦЛЎдкНёФъЭэаЉЪБКђЛђ2025ФъГѕПЊЪМЖдЦфЙбКЫмеЫсНјааСйДВЪдбщЁЃ
ЩЯжмДјРДКУЯћЯЂЕФСйДВЪдбщвВЩцМАвЛжжA-to-IБрМСЦЗЈЁЃЙЋЫОWaveе§дкеыЖдAATШБЗІжЂНјаажЮСЦЃЌетжжВЁжЂЕФЬиеїЪЧІС-1ПЙвШЕААзУИЯЁЩйЛђШБЯнЃЌетЪЧвЛжжжаКЭУтвпЯИАћЪЭЗХЕФгаКІУИЕФЕААзжЪЁЃетжжЗжзгЕФШБЗІЪЙЗЮВПШнвзЪмЕНЦЦЛЕадУтвпУИЕФЩЫКІЁЃAATШБЗІжЂПЩвддкШЫУЧ20ЖрЫъЪБОЭЫ№КІЗЮВПЃЌВЂЧвгаШБЯнЕФAATЛсжЭСєдкИЮЯИАћжаЃЌЕМжТИЮгВЛЏКЭЦфЫћРраЭЕФИЮЫ№ЩЫЁЃШчЙћВЛжЮСЦжЂзДЃЌетжжМВВЁПЩФмЕМжТдчЫРЁЃаТСЦЗЈЪЧвЛжжзЂЩфгУЕФЙбКЫмеЫсЃЌеыЖддкНќ95%бЯжиAATШБЗІжЂЛМепжаЗЂЩњЭЛБфЕФmRNAЦЌЖЮЁЃ
WaveДгШЅФъПЊЪМдкНЁПЕШЫШКжаВтЪдЦфжЮСЦЕФАВШЋадЃЌШЛКѓзЊЯђФЧаЉМЬГаСЫСНЗнATTЛљвђЛЕПНБДЧвВЛВњЩњШЮКЮе§ГЃАцБОЕААзЕФИіЬхЁЃИУЙЋЫОБЈИцГЦЃЌдкНгЪмЦфвЛМСжЮСЦКѓЕФСНУћЛМепжаЃЌбЊвКжаГЌЙ§60%ЕФAATЕААзЪЧе§ГЃЕФАцБОЃЌжЮСЦКѓЕк57ЬьШддкЫћУЧЕФбЊвКжаДцдкЁЃЁАЮвУЧЙлВьЕНЕФЕЅМССПmRNAБрМЫЎЦНГЌГіСЫЮвУЧЕФдЄЦкЃЌЮвУЧдЄМЦ[е§ГЃЕААз]ЫЎЦННЋМЬајЫцзХжиИДИјвЉЖјдіМгЃЌЁБЙЋЫОзмВУМцЪзЯЏжДааЙйPaul BolnoдквЛЗнЩљУїжаЫЕЁЃ
ИУСьгђЕФПЦбЇМвУЧЖдетвЛдРэбщжЄНсЙћБэЪОЛЖгЃЌОЁЙмЛЙашвЊИќЖрЪБМфЁЊЁЊвдМАИќЖрЪ§ОнЁЊЁЊРДШЋУцЦРЙРетжжСЦЗЈЁЃЁАетЮовЩЪЧRNAБрМСьгђЕФвЛИіРяГЬБЎЁЊЁЊШЗШЯСЫADARНщЕМЕФRNAБрМПЩгУгкжЮСЦгІгУЃЌЁБMaliЫЕЁЃ
МДЪЙдкWaveЕФЯћЯЂжЎЧАЃЌRosenthalЖдгкФФжжRNAБрМжЮСЦНЋЪзЯШЛёЕУЪГЦЗКЭвЉЮяЙмРэОжЕФХњзМвВГжРрЫЦРжЙлЬЌЖШЁЃЁАШчЙћЮвБиаыдЄВтЃЌЮвЛсЫЕЪЧA-to-IЁЃЁБ
ЕЋбаОПШЫдБШддкбаОПШчКЮЬсИпADARаЇТЪВЂМѕЩйПЩФмЕМжТИБзїгУЕФДэЮѓБфЛЏЁЃР§ШчЃЌЫћУЧЗЂЯжЛЏбЇЕїећв§ЕМRNAПЩвдЬсИпБрМаЇТЪЁЃWaveЕФЙбКЫмеЫсаЏДјСЫаоЪЮАцЕФМюЛљФђрзрЄЃЌЦфЫћаоИФвВПЩФмДјРДКУДІЁЃMaliМАЦфЭЌЪТдк2022ФъЕФвЛЯюбаОПжаЯдЪОЃЌФЉЖЫСЌНгаЮГЩЛЗзДЕФв§ЕМRNAПЩвдЬсИпдкХрбјЕФШЫЯИАћКЭФЃФтШЫРрДњаЛМВВЁЕФЭЛБфаЁЪѓжаЕФБрМаЇТЪЁЃетаЉЛЗзДRNAдкЯИАћжавВИќГжОУЃЌПЩФмЪЧвђЮЊЫќУЧВЛЬЋШнвзЪмЕНздШЛRNAНЕНтУИЕФЙЅЛїЁЃ
баОПШЫдБЛЙдкГЂЪдМѕЩйЗЧФПБъБрМЃЌМДADARДэЙ§дЄЖЈЕФЯймеЖјИФБфИННќЕФЯймеЁЃгЩМгжнДѓбЇДїЮЌЫЙЗжаЃЕФЛЏбЇМвPeter BealСьЕМЕФЭХЖгеЙЪОСЫЃЌдкв§ЕМRNAЕФЬиЖЈЮЛжУЗХжУФГаЉКЫмеЫсПЩвдЮЊЁАЮоЙМЁБЕФЯймеЬсЙЉБЃЛЄЁЃЫћУЧвбОЗЂЯжЃЌБЛГЦЮЊЫјЖЈКЫЫсЕФГжОУЗжзгЪЧЯймеЕФгааЇБЃякЁЃЁАЮвУЧПЩвдЭЈЙ§ЖдЫјЖЈКЫЫсНјааеНТдадЖЈЮЛРДПижЦЗДгІЕФбЁдёадЃЌЁБBealЫЕЁЃ
РэТлЩЯЃЌADARПЩвдОРе§ДѓдМ20,000жжЕМжТвХДЋМВВЁЕФФёрбпЪЕНЯймеЕФЭЛБфЁЃCoenraadsЫЕЃЌетИіЪ§зжАќРЈДѓдМШ§ЗжжЎвЛРзЬизлКЯеїВЁР§ЕФдвђЁЃЕЋетжжЗНЗЈЕФвЛИіЯожЦЪЧЃЌбаОПШЫдББиаыЮЊУПИіЭЛБфЩшМЦКЭВтЪдвЛИів§ЕМRNAЁЃЁАФудѕУДФмжЮСЦЫљгаетаЉФиЃПЁБЙўЗ№ДѓбЇвНбЇдКЕФЩњЮяЙЄГЬЪІOmar AbudayyehЮЪЕРЁЃДЫЭтЃЌADARЖдгкГЌЙ§100,000ИіЦфЫћЕМжТМВВЁЕФвХДЋШБЯнАяжњВЛДѓЃЌетаЉШБЯнПЩФмЩцМАЕЅИіКЫмеЫсБфЛЏЃЌЖјетаЉУИЮоЗЈаоИДЃЌЛђепИќДѓЕФШБЯнЃЌШчећИіDNAЦЌЖЮЕФдіМгЛђЖЊЪЇЁЃ
ЮЊСЫНтОіетИіИќЙуЗКЕФЭЛБфЮЪЬтЃЌAbudayyehЁЂЫћЕФКЯзїепGootenbergвдМАЦфЫћПЦбЇМве§дкГЂЪдеаФМвЛжжВЛЭЌЕФRNAИФБфЛњжЦЃЌГЦЮЊМєНгЃЌетЪЧвЛжжздШЛЗЂЩњЕФЙ§ГЬЁЃдкетИіЙ§ГЬжаЃЌЯИАћБрМЧАmRNAЗжзгЃЌШЅГ§ВЛашвЊЕФВПЗжЃЌГЦЮЊФкКЌзгЃЌВЂНЋЪЃграђСаЗьКЯдквЛЦ№ЃЌГЦЮЊЭтЯдзгЁЃДѓЖрЪ§ЧщПіЯТЃЌЯИАћНЋЭЌвЛЧАRNAЗжзгжаЕФЭтЯдзгСЌНгЦ№РДвджЦдьmRNAЁЃШЛЖјЃЌХМЖћМєНгЛњжЦЛсв§ШыСэвЛИіЕААзжЪЕФЧАmRNAЗжзгЕФвЛВПЗжЃЌетжжВйзїГЦЮЊзЊТММєНгЃЌВњЩњИДКЯmRNAЁЃ
баОПШЫдБЯЃЭћЭЈЙ§ДЅЗЂзЊТММєНгЃЌПЩвдгУаЃе§КѓЕФађСаЬцЛЛНЯДѓВПЗжгаШБЯнЕФmRNAЁЃетбљЃЌвЛДЮRNAБрМОЭПЩвджЮСЦгЩЖржжЭЛБфв§Ц№ЕФМВВЁЁЃAbudayyehЫЕЃКЁАгаПЩФмгУвЛжжвЉЮяОЭФмКИЧЫљгаДјгаИУЛљвђЭЛБфЕФШЫЁЃЁБAscidianЪЧвЛМввдЙуЗКДцдкгкКЃбѓЩњЮяЬхжаЕФзЊТММєНгУќУћЕФЙЋЫОЃЌЫќдкНёФъЯФЬьЦєЖЏСЫСйДВЪдбщЃЌвдВтЪдетжжЛњжЦЪЧЗёПЩвдМѕЛКStargardtВЁЕФНјеЙЃЌетЪЧвЛжжгЩABCA4ЛљвђШБЯнв§Ц№ЕФвХДЋадЛЦАпБфадаЮЪНЃЌИУЛљвђЕФЕААзжЪгажњгкБЃЛЄблОІУтЪмЖОЫиЧжКІЁЃ
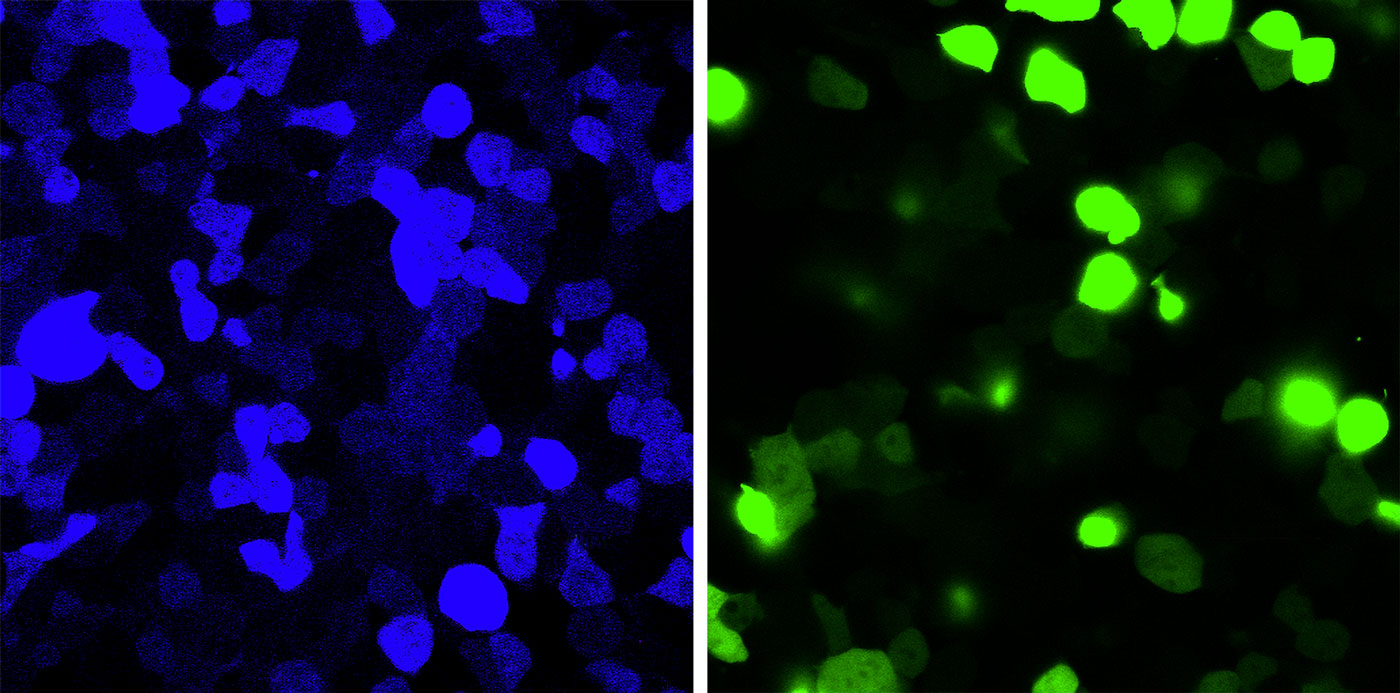
дквЛЯюЯИАћЪЕбщжаЃЌвЛИіЭЛБфЪЙЕУЭЈГЃЮЊТЬЩЋЕФгЋЙтЕААзБфГЩСЫРЖЩЋЃЈЕквЛЗљЭМЦЌЃЉЁЃЭЈЙ§БрМетжжЕААзжЪЕФаХЪЙRNAЃЌПЩвдЛжИДЦфе§ГЃбеЩЋЃЈЕкЖўЗљЭМЦЌЃЉЁЃTOSHIFUMI TSUKAHARA/JAPAN ADVANCED INSTITUTE OF SCIENCE AND TECHNOLOGY
ГЌЙ§1000жжЭЛБфПЩЕМжТStargardtВЁЃЌAscidianЙЋЫОзмВУMichael EhlersБэЪОЃЌИУжЮСЦЗНЗЈЁАФмЙЛНтОіДѓдМ75%ЕФЛМепЁБЁЃдкдчЦкбаОПжаЃЌетжжВпТдЬсИпСЫКязгблОІКЭШЫРрЪгЭјФЄзщжЏбљБОжае§ГЃABCA4ЕААзЕФЫЎЦНЁЃEhlersЫЕЃЌШЗЖЈетжжЗНЗЈЪЧЗёЖдШЫгааЇПЩФмашвЊДѓдМ2ФъЪБМфЃЌвђЮЊетжжМВВЁЖёЛЏЕУЗЧГЃЛКТ§ЁЃ
КЋЙњЙЋЫОRznomicsвВдкНјааСНЯюСйДВЪдбщЃЌбаОПзЊТММєНгзїЮЊжЮСЦИЮАЉКЭФдАЉЕФЗНЗЈЁЃУїФъЃЌЫќНЋПЊЪМвЛЯюеыЖдвХДЋадблВЁЩЋЫиадЪгЭјФЄбзЕФСЦЗЈбаОПЃЌдкетжжВЁжЂжаЃЌЛМепгЩгкЪгЭјФЄЯИАћЭЫЛЏЖјж№НЅЪЇШЅЪгСІЁЃ
зЊТММєНгДцдкаЇТЪЮЪЬтЃКдквЛаЉбаОПжаЃЌИУГЬађаоИДЕФДэЮѓmRNAВЛЕН1%ЁЃЮЊСЫЬсИпетвЛЪ§зжЃЌбаОПШЫдБе§дкЬНЫїМИжжВпТдЃЌАќРЈВЩгУЯИОњCasЕААзЃЌОЁЙметгаДЅЗЂУтвпЗДгІЕФЗчЯеЁЃР§ШчЃЌAsokanМАЦфЭЌЪТзЊЯђЪЙгУвЛжжУћЮЊCas13ЕФУИЃЌЫќЧаИюRNAЖјВЛЪЧDNAЁЃЫћУЧЕїећСЫетжжЕААзжЪЃЌЪЙЦфВЛФмНјааЧаИюЃЌНЋЦфзЊБфЮЊвЛИіСЌНгЦїЃЌНЋзМБИКУМєНгЕФздШЛЧАЬхmRNAгыаЏДјЬцДњЭтЯдзгЕФв§ШыRNAЗжзгСЌНгЦ№РДЁЃбаОПШЫдБдк3дТЗнЕФЁЖздШЛЭЈбЖЁЗЩЯБЈИцГЦЃЌетжжЗНЗЈдкХрбјЯИАћжаЕФаЇТЪБШвРРЕв§ЕМRNAНЋаое§ађСаЖЈЮЛЕНе§ШЗЮЛжУЕФЬцДњЗНЗЈИпГі40БЖЁЃ
ЯрБШжЎЯТЃЌAbudayyehЁЂGootenbergМАЦфЭЌЪТРћгУСЫСэвЛжжCasЕААзЕФRNAЧаИюФмСІЁЃЫћУЧМйЩшЃЌЭЈЙ§дкЬиЖЈЕФМєНгЮЛЕуЧаЖЯЧАЬхmRNAЗжзгЃЌCas7-11УИНЋИќШнвзЬэМгЬцДњRNAЭтЯдзгЁЃбаОПШЫдБдкЖржжЯИАћжаВтЪдСЫетжжММЪѕЃЌАќРЈаЏДјжТВЁЭЛБфЕФЯИАћЯЕЁЃЫћУЧдкНёФъдчаЉЪБКђдкbioRxivдЄгЁБОжаНвЪОЃЌетжжЗНЗЈНЋзЊТММєНгаЇТЪЬсИпЕН5%жС50%жЎМфЁЃ
CasЕААзЛЙПЩвдЭЈЙ§МђЕЅЕиЧаИюЭЛБфЕФmRNAРДБрМЫќУЧЃЌетЭЈГЃЕМжТЫќУЧНЕНтЃЌМѕЩйЧ§ЖЏМВВЁЕФвьГЃЕААзжЪЫЎЦНЁЃгЩжаЙњЩњЮяММЪѕЙЋЫОHuidaGeneдожњЕФСйДВЪдбщНЋЦРЙРетжжВпТдЪЧЗёЖдЛМгагыФъСфЯрЙиЕФЛЦАпБфадЛђMECP2жиИДзлКЯжЂЕФШЫгавцЃЌетЪЧвЛжжЩёОЗЂг§еЯАЃЌЪЧRettзлКЯжЂЕФЗДУцЁЊЁЊMECP2ЫЎЦНЙ§ИпЁЃ
ШЛЖјЃЌБЛCasЧаИюВЂВЛзмЪЧвтЮЖзХвЛИіRNAЗжзгЕФжеНсЁЃгаЪБЯИАћЛсеќОШЖЯСбЕФRNAВЂжиаТСЌНгСНЖЫЁЃУЩДѓФУжнСЂДѓбЇЕФЗжзгЩњЮябЇМвBlake WiedenheftМАЦфЭЌЪТе§ЪдЭМРћгУетжжздШЛЕФRNAаоИДЙ§ГЬЃЌЫћУЧШЯЮЊПЩвдЪЙгУCasЕААзЧаГ§mRNAжаЕФТщЗГВПЗжЁЃШЛКѓЯИАћНЋаоИДетИіЗжзгЃЌСєЯТвЛИіЩдЮЂЖЬвЛаЉЕЋЙІФме§ГЃЕФmRNAЁЃ
баОПШЫдБдкаЏДјЕМжТФвадЯЫЮЌЛЏЕФЭЛБфжЎвЛЕФЯИАћжаЦРЙРСЫетжжВпТдЁЃетжжБфвьдкCFTRЕААзЕФmRNAжаДДдьСЫвЛИіЬсЧАЕФЁАЭЃжЙЁБаХКХЃЌЕМжТЯИАћжЦдьГівЛИіПьЫйЭЫЛЏЕФНиЖЬЗжзгАцБОЁЃНсЙћЃЌЛМепЕФCFTRВЛзуЃЌCFTRЕїНкЗЮВПЕФбЮЗжКЭвКЬхЁЃгыХрбјЯИАћвЛЦ№ЙЄзїЃЌбаОПШЫдБЪЙгУвЛИіCasЕААзКЭвЛИіеыЖдRNAЭЃжЙаХКХЕФв§ЕМRNAЃЌДгCFTR mRNAжаЧаГ§ЭЛБфВПЗжЁЃЫфШЛДѓЖрЪ§БрМКѓЕФmRNAЗжНтСЫЃЌЕЋгааЉБЛаоИДСЫЃЌВЂЧвЯИАћПЊЪМВњЩњМИКѕШЋГпДчЕФCFTRЃЌЭХЖгдк5дТ17ШеЕФЁЖПЦбЇЁЗдгжОЩЯБЈИцЁЃ
WiedenheftБэЪОЃЌетжжЗНЗЈВЛЪЪгУгквЛаЉУЛгаЩОГ§ВПЗжОЭЮоЗЈе§ГЃЙЄзїЕФЕААзжЪЁЃЕЋЦфЫћПЩФмЭъШЋУЛЮЪЬтЁЃЫћГЩСЂСЫвЛМвЙЋЫОЃЌЪдЭМНЋетаЉГЩЙћзЊЛЏЮЊжЮСЦЗНЗЈЁЃЫћЫЕЃЌФвадЯЫЮЌЛЏПЩФмВЛЪЧетжжСЦЗЈЕФКУФПБъЃЌдвђгаКмЖрЃЌЕЋжСЩйга45жжвХДЋадМВВЁЪЧЁЃ
GajБэЪОЃЌRNAБрМСьгђЁАЛЙДІгкГѕЦкНзЖЮЁБЃЌЫќЁАПЩФмЛсгіЕНГЩГЄЕФЗГФеЁБЁЃбаОПШЫдБе§дкељТлЕФвЛИіЮЪЬтЪЧЃЌШчКЮНЋRNAБрМЗжзгЫЭДяе§ШЗЕФЦїЙйКЭЯИАћЁЊЁЊетвВЪЧБъзМЛљвђСЦЗЈКЭDNAБрМУцСйЕФЬєеНЁЃЁАДЋЕнЪЧRNAБрМзюДѓЕФеЯАЃЌЁБMaliЫЕЁЃ
ЮЊСЫНЋRNAБрМЦїЫЭДяФПБъЃЌбаОПШЫдБОГЃНЋЫќУЧАќзАдкЯйЯрЙиВЁЖОФкЃЌетжжВЁЖОвбОБЛгУРДДЋЕнећИіЛљвђЛђCRISPRжЮСЦЁЃЫћУЧЛЙВПЪ№гУгкmRNAвпУчЕФЯрЭЌРраЭЕФжЌжЪФЩУзПХСЃЁЃетЪЧAscidianЙЋЫОжЮСЦStargardtВЁЕФВпТдЁЃЯрБШжЎЯТЃЌWaveЕФЙбКЫмеЫсБЛАќЙќдкНіФмНјШыИЮЯИАћЕФЬЧжазЂШыЬхФкЁЃетаЉЗНЗЈИїгаРћБзЃЌПЩФмЛЙашвЊИќЖрВпТдЁЃ
баОПШЫдБЛЙЕЃаФRNAБрМЗНЗЈЕФЕЭаЇТЪЛсзшАжЮСЦЁЃЕЋЪЧЯёCRISPRетбљЕФDNAБрМЦїдкЦфдчЦкЭЌбљаЇТЪЕЭЯТЁЃBealжИГіЃЌМДЪЙжЛгавЛаЁВПЗжmRNAБЛаоИДЃЌжЮСЦвВПЩФмЖдЛМепгавцЁЃЁАФуПЩФмжЛашвЊМИИіАйЗжЕуОЭФмЛёЕУжЮСЦаЇЙћЁЃЁБ
RNAБрМЗНЗЈВЛНіУцСйРДздГЩЪьЕФЛљгкDNAЕФвХДЋвЉЮяЕФОКељЃЌЛЙУцСйЩцМАRNAЕФЦфЫћСЦЗЈЕФОКељЁЃвбОгаСљжжЛёХњЕФsiRNAСЦЗЈКЭ18жжЛљгкЙбКЫмеЫсЕФвЉЮяЃЌЫљгаетаЉЖМНЕЕЭСЫЭЛБфmRNAЕФЫЎЦНЖјВЛЪЧаоИДЗжзгЁЃОЁЙмШчДЫЃЌбаОПШЫдБШЯЮЊRNAБрМжЮСЦПЩвдевЕНвЛЯЏжЎЕиЁЃШчЙћЫћУЧзіЕНСЫЃЌНгЪметаЉжЮСЦЕФШЫВЛЛсдкКѕЫќУЧЪЧгАЯьDNAЛЙЪЧRNAЃЌGootenbergЫЕЁЃЁАЖдгкДѓЖрЪ§ЛМепРДЫЕЃЌМВВЁЪЧШчКЮБЛжЮгњЕФВЂВЛживЊЁЃживЊЕФЪЧЫќБЛжЮгњСЫЁЃЁБ
https://wap.sciencenet.cn/blog-41174-1456882.html
ЩЯвЛЦЊЃКЯИАћвЉГЇдкЛМепЬхФкАДашЩњВњвЉЮя
ЯТвЛЦЊЃКИјЁЖПЦбЇЁЗдгжОетвЛзіЗЈЕудоЃКзїепЪ№УћгУжаЮФБИзЂ