博文
过敏特异性B记忆细胞
 精选
精选
||
对过敏原的免疫反应的特征是 2 型表型和 T 辅助性 2 (TH2) 分泌白细胞介素-4 (IL-4)、IL-5 和 IL-13 的细胞。这些细胞因子激活过敏原特异性 B 细胞,诱导它们分化为产生记忆 B 细胞 (Bmem) 和免疫球蛋白 E (IgE) 的浆细胞。记忆 T 细胞和具有过敏原特异性的 Bmem 的存在使得在第二次遇到过敏原时继续“过敏性”2 型免疫反应。这些免疫事件的关键是存在对过敏原成分具有特异性的 IgE。IgE 与肥大细胞和嗜碱性粒细胞表达的高亲和力 IgE 受体 FcεRI 结合。随后的过敏原暴露诱导结合的 IgE 交联,触发肥大细胞和嗜碱性粒细胞脱颗粒,释放包括组胺在内的炎症介质。然而,分泌型 IgE 的来源尚不清楚,因为 IgE Bmem 极为罕见,这可能是由于翻译欠佳导致的 IgE 表面表达低。在本期《科学转化医学》中,两项研究报告了一种 2 型极化 Bmem 亚群,该亚群有望转换为 IgE,从而赋予对多种过敏原过敏的个体过敏原特异性 。使用不同的患者队列和技术,Ota 等和 Koenig 等两者都发现了这种2型Bmem群体,其特征是IgG、CD23(低亲和力IgE受体,FcεRII)、IL-4受体(IL-4R)和种系IGHE的表达。
在他们的研究中,Ota等人检查了一组花生过敏儿童的循环Bmem。作者发现,在血清花生特异性IgE浓度高的儿童中,CD23 Bmem频率增加(>100 kU+一个/升)与花生特异性 IgE 低 (<5 kU一个/升)和非过敏个体。CD27 B 细胞的单细胞 RNA 测序分析揭示了所谓的“2 型标记”IgG1 Bmem 群体,其 IL4R、FCER2(编码 CD23)和种系 IGHE 的基因表达增加,以及高度突变的 B 细胞受体。在花生特异性 IgE 高的花生过敏儿童中,在花生过敏原 Ara h 2 特异性 B 细胞中鉴定出收敛 Ig 基因序列,这些 Ig 序列来源于 2 型 Bmem 群体。他们得出的结论是,转录种系IGHE的2型Bmem细胞包括一个独特的群体,该群体在花生过敏儿童中富集,并有可能分化为产生高亲和力的IgE浆细胞。
Koenig等人的报告在过敏和非过敏个体中鉴定出 2 型极化 Bmem 群体,种系 IGHE、FCER2、IL4R 的基因转录增加,CD32 的转录IL13RA1但转录较低。在他们的队列中,对桦树花粉或室内尘螨过敏的成年人比非过敏个体具有更多的循环IL-4RαCD23 2型Bmem。这些 Bmem 富集了表达 IgG1 和 IgG4 的细胞,并携带高度多样化的 Ig 基因库,但没有证据表明 V 基因使用存在趋同或偏倚。虽然过敏原特异性 Bmem 映射到 2 型 Bmem 人群,但来自同一供体的严重急性呼吸系统综合症冠状病毒 2 (SARS-CoV-2) 抗原特异性 Bmem(代表 1 型免疫力)没有,这表明 2 型表型与过敏性疾病相关。此外,2 型 Bmem 在舌下免疫治疗 (SLIT) 1 个月后在体内分化为产生 IgE 的浆细胞,其中过敏原常规在舌下给药,目的是减少过敏反应,如 SLIT 前 2 型 Bmem 与 SLIT 后 IgE 之间的克隆关系所示。作者还表明,在不同途径的过敏致敏后,小鼠模型中诱导了过敏原特异性 2 型 Bmem。虽然不需要生发中心和循环 IgE,但 IL-4 对于诱导 2 型表型至关重要。这些数据表明,2 型 Bmem 是过敏的致病人群和 IgE 的宿主。
这些发现产生的一个重要问题是,2型Bmem是如何形成的(图1)。Koenig 等人显示过敏原特异性Bmem定位于2型Bmem群体,并携带高亲和力表面Ig;同样,Ota 等显示过敏原特异性B细胞高度突变并转录FCER和种系IGHE。2 型 Bmem 的形成不依赖于生发中心,但在卵清蛋白过敏小鼠模型中确实需要 IL-4 。IL-4 是过敏中 2 型免疫反应的驱动因素,可能是体内较高的 IL-4 浓度(无论是在致敏期间还是在过敏时的 2 型免疫反应)都会驱动 2 型 Bmem 的产生。另一种 2 型 Bmem 标志物 FcεRII/CD23 的表达与循环 IgE 浓度呈正相关,因为 IgE 结合可稳定 FcεRII 并增加表面 CD23 丰度。尽管如此,CD23 似乎是一种稳定的 2 型 Bmem 标志物,因为 Koenig 等人表明 CD23 2 型 Bmem 群体在 IgE 缺陷小鼠和野生型小鼠中的数量相似。总之,这些数据表明过敏原特异性 2 型 Bmem 是在致敏过程中形成的,并且可以通过稳定的标志物来定义。+
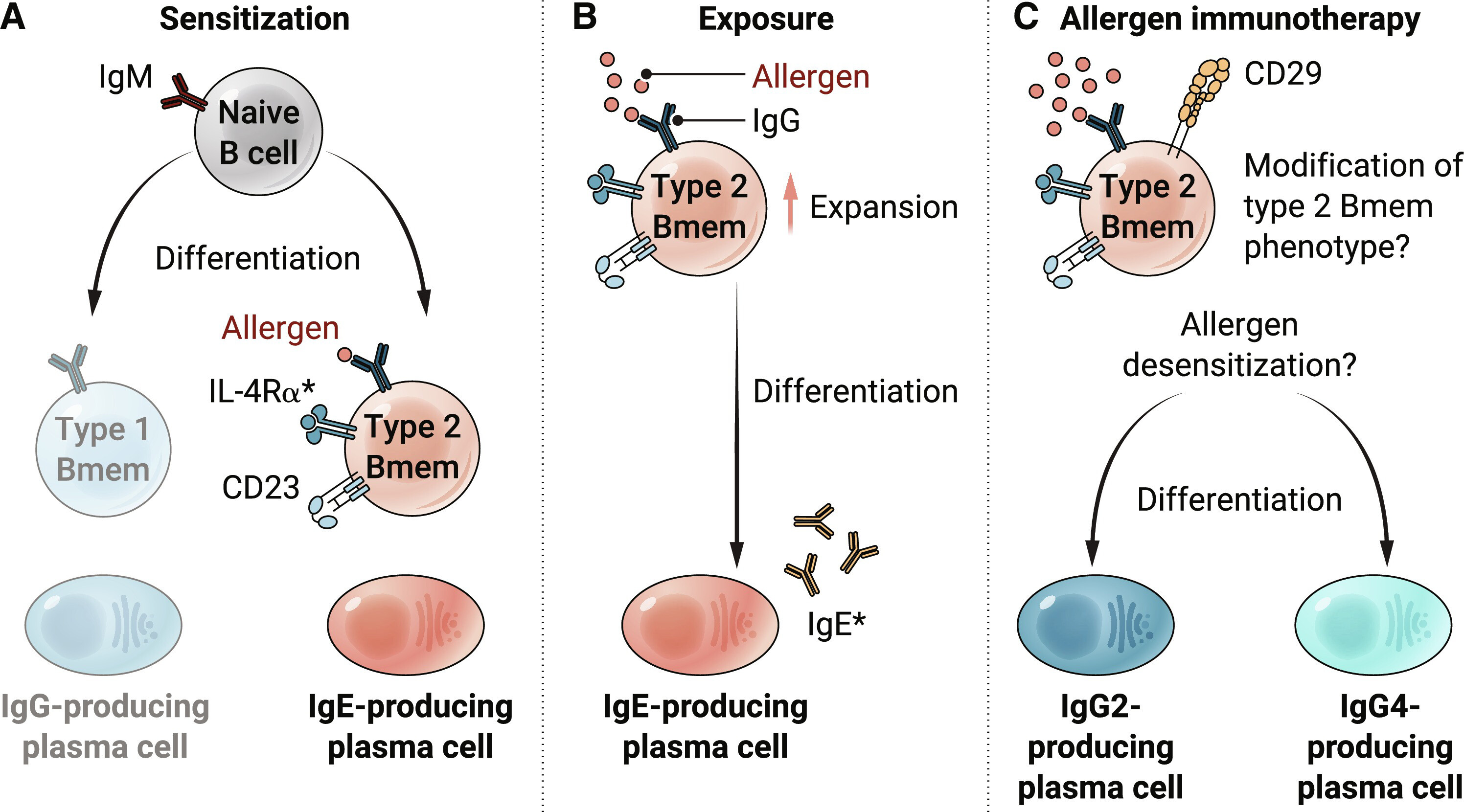
图 1.产生 IgE 的细胞的形成需要具有 2 型表型的过敏原特异性 Bmem。
(A) 过敏致敏与幼稚 B 细胞分化为 2 型 Bmem(棕色)而不是 1 型 Bmem(灰色)以及产生 IgE 的浆细胞的存在有关。(B) 在再次暴露过敏原时,2 型 Bmem 被激活、扩增并准备分化为产生 IgE 的浆细胞。星号表示可溶性 IgE 和 IL-4Rα 可通过单克隆抗体进行治疗性靶向治疗,以治疗过敏 。(C) 通过控制舌下接触过敏原(称为 SLIT)进行过敏原免疫疗法,假设会导致 2 型 Bmem 的扩增和其免疫表型的改变。这些细胞现在能够分化为产生 IgG2 和 IgG4 的浆细胞,这有助于过敏原脱敏。
因此,过敏中的致病性 B 细胞群似乎有两个要求:2 型表型和对过敏原特异性的高亲和力 B 细胞受体。Koenig等人的观察结果支持了这一点。SARS-CoV-2 特异性 Bmem 没有 2 型表型 。此外,2 型 Bmem 在非过敏个体中的出现频率低于过敏个体 。尽管如此,仍然需要获得因果关系的正式证据,理想情况下是通过在临床前模型中靶向和消耗 2 型 Bmem,然后测试由此产生的过敏反应。或者,可以通过评估针对非致敏人群中常见食物过敏原(如花生)或空气过敏原(如屋尘螨)的 Bmem 表型来获得进一步的支持证据。此外,过敏和非过敏个体的 2 型 Bmem 特异性及其对某些过敏原的潜在克隆扩增仍有待阐明。
目前尚不清楚是什么驱动表达 IgG 的 2 型 Bmem 分化为产生 IgE 的浆细胞。Koenig 等人显示过敏原免疫治疗 1 个月后的 IgE 转录本在治疗开始前定位于 2 型 Bmem 簇。IL-13 由 T 滤泡辅助细胞产生,驱动 B 细胞的体细胞超突变和高亲和力过敏原特异性 IgE 的产生。事实上,IL4R 和 IL13RA1(共同编码 IL-13 受体)的表达在 2 型 Bmem 中上调,表明这些细胞可接受 IL-13。然而,流式细胞术无法确认表面标志物表达,这与我们之前对黑麦草花粉过敏个体过敏原特异性 Bmem 的观察类似。因此,需要进一步的研究来揭示驱动 2 型 Bmem 分化为产生过敏原特异性 IgE 的浆细胞的因素。
目前还不清楚 2 型 Bmem 是否反映了 TH2 个具有独特转录因子的细胞,决定了它们的表型和功能,或者这些细胞是否是具有可塑性表型和功能的极化 Bmem,类似于调节性 B 细胞。 2 型 Bmem 中的特定转录因子,表明 Bmem 极化可能在功能上与 T 细胞不同。表达 IL-10 的调节性 B 细胞也是如此,这些细胞在功能上是明确的,不构成单个亚群或单独的谱系。进一步调查过敏和非过敏个体中 2 型 Bmem 的纵向转录组可以更清楚地了解其定义和可塑性。
Koenig 等人通过分析接受过敏原免疫治疗的患者样本,检查过敏原暴露对 2 型 Bmem 的影响。过敏原免疫疗法是唯一可用的过敏疾病改善疗法。通过持续定期舌下或皮下注射过敏原,2 型免疫力会发生变化,从而使患者对过敏原脱敏。虽然疗效可以达到80%,但这是一个数月至数年的长期过程。Koenig 等人显示,桦树花粉SLIT1个月后,过敏原特异性2型Bmem频率增加。重要的是,1个月仍处于治疗的早期,通常在脱敏开始之前。因此,SLIT 对 2 型 Bmem 数和免疫表型的影响尚不清楚。我们之前表明,对黑麦草花粉过敏的个体进行为期 4 个月的 SLIT 疗程可减轻过敏症状并改变 Bmem 对黑麦草花粉的主要过敏原 Lol p 1 特异性的表型。通过单细胞 RNA 测序,在 SLIT 4 个月后扩增了 2 个 Lol p 1 特异性 Bmem 簇,其中一个簇的特征是 IGHE、FCER2、IL4R 和 IL13RA1 上调,表明过敏原特异性 2 型 Bmem 扩增。这就提出了一个问题,即 2 型 Bmem 是致病的还是保护性的。重要的是,SLIT 后的 2 型 Bmem 簇还显示 IGHG4 和 ITGB1 上调,后者编码 CD29(整合素 β1)并负调控表面 Ig 信号转导。需要进行纵向研究以确定该亚群的表型变化是否有助于耐受性或疾病。
另一个前景是用生物制剂靶向 2 型 Bmem。合乎逻辑的候选药物是度普利尤单抗,这是一种 IL-4Rα 阻断抗体,具有双重作用,因为它可阻止 IL-4 和 IL-13 与其受体结合。第二种候选药物是奥马珠单抗,这是一种抗IgE抗体,可与IgE的Fc片段结合,从而阻止IgE与肥大细胞和嗜碱性粒细胞上的FcεRI结合。几项研究已经确定,在接受这两种抗体治疗的个体中,过敏症状和过敏性哮喘发作有所减少,但到目前为止,高昂的成本减缓了广泛摄取的速度。另一种治疗途径是将过敏原免疫疗法与靶向IL-4R或IgE的生物制剂相结合,这可以进一步减弱2型Bmem,并通过改变或消除致病性IgE的来源来提供长期益处。
总之,Ota 等人和 Koenig 等人两者都确定了在过敏性疾病患者中扩展的 2 型 Bmem 亚群。尽管该亚群表达表面膜 IgG1,但它也表达 FcεRII、IL-4Rα 和种系 IGHE 转录本,使其在 2 型环境中激活后有望分化为产生 IgE 的浆细胞。因此,过敏个体中致病性 IgE 的来源似乎是 B 细胞,该 B 细胞具有 (i) 对相关过敏原成分的高亲和力和 (ii) 具有切换到 IgE 倾向的 2 型表型。换句话说,它需要两个。
https://wap.sciencenet.cn/blog-41174-1421434.html
上一篇:血管周围成纤维细胞可能是ED的基础
下一篇:“比尔·盖茨问题”:亿万富翁慈善家是否扭曲了全球健康研究?