博文
促进肠道共生菌的适应性
|
改善有益微生物在人体肠道中的定植、存活和持久性具有巨大的治疗潜力,因为它们在健康和疾病中起着关键作用。特别是,肠道共生细菌携带许多基因,这些基因在它们所居住的宿主中没有同源物,因此它们能够实现宿主基因组中未编码的各种功能。对于哺乳动物来说,这些功能包括从其他难以消化的膳食纤维中提取能量、维生素产生和对病原体的抵抗力。人体肠道菌群的破坏与代谢紊乱、免疫缺陷、对药物的易感性改变、心理健康问题和某些类型的癌症有关。为了利用肠道共生菌作为益生菌的益处,确定细菌决定因素和宿主条件(例如饮食和饮食模式(例如禁食))至关重要,这些因素可以促进其健康。
Advancing the fitness of gut commensal bacteria | Science
健康成年人胃肠道中的大多数微生物属于两个细菌门:芽孢杆菌门(以前称为厚壁菌门)和拟杆菌门。在拟杆菌属中,拟杆菌属的物种是革兰氏阴性厌氧菌,在人类中广泛分布,并提供重要的健康益处,例如分解营养丰富的蔬菜中复杂多糖的能力。因此,揭示有益共生菌在肠道中适应的机制将有助于设计具有理想特性的益生菌,例如增加在这种环境中的持久性。
肠道内单个微生物物种的丰度主要归因于宿主遗传因素和环境扰动,尤其是饮食。饮食的影响反映了肠道微生物物种在吸收和分解特定营养物质的能力方面存在差异。例如,共生细菌 Bacteroides thetaiotaomicron (多形拟杆菌)具有使用多种复合碳水化合物的非凡能力,包括膳食植物多糖、宿主聚糖和乳低聚糖。这种能力构成了食物网的基础,为肠道微生物居民及其宿主提供营养和维生素。此外,这种活性的广度反映了近 18% 的 多形拟杆菌基因致力于碳水化合物的利用。多形拟杆菌在瘦和健康人类中含量丰富,正在被评估为胃肠道疾病(包括溃疡性结肠炎和克罗恩病)的益生菌。
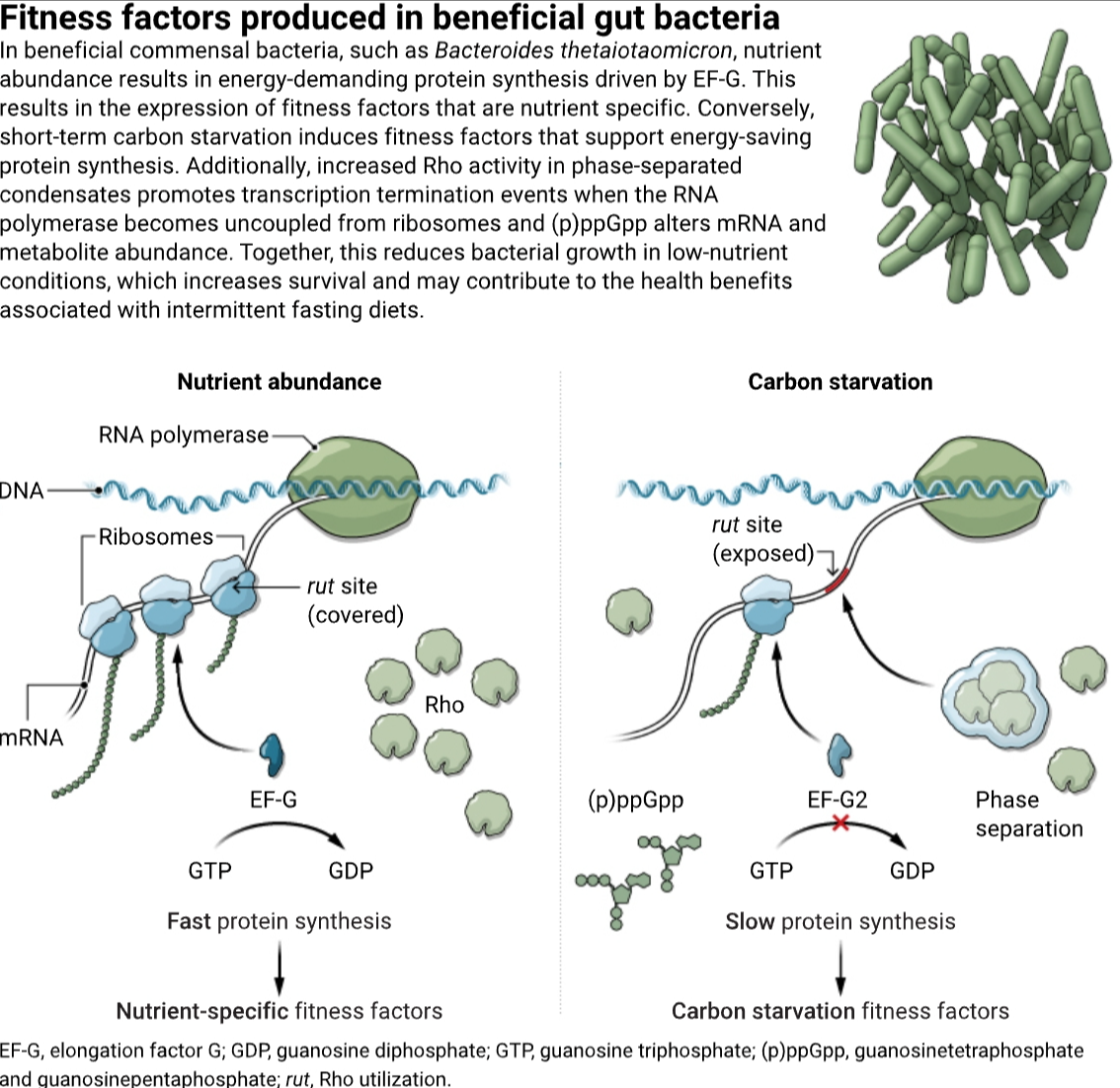
某些基因以宿主饮食依赖性方式促进肠道中的细菌适应性,因为它们能够利用膳食营养素。然而,肠道微生物每天面对的营养有限。例如,人类通常不会在夜间摄入营养物质,老鼠等夜行动物白天不进食,爬行动物可以在不进食的情况下存活数周。因此,肠道微生物表现出饥饿反应,即使许多微生物可以消耗肠上皮内壁的低聚糖并获取其他肠道微生物产生的副产物。在与宿主共同进化后,微生物可能会利用饥饿或某些营养物质的限制作为线索,帮助它们在营养波动的肠道环境中持续生存和生存。此外,如果营养限制本身促进了有益肠道细菌的健康,它是否也解释了人类似乎从热量限制或间歇性禁食饮食中获得的一些健康益处?
在实验室培养基中生长期间,在短时间内剥夺拟杆菌的碳水化合物来源(即碳饥饿)会增加肠道适应性决定因素的丰度或活性。这些决定簇控制着数百种基因、蛋白质和代谢物,这与响应特定饮食衍生营养素而产生的因子不同,后者通常调节的基因、蛋白质和代谢物要少得多。碳饥饿诱导的决定因素如何促进肠道中的细菌适应性?这些对人类健康有贡献吗?
碳水化合物利用的主要转录调节分子 — 碳水化合物利用调节分子 (Cur,也称为 BT4338) — 对于 多形拟杆菌 和其他拟杆菌属在小鼠肠道中的适应性至关重要 。Cur 在实验室培养基中出现碳饥饿的多形拟杆菌后 10 分钟内改变了数百个基因的转录。例如,负责利用单糖和多糖的几个基因的表达在碳饥饿时以 Cur 依赖性方式上调。
矛盾的是,在碳饥饿时以 Cur 依赖性方式诱导程度最高的 多形拟杆菌基因编码必需延伸因子 G (EF-G)的旁系同源物,这是唯一参与两个不同翻译步骤的蛋白质合成因子:在将每个氨基酸掺入生长的多肽链后,它将 mRNA 的运动和通过核糖体转移 RNA (tRNA) 加速 10,000 倍, 一旦核糖体到达终止密码子,它就有助于回收核糖体。经典 EF-G 蛋白在每个核糖体易位步骤中水解一个三磷酸鸟苷 (GTP) 分子,在核糖体回收过程中水解一个 GTP 分子。因此,伸长是蛋白质合成中最耗能的步骤,也是最耗能的细胞过程。
EF-G 旁系同源物(称为 EF-G2)具有迄今为止描述的所有 EF-G 蛋白所没有的独特特性:它催化核糖体易位而不水解 GTP,尽管速度比 EF-G 慢。此外,这种 EF-G2 介导的节能蛋白合成对 多形拟杆菌在小鼠肠道中的适应性至关重要 。EF-G2 在从小鼠身上收获的 多形拟杆菌 中的丰度是典型 EF-G 的 >10 倍,这表明这种细菌在小鼠肠道中经历碳饥饿。相比之下,在实验室培养基中细菌快速生长期间,EF-G 比 EF-G2 丰度高得多。
在碳饥饿期间部署 EF-G2 对多形拟杆菌有明显的益处,因为与经典的 EF-G 不同,EF-G2 在与空置(非翻译)核糖体结合时不会水解 GTP,这更有可能发生在营养限制条件下,因为非翻译核糖体的比例增加,带电的 tRNA 池减少(见图)。然而,EF-G2 不能完全取代必需的 EF-G,因为核糖体循环严格依赖于 GTP 水解,并且 EF-G2 缺乏鸟苷三磷酸酶 (GTP ase) 活性。EF-G2 在拟杆菌属中非常保守,与 多形拟杆菌 EF-G2 蛋白具有 75% 至 100% 的同一性 (9),包括在需要 EF-G2 才能适应小鼠肠道的物种中。拟杆菌 EFG2 蛋白具有 26 个氨基酸的延伸,尽管在拟杆菌门外的典型 EF-G 蛋白或 EF-G2 蛋白中不存在,但该延伸对蛋白合成至关重要。
Cur 编码 fusA2 基因的 EF-G2– 转录激活是多形拟杆菌适应小鼠肠道所必需的,其他拟杆菌属也表现出来 (8)。通过促进fusA2转录,Cur使细菌能够在碳饥饿损害能量可用性时进行节能的蛋白质合成。
在碳饥饿期间,双歧杆菌积累鸟苷四磷酸 (ppGpp) 和鸟苷五磷酸 (pppGpp),统称为 (p)ppGpp。这些分子是抗碳饥饿存活和细菌在小鼠肠道中适应所必需的。因此,多形拟杆菌可能在碳限制期间在肠道中特异性合成 (p)ppGpp。(p)ppGpp 以两种主要方式促进多形拟杆菌适应性:当细菌在小鼠肠道中经历碳饥饿时,通过改变 ~60% 基因的 mRNA 丰度,以及通过修饰数十种代谢物的丰度。例如,三羧酸循环代谢物琥珀酸和α-酮戊二酸(αKG)的浓度在碳饥饿期间以(p)ppGpp依赖性方式增加。αKG 积累对于抗碳饥饿的生存至关重要,因为补充 αKG 前体足以恢复缺乏 (p)ppGpp 的 多形拟杆菌 突变体的存活。
代谢物的(p)ppGpp依赖性变化可能是由于对(p)ppGpp结合形式的RNA聚合酶敏感的启动子的基因表达变化以及由(p)ppGpp变构调节的酶活性的变化引起的。多形拟杆菌与远亲共有的 (p)ppGpp 调控特性是能够降低蛋白质合成机制组分和相关因子的表达。总之,通过(p)ppGpp降低总蛋白质合成和使用EF-G2可能会导致细菌生长速率的降低,这可能有利于肠道细菌的存活,因为它赋予了对宿主来源的抗菌剂的耐药性,这些抗菌剂杀死了活跃生长的微生物。
在革兰氏阴性细菌中,转录和翻译是耦合的,因此它们以相同的速率发生。因此,面临碳饥饿的 多形拟杆菌翻译速度减慢可能导致两个过程的解耦。这种解偶联将增加转录终止因子 Rho 进入 mRNA 中 Rho 利用 (rut) 位点并在基因或操纵子末端之前终止转录的可能性。当转录与翻译脱钩时,通常由紧密尾随的核糖体 RNA 聚合酶保护的车辙位点变得暴露无遗。在面临碳饥饿时,多形拟杆菌如何应对对 Rho 活性增加的预期需求?
碳饥饿促进了 多形拟杆菌中 Rho 的液-液相分离 (LLPS),从而将 Rho 隔离到无膜隔室中。这种隔离可提高 Rho 在某些位点终止转录的能力,并改变数百个基因的 mRNA 丰度 。Rho 的 LLPS 受 Rho 蛋白中固有无序区域的控制,该区域也存在于除 多形拟杆菌以外的拟杆菌属中,但在远缘细菌(如大肠杆菌)中不存在 Rho。这种 LLPS 使 Rho 能够在更多位点终止转录,其中一些位点对应于控制肠道细菌适应性的基因。Rho活性的增加也可能影响其他过程,包括抑制普遍转录、抑制水平获得的基因、维持染色体完整性以及防止RNA-DNA杂交形成。
短期碳饥饿促进了 多形拟杆菌中健康决定因素的积累,这可能有助于报告归因于需要限制卡路里或间歇性禁食的饮食对人类健康的改善。某些营养素的限制可能有利于某些肠道物种的定植、存活和持久性。例如,卡路里限制饮食与人肠道中拟杆菌数量增加和芽孢杆菌丰度降低有关 ,间歇性禁食与人肠道中拟杆菌数量增加有关。然而,拟杆菌门和芽孢杆菌群丰度的这些变化可能反映了膳食成分的变化,而不是热量限制本身,这可能直接导致人类健康的改善。目前尚不清楚促进小鼠肠道适应性的 多形拟杆菌决定因素是否也在人类肠道中发挥作用。
如何利用对饮食和细菌适应性决定因素之间相互作用的日益增长的了解来开发促进人类健康的益生菌?在喂食单糖饮食的小鼠中,当一种被设计为抵抗单糖抑制健身促进转录因子 Roc 沉默的 多形拟杆菌菌株胜过野生型 多形拟杆菌时,建立了原理证明。该实验证明了工程化 多形拟杆菌如何以饮食依赖性方式在小鼠肠道中赋予适应性优势,其中适应性决定簇的产生不受饮食信号的影响。值得注意的是,利用拟杆菌属与人类健康相关的特性还可能需要灭活某些基因,以防止因逃逸胃肠道或帮助肠道病原体肠道定植而导致的致病结果。还可以纳入指定理想性状的其他基因。工程益生菌和饮食干预的综合作用可能会扩大治疗选择,例如仅根据特定的饮食成分改变工程益生菌的丰度。
https://wap.sciencenet.cn/blog-41174-1409954.html
上一篇:英国率先批准β地中海贫血CRISPR基因编辑疗法
下一篇:医学不科学吗?