博文
3D打印生物混凝土实现软骨高质量再生修复
||
3D打印生物混凝土实现软骨高质量再生修复
【背景】关节软骨损伤是常见问题,会导致部分关节功能丧失,并显著影响生活质量。然后现有研究多将关节软骨视为均一结构,忽视了其内部纵横交错的复杂ECM结构,导致难以再生出天然的关节软骨。
为了应对这一挑战,EFL团队仿生天然细胞外基质(ECM)的结构,从钢筋混凝土结构中汲取灵感,提出了“生物混凝土”的设计理念。该设计旨在仿生出组织的物理及生化微环境,重建出ECM的物理结构及与生化3D环境,从而促进加速缺损组织的功能化重建。具体而言,这种仿生组织构建体由三部分组成:生物水泥、可降解的生物钢筋以及生物活性石子。
a) 生物水泥:通过调配并筛选多种生物水凝胶(甲基丙烯酰胺化明胶(GelMA)、甲基丙烯酰胺化透明质酸(HAMA)和甲基丙烯酰胺化硫酸软骨素(ChSMA))以开发一种能够模拟软骨ECM三维生化微环境的生物水泥。这种生物水泥不仅为细胞提供了生物活性粘附位点,还通过调节各组分的比例,实现了机械性能和生化性能的可调性。
b) 生物钢筋:3D打印的超细纤维网络作为可降解的生物钢筋,其纤维取向从平行过渡到垂直,复制了天然软骨的复杂结构。通过调整UFNs的纤维尺度和间距,能够调控仿生软骨的机械性能使其与天然软骨压缩力学性能相匹配。
c) 生物活性石子:干细胞作为“生物活性石子”,在生物水泥和生物钢筋的协同作用下,促进了软骨组织的再生。
相关研究以“Biological reinforced concrete for cartilage repair with 3D printing” 为题发表在《Advanced Science》。浙江大学贺永教授、贵州大学李家春教授和浙江大学附属口腔医院谢志坚教授为论文共同通讯作者,贵州大学陈跃威副教授、浙二医院的傅涛医师及贵州理工学院的邹中妃副教授为论文的共同一作。
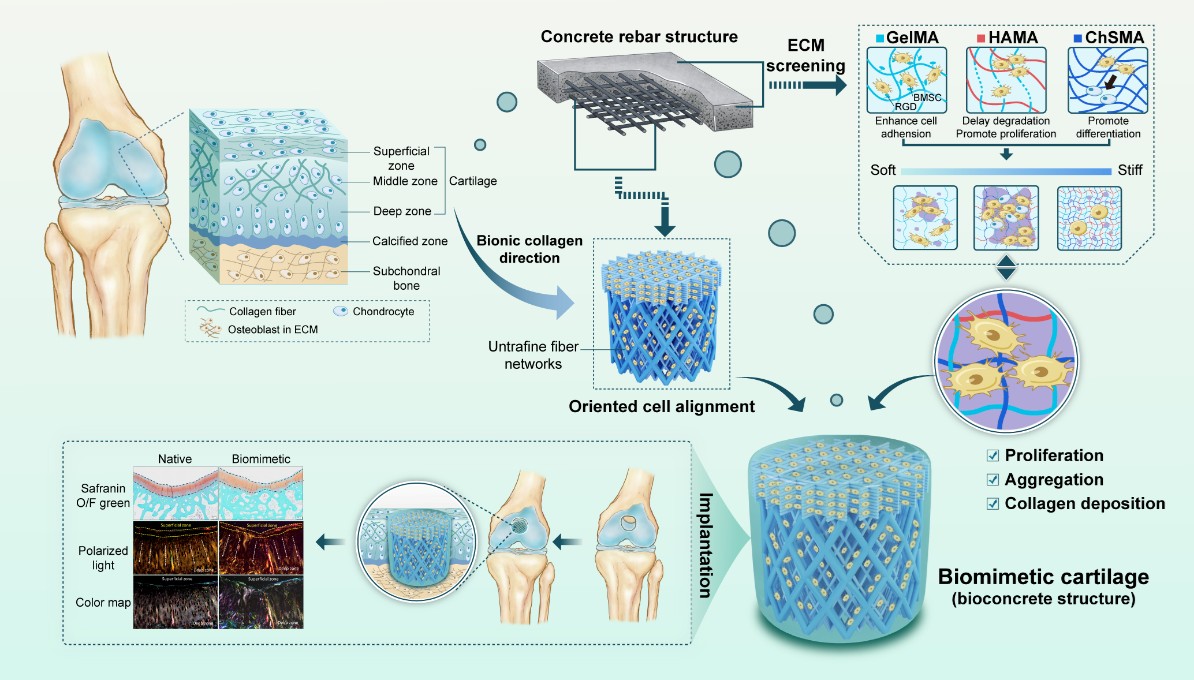
图 1. 生物钢筋混凝土仿生软骨构建体的设计与制造原理图
在人体内,几乎所有细胞都处于ECM三维基质中。ECM主要由三维网络构成,并富含生物活性信号分子,它支持细胞存活并决定细胞命运。细胞与ECM三维微环境之间的交流是通过生化和机械信号来调节的。从软骨ECM的组成中汲取灵感,本研究设计了一种明胶基复合生物水凝胶作为生物水泥。这种生物水泥以 GelMA 为骨架,并通过调节 HAMA 和 ChSMA 的比例来构建一个机械和生化特性均可调节的配方,从而有效地模拟ECM三维生化微环境。因此,研究人员通过固定GelMA的浓度并调整 HAMA 和 ChSMA 的浓度,设计了七种梯度刚度的基质配方以提供广泛的可调节模量范围。
在成软骨分化及再生过程中,间充质干细胞(MSCs)会表现出一系列细胞行为,例如增殖、迁移、聚集和分化。这个过程涉及软骨基质的分泌,最终导致组织重塑。在设计促进 hBMSC 分化并再生软骨的复合生物水凝胶时,必须充分考虑这些关键的细胞行为。因此,系统地研究并筛选了促进软骨基质沉积的最优复合生物水凝胶配方,以模拟软骨ECM三维生化微环境。

图 2 在体外3D培养hBMSC筛选促干细胞增殖、迁移和聚集的最优复合水凝胶配方

图 3 在体外3D培养hBMSC向软骨分化及分泌ECM情况
2、仿生软骨构建体的制备及其力学性能
最优复合生物水凝胶的压缩模量为 4.45 kPa,显著低于天然软骨的模量。尽管该复合生物水凝胶基质能够调节hBMSC的三维活性,且胶原基质的沉积有助于增加机械应力,但其弹性模量与天然软骨相比仍存在显著差异。值得注意的是,在缺乏拓扑线索的三维微环境中,细胞的生长和迁移以及软骨基质的分布和排列呈现无序和随机的特征。为此,研究人员借鉴了天然软骨中胶原纤维的形态与排列方式,通过近场直写技术构建超细纤维网络以模拟拓扑线索。具体而言,采用正交超细纤维网络模拟软骨表层区域平行排列的胶原纤维,而将多尺度45°菱形超细纤维网络卷曲成圆柱形以模拟中间过渡区。最终,将含有hBMSCs的最优生物水凝胶复合拓扑结构并固化以形成仿生软骨构建体。此外,通过调控纤维网络的设计、纤维直径与间距,使仿生软骨构建体的压缩力学性能接近天然软骨。

图4仿生软骨构建体的制备及其力学性能
3、在生物增强混凝土三维微环境中 hBMSC 迁移并分泌软骨基质
在模拟生理三维环境中,细胞向各个方向无规则的生长,然而,这种相对无序和混乱的生长模式常常不足以修复具有精确结构的组织。软骨的胶原纤维排列结构对其正常功能至关重要。在软骨再生过程中,表现出无方向性生长或混乱排列的细胞所分泌的软骨基质往往也是无序的,但是胶原纤维的排列与细胞取向密切相关,这强调了细胞排列在产生结构化和功能性软骨基质中的重要性。在生物钢筋混凝土的三维微环境中,细胞与生物水凝胶相互作用,经历增殖、迁移、聚集和分化,还需进一步探索超细纤维网络与细胞之间的相互作用。研究结果表明,相比于仅依赖生物水凝胶三维环境下细胞分泌的无方向性Ⅱ型胶原,在含有拓扑线索的生物水凝胶三维环境中,不仅能引导hBMSCs定向迁移,还能增强软骨分化并促使软骨基质的有序沉积。

图5 在生物增强混凝土三维微环境中 hBMSC 迁移并分泌软骨基质情况
4、验证仿生软骨构建体在体内修复软骨缺损的有效性
在体内实验中,研究人员将仿生软骨构建体植入兔子的骨软骨缺损处,并在术后8周和16周进行了生物学评估。结果表明,仿生软骨组的修复效果显著优于空白对照组。在术后16周时,仿生软骨组的软骨缺损几乎被新生软骨完全填充,表面光滑,与周围组织良好融合。根据国际软骨修复学会的评分标准,仿生软骨组的评分接近正常组。此外,微计算机断层扫描的3D重建图像进一步证实了仿生软骨构建体在促进骨下骨再生方面的具有显著优势。

图6 术后 8 周和 16 周的体内修复评估
为了评估修复后再生软骨中胶原的形态和排列方向,并进一步证实仿生软骨构建体在促进软骨再生方面的潜力,对组织切片进行了天狼星红染色,并在偏振光显微镜下进行了观察。结果表明,仿生软骨组的再生软骨在结构上与天然软骨相似,表现在浅层和深层的胶原纤维取向与天然软骨接近。

图 7 术后 8 周和 16 周各组胶原纤维分布的定量分析
综上所述,生物混凝土作为一种新型的组织再生设计理念,能成功地模拟了天然软骨的ECM微环境和拓扑结构,实现了与天然软骨相近的机械性能,并在体内实验中展现出优异的软骨修复效果。这一策略不仅可为软骨损伤的临床治疗提供新的手段,还为组织工程和再生医学领域的发展开辟新的路径。
全文链接:https://doi.org/10.1002/advs.202416734
https://wap.sciencenet.cn/blog-2159320-1478839.html
下一篇:仿海参原理的3D打印软/硬自由切换水凝胶