博文
[转载]幽门螺杆菌毒力靶向:消化致病菌识别和精准干预
||
幽门螺杆菌(Helicobacter pylori, H. pylori), 一个感染了全球近半数人口的细菌,被世界卫生组织(WHO)下属的国际癌症研究机构(IARC)列为 I 类致癌物。
它为何如此普遍?
它与胃癌之间究竟有多大距离?
当体检报告出现”阳性”时,我们是恐慌还是坦然面对?
......
本文将整合最新的临床指南与科研数据,系统拆解幽门螺杆菌的“前世今生”。从认识这个细菌开始,深入剖析其致病机制、健康危害、精准检测方法,并重点探讨当前面临的治疗挑战(尤其是抗生素耐药性),结合谷禾最新的肠道菌群+tNGS检测技术,最终提供一套科学、实用、可执行的预防与管理策略,消除知识盲区,告别“幽门焦虑”。
01认识胃中幽灵——幽门螺杆菌是什么?建立对幽门螺杆菌的基本认知,是科学应对的第一步。了解它的生物学特性、发现历史和全球流行状况,能帮助我们更理性地理解它。
幽门螺杆菌:强酸性胃液中生存和繁衍
幽门螺杆菌是一种革兰氏阴性、微需氧的螺旋状细菌。它独特的螺旋形态和顶端的多根鞭毛,赋予了其强大的运动能力,使其能够像螺旋桨一样钻透胃黏膜表面的黏液层,到达一个相对中性的避难所-胃上皮细胞表面进行定植。这种独特的生物学特性,是它能在pH值低至1-2的强酸性胃液中生存和繁衍的关键。

图源:bio.libretexts.org
诺奖级的发现:颠覆传统医学的认知
在20世纪80年代之前,医学界普遍认为,没有任何细菌能够在胃的强酸环境中生存,因此胃炎和消化性溃疡主要归因于压力和生活方式。
然而,澳大利亚科学家巴里·马歇尔(Barry Marshall)和罗宾·沃伦(Robin Warren)挑战了这一权威观点。沃伦首先在胃炎患者的胃黏膜活检样本中观察到了这种弯曲的细菌,而马歇尔则进一步推断它就是致病元凶。
马歇尔“以身试菌”——幽门螺杆菌是罪魁祸首
为了证明这一颠覆性的假说,在多次动物实验失败后,马歇尔勇敢地喝下了一杯含有幽门螺杆菌的培养液。
几天后,他出现了急性胃炎的症状,并通过胃镜检查证实了胃部的炎症和细菌感染。这一“以身试菌”的壮举,最终证实了幽门螺杆菌是胃炎和消化性溃疡的罪魁祸首。
这项发现彻底改变了消化病学的认知和治疗模式,使原本需要长期服药甚至手术的消化性溃疡,变成了一种可以通过短期抗生素治疗而治愈的感染性疾病。为此,两位科学家共同荣获了2005年诺贝尔生理学或医学奖。
全球流行病学数据:普遍存在的健康问题
幽门螺杆菌是全球最常见的慢性细菌感染之一,但其感染率在全球范围内分布不均,呈现出显著的地域差异。
➦ 总体感染率与趋势
根据一项涵盖1980年~2022年的大规模系统回顾分析,全球幽门螺杆菌的感染率呈现下降趋势。
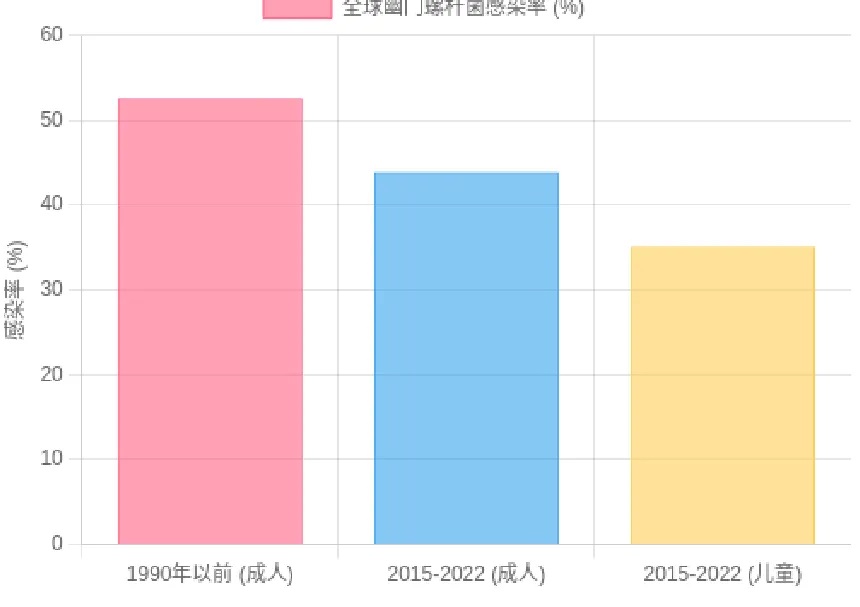
在2015年~2022年期间,全球成人的粗略感染率约为43.9%,儿童约为35.1%。
相比之下,1990年以前的成人感染率高达52.6%(Gastroenterology, 2024) 。
这一下降趋势主要归因于全球卫生条件的改善和治疗手段的普及。
➦ 地域差异显著
感染率与社会经济发展水平和卫生条件密切相关。
在许多发展中国家,感染率依然居高不下,例如非洲地区可达70-80%,拉丁美洲为60-70%。
而在发达国家,如北美和北欧,感染率则相对较低,约为30%-35% 。
这种差异凸显了公共卫生措施在控制感染中的重要作用。
doi.org/10.1186/s12951-025-03455-2
全球幽门螺杆菌感染率变化趋势
很多幽门螺杆菌感染者终身无症状,但携带某些菌株的胃黏膜却如同埋着微型炸弹,传统尿素呼气试验只能确认感染存在,而现代tNGS技术却能透视菌株毒力基因分布,这又是如何破局潜伏威胁?
接下来的章节,我们来看一下幽门螺杆菌如何致病,以及哪些幽门螺杆菌会致病,如何识别高风险菌株的检测方式等。
02潜伏的破坏者——幽门螺杆菌的致病机制与危害幽门螺杆菌并非一个温和的定居者,它拥有一套精密的武器库,能够系统性地破坏胃黏膜屏障,引发持续的炎症反应,并最终可能导致严重的胃部疾病。
其致病过程可概括为“生存-定植-攻击-致病”四部曲。
1酸中求生核心武器:尿素酶
胃腔内极端的酸性环境是抵御外来病原体的第一道防线。幽门螺杆菌能够在此环境中生存,其最关键的武器是尿素酶。这种酶能高效地将胃液中微量的尿素分解为氨气和二氧化碳。
氨气是碱性的,它可以在细菌周围形成一层“氨云”,有效中和局部胃酸,为细菌创造一个pH值接近中性的“微环境避难所”,从而保护自身免受强酸侵蚀。这一机制是幽门螺杆菌成功定植的先决条件(Int J Mol Sci, 2021)。
2精准移动与定植——鞭毛与黏附素
成功在胃酸中存活后,细菌需要穿透覆盖在胃壁上方的黏液层,并牢固地附着在胃上皮细胞上,才能避免被胃的蠕动排空。
动力系统:鞭毛
幽门螺杆菌拥有数根鞭毛,其螺旋状的结构和高效的摆动,使其能像潜水艇一样在黏稠的胃黏液中快速穿行,直达胃上皮细胞表面。
黏附工具:黏附素
到达目的地后,细菌会利用其表面的多种黏附分子,如血型抗原结合黏附素(BabA) 和唾液酸结合黏附素(SabA),像钩子一样与胃上皮细胞表面的特定受体结合。这种牢固的黏附是其长期定植和发挥致病作用的基础(World J Gastroenterol, 2018)。
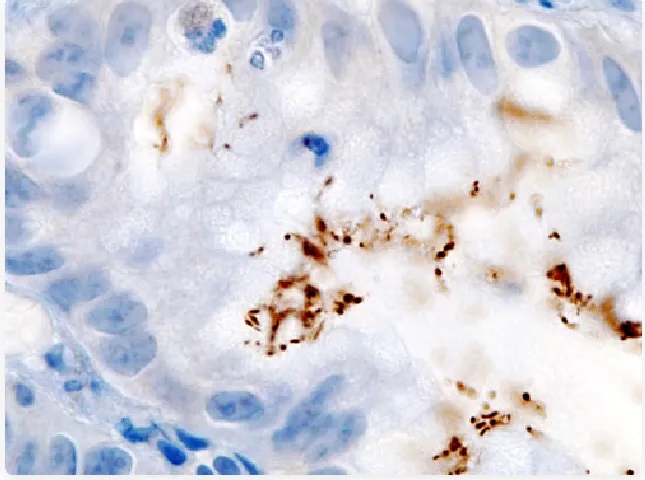
显微镜下,幽门螺杆菌(深色杆状物)紧密附着在胃上皮细胞表面
3释放毒素与组织损伤-CagA与VacA
成功定植后,幽门螺杆菌便开始释放一系列毒力因子,直接攻击宿主细胞,其中最臭名昭著的是 CagA 和 VacA。
“癌蛋白”CagA
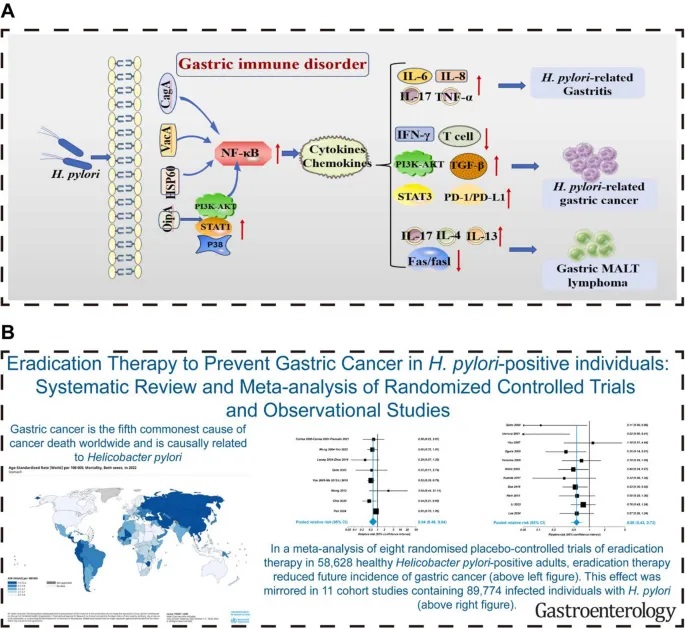
细胞毒素相关基因A (Cytotoxin-associated gene A, CagA) 是幽门螺杆菌最强的毒力因子,仅存在于部分菌株中 (即CagA阳性菌株)。这些菌株能通过一个针状的“IV型分泌系统”,像注射器一样将CagA蛋白直接注入胃上皮细胞内部。
进入细胞后, CagA会干扰细胞正常的信号传导通路,导致细胞骨架重排、细胞间连接破坏、促进细胞异常增殖并抑制其凋亡。这些效应共同促进了慢性炎症和细胞癌变, 因此CagA被认为是第一个被确认的“细菌癌蛋白”(National Cancer Institute)。
“空洞制造者”VacA
空泡毒素A (Vacuolating cytotoxin A,VacA)几乎存在于所有幽门螺杆菌菌株中。它能在宿主细胞内形成巨大的空泡,破坏线粒体功能,诱导细胞凋亡。此外,VacA还能抑制T淋巴细胞等免疫细胞的活化,帮助细菌逃避宿主的免疫监视,从而实现长期潜伏感染(Front Microbiol, 2011)。
4从炎症到癌症的演变一科雷亚级联反应
幽门螺杆菌的长期感染会启动一个被称为”科雷亚级联反应”(Correa Cascade) 的病理演变过程,这是目前公认的肠型胃癌发生的主要路径。这个过程是渐进的,通常历时数十年。
正常胃黏膜→慢性浅表性胃炎(H. pylori感染) → 慢性萎缩性胃炎→肠上皮化生→异型增生→胃癌
这个级联反应清晰地揭示了从简单的炎症到恶性肿瘤的演变路径。重要的是,在早期阶段(如慢性胃炎、甚至部分萎缩性胃炎),通过根除幽门螺杆菌,这一进程是可能被阻断甚至部分逆转的。这正是早期筛查和治疗幽门螺杆菌以预防胃癌的核心理论依据(Expert Rev Gastroenterol Hepatol,2010)。
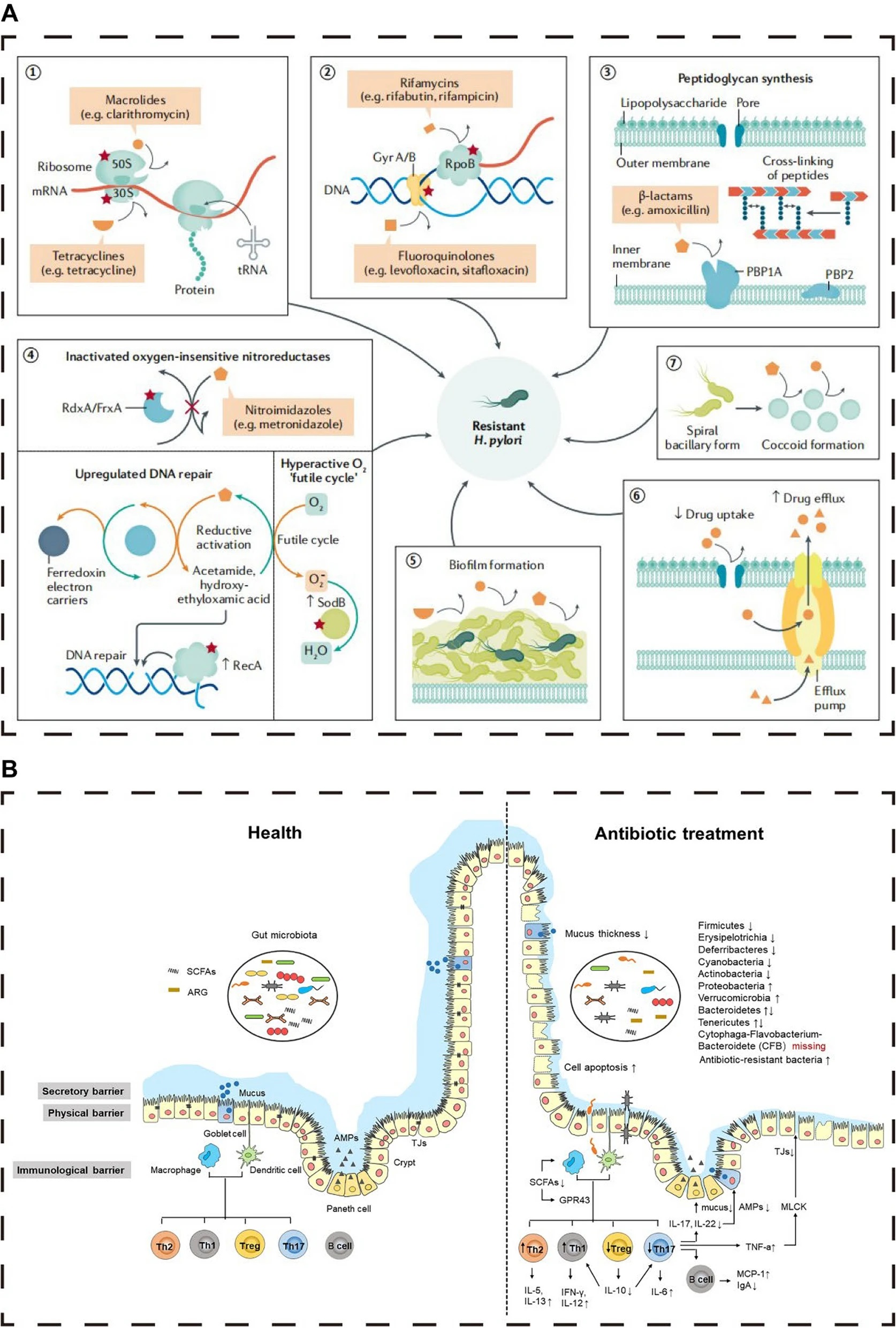
doi.org/10.1186/s12951-025-03455-2
关键要点总结
幽门螺杆菌通过尿素酶中和胃酸生存,利用鞭毛移动并借助黏附素定植
其后通过CagA和VacA等毒素直接损伤胃上皮细胞,诱发慢性炎症
长期的炎症反应会启动“科雷亚级联反应”,逐步从胃炎发展为胃癌
根除幽门螺杆菌是阻断这一进程的关键干预措施
为什么有的感染会导致严重疾病,而有的则相对温和?
需要指出的是,并非所有幽门螺杆菌菌株的毒力都相同。事实上,不同菌株的毒力差异巨大,这直接影响感染后疾病的严重程度和预后。
通过检测,可以对菌株进行分型,其中最重要的就是检测是否携带CagA、 VacA s1等强毒力基因。(具体检测方法我们会在后面章节详细介绍)
研究表明,感染CagA阳性菌株的患者,其发生消化性溃疡和胃癌的风险显著高于CagA阴性者(J Pers Med,2021)。
虽然目前毒力基因分型用于科研更多,但它代表了个体化风险评估和精准预防的方向。
正是由于不同菌株毒力的差异以及宿主因素的影响,幽门螺杆菌感染后可能导致不同结局。下一章节我们来看一下,幽门螺杆菌会带来哪些影响。
03不只是胃病——幽门螺杆菌的疾病版图幽门螺杆菌的影响远不止于胃部。它像一个系统性的麻烦制造者,其引发的慢性炎症和免疫反应可以波及全身,与多种胃外疾病的发生发展密切相关。
胃内疾病(关联明确)
这是幽门螺杆菌最直接、证据最充分的“犯罪现场”。
➦ 慢性胃炎
几乎所有的幽门螺杆菌感染者都会发生慢性活动性胃炎。虽然大多数人可能没有症状,但胃黏膜的炎症状态是所有后续疾病的基础(Clinical Microbiology Reviews,1997)。
➦ 消化性溃疡
约有15-20%的感染者会发展为消化性溃疡(包括胃溃疡和十二指肠溃疡)。在幽门螺杆菌被发现之前,溃疡被认为是无法治愈的慢性病,而现在,根除细菌已成为治疗和预防溃疡复发的标准方案。
➦ 胃癌
幽门螺杆菌是胃癌最强的独立危险因素。据估计,约1%的感染者最终会发展为胃癌,而全球约75-90%的非贲门胃癌病例都可归因于幽门螺杆菌的长期感染 (Expert Rev Gastroenterol Hepatol,2010)。
➦ 胃黏膜相关淋巴组织(MALT)淋巴瘤
这是一种罕见的B细胞非霍奇金淋巴瘤,其发生与幽门螺杆菌感染有极强的因果关系。神奇的是,对于早期的胃MALT淋巴瘤,单纯的幽门螺杆菌根除治疗就能使超过75%的患者获得肿瘤的完全缓解,堪称“抗生素治愈癌症”的典范 (World J Gastroenterol, 2015)。
胃外疾病(关联性得到证实或高度提示)
越来越多的证据表明,幽门螺杆菌的“长臂管辖”延伸到了胃肠道之外,通过诱发全身低度炎症、自身免疫反应或影响营养吸收等机制,参与多种系统性疾病的发生。
➦ 缺铁性贫血(IDA)
这是除胃肠道疾病外,与幽门螺杆菌关联最明确的疾病。其机制包括:
1)慢性胃炎或溃疡导致的胃黏膜微量出血,造成铁的慢性丢失;
2)细菌自身生长需要铁,与宿主竞争铁元素;
3)胃体萎缩导致胃酸分泌减少,影响膳食中三价铁向易于吸收的二价铁转化(JBiomed Sci, 2018)。
因此,对于不明原因的缺铁性贫血,临床指南推荐进行幽门螺杆菌检测和治疗。
➦ 维生素B12缺乏症
幽门螺杆菌感染,特别是导致胃体萎缩性胃炎时,会破坏分泌“内因子”的胃壁细胞。内因子是维生素B12在肠道吸收所必需的蛋白质,其缺乏将直接导致维生素B12吸收障碍,长期可引发巨幼细胞性贫血和神经系统损害(Frontiers in Microbiology,2022)。
➦ 特发性血小板减少性紫癜(ITP)
ITP是一种自身免疫性疾病,患者免疫系统产生抗体攻击自身的血小板。研究发现,部分ITP患者的血小板反应性抗体与幽门螺杆菌的某些成分(如CagA)存在交叉反应,即”分子模拟”。根除幽门螺杆菌后,约50%的ITP患者血小板计数能得到显著提升(Gastroenterol Res Pract, 2014)。
➦ 其他潜在关联
研究还提示幽门螺杆菌感染可能与多种疾病有关,如心血管疾病(动脉粥样硬化)、代谢综合征、皮肤病(如慢性荨麻疹)、神经系统疾病(如帕金森病)等。其机制可能涉及慢性炎症促进动脉斑块形成、影响脂质代谢或通过肠-脑轴影响神经系统。但这些关联的因果关系尚需更多高质量研究证实(World J Clin Cases, 2020)。
以上我们了解了幽门螺杆菌从胃溃疡、胃癌到缺铁性贫血、特发性血小板减少的全身性破坏力,但比认知疾病谱系更迫切的,是如何在临床症状爆发前精准锁定病原体,下一章节,我们来看一下各种检测方法,以及如何从被动确诊转向主动战略干预。
04如何捕获幽灵——幽门螺杆菌的检测与分型准确的检测是有效管理幽门螺杆菌感染的前提。了解何时需要检测、有哪些方法可选,以及各种方法的优缺点和适用场景,能帮助我们与医生共同做出最合适的决策。
哪些人应该考虑检测?
并非所有人都需要进行幽门螺杆菌检测。根据最新的国际和国内共识,以下人群是推荐进行检测的重点对象:
有消化道症状者
如消化不良(上腹痛、腹胀、早饱、嗳气)、反酸、烧心等。
特定疾病患者
所有消化性溃疡患者、胃MALT淋巴瘤患者。
胃癌高危人群
有胃癌家族史者、患有慢性萎缩性胃炎、肠上皮化生等胃癌前病变者。
计划长期服药者
计划长期服用非甾体抗炎药(NSAIDs,如阿司匹林、布洛芬)的患者,根除可降低溃疡出血风险。
特定胃外疾病患者
不明原因的缺铁性贫血、特发性血小板减少性紫癜(ITP) 患者。
个人意愿
在充分了解利弊后,有强烈检测和治疗意愿的个人。
检测方法大比拼
幽门螺杆菌的检测方法分为两大类:非侵入性检测和侵入性检测(需通过胃镜)。选择哪种方法取决于临床目的、成本效益和患者的具体情况。
非侵入性检测,顾名思义,无需胃镜,过程简便,接受度高。主要包括:
C13/C14呼气试验:这是目前临床上应用最广、最受推荐的“金标准”之一。它灵敏度和特异性均很高,适合初诊和根除治疗后的复查。患者只需吹两口气,即可判断是否存在现症感染。
粪便抗原检测:通过检测粪便中的幽门螺杆菌抗原,来判断是否存在现症感染。其准确性也较高,尤其适合儿童和不便进行呼气试验的人群。
血清学抗体检测:通过抽血检测血液中的幽门螺杆菌抗体。其优点是方便快捷,不受近期用药影响。但缺点是,它只能说明“曾经感染过”,无法区分是“现症感染”还是“既往感染”。因为即使细菌被根除,抗体仍可能在体内存在数月甚至数年。因此,它不适用于治疗后的复查。
将tNGS技术(靶向新一代测序)与肠道菌群检测技术结合,单次粪便检测实现突破。
谷禾肠道tNGS精准检测一次检测,全面解析
★ 超多重PCR+NGS技术
靶向扩增富集,高通量测序
★ 全面病原体覆盖
125种消化道病原体
细菌 | 病毒 | 真菌 | 寄生虫 覆盖传统16S无法检测的病原体
★ 精准耐药基因检测
1205个耐药基因/基因型
10种 毒力基因型
为临床精准用药提供科学依据
避免抗生素滥用,提高治疗效果
★ 超高灵敏度与特异性
灵敏度 95%| 特异性 99%
检测下限 50 copies/mL
使用定量内参,获取病原菌绝对定量
确保微量病原体也能被检出
★ 针对性特殊检测
幽门螺杆菌精准分型
Ure、CagA、VacA三种主要毒力基因
精确区分强毒性与弱毒性菌株
艰难梭菌毒力基因检测
新增 tcdA 和 tcdB 毒力基因检测
明确致病性,指导精准治疗
多靶点大肠杆菌分型
有效准确检出和区分不同类型感染
▼案例:谷禾tNGS检测报告在无症状人群中的预警价值刘先生平时身体硬朗,偶有饭后腹胀但并不留意,经过谷禾肠道菌群+tNGS检测,意外发现,幽门螺杆菌感染。

<来源:谷禾肠道菌群+tNGS检测报告>
于是刘先生前往医院检查,经过C14幽门螺杆菌测定:检测值达到1030,阳性++

谷禾报告毒力基因分析 → 治疗紧迫性判断
同时,谷禾肠道菌群+tNGS检查报告中还指出,他的幽门螺杆菌 VacAM、UreA均呈现阳性。
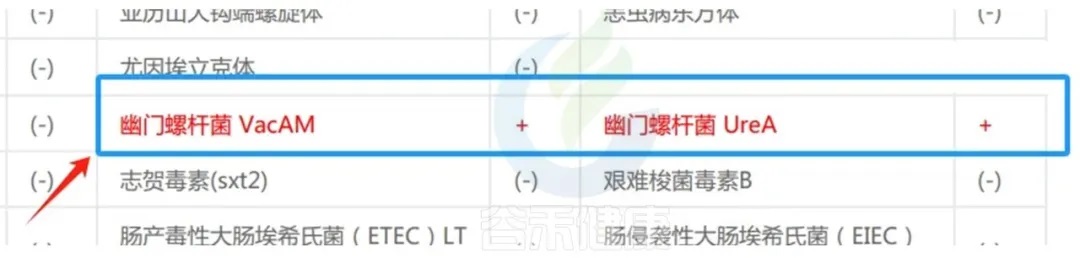
<来源:谷禾肠道菌群+tNGS检测报告>
这些字母究竟是什么意思呢?
有些小伙伴觉得看不懂。
是不是幽门螺杆菌检出来就要治疗呢?
......
别慌!谷禾检测报告中都有详细解释。
毒力基因标识,提示风险

<来源:谷禾肠道菌群+tNGS检测报告>
对于该患者而言,由于检出的幽门螺杆菌VacAM、UreA是强毒性感染,会致使组织炎症,易引发胃炎及溃疡病,因此建议进行根除治疗。
该案例突破症状限制,在胃黏膜不可逆损伤前,火速拦截感染进程。
具体根除治疗又有哪些策略?
tNGS报告在治疗中有哪些应用?
详细请看下一章节。
05驱逐幽灵之战——治疗策略与耐药挑战根除幽门螺杆菌是预防其相关远期并发症(尤其是胃癌)的最有效手段。然而,日益严峻的抗生素耐药问题,使得这场驱逐战变得复杂和充满挑战。
现代治疗原则:目标是根除而非缓解
治疗幽门螺杆菌的核心目标是彻底清除细菌,而非仅仅缓解胃部不适症状。一个成功的治疗方案,其根除率应达到90%以上。为实现这一目标,目前的治疗普遍采用多种药物联用的策略,以增强杀菌效果并降低耐药风险。
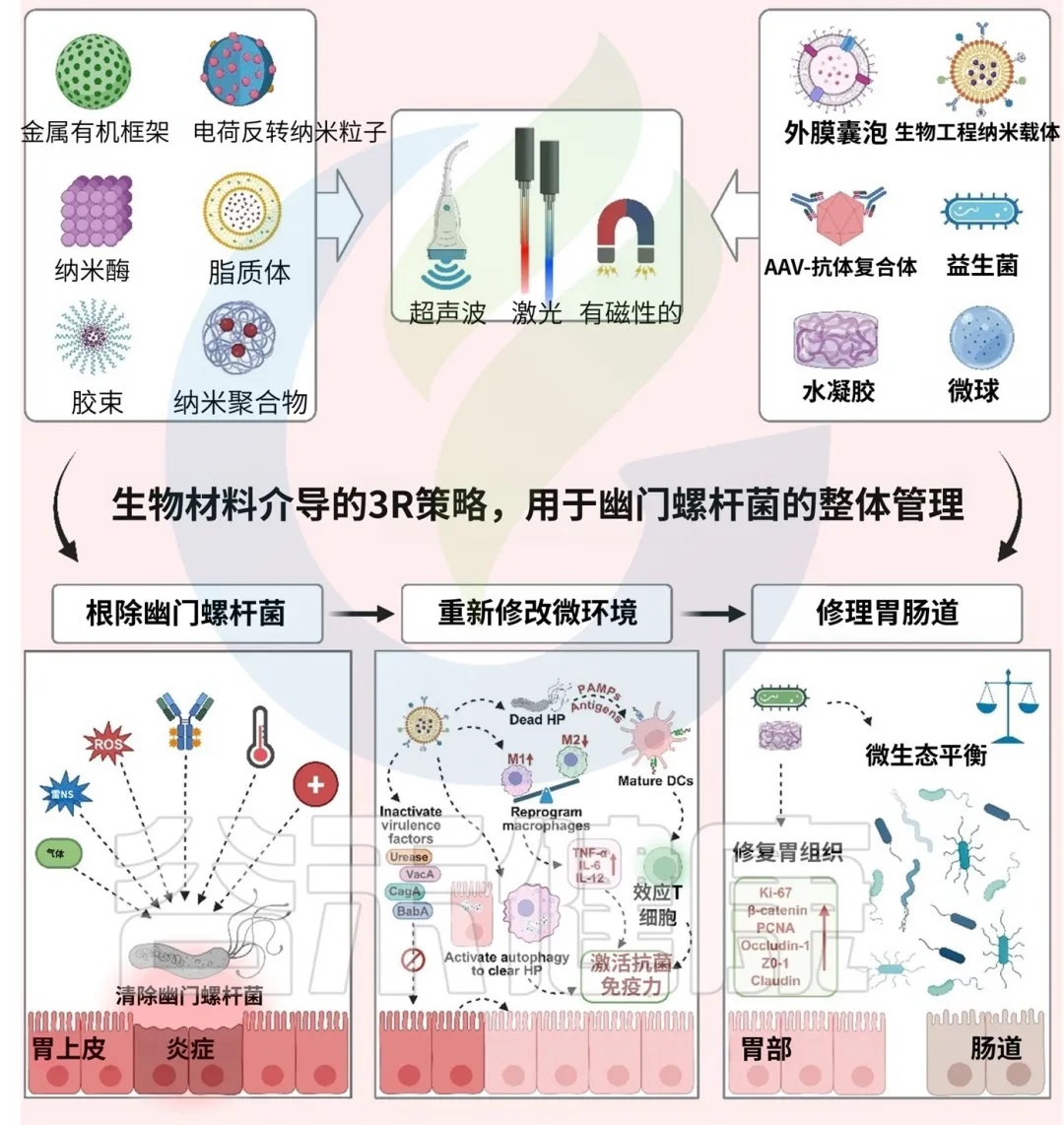
doi.org/10.1186/s12951-025-03455-2
一线治疗方案:告别传统,拥抱四联
由于克拉霉素在全球范围内的耐药率急剧攀升(许多地区已超过15-20%的警戒线),曾经广泛使用的“PPI+克拉霉素+阿莫西林/甲硝唑”三联疗法,在大多数地区已不再被推荐为经验性一线治疗。
根据美国胃肠病学会(ACG)2024年最新发布的临床指南,目前首选的一线治疗方案是:
含铋剂四联疗法(Bismuth Quadruple Therapy)
该方案由质子泵抑制剂 (PPI) +枸橼酸铋钾+两种抗生素组成,标准疗程为14天。常用的抗生素组合是甲硝唑和四环素。
铋剂不仅能保护胃黏膜,还具有直接的杀菌作用,且不易产生耐药,它的加入显著提高了对耐药菌株的根除率 (ACG Clinical Guideline, 2024)。
备选方案
在特定情况下,如对首选方案药物过敏或不耐受,医生可能会考虑其他方案,如包含利福布汀的三联疗法,或使用新型抑酸药物——钾离子竞争性酸阻滞剂(P-CAB,如伏诺拉生)的二联或三联疗法。
核心挑战:抗生素耐药
抗生素耐药是导致幽门螺杆菌根除失败的最主要原因,这是一个全球性的公共卫生危机。
严峻现状
除了克拉霉素,甲硝唑的耐药率在许多地区甚至更高,可达40%~90%。左氧氟沙星等二线药物的耐药率也在快速上升。这种多重耐药的趋势,使得经验性治疗(即不经药敏测试直接用药)的成功率大打折扣(Healio, 2022)。
耐药机制
幽门螺杆菌主要通过以下方式抵抗抗生素:
1
靶点基因突变
这是最主要的机制。
细菌的特定基因(如23S rRNA基因对应克拉霉素,gyrA基因对应左氧氟沙星)发生突变,导致抗生素无法与靶点结合,从而失效。
2
外排泵系统
细菌细胞膜上存在一些“泵”蛋白,能主动将进入菌体内的抗生素“泵”出,使其无法达到有效浓度。
3
生物膜形成
细菌可以聚集在一起,分泌多糖等物质形成一层保护性的生物膜。这层膜像一个堡垒,阻碍抗生素渗透,同时膜内的细菌代谢缓慢,对药物不敏感(Antibiotics (Basel), 2023)。
幽门螺杆菌主要抗生素耐药状况(示意)
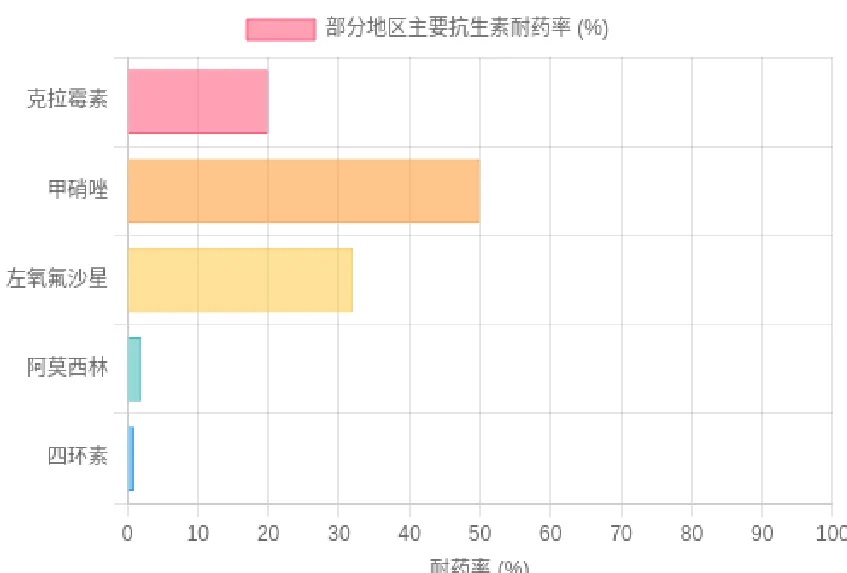
注:具体耐药率因地区差异巨大,数据仅为示意,临床需参考本地数据。
案例:谷禾tNGS检测报告在临床治疗中的应用在“多重耐药迷宫”中精准规划路线
前面提到的刘先生,去医院得到了检测结果,医生建议进行根除治疗,而谷禾tNGS报告中给出了详细的耐药基因突变,也就是说这些基因突变可能会使得某些抗生素治疗失效。

<来源:谷禾肠道菌群+tNGS检测报告>
谷禾报告耐药基因分析 → 个体化方案制定
➤ 幽门螺杆菌 PBP1 突变
如果在肠道样本中检测到幽门螺杆菌 PBP1 突变,提示可能存在对β内酰胺类抗生素(如阿莫西林)耐药的幽门螺杆菌,PBP1基因编码青霉素结合蛋白 1 (Penicillin-Binding Protein 1),是细菌细胞壁合成过程中的关键酶。 β-内酰胺类抗生素通过与 PBP1 结合发挥抗菌作用。 PBP1 基因突变可导致 β-内酰胺类抗生素结合能力下降,从而产生耐药性。
➤ 幽门螺杆菌 rdxA 突变
在肠道样本中检测到幽门螺杆菌 rdxA 突变提示可能存在对甲硝唑、呋喃唑酮耐药的幽门螺杆菌。 rdxA 基因编码硝基还原酶,该酶可将甲硝唑转化为具有细胞毒性的活性代谢物。 rdxA 基因突变可导致硝基还原酶活性下降,从而降低甲硝唑的杀菌效果。
优先选择受耐药影响较小的铋剂四联疗法(质子泵抑制剂 + 铋剂 + 四环素 + 阿莫西林)。
➤ 幽门螺杆菌 gyrA 突变
检测到幽门螺杆菌 gyrA 突变提示可能存在对喹诺酮类抗生素(如左氧氟沙星)耐药的幽门螺杆菌。 gyrA 基因编码 DNA 促旋酶亚基 A,该酶是细菌 DNA 复制过程中必需的酶。喹诺酮类抗生素通过抑制 DNA 促旋酶发挥抗菌作用。 gyrA 基因突变可导致喹诺酮类抗生素结合能力下降,从而产生耐药性。
左氧氟沙星通常不作为一线治疗方案使用,而是被视为重要的二线或三线“补救治疗”方案的组成部分。
➤ 23S rRNA突变
最近谷禾检测报告中更新了幽门螺杆菌的突变增加了23S rRNA突变,检出表明存在对克拉霉素耐药的幽门螺杆菌,克拉霉素就无法正常结合到细菌的核糖体上,从而导致细菌产生耐药性,使得包含克拉霉素的根除方案失效。
应对方案为选择不含克拉霉素的方案,例如:
铋剂四联疗法(质子泵抑制剂 + 铋剂 + 两种抗生素如甲硝唑和四环素),这是目前指南推荐的一线替代方案。
高剂量二联疗法(高剂量的质子泵抑制剂 + 高剂量的阿莫西林)。
伴同疗法或序贯疗法(使用多种抗生素组合,避开克拉霉素)。
临床价值核心
谷禾tNGS检测报告通过锁定耐药基因,杜绝抗生素滥用,指导精准替代方案(如避开阿莫西林改用四环素), 缩短疗程,降低治疗相关性腹泻风险,为临床精准用药提供科学依据,避免耐药危机升级。
探索新疗法
面对耐药挑战,科学界正在积极探索新的应对策略:
考虑新型药物
对于多重耐药的棘手病例,可以考虑使用利福布汀、呋喃唑酮等耐药率相对较低的药物,但这必须在经验丰富的医生指导下进行。
疫苗研发
开发有效的幽门螺杆菌疫苗是预防感染、从根本上解决问题的终极希望。目前已有多种候选疫苗(如口服重组疫苗)进入临床试验阶段,并显示出一定的保护效果,但距离上市应用仍有很长的路要走(Vaccine,2019)。
新型疗法探索
包括利用纳米材料靶向递送药物、光动力/声动力疗法、噬菌体疗法、以及利用AI设计新型抗菌肽等前沿研究,为对抗耐药菌株提供了新的思路(Frontiers in Immunology,2024)。
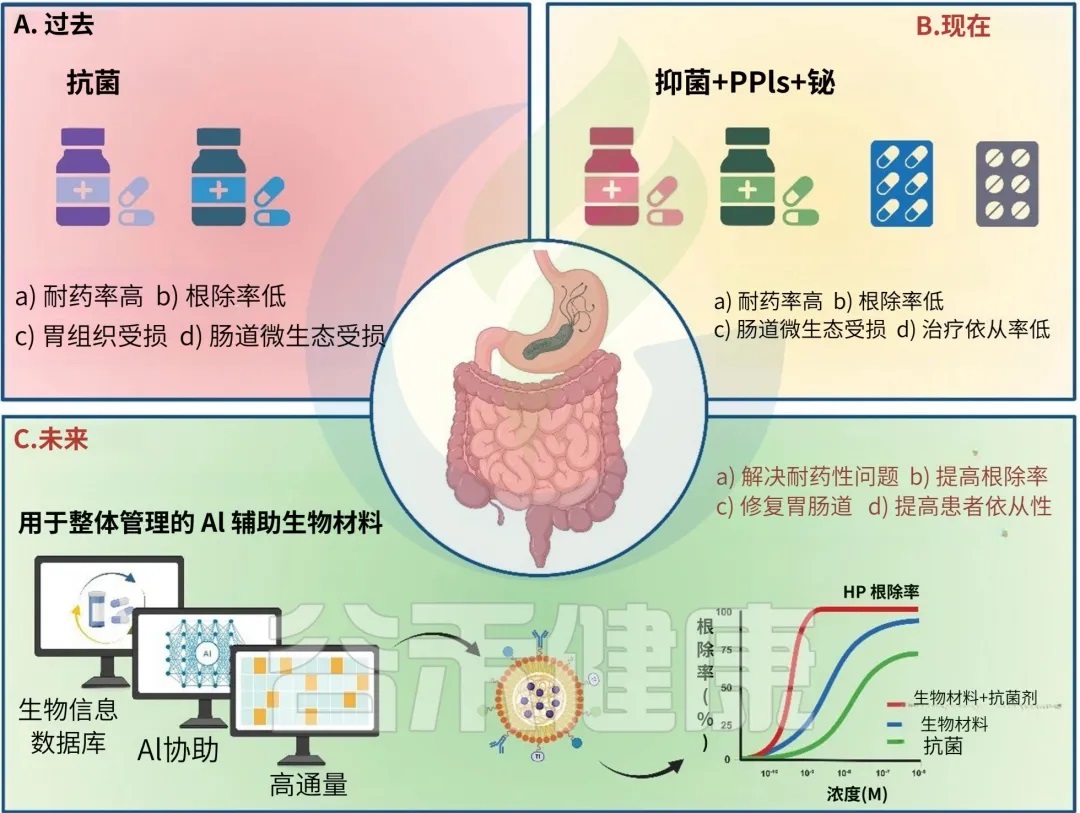
doi.org/10.1186/s12951-025-03455-2
对于普通人而言,了解如何预防感染和管理健康,比了解复杂的致病机制更为重要。下面章节,我们将提供一套具体、可操作的日常生活指南。
06防"幽"于未然——个人预防与健康管理终极指南切断传播途径是关键
幽门螺杆菌是传染性病菌,人是其唯一确认的传染源。了解其传播途径,是有效预防的第一步。
明确三大途径
1
口-口传播
这是最主要的途径。通过共用餐具、杯子,以及唾液接触(如亲吻、咀嚼食物喂养婴幼儿) 传播。
2
粪-口传播
感染者的粪便污染了水源或食物,健康人摄入后被感染。这在卫生条件较差的地区尤为常见。
3
胃-口传播
通过接触感染者的呕吐物传播,较为少见。
家庭内传播是重灾区
由于共同生活、饮食习惯密切,家庭成员之间的交叉感染极为普遍。研究显示,如果父母感染,其子女的感染风险会显著增高。因此,预防策略应以家庭为单位(湖南中医药大学第二附属医院)。
个人与家庭预防实用清单
以下措施能有效降低初次感染和再感染的风险:
【卫生习惯】
勤洗手:饭前、便后、处理食物前后,必须使用肥皂或洗手液,并用流动的清水彻底冲洗。
口腔卫生:坚持早晚刷牙,餐后漱口。定期更换牙刷(建议每3个月),牙杯分开使用并定期消毒。
【饮食习惯】
分餐制与公筷:无论是在家还是外出就餐,都应大力提倡和坚持使用公筷、公勺,这是预防口-口传播最有效的方法之一。
杜绝不良喂养习惯:坚决摒弃将食物嚼碎后喂给婴幼儿,或与孩子共用奶瓶、勺子等行为。
食品安全:不喝生水,不吃生的或未完全煮熟的食物。蔬菜水果在食用前应充分清洗干净。
餐具消毒:家庭餐具应定期消毒,最简单有效的方法是煮沸消毒,将餐具完全浸没在水中,煮沸15-30分钟。
饮食调理与营养支持
合理的饮食结构虽不能直接杀灭细菌,但能改善胃部环境,增强胃黏膜的抵抗力,辅助治疗并降低风险。
“助幽”食物黑名单:
高盐饮食:会直接损伤胃黏膜屏障,为细菌定植创造条件。
腌制、熏制食品:含有大量亚硝酸盐,可能在胃内转化为致癌物亚硝胺。
辛辣刺激食物:会刺激胃酸分泌,加重胃黏膜炎症。
“抑幽”食物推荐榜:
富含抗氧化剂的食物:新鲜蔬菜和水果(如蓝莓、草莓)富含维生素C、E等多酚类物质,有助于减轻炎症。
十字花科蔬菜:西兰花、卷心菜、花椰菜等富含的萝卜硫素,在体外实验中显示出对幽门螺杆菌的一定抑制作用。
富含Omega-3脂肪酸的食物:如深海鱼、亚麻籽油,有助于减轻全身炎症反应。
益生菌、益生元:酸奶、开菲尔等富含益生菌的食物,有助于维持肠道菌群平衡,部分研究表明可在一定程度上提高根除率并减轻抗生素带来的腹泻等副作用(UCF Health)。
根除治疗后的管理
成功根除并非一劳永逸,后续管理同样重要。
务必复查
在完成治疗后,停药至少4周,然后进行复查(首选C13/C14呼气试验),以确认细菌是否被彻底清除。
家庭成员筛查与治疗
为防止再感染,强烈建议与感染者共同生活的家庭成员(尤其是配偶和子女)也进行筛查。如果发现阳性,应在医生指导下同步治疗,以彻底清除家庭内部的传染源。
保持警惕,长期坚持
虽然成人根除成功后的年再感染率不高(约1.5%),但风险依然存在。长期坚持上述良好的个人和家庭卫生习惯,是防止“卷土重来”的根本保障 (Medicine(Baltimore),2021)。
07与“幽”共存的智慧——心理调适与社会认知除了生理上的影响,幽门螺杆菌阳性的诊断也可能给个体带来心理压力和社会交往的困扰。建立科学的认知,进行合理的心理调适,是全面健康管理不可或缺的一环。
告别"幽门焦虑症"
得知自己感染幽门螺杆菌后,许多人会产生焦虑、恐惧,甚至影响正常的社交活动。
以下几点认知有助于缓解这种“幽门焦虑”:
正视普遍性
要认识到全球有近半数人感染,这是一个非常普遍的现象,并非罕见病。您身边的大多数朋友、同事可能都是“战友”,无需因此感到孤立或自卑。
幽门螺杆菌感染是可以治愈的
通过规范的四联疗法,绝大多数患者都能成功根除。它不是一个会伴随终身、无法摆脱的烙印。
感染不等于一定会得胃癌
从感染到胃癌是一个漫长、多因素参与的过程,只有极少数(约1%)感染者会走到那一步。更重要的是,通过根除治疗,可以有效阻断这一进程,将风险降至最低。
心理与生理的相互影响
研究表明,长期的焦虑、抑郁等负面情绪会影响胃肠功能,削弱胃黏膜的防御屏障,可能增加感染的易感性或加重症状。反之,成功根除细菌后,许多患者的焦虑和抑郁情绪也得到了显著改善(世界华人消化杂志,2015)。因此,保持积极心态本身就是一种治疗。
纠正常见的社会认知误区
错误的认知会加剧不必要的恐慌和歧视。我们需要用科学事实来武装自己和影响身边的人。
✖ 误区1:一起吃顿饭就会被传染
✔ 纠正:
幽门螺杆菌的传染力相对较弱,需要长期、密切的共同生活接触,或卫生习惯不佳(如共用餐具)才容易发生传播。偶尔的聚餐,尤其是在使用公筷的情况下,感染风险极低。
✖ 误区2:根除后很快就会复发
✔ 纠正:
对于成年人,只要家庭内的传染源被清除(家庭成员同步治疗),并保持良好的卫生习惯,真正的“再感染”率很低(年再感染率约1.5%)。
许多所谓的“复发”其实是初次治疗并未彻底根除(假阴性) (山东大学齐鲁医院)。
✖ 误区3:使用杀幽牙膏或吃神药就能治好
✔ 纠正:
目前没有任何单一的食物、保健品或日用品被证实可以有效根除幽门螺杆菌。这些产品最多只能起到辅助或改善口腔环境的作用,不能替代由PPI、铋剂和两种敏感抗生素组成的规范四联疗法。
建立科学健康观:个体化决策与生活方式
最终,应对幽门螺杆菌的核心在于建立一种科学、理性的健康观念。
个体化决策
是否需要检测、何时检测、查出阳性后是否需要立即治疗,这些都不是一刀切的。应与专业医生充分沟通,结合自身年龄、症状、家族史、生活地区流行病学特点等因素综合判断。例如,对于无症状的年轻人,可以考虑观察;而对于有胃癌家族史或消化性溃疡的患者,则应积极治疗。
生活方式是基石
无论是否感染幽门螺杆菌,健康的生活方式 ——均衡的饮食、规律的作息、适度的运动、良好的心态,都是维护胃肠道健康、增强全身免疫力的根本。这不仅能降低感染风险,也能在感染后减轻症状,并为根除治疗创造更好的身体条件。
关键要点总结
面对幽门螺杆菌,无需过度恐慌。它普遍存在、可以治愈、风险可控。
关键在于破除认知误区,与医生合作进行个体化决策。将预防融入日常生活,通过分餐、勤洗手等习惯保护自己和家人。最终,掌控科学知识,采取理性行动,才是对自己健康最负责任的态度。
08结语掌控知识,成为自己健康的第一责任人
幽门螺杆菌,既是一个普遍存在的健康挑战,也是现代医学进步的一个缩影。从最初的未知与误解,到诺奖级的发现,再到如今面临的耐药困境与精准医疗的曙光,我们对它的认知在不断深化。
对它的恐惧往往源于未知,而掌控感则来自科学的认知。
本文为您提供了详尽的地图,旨在助您理解其核心逻辑,通过改善生活习惯切断传播,通过科学检测明确状态,通过规范治疗解决问题,通过理性认知管理风险。最重要的不是记住每一个复杂的医学术语,而是将这些知识转化为切实的行动。
您是自己健康的第一责任人。主动学习,与医生建立信任和良好的沟通,共同决策,积极、科学地管理您的胃肠健康,就能将幽门螺杆菌带来的风险降至最低,拥抱一个更健康、更安心的未来。
精准用药(耐药基因)、风险分层(毒力分型)、预防升级(传播链阻断)
谷禾tNGS检测技术正重新定义感染性疾病的防控边界,从幽门螺杆菌的耐药基因精准爆破,到艰难梭菌的毒力分型解构,更快发现问题,使临床决策效率提升,用药更精准,迈向精准胃肠健康的下一程。
谷禾肠道tNGS检测带您开启精准导航★ 适用人群精准匹配
适用于消化道感染或存在不明原因发热、呕吐、腹痛、腹泻、腹部压痛及反跳痛、腹肌紧张等人群。
★ 突破性应用场景
▸ 艰难梭菌毒力分型
传统检测仅报告阳性,而tNGS检测可针对之前艰难梭菌检出但无法确定是否为毒力菌株的情况,增加了艰难梭菌 tcdA 和tcdB 毒力基因的检测。
▸ 食物中毒、感染型大肠杆菌
对常见的食物中毒和感染型大肠杆菌的分型也加入了多个检测靶点,可有效准确检出和区分不同类型大肠杆菌感染。
包括例如,肠产毒性(ETEC)、肠侵袭性(EIEC)、肠集聚性等,知道是哪种类型的大肠杆菌,可以用药更精准,使抗生素误用率降低,病程缩短。
▸ 病原广谱性
对于肠道病毒、真菌感染、寄生虫感染等原单纯16S无法检测到的病原进行了全面覆盖,大大增强了病原体的广谱性。
主要参考来源:
Zhang, T., Zheng, Y., Chen, T. et al. Biomaterials mediated 3R (remove-remodel-repair) strategy: holistic management of Helicobacter pylori infection. J Nanobiotechnol 23, 475 (2025).
Chen YC, Malfertheiner P, Yu HT, Kuo CL, Chang YY, Meng FT, Wu YX, Hsiao JL, Chen MJ, Lin KP, Wu CY, Lin JT, O'Morain C, Megraud F, Lee WC, El-Omar EM, Wu MS, Liou JM. Global Prevalence of Helicobacter pylori Infection and Incidence of Gastric Cancer Between 1980 and 2022. Gastroenterology. 2024 Apr;166(4):605-619.
Burucoa C, Axon A. Epidemiology of Helicobacter pylori infection. Helicobacter. 2017 Sep;22 Suppl 1. doi: 10.1111/hel.12403. PMID: 28891138.
Baj J, Forma A, Sitarz M, Portincasa P, Garruti G, Krasowska D, Maciejewski R. Helicobacter pylori Virulence Factors-Mechanisms of Bacterial Pathogenicity in the Gastric Microenvironment. Cells. 2020 Dec 25;10(1):27.
Kao CY, Sheu BS, Wu JJ. Helicobacter pylori infection: An overview of bacterial virulence factors and pathogenesis. Biomed J. 2016 Feb;39(1):14-23.
Jones KR, Whitmire JM, Merrell DS. A Tale of Two Toxins: Helicobacter Pylori CagA and VacA Modulate Host Pathways that Impact Disease. Front Microbiol. 2010 Nov 23;1:115.
Asano N, Iijima K, Koike T, Imatani A, Shimosegawa T. Helicobacter pylori-negative gastric mucosa-associated lymphoid tissue lymphomas: A review. World J Gastroenterol. 2015 Jul 14;21(26):8014-20.
本文转自:谷禾健康
https://wap.sciencenet.cn/blog-2040048-1494409.html
上一篇:[转载]改善慢性代谢炎症和调节肠道稳态:茶作为一种潜在的疗法
下一篇:[转载]弓形菌属(Arcobacter)——一种新兴的食源性肠道病原菌