博文
BioTech 细胞永生化技术:探索分子机制和应用前景
||
文章导读
在生命科学领域,人类体细胞只能分裂有限次,这种现象被称为海弗利克极限 (Hayflick limit),一直是研究的重点和难点。这一现象由Leonard Hayflick和Paul Moorhead在20世纪60年代首次发现,其分子基础在于端粒的逐渐缩短。然而,某些细胞 (如胚胎干细胞和癌细胞) 却能够通过激活端粒酶或替代性端粒延长机制 (ALT) 突破这一限制,实现无限增殖。来自国际神经修复中心、古巴热带医学研究所等机构的科研团队在BioTech期刊发表了一篇综述文章,系统阐述了细胞永生化的分子机制及体外获取永生细胞的技术方法,为细胞生物学研究和药物筛选提供了重要工具。
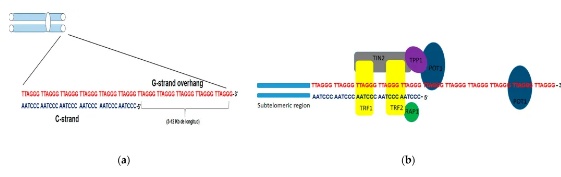
人类端粒的结构图
研究过程与方法
细胞永生化技术通过模拟癌细胞或干细胞的无限增殖能力,为科学研究提供了稳定的细胞模型。这一技术不仅能够避免频繁传代带来的繁琐操作,还能减少实验结果的批次差异,在药物开发、疾病模型构建和再生医学等领域具有广泛应用前景。然而,如何安全、高效地实现细胞永生化仍是科研人员面临的重大挑战。
关键发现与创新
1. 端粒与端粒酶的作用
端粒是位于染色体末端的核蛋白复合体,其长度随细胞分裂逐渐缩短,最终触发细胞衰老或凋亡。端粒酶是一种能够延长端粒的逆转录酶,由TERT (催化亚基) 和TERC (RNA模板) 组成。研究表明,约90%的癌细胞通过激活端粒酶维持端粒长度,从而获得永生能力。此外,端粒酶表达还受TERT启动子突变 (TPM) 的调控,这些突变在多种癌症中普遍存在,并与不良预后相关。
2. 选择性端粒延长 (ALT) 机制
约10%-15%的癌细胞通过ALT机制维持端粒长度,这一途径依赖于同源重组 (HR) 和断裂诱导复制 (BIR)。ALT细胞表现出端粒长度高度异质性、PML核体 (APBs) 的形成以及染色体姐妹交换 (T-SCE) 频率增加等特点。研究还发现,ALT机制在间叶组织来源的肿瘤 (如骨肉瘤和软组织肉瘤) 中更为常见。
3. 体外永生化技术
为实现细胞永生化,研究人员开发了多种技术:
病毒癌基因:如SV40 T抗原和HPV的E6/E7蛋白,通过抑制p53和Rb等抑癌基因激活端粒酶。
Myc基因家族:c-Myc等基因的过表达可促进细胞增殖,但其潜在的致瘤性需通过条件性调控 (如Tet-on系统) 加以控制。
端粒酶催化亚基 (hTERT):直接引入hTERT可延长细胞寿命,但某些细胞类型需联合其他基因修饰才能实现永生化。
CRISPR/Cas9基因编辑:新兴技术通过模拟肿瘤相关基因突变实现永生化,具有广阔的应用潜力。
研究总结
细胞永生化技术是一种极具价值的工具,能够帮助研究者获得具有无限增殖潜能的细胞系——只要提供适宜的生长条件和营养支持。通过这一技术,细胞可以突破海弗里克极限 (Hayflick limit),规避复制性衰老及相关凋亡过程。对体内这一现象 (癌细胞的重要特征之一) 分子机制的深入认知,使得体外应用该技术成为可能。目前,科学家已能通过调控病毒癌基因/癌蛋白、端粒酶TERT组分以及细胞周期相关基因的表达,实现条件性永生化。新兴分子技术开发的条件性永生化治疗性细胞系,将为细胞治疗带来潜在治愈或再生效果。此外,永生化细胞系的使用还规避了某些干细胞类型涉及的伦理问题。
虽然永生化细胞系为肿瘤发生机制研究和药物筛选提供了重要工具,但其临床应用仍存在显著限制:永生化过程可能引发基因组不稳定或导致肿瘤表型产生。而通过分子开关系统实现的条件性永生化技术,可在细胞移植前永久沉默永生化基因,从而有效解决这一问题。
阅读英文原文:https://www.mdpi.com/2098940
期刊主页:https://www.mdpi.com/journal/biotech
BioTech 期刊介绍
主编:Massimo Negrini, University of Ferrara, Italy
期刊涵盖生物技术各个领域的实验和理论结果,包括生物制药;开发转基因植物、动物或水生生物,以解决农业食品的生产或质量问题,以及医学上的新方法;在环境部门的应用,旨在维持生物多样性和清除污染物;开发生物体或酶以生产有用化学品或销毁危险/污染化学品;生物信息学方法。
2023 Impact Factor:2.7
2023 CiteScore:3.7
Time to First Decision:26.1 Days
Acceptance to Publication:2.6 Days


https://wap.sciencenet.cn/blog-3516770-1486471.html
上一篇:Polymers:山东大学王灯旭教授合作创建特刊——多孔聚合物材料
下一篇:Land 城市复兴的绿色密码:生态系统服务与景观修复如何逆转土壤消耗