博文
Biology 香港中文大学医学院:氟化NAD前体通过激活SARM1增强FK866对胶质母细胞瘤细胞的毒性
||
胶质母细胞瘤 (Glioblastoma) 是一种高度侵袭性的脑肿瘤,治疗难度极大,患者预后较差。近年来,针对NAD (烟酰胺腺嘌呤二核苷酸) 代谢的调控成为癌症治疗的新策略。NAD是细胞能量代谢的核心分子,其异常代谢与肿瘤细胞的快速增殖和生存密切相关。NAMPT (烟酰胺磷酸核糖转移酶) 抑制剂FK866通过消耗NAD抑制肿瘤生长,但其单药治疗效果有限。
近期,一项发表在 Biology 期刊上的研究提出了一种创新方法:通过氟化NAD前体 (F-NR) 与FK866联合使用,显著增强其对胶质母细胞瘤细胞的杀伤效果。
F-NR的双重作用机制
抑制NRK途径:F-NR通过竞争性抑制NRK (烟酰胺核糖激酶),阻断NAD的合成。
激活SARM1:F-NR在细胞内被代谢为F-NMN,后者激活NAD消耗酶SARM1,进一步加剧NAD的耗竭。
协同效应
F-NR与FK866联合使用时,能够更彻底地耗尽细胞内的NAD和ATP,导致肿瘤细胞死亡。
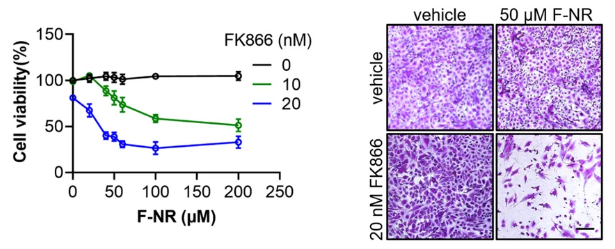
图1为F-NR和FK866抑制胶质母细胞瘤细胞生长的协同作用。
代谢分析
通过代谢组学研究发现,F-NR不仅影响NAD代谢,还干扰了其他关键代谢途径,如脂质代谢和能量供应。
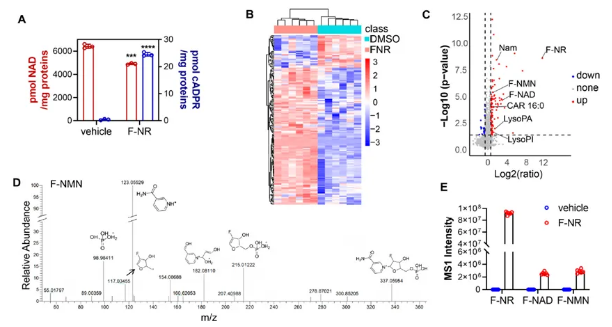
图2为F-NR对胶质母细胞瘤代谢的影响。
研究意义与启发
这项研究不仅揭示了F-NR和FK866协同作用的分子机制,还为胶质母细胞瘤的治疗提供了新的思路:
靶向NAD代谢的联合疗法:通过同时抑制NAD合成 (FK866) 和激活NAD消耗 (F-NR/SARM1),可以更有效地杀死肿瘤细胞。
SARM1的潜在治疗价值:SARM1作为NAD代谢的关键调控因子,可能成为未来癌症治疗的新靶点。
新型化合物的开发:F-NR的合成相对简单,且具有较高的细胞渗透性,为开发更高效的NAD代谢调节剂奠定了基础。
值得注意的是,该研究提示,基于碱基交换反应的SARM1的小分子调节剂——吡啶碱基衍生物 (例如碘代异喹啉、vacor、G10等),以及其他核苷类化合物 (如本文的F-NR),能够进入NAD代谢网络,影响范围广泛,不仅限于SARM1,需要。这一发现为设计更广泛的代谢干预策略提供了重要启示。
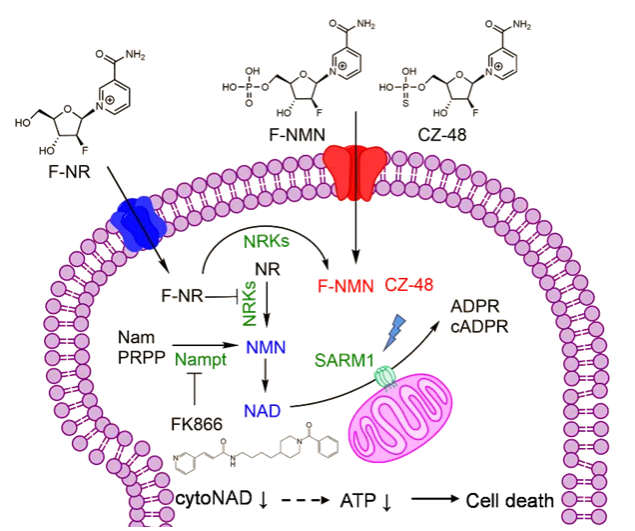
图3为NAD合成前体对细胞代谢和生存的影响模式图。
未来展望
未来研究将进一步探索F-NR在动物模型中的效果,并优化其与现有疗法的联合应用。这项研究为胶质母细胞瘤的治疗开辟了新的方向,也为其他依赖NAD代谢的癌症提供了潜在的治疗策略。
原文出自 Biology 期刊:https://www.mdpi.com/2924810
期刊主页:https://www.mdpi.com/journal/biology
Biology 期刊介绍
主编:Jukka Finne, University of Helsinki, Finland;Andrés Moya, University of Valencia and CSIC, Spain
期刊主要涵盖细胞生物学、发育生物学、进化生物学、生物化学与分子生物学、微生物学等所有生物领域。期刊被Scopus, SCIE (Web of Science), PubMed 等重要数据库收录。
2023 Impact Factor:3.6
2023 CiteScore:5.7
Time to First Decision:16.4 Days
Acceptance to Publication:2.5 Days


https://wap.sciencenet.cn/blog-3516770-1486614.html
上一篇:Inorganics 华东理工大学李大伟教授和陈斌斌博士团队——室温下席夫碱反应驱动碳点的大规模合成
下一篇:Nanomaterials:中国科学院宁波材料技术与工程研究所杨其浩副研究员等创建特刊——可持续二氧化碳捕集与催化转化