博文
主动脉注射氢气生理盐水给氢气可行性概念验证
||
主动脉注射氢气生理盐水给氢气可行性概念验证
摘要
背景:复苏性主动脉内球囊阻断术(REBOA)用于躯干失血性休克,已成为确定性止血前的过渡手段,应用日益广泛。氢分子可随血流分布并减轻缺血损伤,但在REBOA应用期间无法到达缺血器官。本研究旨在探讨在失血性休克家猪模型中,REBOA下经主动脉内灌注富氢生理盐水能否将氢气输送至肠道。
方法:对40 kg雌性家猪建立容量控制性失血性休克模型,随后通过置于REBOA球囊远端的主动脉内导管灌注富氢生理盐水。在四种模型中测定门静脉氢气浓度:
1. 控制性失血性休克+REBOA完全阻断+标准阻断时间;
2. 合并肝损伤的非控制性失血性休克+REBOA完全阻断+延长阻断时间;
3. 合并肝损伤的非控制性失血性休克+REBOA部分阻断+延长阻断时间;
4. 对照组:控制性失血性休克+REBOA完全阻断+标准阻断时间+灌注不含氢的生理盐水。
结果:
- 模型1(完全阻断):门静脉氢气浓度 0.224 mg/L(13.998%)
- 模型2(肝损伤+完全阻断):0.049 mg/L(3.063%)
- 模型3(肝损伤+部分阻断):0.018 mg/L(1.125%)
- 对照组:0.002 mg/L(0.015%)
结果显示,不同REBOA应用方式下门静脉均可检测到氢气。
结论:门静脉氢气浓度升高提示氢气成功输送至肠道,为REBOA期间的药物输注提供了新思路。但该方法的临床应用仍需进一步研究。
1 引言
失血性休克是患者早期死亡的重要原因[1]。近年来,复苏性主动脉内球囊阻断术(REBOA)用于躯干失血性休克,作为确定性止血的过渡治疗手段,应用日趋普遍。REBOA可临时控制出血、维持脑与冠状动脉血流[2-4]。该操作较主动脉夹闭简便,有望用于主动脉瘤破裂、消化道出血、产后出血等多种疾病(含非创伤性疾病)[5-7]。
然而REBOA存在明显缺陷:为维持心脑灌注,会阻断肠道等远端脏器血流[7],存在缺血损伤风险,因此主动脉阻断时间受限[8]。部分阻断、间断放气等策略被用于减轻缺血损伤[9],但技术复杂、缺乏统一方案。此外,即便优化球囊管理以保留远端灌注,仍需辅助手段在主动脉阻断期间向缺血脏器给药,减轻缺血再灌注损伤[9-11]。
氢气(H₂)作为选择性抗氧化与细胞保护剂,已被广泛用于缺血再灌注损伤与炎症的研究。大量基础与临床研究探索了多种给药途径:吸入、静脉/肠道给予富氢液、纳米载体、富氢器官灌注液等,涉及心、脑、肾、肝、肠等器官[12-22]。但多数氢气递送依赖完整的全身或内脏灌注,在主动脉完全阻断时能否足量到达远端脏器尚不明确;近期实验提示,REBOA后吸入氢气难以有效减轻相关缺血再灌注损伤[19]。
为克服主动脉阻断造成的给药障碍,本研究探索在REBOA期间,通过向球囊远端主动脉灌注富氢生理盐水,能否将氢气输送至远端内脏循环。本概念验证研究以家猪为对象,在临床相关的REBOA场景下定量检测门静脉氢气浓度,评估该远端主动脉给药方式的可行性与药代动力学可检测性。本研究未评估治疗效果与组织保护作用。
2 材料与方法
2.1 研究概况
本研究经庆应义塾大学研究所伦理委员会与动物护理使用委员会批准(20005-(2))。选用4只雌性家猪(39–42 kg),单笼饲养于温控、光控环境(20 °C,12 h明暗循环)。实验动物经专门培育、驯化、疫苗接种,无常见家猪疾病,实验前自由摄食饮水。研究遵循ARRIVE指南。
2.2 研究设计
本研究为概念验证研究,采用转化型家猪模型,探讨REBOA期间药物递送的可行性。目的为证实具有抗缺血作用的氢气能否在REBOA期间到达肠道。通过检测不同失血性休克模型(合并/不合并实质脏器损伤)中门静脉氢气浓度,判断经主动脉灌注富氢生理盐水能否将氢气输送至肠道。
2.3 动物准备
动物术前肌肉注射咪达唑仑(0.2 mg/kg)、美托咪定(20 μg/kg)、布托啡诺(0.2 mg/kg)。异氟烷诱导麻醉并气管插管,以2%异氟烷维持麻醉。容量控制机械通气(FiO₂ 21%,潮气量10–15 mL/kg,呼吸频率15–20 次/min),使用37 °C加温毯保温。暴露右颈总动脉与双侧股动脉,建立动脉通路用于采血与血流动力学监测。
经右颈总动脉置入5 F鞘管测量近端主动脉压,经左股动脉逆行置入5 F鞘管测量远端主动脉压。开腹后经胰腺静脉将中心静脉导管置入门静脉采血(图1)。
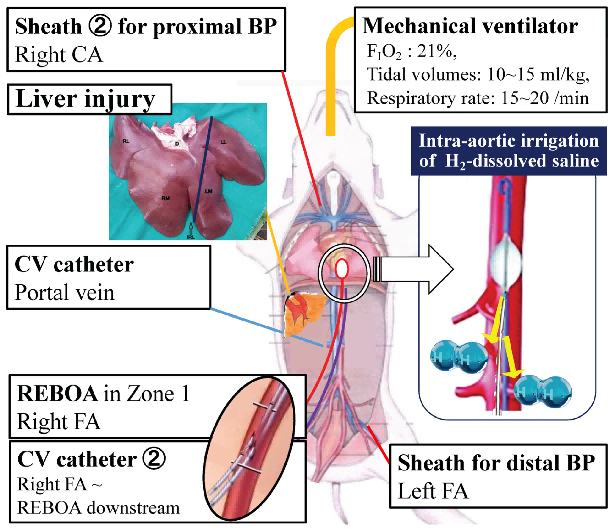
图1 实验装置示意图。Ⅰ区REBOA球囊远端放置主动脉内导管用于灌注富氢生理盐水,经中心静脉导管注入REBOA阻断远端主动脉。实验所用富氢生理盐水浓度为2.2 mg/L。
BP:血压;CA:颈动脉;CV:中心静脉;FA:股动脉;REBOA:复苏性主动脉内球囊阻断术。
2.4 REBOA置入与氢气给药途径
经右股动脉逆行置入7 F REBOA导管,球囊定位于Ⅰ区(左锁骨下动脉至腹腔干之间),置入前通过体表测量、实验结束后通过触诊确认位置。另将12 G双腔中心静脉导管与REBOA一同经右股动脉逆行置入,导管尖端位于REBOA球囊远端,经该管输注富氢生理盐水(图1)。
2.5 富氢生理盐水制备
富氢生理盐水按既往方法制备[17]。储氢合金罐内含可逆吸放氢的储氢合金,罐内压力不超过1 MPa,不属于日本高压气体安全法定义的高压气体。使用前组装氢气输送装置,通过调压阀将氢气注入生理盐水。表压达0.06 MPa时断开生理盐水袋,剧烈手动振荡30 s,冰浴并开放至大气。本实验制备浓度为2.2 mg/L,高于室温常压下氢气在水中的饱和浓度1.6 mg/L。
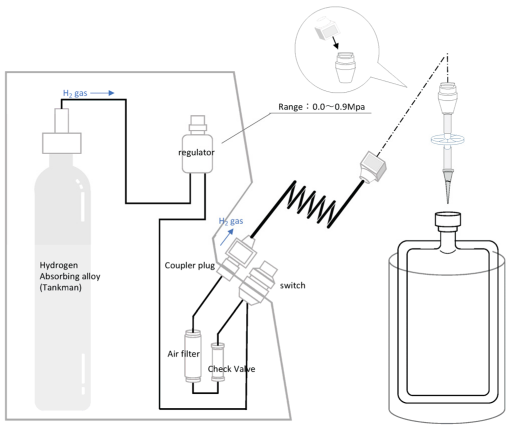
图2 氢气制备装置结构。氢气制备系统中储氢合金释放的氢气经调压阀调至目标压力,注入生理盐水袋。
2.6 实验模型
结合临床与基础研究中REBOA应用场景,建立四种模型:控制性/非控制性失血性休克、标准(60 min)/延长(90 min)阻断时间、合并/不合并实质脏器损伤、完全/部分阻断。肠道菌群可自然产生氢气并吸收入门静脉,因此在未灌注富氢生理盐水的模型中评估门静脉基础氢浓度。每组n=1,分别评估氢气递送可行性。
模型1:控制性失血性休克+REBOA完全阻断+标准时间(60 min)
15 min内按体重抽取20%总血量,建立控制性失血性休克模型[10]。休克诱导后立即充盈REBOA球囊60 min。以左下肢远端脉搏消失、颈动脉平均动脉压升高确认阻断成功。REBOA充盈期间经球囊远端导管输注富氢生理盐水。灌注60 min后氯化钾静脉注射安乐死。
模型2:合并肝损伤的非控制性失血性休克+REBOA完全阻断+延长时间(90 min)
15 min控制性失血后,用大剪刀在Ⅳ段与左外侧肝静脉汇合处远端切断肝实质,建立标准化重度肝损伤模型[10]。切除肝段后快速关腹,立即充盈REBOA球囊90 min并输注富氢生理盐水。90 min后安乐死。
模型3:合并肝损伤的非控制性失血性休克+REBOA部分阻断+延长时间(90 min)
15 min控制性失血后建立重度肝损伤模型,关腹。先完全充盈REBOA球囊10 min以形成血栓稳定循环[9],随后适度放气至远端主动脉波形恢复,实验期间调整充盈程度,维持合适的近远端血压并确保右下肢远端脉搏存在[9]。全程输注富氢生理盐水,90 min后安乐死。
模型4(对照):控制性失血性休克+REBOA完全阻断+灌注生理盐水+标准时间(60 min)
15 min控制性失血后完全充盈REBOA球囊60 min,阻断成功标准同上。期间输注不含氢的生理盐水,60 min后安乐死。
2.7 数据采集
全程连续监测并记录近端颈动脉压、远端股动脉压、心率。于基线及每15 min从门静脉采血检测氢气浓度。
2.8 氢气浓度检测
取1 mL血液注入密封13.5 mL瓶内,立即用蜡密封防止气体逸出。血液中氢气释放至瓶内气相。瓶内初始空气几乎不含氢气(0.5 ppm v/v),因此氢气主要由液相转移至气相。采集瓶内空气(0.2/0.4/1.0 mL),用TRIlyzer mBA-3000气相色谱仪检测氢气浓度。以0、5、50、130 ppm标准氢气建立校准曲线,每份样本检测2次。同时采集环境空气作为空白对照,不含氢的生理盐水作为阴性对照(0.0001 ppm w/w)。样本最终浓度扣除环境空气本底值。
2.9 给药速率
REBOA完全阻断时远端主动脉血流显著减少或消失,需依靠输注实现药物递送。本研究为可行性与药代动力学概念验证,而非剂量优化,故采用基于设备能力与生理合理性的给药策略。
- 完全阻断模型:1.5–2.0 L/h(0.025–0.033 L/min),使用设备最大流速2.0 L/h以确保无血流条件下可检测到药物递送。
- 部分阻断模型:保留部分远端血流,流速降至0.1 L/h,接近临床可行辅助给药速率。
参考既往家猪肠道给氢气的药代动力学数据,以门静脉浓度0.016 mg/L(约1%饱和度)作为参考阈值[20]。
3 结果
3.1 模型1:控制性失血性休克+REBOA完全阻断60 min
3.1.1 血流动力学
放血诱导休克后,颈动脉与股动脉平均动脉压降至约40 mmHg。REBOA首次完全充盈后,颈动脉压立即升高,股动脉脉搏消失,提示阻断成功。实验期间颈动脉平均动脉压维持在约130 mmHg,表明REBOA完全阻断用于失血性休克有效。
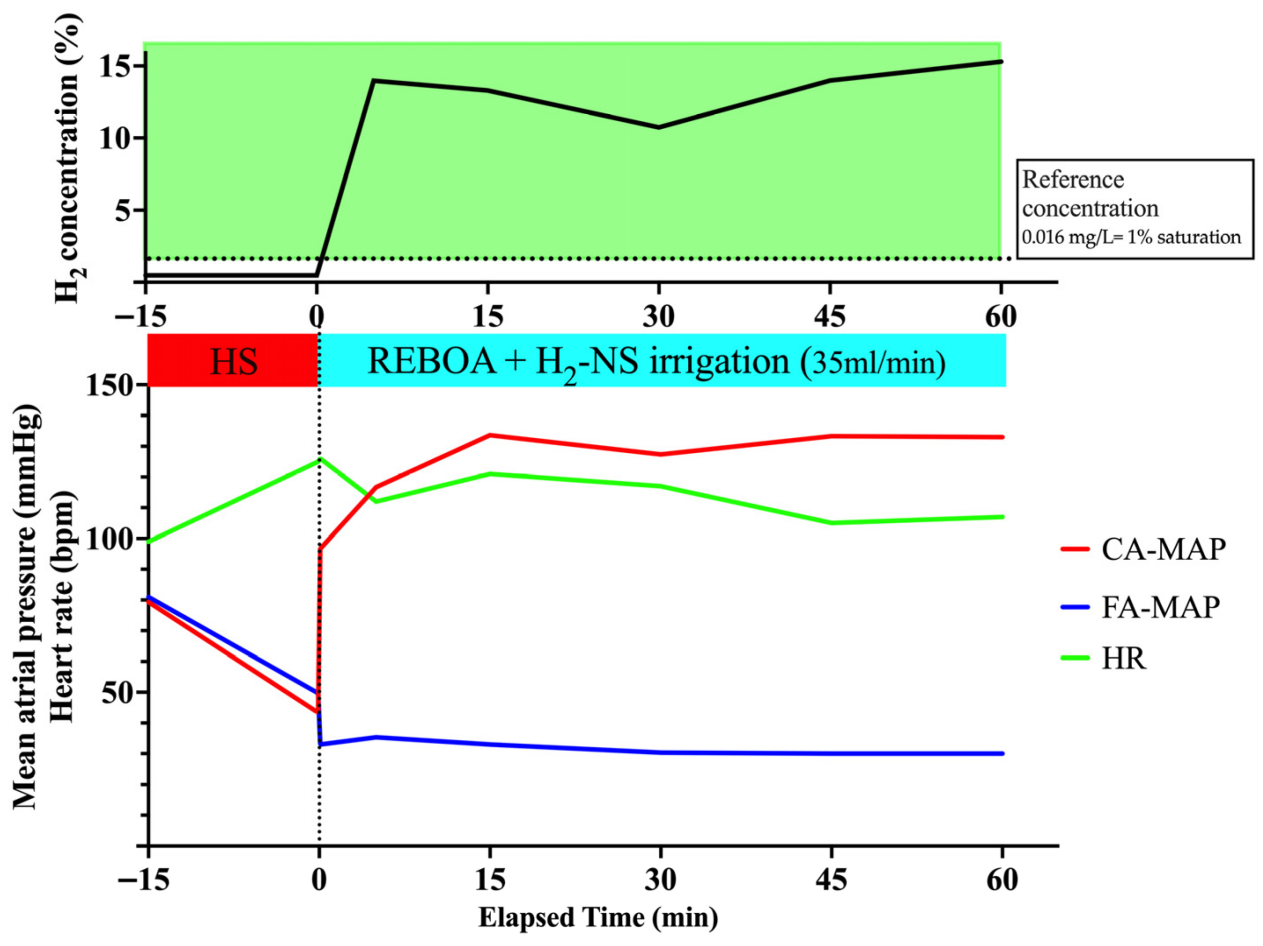
图3 无肝损伤、标准时间完全阻断、控制性失血性休克模型的血流动力学与氢气浓度变化(n=1)。水平虚线为参考浓度(0.016 mg/L;约1%饱和度)。
3.1.2 门静脉氢气浓度
灌注富氢生理盐水后,门静脉氢气浓度迅速升高,5 min达峰值0.224 mg/L(13.998%),并在实验期间维持。结果表明,完全REBOA期间远端灌注可使门静脉氢气浓度高于参考阈值,支持完全阻断下远端给药可行。
表1 门静脉氢气浓度变化

3.2 模型2:合并肝损伤的非控制性失血性休克+REBOA完全阻断90 min
3.2.1 血流动力学
放血+肝切除后,颈动脉与股动脉平均动脉压降至约40 mmHg。REBOA完全充盈后颈动脉压升高、股动脉脉搏消失。延长阻断90 min期间,颈动脉压仍维持升高,提示REBOA应用成功。实验结束时腹腔出血量580 mL。
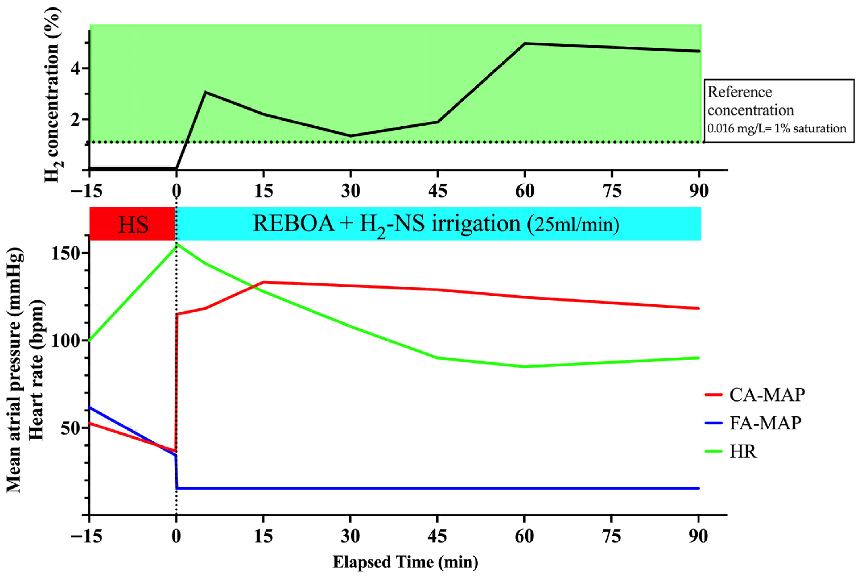
图4 合并肝损伤、延长时间完全阻断、非控制性失血性休克模型的血流动力学与氢气浓度变化(n=1)。
3.2.2 门静脉氢气浓度
门静脉氢气浓度迅速升高,峰值0.049 mg/L(3.063%)。提示即使在合并肝损伤的非控制性失血性休克中,延长时间完全REBOA期间远端灌注仍可使门静脉氢气浓度高于参考阈值。
3.3 模型3:合并肝损伤的非控制性失血性休克+REBOA部分阻断90 min
3.3.1 血流动力学
放血+肝切除后平均动脉压降至约40 mmHg。REBOA完全充盈10 min后转为部分阻断,颈动脉压下降但维持约40 mmHg,股动脉压升高约20 mmHg,提示部分阻断成功。实验结束时腹腔出血量800 mL。
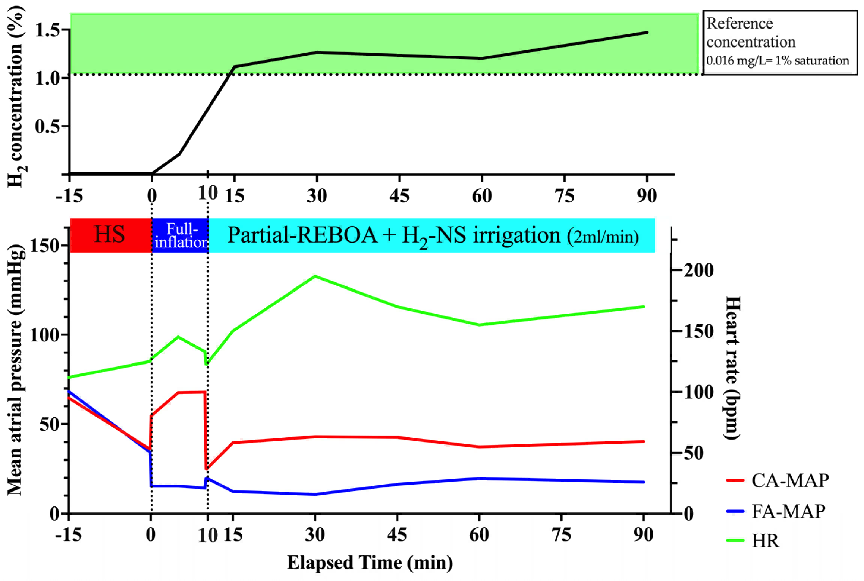
图5 合并肝损伤、延长时间部分阻断、非控制性失血性休克模型的血流动力学与氢气浓度变化(n=1)。
3.3.2 门静脉氢气浓度
初期完全阻断期间灌注速率较慢,氢气浓度早期升高不明显;转为部分阻断后,门静脉氢气浓度升至0.0178 mg/L(1.125%)并维持。表明在合并肝损伤的非控制性失血性休克、REBOA部分阻断时,远端灌注可使门静脉氢气浓度接近参考阈值。
3.4 模型4(对照):控制性失血性休克+REBOA完全阻断+灌注生理盐水60 min
3.4.1 血流动力学
放血后平均动脉压降至约50 mmHg。REBOA完全充盈后颈动脉压升高、股动脉脉搏消失,阻断成功。实验期间颈动脉压维持在约160 mmHg。
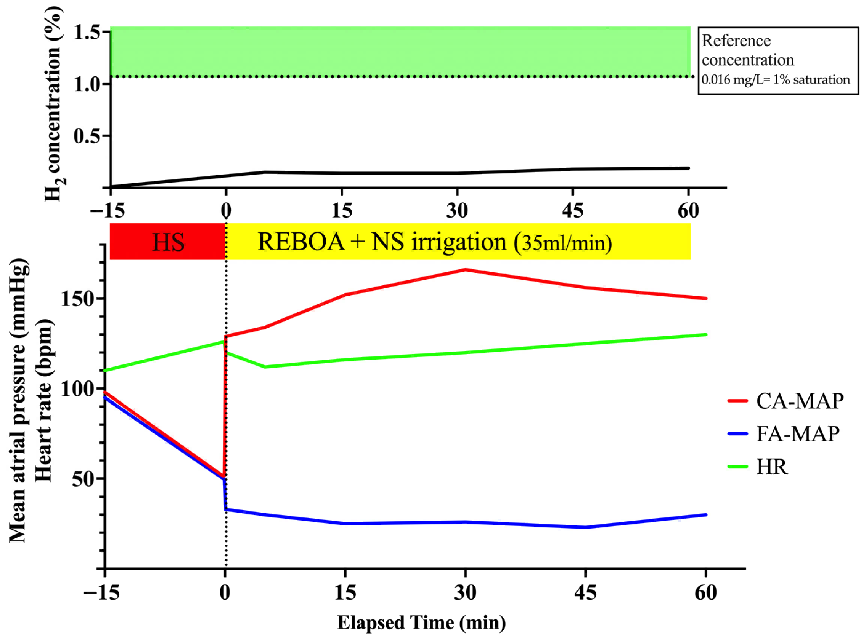
图6 灌注生理盐水、标准时间完全阻断、控制性失血性休克模型的血流动力学与氢气浓度变化(n=1)。
3.4.2 门静脉氢气浓度
因灌注不含氢的生理盐水,门静脉氢气浓度持续低位(≤0.003 mg/L;≤0.188%),远低于参考阈值。该低浓度信号来自肠道菌群自然产生并吸收入门静脉的基础氢气。
4 讨论
本研究证实,REBOA期间经远端主动脉灌注富氢生理盐水,可在家猪门静脉内检测到氢气,提示氢气成功输送至失血性休克家猪的肠道,完成概念验证目标。该结果可为REBOA期间建立新给药途径提供依据,有望向REBOA相关缺血损伤高发的肠道、肝脏递送抗缺血药物。
完全阻断时REBOA远端主动脉无血流,需较高流速才能将富氢生理盐水输送至远端器官。本研究为技术可行性验证,而非剂量探索或药效学研究,故采用阶梯式流速设计:先使用设备最大流速(2.0 L/h)以最大化检出信号;确认可检测后,在肝损伤完全阻断模型中降低流速以减少输注量;在部分阻断模型中进一步降至0.1 L/h,探索低输注量下的可行性。上述流速仅用于信号检测与可行性验证,不代表最优或临床推荐剂量。
肠道菌群可自然产生氢气,但对照组门静脉基础浓度极低,提示本研究的给药系统可有效将氢气递送至肠道。本研究未开展组织学损伤评估,疗效仍需进一步验证。作为概念验证研究,结果可为REBOA远端药物灌注的适宜给药速率提供参考。
本团队既往研究显示,吸入氢气可减轻缺血损伤、延缓重度出血向不可逆休克进展[15]。但吸入的氢气经血流分布,在REBOA阻断血流时无法在缺血脏器发挥作用[19]。Ichihara等报道口服富氢生理盐水可升高门静脉氢气浓度[20],但失血性休克时口服给药困难且难以持续。氢气无需代谢即可发挥作用,可直接经主动脉给药,因此本递送方式可在血流动力学不稳定阶段向缺血脏器输送氢气,无代谢相关顾虑。
本研究存在局限性:
1. 为REBOA期间经主动脉内向内脏(肠道)给药的概念验证,未评估疗效与最优给药速率;家猪最低有效浓度尚不明确,仅参考人与其他动物数据(0.016 mg/L,1%)[20]。
2. 采用现有导管与REBOA联用,临床需开发球囊远端带给药端口的二合一REBOA装置;器械尺寸增加可能减少肾、下肢等远端器官血流。
3. 大剂量主动脉内给药存在空气栓塞、血液稀释、腹腔间隔室综合征、插管侧下肢灌注改变等风险,临床前需评估并发症并建立安全机制。
4. 样本量小,为多模型探索性设计,给药速率选择依据不足,完全阻断时的高流速难以直接用于临床,需扩大样本验证临床适用流速与安全性。
5. 仅关注肠道给药,未评估肝、肾、下肢等其他缺血器官的药物递送,需进一步实验验证。
5 结论
本概念验证研究显示,在多种REBOA场景下,经远端主动脉灌注富氢生理盐水后,家猪门静脉均可检测到氢气,浓度升高提示氢气成功递送至肠道。本研究未评估该递送方式的生理获益,其临床应用价值仍需深入研究。
https://wap.sciencenet.cn/blog-41174-1523079.html
上一篇:巨型病毒劫持宿主蛋白质合成工厂
下一篇:衰老导致脑漏,运动可加固血脑屏障《细胞》