博文
分子动力学研究揭示本体氢纳米气泡在水和甲醇中的稳定性
||
分子动力学研究揭示本体氢纳米气泡在水和甲醇中的稳定性
Molecular Dynamics Insights into the Stability of Bulk Hydrogen Nanobubbles in Water and Methanol
摘要 本体氢纳米气泡(NBs)在氢气生成与利用中起着关键作用,但其在不同溶剂中的稳定机制尚未完全明确。本研究通过分子动力学模拟,结合实验测量,探究了氢纳米气泡在水和甲醇中的稳定性及演化过程。结果表明,甲醇中的纳米气泡在较低初始气体密度下易溶解,稳定性低于水中的纳米气泡。稳定条件下,水中约80%的氢分子保留在气泡内,而甲醇中仅约40%,这与实验观测到的甲醇更高氢气溶解度一致。进一步分析显示,水中氢纳米气泡的气液界面更薄,内部压力和气体密度更低,这与其较低的氢气溶解度相关。利用力学平衡和临界半径理论,确定纳米气泡稳定存在的氢气浓度阈值:水中为0.96-1.44 mol/L,甲醇中为2.69-2.88 mol/L。此外,甲醇中的氢分子运动更剧烈,气液相互作用更强,氢键网络更弱。本研究为不同溶剂中本体氢纳米气泡的稳定机制提供了分子层面的见解。
Abstract
Bulk hydrogen nanobubbles (NBs) play a key role in hydrogen generation and utilization. However, their stabilization mechanisms in different solvents remain not fully understood. This study employs molecular dynamics simulations to investigate the stability and evolution of bulk hydrogen NBs in water and methanol, with experimental measurements providing validation. The results show that NBs in methanol tend to dissolve at lower initial gas densities, indicating a lower stability compared to those in water. Under stable conditions, approximately 80% of hydrogen molecules remain inside NBs in water, while only about 40% remain in methanol, consistent with methanol's higher hydrogen solubility observed experimentally. Further analysis reveals that hydrogen NBs in water exhibit a thinner gas-liquid interface as well as lower internal pressure and gas density, mainly related to its lower hydrogen solubility. Utilizing mechanical equilibrium and critical radius theory, we identify the hydrogen concentration thresholds for NB stability to be 0.96-1.44 mol/L in water and 2.69-2.88 mol/L in methanol. Additionally, hydrogen molecules in methanol exhibit more vigorous motion, stronger gas-liquid interactions, and a weaker hydrogen bond network. This study provides molecular-level insights into the stabilization of bulk hydrogen NBs in different solvents.

AI总结:
本文主要通过分子动力学模拟和实验测量研究了水和水溶液中氢纳米气泡(NBs)的稳定性和演化机制,具体内容如下:
1. 研究背景
1. 氢NBs在氢气生成和利用中起关键作用,但其在不同溶剂中的稳定机制尚不完全清楚。
2. 现有理论如皮肤模型、动态平衡理论等对NBs稳定性有一定解释,但对不同溶剂中NBs稳定性的理解仍不足。
3. 分子动力学(MD)是研究纳米尺度现象的有力方法,但目前对NBs稳定性的MD研究主要集中在水溶液中。
2. 研究目的和方法
1. 目的:比较研究水和甲醇体系中氢NBs的界面特性和稳定机制。
2. 方法:采用全原子MD模拟,构建包含氢分子、水和甲醇分子的模拟系统,设置不同初始气体密度,进行能量最小化、热平衡和NB动力学模拟。同时开展实验测量以验证计算结果。
3. 研究结果
1. NBs演化过程:在热平衡阶段,氢分子从NB扩散到周围液体,由于无压力控制,甲醇系统中NB几乎消失,而水中NB几乎保持完整;在NPT阶段,部分溶解的氢分子重新进入NB,约5 ns后NB内氢分子数量稳定,水中NB稳定,甲醇系统中初始氢分子数为2800时NB完全溶解。水中约80%的氢分子留在NB内,甲醇中约40%,表明甲醇氢溶解能力更强。
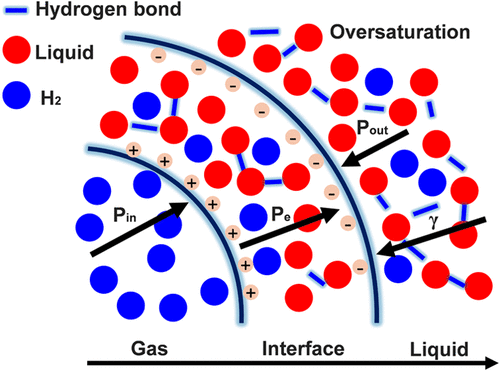
2. NBs界面特性:水中NB的平衡半径随气体分子数增加略有增大,甲醇系统中NB的气 - 液界面更厚,增加了气液分子接触面积,加速了气体扩散,导致内部气体密度低于水中NB。压力分布均符合超压方程,甲醇系统中NB内部压力低于水中NB。界面处存在双电层电荷分布,水中的净电荷密度差更明显,有助于提高水中NB的稳定性。
3. NBs稳定性和消失机制:稳定状态下NB呈不规则布朗运动,甲醇中NB的位移更大。通过机械平衡方程分析发现,表面张力平衡内部 - 外部压力差,过剩气体溶解度抑制进一步溶解,甲醇系统中表面张力较低,加速了氢分子逃逸和溶解过程。根据临界半径理论,存在临界氢浓度,水中约为0.96 - 1.44 mol/L,甲醇中约为2.69 - 2.88 mol/L,甲醇中NB稳定性较弱。
4. 实验验证:实验观察到水中NB平均直径波动较小,甲醇中NB在24小时内完全消失,验证了计算结果。
5. 结构分析:甲醇系统中氢分子的均方位移和自扩散系数大于水系统,与液态分子的相互作用能也更大。气 - 液分子的径向分布函数表明甲醇系统中靠近气相的比例更高。水系统中氢键数量多于甲醇系统,氢键网络可减缓NB溶解。
4. 研究结论
1. 氢NBs在甲醇中不如在水中稳定,尤其在低初始气体密度下。实验测量支持这一结论,水中NB尺寸波动小,甲醇中NB在24小时内消失。
2. 水中NB具有更高的气体密度、内部压力和更薄的气 - 液界面,甲醇系统中氢分子运动更剧烈,气 - 液相互作用更强,氢键网络更弱。
3. 稳定NB呈不规则布朗运动,存在临界氢浓度阈值,不同溶剂中氢溶解度特性不同。结构分析显示甲醇系统中氢分子相关特性与水系统有差异。
4. 该研究为氢气生成和生产过程提供了分子水平理解,加深了对不同溶剂中氢NBs稳定机制的认识,但存在一定局限性,未来需进一步研究。
疑问,氢气在水中的溶解度是0.6mM,这里理论上稳定浓度是1M,这是1500倍的差距。真有这么高浓度吗?
https://wap.sciencenet.cn/blog-41174-1487620.html
上一篇:氢气通减轻创伤性脑损伤后肺损伤机制研究
下一篇:逆向电子传递驱动肥胖中的代谢变化