神奇疗法成为常规药物的在体编辑CAR-T进行时!
这种治疗方法比较符合精准医疗的逻辑,就是精准消灭目标细胞,对癌症治疗如此,其他如自身免疫性疾病也是如此(上海长征医院这种策略已成功),理论上也能用于衰老细胞清除的抗衰老治疗。对癌症治疗来说,预防永远应该作为上策,这种疗法解决超早精确诊断的技术,对某些超早癌症,特别是癌前病变,将能带来革命性影响。
以上为博主观点。

20世纪90年代,当布鲁斯·莱文和他的同事开始尝试对免疫细胞进行工程改造以对抗癌症时,很少有人认为他们会成功。费城宾夕法尼亚大学佩雷尔曼医学院的免疫学家莱文说:“整个领域都非常怀疑。”当他们在会议上展示研究成果时,“我们被安排在最后一天的最后一场,在一个没人找得到的房间里”。
如今,这些经过工程改造的免疫细胞,即CAR-T细胞,是肿瘤学家治疗多种血液癌症的最有效疗法之一。研究表明,它们可能对脑癌和其他实体瘤以及自身免疫性疾病和其他疾病有治疗前景。一家研究公司估计,CAR-T疗法市场的价值预计今年将达到110亿美元,到2034年将增长到近1900亿美元。
但CAR-T疗法有一个严重的缺点——制作费力且难以施用。医生从人的血液中取出称为T细胞的免疫细胞后,将它们送到制造商那里,在那里技术人员对细胞进行基因工程改造,使其表面携带一种称为嵌合抗原受体(因此称为“CAR-T”)的特殊蛋白质。这些细胞被培养并扩增到数亿个更多的细胞,冷冻后送回医院进行回输。由于过程复杂,美国只有约200个中心提供这种疗法。
增强抗癌T细胞的竞赛
同样在佩雷尔曼医学院的血液学家和肿瘤学家萨尔·吉尔说:“整个过程效率太低了。如果我有一个癌症患者,我可以开化疗处方,他们明天就能开始治疗。”然而,对于商业CAR-T疗法,人们必须等待数周才能接受治疗。这种延迟,加上治疗费用高昂,以及在接受CAR-T细胞治疗前需要进行化疗,意味着许多本可以从CAR-T疗法中受益的人从未接受过治疗。吉尔说:“我们都希望CAR-T细胞能更像一种药物。”
一些生物技术公司有了一个办法:改为在体内改造T细胞。将CAR蛋白的基因输送到血液细胞中的治疗方法可以大规模生产并按需提供——理论上,其价格比目前的CAR-T疗法低得多。一剂商业CAR-T疗法的成本约为50万美元。一剂体内治疗的成本可能会低一个数量级(5万美元仍然太贵了)。
这个想法有一些知名的支持者。位于加利福尼亚州圣地亚哥的Capstan Therapeutics公司专门从事体内细胞治疗,其创始人包括CAR-T先驱莱文和卡尔·朱恩,以及因在信使RNA疫苗方面的工作而获得诺贝尔奖的德鲁·韦斯曼。CRISPR-Cas9先驱、诺贝尔奖得主詹妮弗·杜德纳共同创立了另一家公司,位于加利福尼亚州伯克利的Azalea Therapeutics,该公司正在开发体内CAR-T疗法。大型制药公司也在关注。3月,生物制药公司阿斯利康同意支付高达10亿美元收购总部位于比利时的体内CAR-T公司EsoBiotec,该公司于1月启动了其体内CAR-T疗法的首次人体试验。
尽管人体试验才刚刚开始,但许多研究人员对更简单版本的CAR-T疗法的潜力感到兴奋。堪萨斯城堪萨斯大学医学中心研究细胞疗法的血液学家和肿瘤学家约瑟夫·麦吉尔克说:“如果它有效且安全,它真的可能挑战当前的模式。”而且“我们需要挑战当前的模式”。
将体外的方法引入体内
许多正在开发的体内CAR-T疗法借鉴了体外疗法的经验。与已获批的疗法类似,体内疗法旨在摧毁称为B细胞的白细胞,从而治疗在这些细胞中形成的癌症。(CAR-T疗法也会摧毁健康的B细胞,但人们没有这些细胞也能生存。)
与体外疗法一样,许多体内疗法依赖于一种经过工程改造的慢病毒来附着在T细胞上,并将CAR蛋白的基因输送到细胞的基因组中(见“体内制造”)。但在体内对细胞进行工程改造是一项棘手的工作。对于体外疗法,T细胞已经从体内取出,所以研究人员不必担心将基因引入其他细胞类型。但在体内,许多细胞有共同的受体,所以研究人员必须找到专门针对T细胞或其他可以参与战斗的免疫细胞的方法。
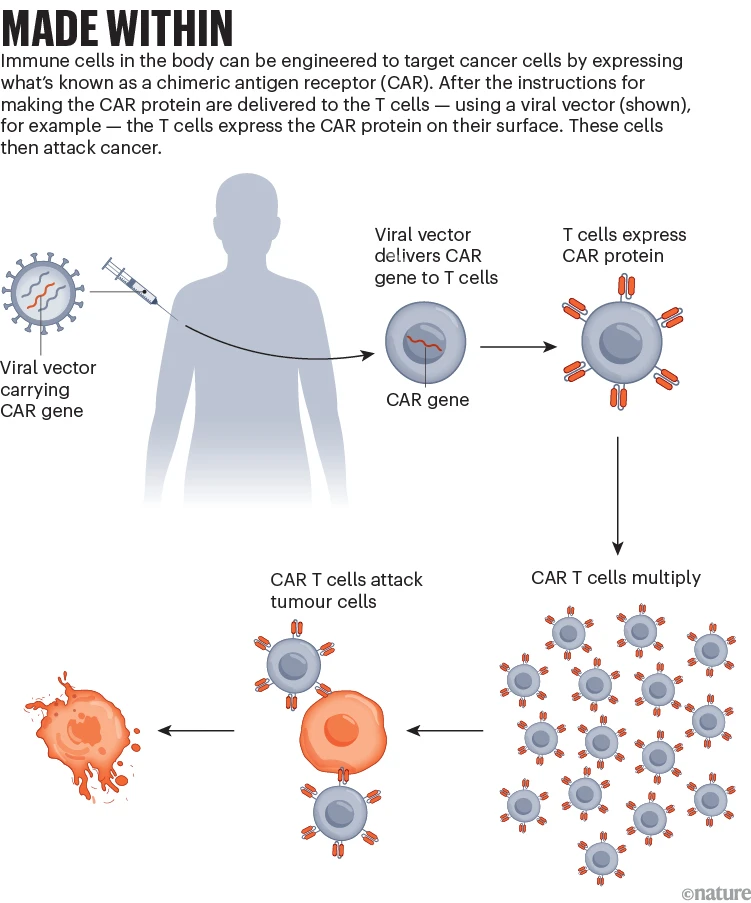
体内制造:信息图表展示了如何使用病毒载体在体内将CAR基因输送到T细胞,以便身体可以制造自己的CAR-T细胞来靶向癌症。
“障碍在于,如何在正确的时间将其送到正确的细胞、正确的位置?”纽约市哥伦比亚大学细胞工程与治疗哥伦比亚倡议主任、遗传工程师、另一位CAR-T先驱米歇尔·萨德莱恩说。
每家公司都开发了自己的方法来解决这个问题,并且每家公司都以不同的方式调整了其载体。例如,由吉尔共同创立的费城生物技术公司Interius BioTherapeutics正在测试一种附着在CD7上的载体,CD7是一种仅在T细胞和自然杀伤细胞上发现的蛋白质。
华盛顿州西雅图的Umoja Biopharma正在测试一种慢病毒载体,其装饰有一种蛋白质,可以同时靶向T细胞上的三种受体。该公司从动物模型中获得证据,表明这种策略比仅靶向一种受体更有效,并希望它能更紧密地模拟例如感染后T细胞自然激活时发生的情况。
如果有效,这些方法可以简化制造过程,并更快地将CAR-T疗法提供给更多的人。麦吉尔克指出,当体外CAR-T疗法Carvykti(西达基奥仑赛)在2025年被批准用于治疗多发性骨髓瘤时,制造商的生产能力有限,导致等待时间很长。
麦吉尔克说:“我们的等待名单上一次有50名患者。其中超过一半的患者在我们为他们争取到生产名额之前就去世了。”
尖端的CAR-T细胞疗法会致癌吗?数据怎么说
除了简化生产,体内治疗还有另一个潜在优势。对于体外疗法,人们在CAR-T治疗前接受化疗,以消除未编辑的T细胞,为编辑后的T细胞增殖腾出空间。其理念是创造一个空白状态。但对于体内疗法,人们将无需进行治疗前的化疗。吉尔说:“我们不想杀死我们希望转导的T细胞。”这将消除与化疗相关的副作用,例如更高的感染风险。这也可能意味着那些病情太重而无法接受化疗的人仍然有资格接受CAR-T疗法。
然而,通过病毒载体进行的体内CAR-T疗法是否能消除体外疗法带来的所有副作用,目前还不完全清楚。输注后,CAR-T细胞在体内增殖并释放增强免疫系统的化学物质。在某些情况下,它们会引发一种称为细胞因子释放综合征的炎症风暴。Capstan Therapeutics的首席科学官阿德里安·博特说:“这就像一列失控的火车。”
一些研究人员怀疑这在体内疗法中可能不是那么严重的问题。明尼苏达州罗切斯特市梅奥诊所的血液学家和肿瘤学家伊琳说,这是因为经过工程改造的T细胞将在其他免疫细胞的存在下增殖,包括那些可以帮助抑制失控免疫反应的细胞。她说,因此,副作用可能会更轻微。
即便如此,这些体内疗法不太可能消除过去几年出现的关于CAR-T疗法导致继发性癌症的担忧。尽管风险很低,但许多国家要求CAR-T疗法贴上详细说明这种风险的警告标签。问题在于慢病毒载体将CAR基因永久整合到T细胞的基因组中。每次细胞分裂,都会产生更多的CAR-T细胞。这意味着T细胞可能会长期攻击它们的目标——在某些情况下是数年。
尽管这可能是一个优势,但研究人员对慢病毒在基因组中的插入位置没有太多控制权。如果它插入到错误的位置,可能会促使继发性癌症的形成。公司可以对体外疗法进行这种问题的筛查,但对体内疗法则无法做到。
转向RNA
Capstan和其他几家公司没有使用病毒载体,而是转向纳米颗粒将RNA运送到T细胞中。RNA进入细胞的细胞质,在那里其遗传信息仅在短时间内用于制造CAR蛋白。尽管这种疗法需要多次给药,但它可能被证明更安全。一旦出现严重问题的迹象,医生可以停止治疗,CAR蛋白会在几天或更短的时间内消失。
位于马萨诸塞州沃特敦的生物技术公司Orna Therapeutics正在研究RNA方法,其首席执行官乔·博伦说:“我们的药物更像小分子。你给药,它完成任务后就会消失。”“你持续给药,直到得到你想要的结果。”
德国兰根保罗·埃利希研究所的病毒学家、分子生物技术和基因治疗研究负责人克里斯蒂安·布赫霍尔茨想知道,增加的安全性是否可能以疗效为代价。他说:“不永久性改造T细胞,你能治愈癌症吗?”
CAR-T免疫治疗后癌症缓解达创纪录19年的女性
Orna Therapeutics和其他公司打赌答案是肯定的。为了治疗血液癌症,Orna开发了纳米颗粒,将CAR蛋白的RNA输送到T细胞、自然杀伤细胞和巨噬细胞中。位于马萨诸塞州剑桥的Myeloid Therapeutics已经启动了两项临床试验,测试针对肺癌、乳腺癌、结肠癌和肝癌患者的体内RNA疗法。该公司根本没有改造T细胞;相反,它将RNA输送到巨噬细胞和其他免疫细胞中,促使这些细胞攻击肿瘤。
Capstan将目光投向用于自身免疫性疾病的体内CAR-T疗法,自身免疫性疾病也常常涉及有缺陷的B细胞。尽管体外CAR-T疗法尚未被批准用于自身免疫性疾病,但德国研究人员领导的一个团队报告称,使用它成功治疗了15名狼疮和其他自身免疫性疾病患者(F. Müller等人,《新英格兰医学杂志》,第390卷,第687-700页;2024年)。Capstan的博特等人希望通过RNA方法效仿这种成功,他们认为这种方法的副作用比体外方法少。Orna也计划启动一项试验,测试其治疗自身免疫性疾病的疗法。
目前,任何一种体内策略相对于其他策略的优势大多是理论上的。真正的考验将是人体试验;目前有几项使用慢病毒输送的试验正在进行中。Interius在10月启动了其首次试验,截至2月下旬,已经招募了三名非霍奇金淋巴瘤患者。吉尔在2月于加利福尼亚州洛杉矶举行的美国癌症研究协会免疫学会议上展示了一些初步数据。前两名接受小剂量治疗的患者没有反应。第三名接受了更高剂量的治疗;六天后,他的B细胞几乎被消除,并且已经维持低水平三个月。
Umoja目前正在中国和美国的两项试验中招募非霍奇金淋巴瘤和白血病患者,预计年底将有初步数据。1月,EsoBiotec报告称,在其针对多发性骨髓瘤的中国试验中,第一个接受治疗的人在一个月后没有检测到癌细胞。
Capstan和Orna都计划很快启动RNA试验。博伦说:“我认为2025年和2026年在这个领域将是非常忙碌的两年。”
体内治疗并不是使CAR-T疗法更快、更便宜的唯一选择。去年,阿斯利康收购了一家中国公司,该公司开发了一种生产CAR-T细胞的工艺,只需22小时,而不是几天或几周。其他人正在研究如何从健康供体中改造T细胞和其他免疫细胞,以制造一种现成的疗法。
麦迪逊威斯康星大学医学院和公共卫生学院的儿科血液学家和肿瘤学家克里斯蒂安·卡皮尼蒂说,当研究人员在20世纪90年代初开始对T细胞进行基因工程改造以对抗癌症时,体外方法似乎是最安全的选择。她说:“如果在制造过程中出现一些小问题,你还没有对患者造成任何潜在的伤害,产品仍然可以被调整、挽救或测试。”
但研究人员表示,三十年后,这种疗法已经证明了自己,并且越来越受欢迎。莱文说:“每个人都想进入这个领域。”而这个领域的每个人都希望使CAR-T疗法更简单、更容易获得。
《自然》641, 1090-1092 (2025)
转载本文请联系原作者获取授权,同时请注明本文来自孙学军科学网博客。
链接地址:https://wap.sciencenet.cn/blog-41174-1487482.html?mobile=1
收藏

