博文
基于血液的癌症筛查  精选
精选
|
基于血液的癌症筛查
基于人工智能的风险评估可实现个性化的基于血液的多癌种筛查
在过去的 20 年里,晚期癌症的分子靶向和免疫治疗取得了变革性进展,为许多患者提供了更长的生存期和生活质量。然而,不同癌症治愈的主要决定因素仍然是诊断阶段。在浸润性癌症仍处于局部且没有临床可检测到的转移扩散时发现它,为通过手术和/或放疗根除原发性肿瘤以及通过治疗药物杀死任何播散性微观细胞提供了最佳机会。基于血液的多癌种检测 (MCD) 检测的最新发展,以及成像和人工智能 (AI) 算法的进步,有可能改变早期癌症检测。但这些创新并非没有健康和财务风险,它们的日益普及带来了机遇和挑战,随着致力于早期癌症检测的诊所的推出,这一点显而易见。
以一位 55 岁的女性为例,她最近因癌症失去了一位近亲,并担心自己的风险。她的家族史不符合已知的癌症遗传易感综合征。她有吸烟史,经常锻炼,保持正常体重指数,适量饮酒。她了解最新的癌症筛查建议,包括巴氏涂片检查、乳房 X 光检查和结肠镜检查。她决定支付多癌种检测测试(Galleri)的费用,该测试目前在美国可以购买,但未经美国食品和药物管理局(FDA)批准或保险报销。该测试表明“检测到癌症信号”,卵巢是预测起源的首要组织,但临床检查,包括高分辨率成像和卵巢癌抗原 125 (CA-125) 血液标志物,是阴性的。对于看似健康但血液检查呈阳性癌症信号的患者,应该如何咨询,随着 MCD 筛查的普及,这种情况可能有多普遍?
几种 MCD 检测方法正处于不同的开发阶段,GRAIL 的 Galleri 检测在临床研究中是最先进的,并且正在美国和英国监管机构的批准谈判中 (1)。Galleri 使用 40 毫升血液提取血浆中的游离 DNA,如果存在癌症,其中一部分可能来自肿瘤细胞(即循环肿瘤 DNA、ctDNA)。鉴于整个癌症基因组中 CpG 二核苷酸的大量 DNA 甲基化变化,该测试应用亚硫酸氢盐测序来注释超过 100,000 个基因组位点,使用算法来识别潜在的癌症信号和可能的起源组织,与血液中的正常组织衍生 DNA 混合。其他新兴的基于血液的癌症检测依赖于癌症来源的 ctDNA (DELFI) 的大小分布改变 (2) 或复发性突变和异常蛋白标记物的存在 (CancerSEEK) (3)。除了这些和其他ctDNA衍生的检测之外,癌症相关血液分析物还包括高通量蛋白质组学、循环肿瘤细胞、外泌体、血小板相关RNA和循环游离RNA。
Deploying blood-based cancer screening | Science
开发一种基于血液的单一检测来筛查多种癌症,而不是肿瘤类型特异性检测的论点是,所有癌症的共同分子特征都可以以这种方式利用,提供一种“一种检测适合所有人”的临床范式,可以很容易地在无症状人群中实施。需要注意的是,检测性能和预测能力取决于筛查中癌症的患病率,不同的癌症具有不同的风险人群,以及从单个细胞发展为浸润性癌症将ctDNA脱落到血液中的时间模式各不相同。一个主要的悬而未决的问题是,目前缺乏筛查测试的最致命的癌症(例如胰腺癌和卵巢癌)是否在血浆可检测性和肿瘤转移之间表现出足够的机会窗口来部署根治性手术。
MCD筛查测试在发现早期、可能可治愈的癌症方面有多有效?初步研究 (1) 将已知患有不同类型癌症的患者与健康个体进行了比较,报告称 Galleri 对 I 期癌症的总体敏感性(正确识别癌症患者)为 16.8%,对 II 期癌症的总体敏感性为 40.4%,当检测参数设置为 99.5% 的特异性阈值(正确识别没有癌症的患者)时。在 PATHFINDER 试验中,一项针对 6621 名 50 岁以上明显健康的个体的人群研究,1.4% 的人在 Galleri 测试中显示出阳性癌症信号;其中,38%的癌症(任何阶段)最终得到证实,而62%似乎是假阳性。这种错误信号可能需要昂贵的成像和侵入性检查来排除癌症的存在,并可能导致不必要的焦虑 (4)。在Galleri正确识别为癌症的36例病例中,有14例存在先前未被怀疑的I期或II期癌症,即0.2%的初始筛查人群被发现患有可能治愈的早期癌症。英国国家医疗服务体系 (NHS) 正在进行一项基于人群的重大试验,涉及将 140,000 名年龄在 50 至 75 岁之间的无症状个体随机分配到标准临床癌症筛查方案加上为期 3 年的年度 Galleri 测试组,而不是单独进行临床筛查。本研究的主要终点是 MCD 测试队列中癌症诊断的早期阶段,而不是总体癌症相关生存率的降低。这个终点将提供更方便的试验读数,但缺乏评估重要混杂因素的能力,例如提前期偏倚,当癌症由于研究干预而在病程早期被发现,但不足以及早改变其可治愈性。
关于实施MCD筛查测试的最关键问题可能是,它们是否最好地应用于所有超过一定年龄的人,或者人工智能的进步是否会实现更个性化的基于风险的筛查策略,从而提高基线患病率,从而提高测试的预测价值。癌症风险随着年龄的增长而增加,在西方国家,50 岁时的年发病率估计为 0.5%,65 岁时为 1.5%。筛查试验的阳性预测值 (PPV) 意味着阳性检测结果与真实癌症病例相对应的几率,将检测固有的特异性和敏感性与检测人群中的癌症患病率相结合。因此,当应用于癌症患病率仅为 1% 的人群时,具有 99% 灵敏度和 99% 特异性的假设测试将为每个真阳性结果产生一个假阳性结果(即 PPV 50%)。但是,如果人群中的癌症患病率上升到 5%,则同一测试的 PPV 将跃升至 84%(即假阳性率更少)。
当前一代癌症风险计算器通常专注于单一癌症类型[例如,乳腺癌的Tyrer-Cuzick;前列腺癌、肺癌、结直肠癌和卵巢癌筛查试验(PLCO);以及结直肠癌风险评估工具(CCRAT)],它们使用有限数量的静态风险因素作为输入,生成经过验证的风险预测,可用于选择高危患者进行经典癌症筛查测试[例如, 乳房 X 光检查、低剂量胸部计算机断层扫描 (CT) 和结肠镜检查]。同样,对于携带高度渗透性遗传基因突变的个体进行癌症筛查,也有成熟的算法,这些突变赋予了对黑色素瘤、乳腺癌、乳腺癌、卵巢癌、结肠癌、肾癌和内分泌癌的易感性。然而,有多种风险调节器只能通过复杂的算法获得。人工智能驱动的癌症风险评估方法可能会将传统风险因素与新的或更难评估的因素相结合,包括低外显率遗传变异、不同的环境暴露和其他健康指标。最近的一项研究使用基于机器学习的临床记录分析来预测胰腺癌在特定时间间隔的风险 (5),胰腺癌目前尚无经过验证的风险计算器。此外,现在可以使用人工智能驱动的技术分析非癌组织的放射学图像,以帮助预测个体未来患乳腺癌或肺癌的风险,这些技术不同于对当前病变的传统临床放射学评估(6,7)。 因此,个体化癌症风险评估的发展可能能够更有效地将基于血液的 MCD 筛查靶向癌症患病率增加的人群,从而改善 PPV。
除了 MCD 检测的选择标准外,对具有血液癌症信号的患者进行临床评估对于其部署至关重要。对于Galleri测试,DNA甲基化模式提供了有关起源组织的初步线索,为开始临床检查提供了公式,但如果这没有揭示性,则后续评估尚不清楚。全身成像[例如,正电子发射断层扫描 (PET) 扫描和全身磁共振成像 (MRI)] 是一种考虑,但它的敏感性差、偶然发现和成本高。值得注意的是,在 PATHFINDER 研究中,Galleri 检测呈阳性的 90 名患者中有 44 名接受了侵入性诊断程序,以确定是否存在癌症。GRAIL目前提供免费的重复Galleri测试,如果在最初的阳性测试后没有做出癌症诊断,则在3至6个月内。常规应用基于血液的正交验证检测也可能在减少初始筛查时假阳性结果的比例方面发挥作用。这种二线检测可能包括对癌症相关 DNA 突变或血液中循环肿瘤细胞的高灵敏度检测 (8),或分子探针与高灵敏度成像分析相结合。然而,在没有临床证实的情况下,血液检查的阳性癌症信号要么代表假阳性结果,要么代表尚未检测到的恶性肿瘤,需要持续保持警惕,这是一个未解决的困境,可能是深深焦虑的根源。
根据风险进行多癌种筛查试验
使用年龄作为唯一危险因素的基于人群的筛查可能对人群中检测到的早期癌症总数有最大的益处,但由于疾病患病率低且成本高,因此存在相当多的假阳性。风险分层,可能使用基于人工智能的风险计算器,可能会增加人群患病率,从而提高测试的阳性预测值 (PPV)。应用多癌种检测 (MCD) 检测来评估意义不明的影像学病变可能是另一个具有高 PPV 的相关临床应用。
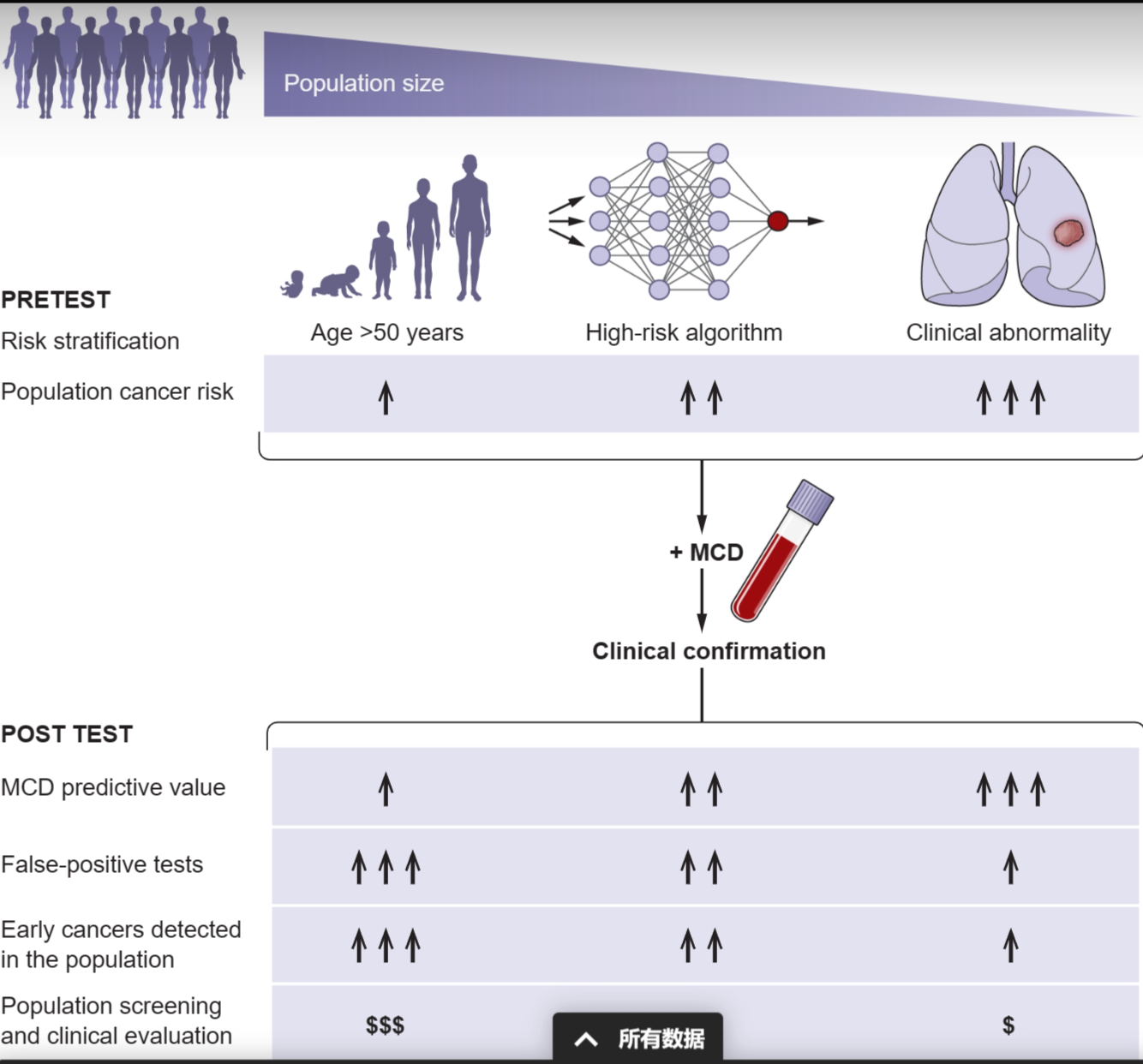
在其他临床场景中,MCD 检测可能有助于早期癌症检测。临床医学充满了针对各种适应症的复杂成像,越来越多地产生意义不明的放射学病变。例如,在接受冠状动脉钙沉积物胸部 CT 评分以进行心脏风险评估的个体中,有 18% 的患者发现了不确定的肺结节 (9),以及偶然发现的 10% 的 70 岁以上个体的胰腺癌前病变前状粘液性肿瘤囊肿 (10).基于血液的 MCD 检测可能在评估此类偶然病变中发挥作用,有助于评估是否需要进行侵入性活检或手术。此外,MCD 检测可能对出现与癌症一致但不能诊断癌症的体征或症状的个体有用。事实上,在如此高危人群中,英国一项针对 5461 名患者的研究报告称,在明确临床诊断之前,疑似患有癌症的患者中,Galleri 测试的 PPV 为 75%(11)(见图)。
随着基于 MCD 的癌症筛查的发展,前列腺癌和肺癌癌症筛查的历史为实施提供了一些独特的经验教训。在 1990 年代过于雄心勃勃地实施后,不再常规推荐使用血液蛋白标志物前列腺特异性抗原 (PSA) 对前列腺癌进行基于年龄的筛查,以致于基于人群的 PSA 检测每挽救一条生命,就会因活检或手术相关并发症而失去另一条生命(12).目前,55至69岁男性的PSA检测由个别患者及其医生自行决定(13)。相比之下,在肺癌中,随机对照试验清楚地表明,重度吸烟者在低剂量胸部CT筛查后,癌症死亡率降低了20%(14)。然而,由于缺乏全面的实施策略、对肺癌结局的虚无主义以及对吸烟的污名化,只有不到 10% 的符合条件的患者接受了肺部筛查 (15)。此外,对于前列腺癌和肺癌筛查,相关风险因素和复杂诊断的可用性在美国不同社区中是不平等的。与白人相比,黑人患前列腺癌和肺癌的几率更高,结果更差,尽管努力改善可及性,但仍然不太可能有资格进行肺癌筛查(15)。公正、公平和负担得起的癌症筛查部署是 MCD 检测部署中应积极解决的主要问题。在这方面,应在实施的所有阶段评估MCD检测的成本效益分析,包括临床确认的下游成本及其与标准筛查方法的结合。
最重要的是,个人对癌症风险的看法通常难以量化,但它是许多患者偏好和决定的基础。MCD筛查与现有的癌症筛查测试没有什么不同,其敏感性不完全,假阳性率高。它可能与公众的看法不同,即分子检测具有诊断水平的确定性,而影像学异常往往被理解为初步的,直到通过确定性活检确认。此外,基于器官的癌症筛查比血液中的多癌种信号更适合临床确认,其来源可能无法立即验证。
因此,MCD筛查作为临床护理领域的一种新工具,既带来了前所未有的机遇,也带来了重大挑战。再加上如此强大的癌症检测技术,客观评估个性化癌症风险的能力增强可能是理性癌症筛查策略中最重要的因素,最大限度地提高预测能力,同时最大限度地减少不必要的焦虑和医疗检查。
https://wap.sciencenet.cn/blog-41174-1419446.html
上一篇:开放获取论文吸引了更多引用!
下一篇:氧化应激和晚期糖基化终产物