博文
肠道微生物通过剥夺营养物质来抵御有害细菌  精选
精选
|
肠道微生物通过剥夺营养物质来抵御有害细菌
通常居住在肠道中的微生物有助于阻止微生物感染。一组生活在人类肠道中的细菌被识别出能够消耗致病性细菌所需的一种营养物。
这组居住在肠道中的微生物,即肠内菌群的成员,是非常排他的,新来的微生物通常通过一个被称为定植抵抗的过程被拒绝。微生态多样性的丧失,通常是抗生素治疗的结果,会破坏定植抵抗并使潜在的有害物种,如细菌病原体肺炎克雷伯菌和其他属于肠杆菌科的物种,侵入肠道并达到高密度1。因此,重建定植抵抗是一个重要临床目标。Furuichi等人在《自然》杂志上发表文章揭示了一组通常居住在肠道中的细菌(共生细菌)如何通过耗尽营养物质来抑制肺炎克雷伯菌的肠道定植。
Furuichi及其同事将人类粪便移植到缺乏自身微生物的小鼠肠道中,然后引入肺炎克雷伯菌以识别因接受的微生物而变得具有定植抵抗性的动物。实现这一目标后,该团队从赋予定植抵抗性的粪便样本中培养了单个共生细菌株,并测试它们对肺炎克雷伯菌和其他肠杆菌科细菌定植的体内抑制作用。研究人员表明,施用从最有效的粪便样本中培养出的包含31个不同菌株的联合体提供了与粪便移植相媲美的定植抵抗水平。接下来,使用这些菌株的各种组合,研究人员将联合体的复杂性减少到了18个菌株,仍然保持了最大的定植抵抗。
这种“F18混合物”的细菌菌株不需要受体小鼠拥有完整的免疫系统就能抑制肺炎克雷伯菌的定植,这表明涉及细菌的机制正在发挥作用。在肠道定植期间对肺炎克雷伯菌基因表达的特征分析揭示了参与碳水化合物和氨基酸代谢的基因被表达,并且当F18混合物与肺炎克雷伯菌共同施用时,这种基因表达显著减弱。
通过检查一系列带有突变基因版本的肺炎克雷伯菌细菌,作者鉴定出了参与碳水化合物代谢的基因,这些基因显著降低了在结肠化小鼠中肺炎克雷伯菌的生存能力。评估粪便碳水化合物的水平显示,F18混合物显著降低了缺乏肠道微生物的小鼠中高浓度的分子葡糖酸盐。饮食补充葡糖酸盐逆转了由F18混合物带来的定植抵抗(图1)。
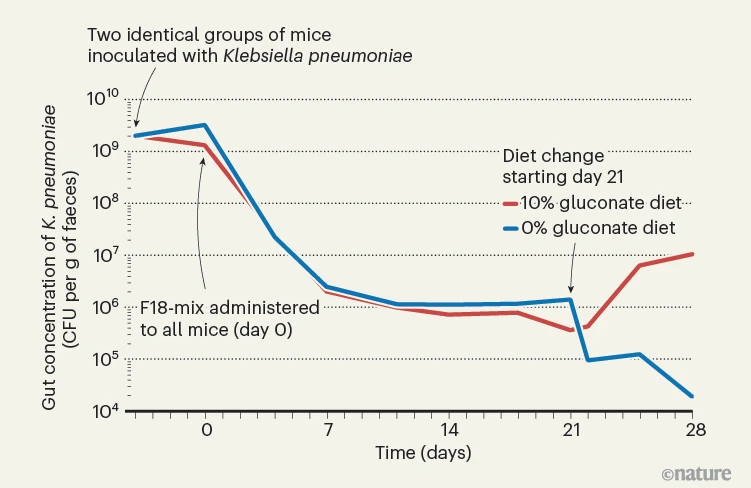
图1 | 一种有害细菌需要分子葡糖酸盐才能在肠道中定植。Furuichi等人研究了通常居住在人类肠道中的细菌如何限制致病性细菌肺炎克雷伯菌的生长。作者使用人类粪便样本鉴定了18种细菌物种(称为F18混合),这些细菌阻碍了肺炎克雷伯菌在肠道中的定植能力。然后他们用肺炎克雷伯菌感染了两组缺乏肠道微生物的小鼠,并在引入F18混合物后观察到肺炎克雷伯菌群体按每克(g)粪便的菌落形成单位(CFU)计量下降。作者确定F18混合物耗尽了肺炎克雷伯菌成功在肠道中生长所需的分子葡糖酸盐。在第21天,作者将其中一组小鼠的饮食切换为含有10%葡糖酸盐的饮食,另一组切换为含0%葡糖酸盐的饮食。含10%葡糖酸盐的饮食使肺炎克雷伯菌群体再次增长。(改编自参考文献2的图3。)
肺炎克雷伯菌如果缺乏产生负调节葡糖酸盐代谢的蛋白质GntR的能力,则更容易被F18混合物清除,与没有这种缺陷的肺炎克雷伯菌相比。鉴于删除编码GntR的基因增强了葡糖酸盐驱动的肺炎克雷伯菌生长,如何持续代谢葡糖酸盐的能力会增强F18混合物清除肺炎克雷伯菌的方式尚不清楚。令人惊讶的是,Furuichi及其同事发现GntR正调节分子氨基葡萄糖的代谢,因此GntR缺陷可能通过降低肺炎克雷伯菌代谢氨基葡萄糖的能力来增强F18混合物的效果。
在医院中,患者肠道内定植抗生素耐药性细菌种类密集是常见的。这种定植与更高的患者间细菌传播率和潜在的致命感染有关。因此,人们越来越感兴趣于引入微生态来重建定植抵抗。粪便微生物移植减少了肠道内抗生素耐药微生物的密度;然而,与使用粪便样本相比,施用经过良好表征的细菌联合体有潜力提供更大的一致性、纯度和可重复性。
之前有报道称,一个由12个成员组成的细菌联合体,名为Oligo-MM12,适度抑制了沙门氏菌(一种高度致病性的肠杆菌科成员)的生长,并且添加三种称为兼性厌氧菌的细菌物种(选择它们是因为它们扩大了联合体中代谢途径的代表范围)增强了定植抵抗力,达到了粪便移植后观察到的水平。
后续研究表明,肠道酸化和产生所谓的短链脂肪酸抑制肠杆菌科,而抗生素治疗增加了肠道中的营养浓度,同时减少了抑制肠杆菌科产生的代谢物。施用半乳糖醇分子可以逆转肺炎克雷伯菌密歇根亚种对致病性大肠杆菌的抑制作用,类似效果也在大肠杆菌和产氧克雷伯菌对沙门氏菌的抑制中被暗示。
人们越来越认识到,定植抵抗的机制取决于饮食、免疫力和微生态组成等因素,并且在肠道的不同区域有所不同。Furuichi及其同事通过展示尽管F18混合物在结肠(氧气浓度低)中耗尽了葡糖酸盐,但葡糖酸盐在小肠(氧气浓度高于结肠)中仍然存在,从而揭示了另一层复杂性。兼性厌氧菌,如肠杆菌科,可以在高氧的毒性效应下存活,并在整个肠道长度上繁荣。目前尚不清楚定植抵抗是否主要或仅部分地在结肠中介导。未来的研究可能会确定F18混合物在结肠中清除肺炎克雷伯菌的速率是否可以通过对包括在小肠中介导定植抵抗的共生联合体的使用来加速。
包括宏基因组学、代谢组学和生物信息学分析在内的各种技术继续识别微生物群落与人类健康之间的许多关联。微生物群落对疾病易感性和抵抗力影响的复杂性变得越来越明显,表明通常存在多种机制同时起作用。
Furuichi及其同事的发现和其他研究人员的工作支持这样一个观点:大多数微生物疗法不会由单一微生物物种或代谢产物介导,也不会通过耗尽单一营养素或激活单一抑制机制来实现。开发针对微生物群落的疗法将需要组装微生物联合体,调整交织的代谢网络以在不同环境中生活的不同个体、吃不同饮食和使用广泛药物的治疗中获得期望的结果。通过定义肺炎克雷伯菌在小鼠结肠中茁壮成长所需的营养素,Furuichi及其同事为活体生物治疗产品的开发提供了更详细的路线图。
https://wap.sciencenet.cn/blog-41174-1451679.html
上一篇:氢气对人类脂肪组织的直接效应研究
下一篇:一个人工智能数小时内提出4000个新颖研究想法!!