博文
癌细胞耐受化疗背后是乳酸作乱  精选
精选
|
博主感言
乳酸是代谢废物,说是废物是因为了解不够,就如二氧化碳是代谢废物一样,也是呼吸的重要刺激因子。一切代谢物,包括最终代谢物,都是生理效应调节剂。这应为生物系统的必然规则。所谓代谢物质对代谢过程的调节,是生物体系的必然。通过长距离调节,则是生物进化的必然后果。所以我们会看到,一切生物分子,都是生物调节分子。这种调节效应甚至是跨物种的,进一步延申,一切生物环境分子,都可能是生物调节物质,也不过分。
乳酸分子是无氧糖代谢的废物,缺氧是癌细胞优先用来产生能量的代谢途径。代谢组学分析显示,肿瘤细胞中的乳酸会促进对化疗的耐药性,并阐明乳酸在癌症中这种意想不到的作用背后的分子机制。
问题提出
无论氧气的可用性如何,癌细胞都会通过糖酵解途径代谢葡萄糖以获得能量,而不是选择更节能的线粒体氧化磷酸化途径。癌细胞对糖酵解的这种特征偏好被称为 Warburg 效应1.目前尚不清楚为什么癌细胞倾向于通过无氧(厌氧)糖酵解产生能量,尽管涉及使用氧气的糖酵解(有氧糖酵解)产生的能量要高得多。越来越多的证据表明,暴露于化疗药物的癌细胞会积累大量的乳酸,而乳酸在介导肿瘤对此类药物的耐药性中发挥作用2,3.修复 DNA 损伤是癌细胞用来抵抗化疗的关键机制,但乳酸是否在此过程中发挥作用尚不清楚。我们深入研究了这个问题,并研究了乳酸在化疗耐药中发挥作用的机制。
研究发现
在对人类肿瘤样本中的蛋白质和代谢分子的分析中,我们观察到化疗耐药肿瘤细胞中的乳酸水平明显高于对化疗敏感的肿瘤细胞中的乳酸水平(图 1a、b)。我们还发现,与化疗敏感的细胞系相比,化疗耐药细胞系中的乳酸水平显着增加,并表明向易受化疗影响的癌细胞中添加乳酸会增加它们的耐药性。乳酸脱氢酶 A (LDHA) 促进乳酸在细胞中的积累,我们发现用一种叫做 stroipentol 的抗癫痫药物抑制 LDHA 可以防止化疗耐药。
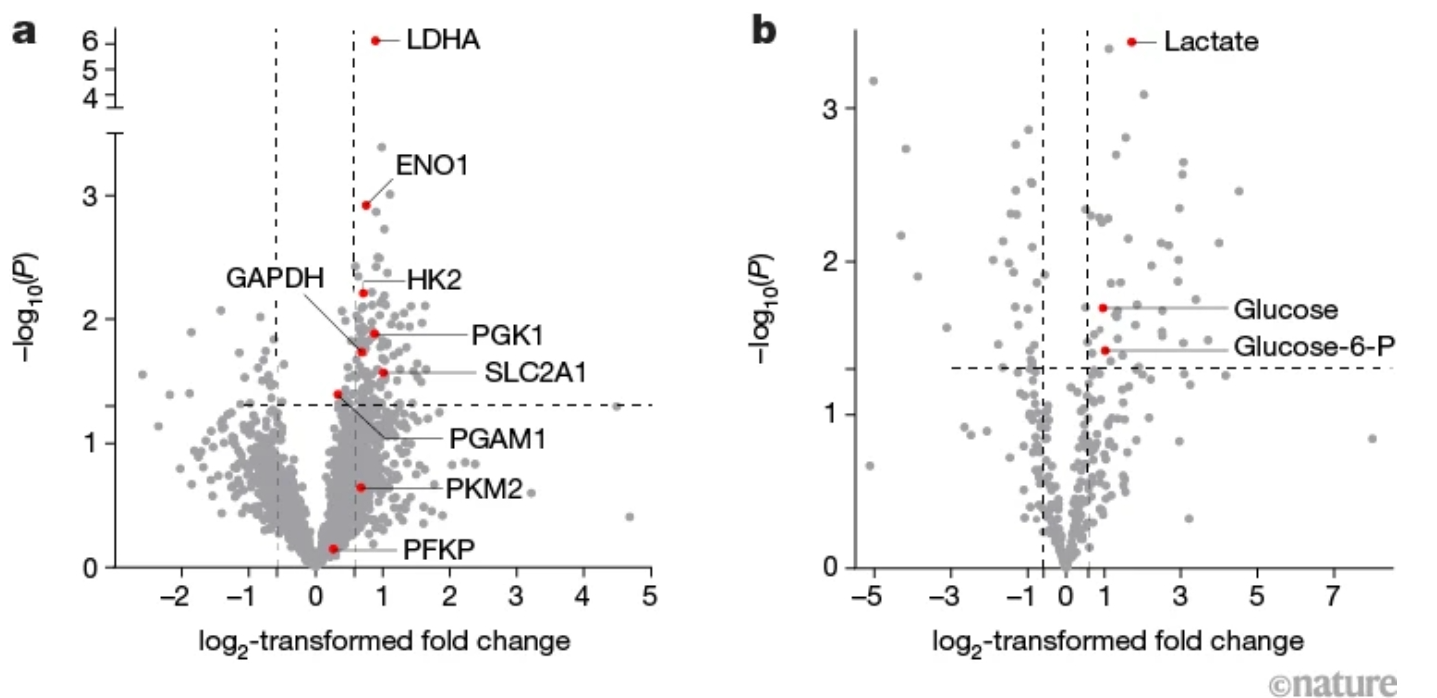
图 1 |乳酸可增强 DNA 修复和对 DNA 损伤化疗的抵抗力。 a,胃癌个体化疗耐药组织和化疗敏感组织之间蛋白质组(细胞或组织产生的蛋白质的完整补充)差异的火山图。红点代表糖酵解途径的酶,糖酵解途径是癌细胞优先用来产生能量的代谢途径。垂直虚线表示原木的截止点2- 转换的折叠变化(0.58 或 –0.58)。水平虚线表示 P 值截断值为 0.05 的值。b,胃癌个体化疗耐药组织和化疗敏感组织之间代谢分子补体差异的火山图。红点是糖酵解途径的代谢产物。垂直和水平虚线如 a.图片来源:Chen, H. et al./自然 (CC BY 4.0)
接下来,我们观察到乳酸处理的癌细胞中受损的 DNA 比未处理的细胞更有效地修复,这表明乳酸通过促进 DNA 修复来增强肿瘤对化疗的抵抗力。使用各种技术,包括 4D 无标记蛋白质组学,我们发现乳酸通过一种称为 NBS1 的蛋白质介导化疗耐药。NBS1 与其他两种蛋白质(称为 MRE11 和 RAD50)一起形成 MRN 复合物。该复合物是激活 ATM 激酶所必需的,ATM 激酶是一种酶,是细胞对 DNA 损伤反应的关键调节因子。源自乳酸的乳酰基通过一种称为 TIP60 的酶添加到 NBS1 的 K388 残基中。K388 位于 NBS1 和 MRE11 相互作用的表面,其乳酰化促进 MRN 复合物的形成,增强 DNA 修复和介导耐药性。此外,ATM 活性的遗传或药理学抑制降低了 TIP60 介导的 NBS1 K388 乳酰化以及 MRE11-RAD50 和 NBS1 之间的相互作用。因此,ATM 在 TIP60 介导的 NBS1 乳酰化和 MRN 复合物的形成中发挥作用。
研究意义
尽管以前的研究提供了癌细胞偏爱产生乳酸的糖酵解的明确证据,但癌细胞如何使用乳酸以及这种营养素在癌症生物学中的作用仍不完全清楚。我们的研究表明癌细胞如何利用厌氧糖酵解产生的乳酸来支持化疗耐药性。高水平的乳酸会增加 NBS1 在 K388 残基处的乳酰化。具有增强 MRN 复合物形成和 ATM 活化的作用,从而促进癌细胞中 DNA 损伤的修复。高水平的 NBS1 K388 乳酸化可能是一个预后因素,表明术前化疗可能无效,我们的研究结果确定乳酸剥夺是提高化疗疗效的潜在治疗策略。这些发现可能激发了测试斯替戊醇(或其他 LDHA 抑制剂)与 DNA 损伤化疗联合使用的临床试验。此外,介导 NBS1 乳酰化的 TIP60 也可以作为药理学靶标。未来,减少 NBS1 乳酸化的药物可用于预防化疗耐药性,这是癌症治疗中的一个关键挑战。— Axel Behrens 在英国伦敦癌症研究所乳腺癌研究中心 Toby Robins 研究中心的癌症干细胞实验室工作,张昌华在中国深圳中山大学附属第七医院工作。
同行看法
本文介绍了一项有趣且具有潜在临床相关性的研究,该研究将癌症中乳酸产生的增加以及随后的关键蛋白的乳酰化与 DNA 修复联系起来。它可能会在癌症治疗耐药领域开辟一个新的方向。— Timothy Wang 在美国纽约哥伦比亚大学哥伦比亚大学欧文医学中心工作。
论文背后故事
中国深圳的C.Z和英国伦敦的A.B实验室有着悠久的合作记录4.当 A.B. 于 2018 年访问深圳时,我们讨论了如何最好地建立患者来源的类器官 (PDO)。随后建立的胃癌 PDO 是我们研究的重要模型系统。在确定乳酸是化疗耐药的标志后,我们合作研究了其功能背后的分子机制。在这项工作期间,第一作者之一 Huafu Li 作为博士后研究员从深圳搬到伦敦。我们建立了有效的国际合作,使我们能够确定乳酸在化疗耐药性中的作用。— A.B. 和 C.Z.
《自然》编辑的看法
这篇论文之所以脱颖而出,是因为它属于癌症代谢的一个新兴领域,在该领域中,代谢物的非常规功能将代谢与其他生物过程联系起来。糖酵解代谢和 DNA 修复之间的联系令人兴奋,因为它解释了为什么一些肿瘤对化疗有耐药性,并可能有助于开发新的治疗组合。— Barbara Marte,Nature 高级编辑
https://wap.sciencenet.cn/blog-41174-1448099.html
上一篇:CD40L是自身免疫疾病治疗的理想靶点
下一篇:氢果冻治疗抑郁症的小鼠研究2024