 精选
精选
杂说生活中的碳(1)碳的单质
我曾经写过杂说生活中的化学元素系列博文,介绍了我们生活中的一些常见化学元素,但是对碳元素却没有专门写文章介绍。其原因实在很简单,因为碳元素对于我们实在是太重要了,组成我们身体的分子,除了水分子之外,几乎都含有碳元素。也正因为碳元素对于我们的身体、生活太过重要,所以用一篇文章来说,就不知道从哪里说起,也不知道说些什么好。如今用几篇文章来专说生活中的碳。
碳元素是组成所有生物最重要的元素。传统上,人们把与生命有关的分子称为有机分子,而有机分子都含有碳元素,研究这些分子组成、性质和反应的学科便是有机化学。
我们要在这个世界上生存、生长,总需要能量。
吃饭,是补充能量,有饭吃,人才能活下去。煮熟的饭,才能更好吃。煮饭也需要能量。
有衣服穿,在冬天才不至于冻毙,如果天气特别冷,还需要取暖,做衣服、取暖都需要能量。
上面所说的这些能量,例如吃饭消化,给身体各部分供给能量,过程非常复杂,但是归根结底,这些能量都来自碳的氧化,即碳元素与氧元素结合生成二氧化碳。
C + O2 = CO2
生活中与这个化学反应方程式最接近的过程就是木炭的燃烧。这个化学反应是放热反应,以热的方式释放出能量。
木炭由干燥的树木在密闭的环境中加热而烧成。白居易的《卖炭翁》说:“卖炭翁,伐薪烧炭南山,满面尘灰烟火色,两鬓苍苍十指黑。”干燥树木的主要成分是纤维素和木质素,这两种化合物都由碳、氢、氧三种元素构成。在木材中,也有少量的蛋白质,这样,除了碳氢氧三种元素之外,还会有少量的氮元素和硫元素。在高温时,纤维素和木质素都会分解,其中的氢气和氧气(以及它们组成的水)和一部分碳以及木柴蛋白质中少量的氮元素和硫元素一起构成烟,散发在周围的空气中,所以烧炭的老翁是“满面尘灰烟火色”。碳的熔点非常非常高,所以在高温下,木柴中的碳元素仍然是固体,留下来的就是黑色的木炭。老翁搬动木炭,手不容易洗干净,就“两鬓苍苍十指黑”。
木炭基本上就是碳的单质了。它的燃烧就是上面所示的那个方程式。
如果我们直接燃烧干燥的木柴或者柴草(柴草的化学成分也主要是纤维素和木质素),那么就会产生火焰和烟气。
细心的朋友会看出来,上面的叙述中,有两个不同的“tan”字,一个是碳,另一个是炭。炭是传统的字,烧炭、木炭等传统生活词汇中都用这个字。作为化学元素,化学家新造了一个碳字,碳是一种非金属元素,它的主要几种单质在常温下都是固体。单质在常温下是固体的非金属元素,其名称用字都有石字旁。
碳元素的单质,过去的教科书上只说有石墨、金刚石和无定形碳。
石墨是一种矿产,很软,具有光泽,呈黑色。在石墨中掺入粘土可以制成铅笔的笔芯。由于刚发现石墨时人们误认为是铅,制成的笔就误称铅笔。以后约定俗成,也就不改了,就称铅笔。其实铅笔里并没有铅。掺入粘土的比例不同,铅笔里软硬程度或颜色深浅程度也不同。掺入粘土少的,铅笔划痕比较黑,英语black(黑),就用B表示。掺入粘土多的,写出来颜色浅而笔芯硬,英语hard(硬),用H表示。6B最软最黑,HB适中,6H最硬最浅。
金刚石是无色透明的晶体,在一般物体中硬度最大。打磨后作为昂贵的饰物。
所谓无定形碳就是木炭、焦炭、烟炱一类的炭。
1985年,人们发现了由60个碳原子组成的分子,C60。以后,人们发现一系列类似于C60的分子,称为富勒烯。本世纪初,人们又制备得石墨烯材料。这样,在最近的40年里,人们就得到了许多种新型的碳的单质。
为什么碳原子能够组成这些多形状和性质都大不相同的单质呢?
这是与碳元素的原子结构有关的。
碳元素是第六号元素。碳原子的原子核里有6个质子,核外有6个电子围绕原子核高速运转。6个电子分内外两层,2个电子在内层,不参与与其他原子的结合,4个电子在外层,可以与其他原子相互作用形成共价键从而连接起来。
根据传统的价键理论,两个原子可以各出一个电子,形成一个单共价键,简称单键。也可以两个原子各出两个电子,形成一个双键。有时候还可以形成叁键。有的时候还可以有多个原子,大家共享多个电子,形成所谓共轭键。
一个碳原子外层四个电子,可以与四个其他原子分别共形成四个单键。
在原子之间通过化学键形成分子时,总是要求使得分子的能量更低一点,这样的分子可以更加稳定。就像我们在地下放置一个球,这个球会滚到地势更低的地方一样,这个球滚到一个坑低,就稳定了。
一个碳原子形成四个单键,这四个单键相互分得最开,能量就更低。相互分得最开的方式,就是如下图所示的那样
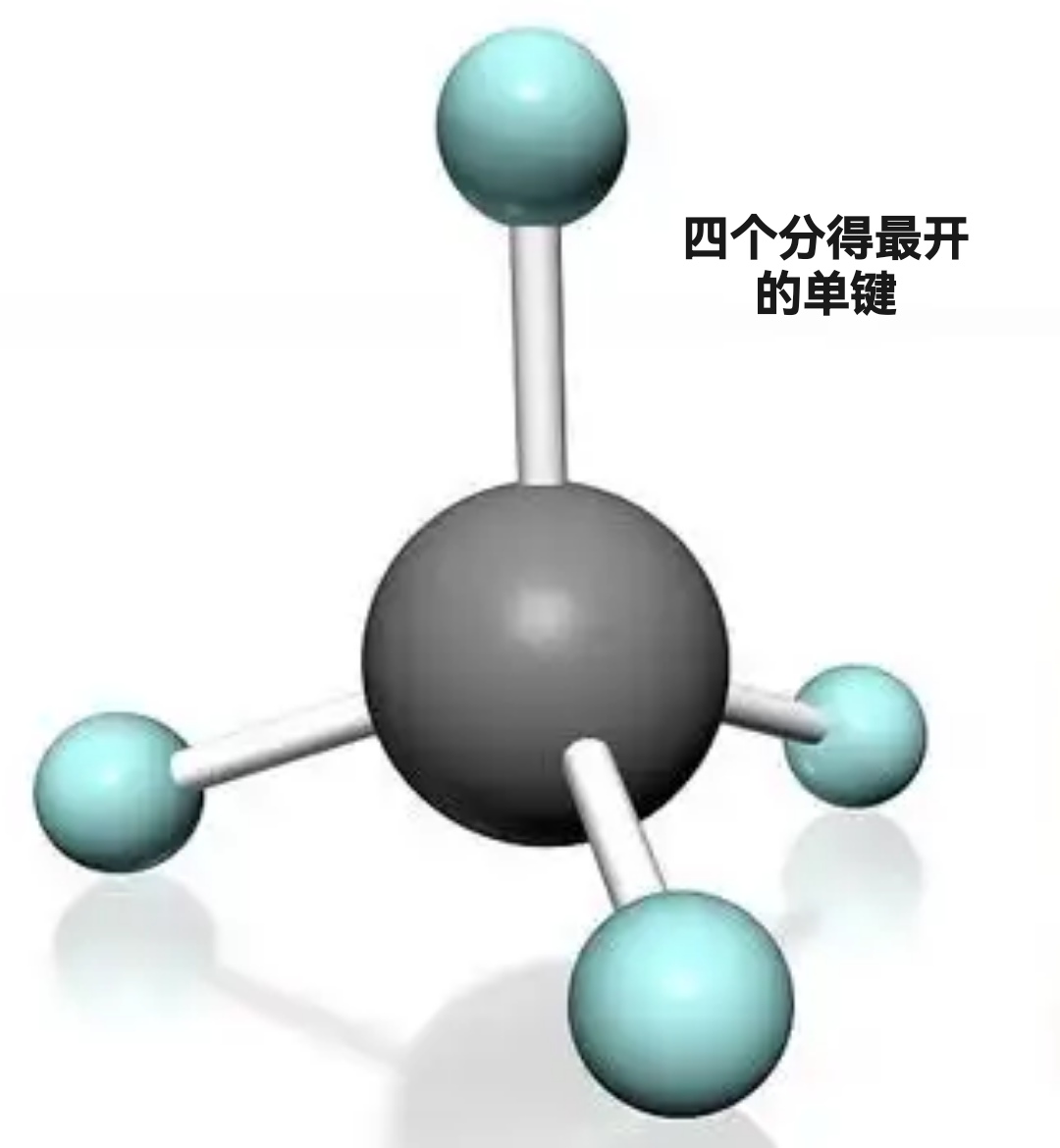
一个原子在中间,其余四个原子位于一个正四面体的四个顶点。
如果位于中心的原子是碳原子,与这个碳原子相连接的四个原子是氢原子,这个分子就是甲烷。我们现在家里燃烧的天然气,主要成分就是甲烷。
如果一个碳原子与四个其他碳原子连接,而每一个碳原子又都与其他碳原子相连接,这样许许多多个碳原子都连起来。如下图那样(图中只画出很少几个,实际上可能会有许多亿亿个),这样的物质就是金刚石。

在金刚石中,临近的两个碳原子间距为0.154纳米即154皮米(1米是10亿纳米,1纳米是1000皮米),相邻的三个原子之间的夹角是109°28′。
由于所有的碳原子都与其他四个原子组成一个不容易变形的四面体,这就使得金刚石非常坚硬。
一个碳原子可以与其他三个碳原子形成有四个电子的共轭键。如果每一个碳原子都是如此,许许多多碳原子就可以形成一个薄片,每六个碳原子形成一个正六边形。许许多多六边形组成一个大的平面。如下图所示,图中画出了上下共三层这样的薄片。
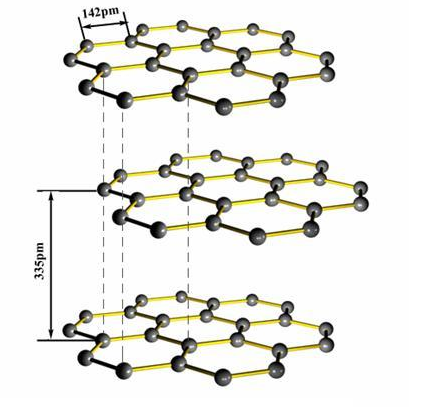
一个薄片就像一个巨大的分子。而薄片之间也有相当大的相互作用,这样的许多层组成了石墨的晶体。在石墨中,同一层中相邻碳原子的间距是142皮米。每两层之间距离是335皮米。由于两层之间距离大,相互作用就相对小了,所以层间就容易滑动。这就使得石墨很软,也容易被留在别的物体上从而形成黑色的划痕。
碳-碳之间的键,主要就是以上两种。所谓无定形碳,其微观结构,也就是这两种键,不过比较杂乱地排列罢了。其所以杂乱排列,主要原因是由于碳原子在结晶时处在高温状态,迅速结合的缘故。
例如,人们燃烧树木,火焰中含有碳原子,迅速冷却成黑烟,收集起来,就是烟炱,也就是炭黑,是一种无定形碳。古人收集炭黑,加入胶水,晾干后就是墨。炭黑现在又写作碳黑,约定俗成,两种写法都可以。
C60是由60个碳原子组成的球状分子。
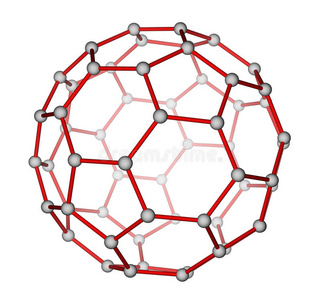
C60分子中相邻的碳原子构成了20个正六边形和12个正五边形。每一个五边形的周围是5个六边形,每一个六边形的周围是3个五边形和3个六边形。分子像一个足球的形状,中间是空的,所以又称笼状分子。
自从C60分子被发现以后,人们又发现了一系列类似的碳单质。
这些分子有的呈笼状,有的呈圆柱形;有的笼中有笼,有的管中有管。这些分子中碳原子的成键都有类似石墨那样的共轭键结构,因为这个分子与建筑学家巴克明斯特·富勒的建筑作品很相似,所以人们称之为富勒烯(Fullerene)。下图是一种圆柱状的富勒烯。
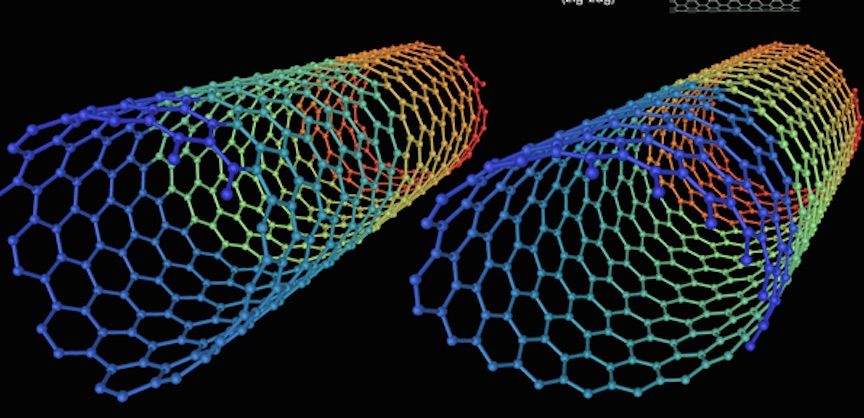
本世纪初,人们又制备成功单层的石墨,被称为石墨烯。
石墨烯和富勒烯具有特殊的光学性质、电导性及化学性质。它们的尺寸一般又都在纳米数量级,所以往往称纳米碳材料。
据说,纳米碳材料已应用于储能器件、传感器、复合材料及生物医学等领域,如航空航天中的高强度纤维、抗菌材料和光催化制氢技术。
转载本文请联系原作者获取授权,同时请注明本文来自冯大诚科学网博客。
链接地址:https://wap.sciencenet.cn/blog-612874-1507740.html?mobile=1
收藏

