氢水辅助粪菌移植治疗孤独症安全性与有效性试验
一种无需抗生素与肠道清洁、采用氢纳米气泡水的新型粪便微生物群移植疗法在孤独症谱系障碍儿童中的安全性与有效性:一项显示核心症状及共病症状改善的开放标签、单臂研究
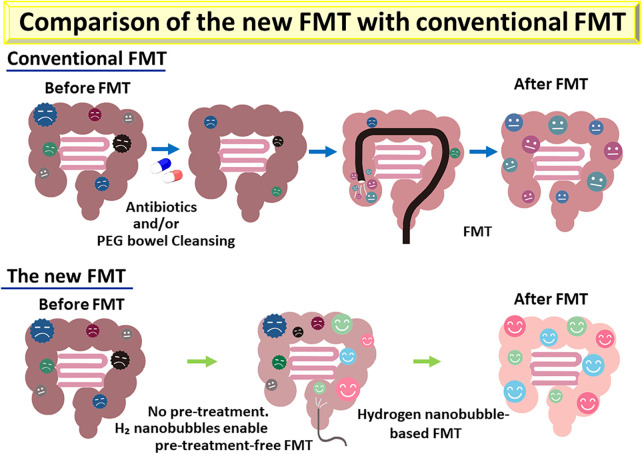
背景
孤独症谱系障碍(ASD)患病率持续上升,但其核心症状的有效治疗手段仍十分有限。粪便微生物群移植(FMT)展现出良好前景;然而,传统方法通常需要使用抗生素与肠道清洁准备,引发了对安全性与可持续性的担忧。本研究开发了一种基于氢纳米气泡水的新型粪便微生物群移植方法,并探究其疗效与安全性。
方法
本项前瞻性、单臂、自身前后对照研究纳入30名5–12岁孤独症谱系障碍患儿,严格按照纳入与排除标准筛选。将符合药品生产质量管理规范(GMP)级别的健康供体粪便微生物制剂SHIN‑1混悬于氢纳米气泡水中,经灌肠方式给药。主要结局指标为社交反应量表第2版(SRS‑2),并采用眼动追踪系统Gazefinder验证结果客观性。次要结局指标包括:感觉量表(简版感觉量表SSP)、胃肠道症状(胃肠道症状评分量表GSRS、布里斯托粪便性状量表BSFS)及患者健康问卷4项版(PHQ‑4)。统计学分析采用配对t检验或Wilcoxon符号秩检验(α=0.05)。
结果
治疗30周时观察到肠道微生物群重构,产短链脂肪酸菌及健康发育儿童中丰度较高的典型菌群显著增加。SRS‑2评分下降29%(p<0.001),疗效可持续至1年。严重程度分级改善如下:19例重度转为轻度,6例恢复至正常水平。无胃肠道共病患儿改善更为显著(45% vs 24%)。社交沟通与互动(SCI)、局限兴趣与重复行为(RRB)及其各子量表均得到一致改善;感觉、胃肠道及情绪症状改善幅度达30%–61%。研究期间未发生任何不良事件。
结论
这种基于氢纳米气泡水的新型粪便微生物群移植方法安全有效,可同时改善孤独症谱系障碍的核心症状与外周症状,提示其通过肠道微生物‑脑轴发挥广泛获益。
临床试验注册:jRCTs031230041
1 引言
孤独症谱系障碍(ASD)是一种神经发育障碍性疾病,其核心症状表现为持续性社交沟通与交往障碍、兴趣狭隘和重复性行为,以及感觉异常(1–3)。ASD发病率呈上升趋势,已成为重大社会问题。根据美国疾病控制与预防中心(CDC)2023年报告,2020年美国8岁儿童ASD患病率为1/36,较过去十年翻倍(4)。然而,目前仍缺乏针对ASD的有效治疗方法。
缓解ASD核心症状及其所致功能障碍的手段主要包括行为治疗和部分药物治疗。前者包括应用行为分析、社交技能训练(SST)、家长培训以及环境调整等多种行为疗法,已被证实有效(5,6)。但行为治疗需要进行详细的行为评估,高度个体化且依赖评估者的专业技能,质量保障难度较大。与此同时,非典型抗精神病药、选择性5‑羟色胺再摄取抑制剂和抗焦虑药物等药物治疗也被应用,但仅对外周症状有效,无法改善核心症状(7,8)。
因此,目前尚无能够为所有ASD患者提供稳定、持续疗效的有效治疗方案,亟需开发新型治疗方法。
ASD的发病机制尚未完全阐明,但遗传与环境因素被认为发挥重要作用。近年研究表明,肠道微生物群组成在ASD发病中具有关键作用,并可通过包含神经内分泌、神经免疫和自主神经系统在内的肠道微生物‑肠‑脑轴影响脑功能(9,10)。
Xu等人对超过1000名儿童(包括ASD患儿和正常发育儿童)的肠道微生物16S rRNA数据集进行分析后发现,尽管ASD组与正常发育组的肠道微生物α多样性无显著差异,但菌群组成存在显著差异(11)。此外,大量小鼠研究结果表明,肠道微生物群组成显著影响ASD核心症状(12,13)。
在这一研究背景下,通过干预肠道微生物群开发ASD治疗方法成为研究热点。
尽管针对益生元和益生菌开展了大量临床研究,但均未展现出明确且可重复的治疗效果(14,15)。另一方面,一项针对少数ASD儿童的万古霉素干预试验报道,患儿的沟通能力及部分行为异常等ASD特征得到显著改善(16)。然而,该疗效无法持续,数周内因梭菌芽孢形成而消失(16)。
与上述研究同步,研究者正在探索通过粪便微生物群移植(FMT) 重构肠道菌群组成、调控肠脑轴以治疗ASD(16)。
Kang等人对ASD儿童连续两周使用抗生素万古霉素,随后采用聚乙二醇(PEG)进行肠道清洁,再实施FMT(灌肠2天+口服给药50天)(17)。
该研究结果显示,FMT术后2年,经社交反应量表(SRS)评估,47%的重度ASD儿童病情改善至中度、轻度或正常水平。
但该方法需在FMT术前持续使用万古霉素(17),常引发不良事件。此外,还需进行PEG肠道清洁、FMT期间长期持续使用质子泵抑制剂,并输注大量供体菌群,这些流程对ASD儿童而言负担极大。
与之不同,Li等人在未使用万古霉素的情况下对ASD儿童实施FMT(尽管输注的粪便菌量约为Kang等人研究的100倍)。他们在PEG肠道清洁后通过灌肠或口服方式进行FMT。治疗后ASD严重程度虽有所降低,但疗效无法持久,随时间推移显著减弱(18)。
此外,Wu等人采用了一种相对患儿友好的方案:FMT术前3天每日口服利福昔明和聚乙二醇进行肠道准备,随后连续6天实施FMT。结果发现,治疗后3个月儿童孤独症评定量表(CARS)评分较基线降低14.6%,胃肠道症状等共病也得到缓解(19)。
上述结果表明,不使用万古霉素、利福昔明等抗生素,难以完成有效的FMT流程。因此,亟需一种无需抗生素、无需肠道清洁剂、低剂量(低菌量)且患儿友好的FMT方法。
近期,Shimizu等人开发了一种采用健康粪便与氢纳米气泡水制备的新型FMT方法,该方法无需使用抗生素,且可在极低剂量下完成FMT(20,21)。据此,本研究探究该新型FMT对ASD儿童的疗效与安全性。
2 材料与方法
2.1 研究设计
2.1.1 研究设计与伦理
本研究为前瞻性单臂、自身前后对照研究,研究流程如图1A、B所示。
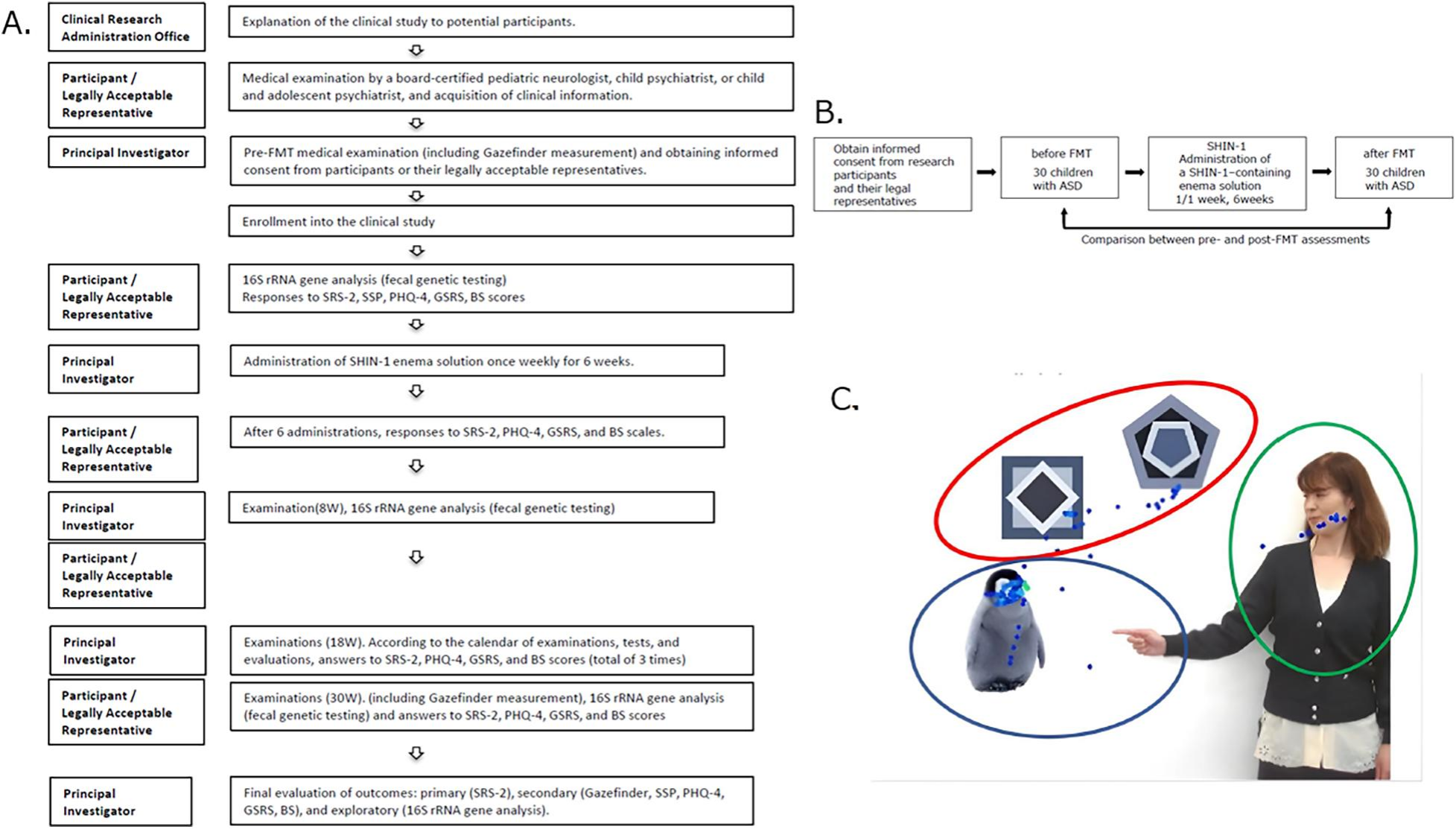
图1
A面板展示了详细的临床研究工作流程,明确了受试者、法定监护人和研究者的角色与操作步骤,涵盖从获取知情同意、医学检查到基因分析及结局评估的全流程。B面板呈现简化的研究时间轴,对比ASD儿童FMT术前与术后评估,重点为SHIN‑1灌肠液给药过程。C面板显示:右侧为一名女性,头部与身体周围标注眼动追踪点;左上角为红色高亮几何图形;左下角为蓝色圈出的企鹅图案。
研究方案与设计、评估图像(Gazefinder眼动仪)。(A)研究概述如下:左列为参与实施人员与科室,右列为研究具体内容。本临床研究中所有实施项目均按时完成。(B)本研究实验设计见图B,采用FMT术前术后自身对照设计。(C)Gazefinder所用图像。本研究证实,Gazefinder“指向图像”中受试者对人物与几何图形的注视时长,与SRS‑2核心维度社交沟通与交往(SCI)严重程度具有相关性,从而验证本研究SCI结果的客观性。
本研究经服部诊所认证审查委员会(CRB3180027)审批,所有操作均遵循《赫尔辛基宣言》。试验在首例受试者入组前于日本临床试验注册中心注册,注册号:jRCTs031230041。
2.1.2 受试者筛选
2.1.2.1 纳入标准
1. 年龄5–12岁,经儿童神经科医师、认证精神科医师、认证儿童青少年精神科医师或认证儿童精神科医师确诊为ASD(需提供诊断证明,性别不限);
2. 除胃肠道症状外,总体身体健康(由主要研究者判定);
3. 受试者本人可签署书面知情同意,必要时可采用图示或口头同意;
4. 法定监护人签署书面知情同意。
2.1.2.2 排除标准
1. 正在接受药物治疗者;
2. 近3个月内使用过抗生素(局部抗生素除外);
3. 近12个月内接受过粪便微生物群移植者;
4. 存在单基因病伴ASD样症状(如脆性X综合征、Rett综合征、Joubert综合征等,可能影响疗效评估);
5. 有神经外科手术史或患有神经系统疾病者;
6. 管饲喂养者;
7. 体重不足/营养不良(低于理想体重65%);
8. 近1年接受过手术或未来6个月计划手术者;
9. 正在参与其他临床试验者;
10. 主要研究者判定其他不适合参与研究者。
2.1.2.3 受试者人口学特征
受试者年龄、性别、身高、体重、体重指数(BMI)及ASD严重程度见表1。
表1 研究受试者人口学特征
本研究受试者男女比例约为3:1。
与此同时,信州大学Shinoyama等人近期开展的一项大规模研究显示,2009–2019年日本出生的约600万儿童中,约21万被确诊为ASD,其中男性占76.1%,女性占23.9%(22)。
这表明本研究受试者性别比例符合日本全国平均水平。
30名受试者中,1例经儿童神经科医师确诊ASD,但其SRS‑2原始总分为42分(T分:56分),处于正常范围。详见后续章节,给药24周后该分数降至27分(T分:48分)。
2.1.3 知情同意
向受试者监护人书面说明研究内容并获取同意;同时根据需要以书面、图示或口头方式向患儿本人说明并获取同意。
2.1.4 SHIN‑1制备
下述SHIN‑1原液制备全流程均遵循试验用药品药品生产质量管理规范(GMP) 要求。
2.1.4.1 供体筛选与粪便保存
研究者每2个月通过多项检测与访谈筛选6名候选供体,同时采用16S rRNA基因分析评估各供体粪便菌群组成。最终选定1名健康状态稳定、粪便菌群组成最稳定的供体(各项检测与基因分析结果见补充材料2)。本临床试验使用该选定供体的粪便开展。
2.1.4.2 供体粪便采集与保存
采集的供体粪便经多项检测(补充数据),包括16S rRNA基因分析后,于‑80°C保存。使用前24小时内逐步升温至2–8°C,用于制备SHIN‑1。
2.1.4.3 氢纳米气泡水
氢纳米气泡水由Shinbiosis公司提供。水中气泡粒径大于200 nm,峰值约450 nm;气泡浓度为2.0×10⁹~7.0×10⁹个/mL。
2.1.4.4 SHIN‑1原液制备、质量控制与保存
室温(20±3°C)下,将约100 g粪便加入250 g氢纳米气泡水中,采用磁力搅拌器(搅拌子长度3 cm)搅拌约90分钟制成混悬液。该混悬液先后经2层、10层、再10层无菌纱布过滤,获得100–150 g SHIN‑1原液。原液稀释1000倍后,菌浓度达100–300个/μL,用于移植。采用一次性细胞计数板测定菌数。制备完成的SHIN‑1原液于2–8°C冷藏保存,在此条件下至少稳定3个月。
2.1.4.5 SHIN‑1灌肠液制备与给药
向SHIN‑1原液中加入生理盐水,每份溶液与100 g生理盐水混合配制灌肠液。分别取3 g、5 g、7 g、9 g、11 g、13 g SHIN‑1原液与100 g生理盐水混合,制备6种不同剂量灌肠液。SHIN‑1原液菌浓度为1×10⁸~3×10⁸个/mL。为最大程度减轻受试者不适,采用直径6.5 mm细软橡胶管给药,患儿对该给药方式抵触极小。
2.1.5 评估方法
以SRS‑2为核心,采用以下(a)–(e)评估体系评价新型FMT对ASD症状的疗效。具体而言,通过社交沟通与交往(SCI)、兴趣狭隘和重复性行为(RRB)评估ASD核心症状;采用简版感觉量表(SSP)评估RRB中的感觉处理障碍;同时测定SCI子维度:社交意识(Awr)、社交认知(Cog)、社交沟通(Com)、社交动机(Mot)。
2.1.5.1 社交反应量表第2版(SRS‑2)
SRS‑2基于DSM‑5 ASD诊断标准,包含SCI和RRB两个量表。SRS‑2原始总分用于评估干预降低ASD严重程度的效果;子项目原始总分则评估各维度严重程度的改善幅度,可全面评价新型FMT的疗效范围与效应量。
ASD严重程度按SRS‑2原始总分划分:重度(>76)、中度(66–75)、轻度(60–65)、正常(<59)。FMT术前术后不同严重程度分级的病例数变化,以校正性别与年龄后的总T分表示。
目前,孤独症诊断观察量表(ADOS)和孤独症诊断访谈修订版(ADI‑R)被公认为ASD诊断金标准,也用于评估儿童ASD严重程度。但此类评估需经严格培训的持证专业人员与家长协作完成,专业人员数量有限,且行为观察与访谈耗时较长,对家长和儿童均造成较大负担。
相比之下,SRS‑2由家长填写、评估者计分,克服了上述局限,可简便、准确地评价新型FMT的疗效。
2.1.5.2 Gazefinder眼动仪
如前所述,作为主要结局指标的SRS‑2已被证实具有高诊断准确性且偏倚小(23,24)。为确保SRS‑2结果可靠无偏,本研究采用ASD客观检测工具Gazefinder作为对照验证结果。Gazefinder对ASD的诊断价值已得到广泛研究(25,26)。Fujioka等人报道,Gazefinder可基于ASD特异性“社交信息”注意模式评估其“社交缺陷”,在区分ASD儿童方面具有高诊断准确性(27,28)。本研究证实,Fujioka等人所用Gazefinder提示图像(图1C)中人物与几何图形的注视时长,与SRS‑2核心维度SCI严重程度相关,支持SRS‑2结果的客观性(27)。
2.1.5.3 简版感觉量表(SSP)
采用SSP评估FMT术前术后新型FMT对感觉过敏、感觉迟钝及反应低下/感觉寻求的疗效。
2.1.5.4 胃肠道症状评分量表(GSRS)与布里斯托粪便性状量表(BSFS)
采用GSRS评估新型FMT对存在胃肠道异常受试者的胃肠道症状疗效;通过BSFS评分变化,评估30名受试者便秘与腹泻改善情况。
2.1.5.5 患者健康问卷4项版(PHQ‑4)
采用PHQ‑4及其子量表抑郁量表(PHQ‑2)、广泛性焦虑量表2项版(GAD‑2),评估新型FMT对伴抑郁/焦虑症状受试者的抑郁、焦虑缓解效果(29)。
2.1.5.6 统计学分析
本研究采用MedCalc软件(22.023版,比利时MedCalc软件公司)进行统计学分析,方法如下:若移植前后临床指标(如SRS‑2)差值符合正态分布,采用配对t检验;若不符合正态分布,采用Wilcoxon符号秩检验。显著性水平(P值)设为5%,P<0.05为差异具有统计学意义。采用Shapiro–Wilk检验进行正态性检验。
3 结果
3.1 新型FMT方法对肠道菌群的重构
与既往研究(30–33)不同,本新型FMT方法不使用抗生素与肠道清洁剂,仅以极低剂量制剂即可对孤独症谱系障碍(ASD)儿童的肠道菌群进行重构并维持稳定。
图2展示了供体及受试者移植前后肠道菌群组成的16S rRNA基因分析典型结果。治疗结束24周后,对肠道环境与免疫系统具有重要作用的产短链脂肪酸拟杆菌属(Bacteroides)丰度升高,治疗前水平偏低的拟杆菌属得到提升。
此外,在ASD儿童中罕见、而在正常发育儿童中丰富的梭菌簇XVIII(Clostridium.Cluster XVIII)丰度升高;在ASD儿童中较少见、正常发育儿童中更常见的普雷沃氏菌属(Prevotella)、阿克曼菌属(Akkermansia)、梭杆菌属(Fusobacterium)和单形拟杆菌(Bacteroides uniformis)丰度亦显著升高(34–38)(图2)。
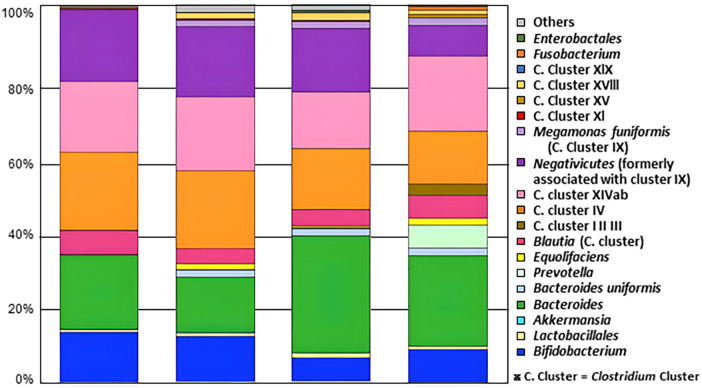
图2
堆叠柱状图显示各肠道菌群类群相对丰度,每种颜色对应右侧色标中不同菌属或簇。
SHIN‑1给药前后ASD儿童肠道菌群组成变化。数据为供体与受试者FMT(SHIN‑1治疗)前后肠道菌群组成16S rRNA基因分析典型结果,观测时点为治疗结束后24周。SHIN‑1自第1周至第6周每周给药1次,共6剂。
3.2 新型FMT的疗效
3.2.1 SRS‑2
以SRS‑2评估新型FMT对ASD严重程度的改善作用,评估时点为FMT启动前、第6、10、14、18及30周。图3A结果显示,新型FMT可显著改善ASD儿童症状:30例受试者ASD严重程度较FMT前降低约29%(p<0.001)。
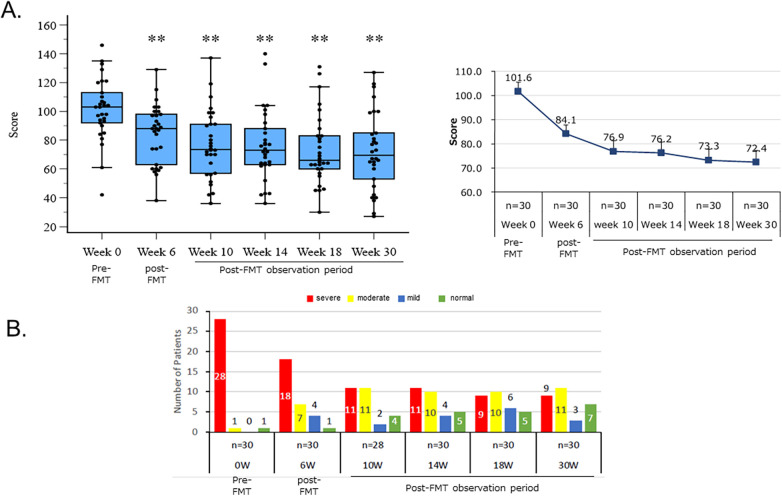
图3
A面板包含两幅图表,总结30例患者FMT治疗前后多时点症状评分。左侧箱线图(含个体数据点)显示自第0周至第30周中位评分持续下降,FMT后差异具有统计学意义;右侧折线图显示平均评分由基线101.6降至30周72.4。B面板为分组柱状图,显示各时点重度、中度、轻度、正常分级病例数,随时间推移呈现由重度向轻度/正常转化的趋势。
新型FMT对ASD严重程度的改善作用。(A)以SRS‑2原始总分评估新型FMT对ASD严重程度的改善。基线(Pre)与SHIN‑1干预30周后(Post)SRS‑2原始总分箱线图。*p<0.001,配对t检验或Wilcoxon符号秩检验。(B)FMT前后不同严重程度病例数变化。每列代表病例数,严重程度按SRS‑2总T分划分:红色=重度,黄色=中度,蓝色=轻度,绿色=正常。
图3B进一步展示FMT给药前及给药30周后严重程度分级病例数变化(按性别与年龄校正SRS‑2总T分)。
FMT前,30例受试者中28例重度、1例中度、1例正常;FMT30周后,28例重度患者中19例(约68%) 及1例中度患者转为轻度,总计20例(约69%) 症状改善,其中6例转为正常。结果表明,新型FMT可显著降低ASD严重程度(图3B)。
既往Kang等与Li等研究中所有受试者均合并胃肠道症状(30–33),而本临床试验纳入22例合并胃肠道症状、8例无胃肠道症状患者,并按有无胃肠道症状分层分析。
合并胃肠道症状的22例受试者ASD严重程度降低24%(p=0.001);无胃肠道症状的8例降低45%(p<0.001),平均SRS‑2评分进入正常范围(数据未展示)。该结果与既往报道相比具有重要意义,有待进一步研究验证。
3.2.1.1 SRS‑2亚量表(SCI与RRB)
图4A、B为符合DSM‑5 ASD诊断标准的社交沟通与交往(SCI) 及狭隘兴趣与重复行为(RRB) 评估结果。
30例受试者SCI平均总分由FMT前80.3降至30周后58.1,降幅28%(p<0.001),与图3所示ASD总体严重程度降幅相当。
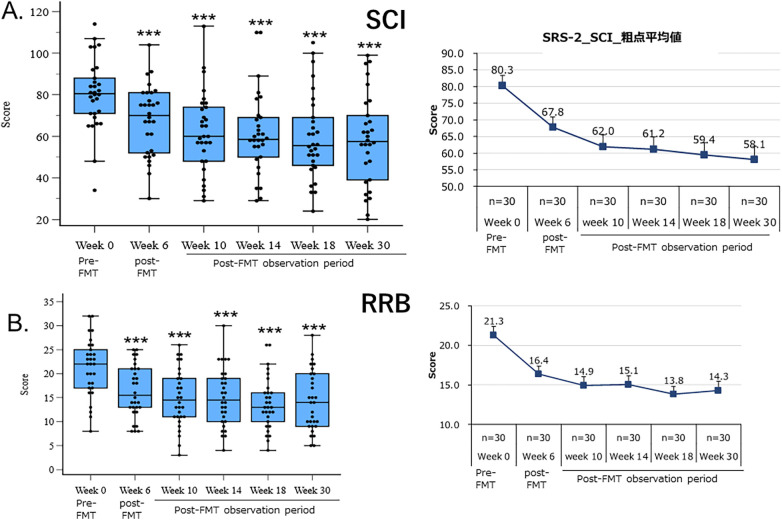
图4
新型FMT对SRS‑2亚类严重程度的改善作用。上图:SCI;下图:RRB。(左)SRS‑2 SCI箱线图,配对t检验或Wilcoxon符号秩检验(FMT后 vs FMT前);*p<0.001。(右)SCI平均评分变化,数据点为n=30的均值±标准误。
同时评估新型FMT对RRB严重程度的影响(图4B):30例受试者RRB平均评分由FMT前21.3降至30周后14.3,降幅约33%(p<0.001)。RRB降幅与ASD总体及SCI降幅相近,提示新型FMT对ASD的改善作用可覆盖SCI与RRB两大核心症状(图4A、B)。
3.2.1.2 SCI亚量表
SCI亚量表包含4项:社交意识(Awr)、社交认知(Cog)、社交沟通(Com)、社交动机(Mot)。新型FMT对各项的改善作用见补充图S1:
- Awr:降幅24%(p<0.001)
- Cog:降幅25%(p<0.001)
- Com:降幅27%(p<0.001)
- Mot:降幅36%(p<0.001)
社交动机(Mot)降幅略高于SCI总体降幅(28%),其余项目降幅相近。结果表明,新型FMT对ASD的改善在SCI与RRB亚类中分布均匀,且在SCI四个亚项中亦呈均衡改善。
3.2.2 Gazefinder眼动仪
本研究以符合DSM‑5诊断标准的SRS‑2作为主要疗效指标,但SRS‑2由家长填写、研究者评分,无法完全排除偏倚。因此,为验证SRS‑2评估可靠性,本研究同步采用ASD客观辅助诊断工具Gazefinder进行对照。
使用图1C所示指向性视频(39),分析SRS‑2社交核心维度SCI与Gazefinder社交评估结果的相关性。
排除3例完全未注视几何图形或人物的受试者,共27例纳入分析。
结果显示:
- SCI严重程度与注视几何图形时长呈显著正相关
- 与注视人物时长呈显著负相关
证实SRS‑2核心维度SCI可靠性高、偏倚极小。
3.2.3 简版感觉量表(SSP)
感觉处理障碍是ASD核心症状之一(尤其属于RRB范畴),约90% ASD患者存在感觉过敏、感觉迟钝、反应低下/感觉寻求等异常(40,41)。
既往针对ASD感觉处理障碍多采用感觉统合治疗(如Ayres感觉统合疗法ASI)及环境调整,虽有阳性报道,但高质量证据仍有限(42);尚无通过益生元、益生菌或FMT等肠道菌群干预治疗感觉处理障碍的尝试,本研究为首次。
本研究对26例经SSP确诊存在感觉处理障碍的受试者,评估新型FMT对感觉过敏、感觉迟钝、反应低下/感觉寻求的改善作用。
如图5A所示,新型FMT使感觉处理障碍严重程度降低约30%(p=0.001),SHIN‑1给药30周后SSP评分最低降至38分。
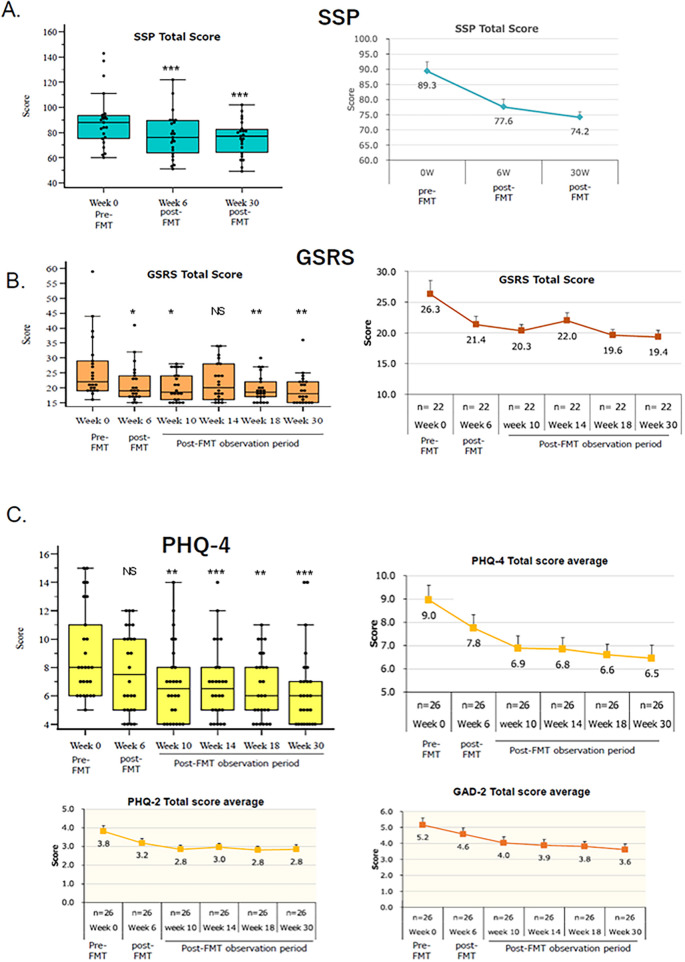
图5
新型FMT对感觉处理障碍及ASD相关症状(胃肠道症状、焦虑抑郁)的改善作用。(A)对感觉处理障碍严重程度的改善。(左)SSP总分箱线图,Wilcoxon符号秩检验(FMT后 vs FMT前);*p<0.001。(右)SSP平均总分变化,数据点为n=22的均值±标准误。(B)对胃肠道症状的改善。(左)GSRS总分箱线图,Wilcoxon符号秩检验;*p<0.05,p<0.01,NS=无统计学意义。(右)GSRS平均总分变化,n=22。(C)对焦虑抑郁症状的改善。(左上)PHQ‑4总分箱线图;*p<0.001,p<0.01。(右上)PHQ‑4平均总分变化,n=26。PHQ‑4由PHQ‑2(抑郁量表)与GAD‑2(焦虑量表)组成。(左下)PHQ‑2平均总分变化,n=26。(右下)GAD‑2平均总分变化,n=26。
补充图S2显示,新型FMT对感觉过敏、感觉迟钝、反应低下/感觉寻求均有显著改善,降幅分别为28%、23%、28%。
感觉处理障碍总体降幅约30%,各亚成分降幅23%–28%,与ASD总体降幅(29%)无显著差异。
3.2.4 GSRS与布里斯托粪便性状量表(BSFS)
多项研究显示30%–70% ASD患者合并胃肠道症状(43,44),最常见为腹痛(59%)、便秘(51%)、腹泻(43%)(43,44)。
以抗生素(16)、益生元、益生菌、FMT等靶向肠道菌群的治疗可改善行为与症状(45–48);Kang等采用抗生素联合FMT对胃肠道症状取得良好效果(17)。
本研究以GSRS与BSFS评估新型FMT对胃肠道症状的疗效:
- GSRS:评估FMT前30例中22例存在胃肠道症状者
- BSFS:评估所有受试者
图5B显示,新型FMT使胃肠道症状严重程度降低约61%(p=0.001),最低降至15分,效应量显著高于ASD核心症状降幅;平均评分降至19.4,接近正常基线15分,多数患者趋于正常。
BSFS为7级粪便分类量表:1–2级为便秘硬便,3–4级为正常,5–7级为软便至腹泻。
FMT前60%受试者为3–4级正常粪便;FMT后理想4级粪便比例逐步升高,30周达87%。
12例粪便异常受试者中约8例恢复正常,改善率67%,与胃肠道症状改善率(61%)一致,证实新型FMT对ASD相关胃肠道症状有效。
3.2.5 PHQ‑4(PHQ‑2与GAD‑2)
Lai等大型荟萃分析显示,ASD患者焦虑症状发生率42%–56%,抑郁症状12%–70%(49,50)。
本研究对26例(占86.7%)合并焦虑抑郁症状的受试者采用PHQ‑4(PHQ‑2+GAD‑2)评估疗效。
如图5C所示,新型FMT使焦虑抑郁症状严重程度降低约50%(p<0.001),显著高于SRS‑2所示ASD核心症状降幅(约29%)。
3.3 新型FMT的不良事件
本临床试验30例受试者中未观察到任何不良事件(包括轻度)。
既往ASD‑FMT研究(17,18,30)无严重不良事件,仅少数病例出现轻度不良事件。
近期传统FMT不良事件调查显示总发生率24%(1347/5688),严重不良事件6%(246/4241)(51,52)。
尽管本研究样本量较小,但结果提示新型FMT不良事件发生率更低,未来大样本队列研究将进一步验证其安全性。
4. 讨论
本研究采用自身前后对照研究而非随机对照试验,评估新型粪便微生物群移植(FMT)疗法对孤独症谱系障碍(ASD)的疗效,原因有二:
(1)FMT治疗ASD属于新型疗法,为确认其有效性与安全性,采用可详细观察治疗前后变化的探索性研究更为合适。
(2)以ASD儿童为研究对象时,将患者随机分配至治疗组或安慰剂组的随机对照试验存在较高伦理门槛,且当患儿家长预期该潜在疗法有效时,可能对被分配至安慰剂组产生抵触。因此,本研究选择所有患者均先接受治疗并观察变化的自身前后对照设计。
4.1 社交反应量表第2版(SRS‑2)
本研究所用SRS‑2由家长填写、评估者计分,无法完全排除偏倚。但SRS‑2的诊断效能已在包含大量ASD儿童与正常发育儿童的大规模研究中得到充分验证。
研究采用受试者工作特征(ROC)曲线衍生指标(包括曲线下面积AUC、灵敏度、特异度、阳性预测值、阴性预测值)评估SRS‑2(或SRS)的诊断效能,各项指标稳定维持在80%~90%以上(22,23)。
此外,将SRS‑2(及SRS)与孤独症诊断观察量表(ADOS)、孤独症诊断访谈修订版(ADI‑R)的诊断效能对比后证实:SRS‑2具有良好的评定者间信度、高内部一致性,且与ADOS、ADI‑R、社交沟通问卷(SCQ)具有良好的聚合效度(23,24,53)。因此,SRS‑2目前已被视为客观评估方法。
为进一步验证由家长填写的SRS‑2结果无偏倚,本研究同时采用眼动检测设备Gazefinder进行客观验证,该工具已被证实与SRS‑2社交技能指标具有相关性。
4.2 新型FMT对ASD核心症状的疗效
本研究对共30例受试者(SRS‑2评定:重度28例、中度1例、正常1例)给予含氢纳米气泡水的粪便微生物制剂SHIN‑1进行新型FMT治疗。
结果显示,FMT治疗6周后受试者SRS‑2严重程度评分即显著改善;30周后评分统计学显著下降约30%。
按严重程度分级人数变化分析:28例重度+1例中度受试者中,20例中有19例转为轻度(含正常),疗效显著。
与之不同,既往FMT治疗ASD的疗效研究(17,18,30,54)仅纳入合并胃肠道症状的ASD儿童。
本临床试验30例受试者中,22例合并胃肠道症状,8例无胃肠道症状,新型FMT在两组间疗效差异显著:
- 合并胃肠道症状的ASD儿童:症状降低24%
- 无胃肠道症状的ASD儿童:症状降低45%,FMT后平均SRS‑2评分进入正常范围
多数探讨ASD症状与胃肠道症状关系的既往研究认为胃肠道症状与ASD严重程度无关(55,56),但亦有报道提示存在相关性,目前尚无明确结论(57)。
本临床试验结果证实FMT疗效因是否合并胃肠道症状存在显著差异,是一项具有创新性的重要发现。未来将扩大样本量(纳入无胃肠道症状的ASD亚组),并探索进一步提升合并胃肠道症状ASD儿童FMT疗效的方法。
此外,新型FMT使ASD两大核心症状社交沟通与交往(SCI)、狭隘兴趣与重复行为(RRB) 均降低约30%;该效应同样见于SCI四个亚量表(社交意识、社交认知、社交沟通、社交动机)及RRB包含的感觉处理障碍,降幅与ASD总体严重程度降幅相近。
关于感觉处理障碍,Watanabe等(58)近期研究提示:ASD核心症状(如兴趣狭隘)等感觉症状与高级认知症状可能存在共同神经基础,这可解释新型FMT对RRB(兴趣狭隘与重复行为)与感觉处理障碍症状的降幅相近。
值得注意的是,新型FMT的疗效还延伸至ASD儿童常见的胃肠道症状、抑郁与焦虑症状,降幅分别为61%、56%、50%,约为ASD核心症状疗效的两倍。
综上,新型FMT仅通过FMT单一手段即可实现对ASD症状的高效治疗,且疗效范围与幅度不仅覆盖ASD核心症状(及其亚类如感觉处理障碍,被认为具有不同神经基础),还可改善胃肠道、抑郁、焦虑症状,体现出广泛而全面的作用特点。
上述结果证实:基于肠道菌群的FMT干预可通过肠‑脑轴广泛影响脑功能。
本研究未观察到任何不良事件,这一点尤为重要。既往研究无严重不良事件,仅2~3例轻微不良事件(17,18);而近期现有FMT不良事件调查显示,26%患者出现不良事件(含严重事件)(51,52)。与之相比,新型FMT显示出卓越的安全性。
此外,本临床试验结果证实:新型FMT无需联用抗生素,仅通过极低剂量微生物制剂即可有效实现菌群定植、重构与维持,是一种高安全性方法。
因此,尽管仍需进一步验证,该新型FMT或可成为比传统方法更安全、更有效的替代方案(18,30)。
如前所述,新型FMT与既往方法不同,不使用抗生素即可维持疗效,但目前其内在机制尚不明确。
近期研究表明,富氢水(HRW) 可抑制肠道炎症、维持肠道屏障完整性,并激活产丁酸菌(59–63)。已有报道证实:厌氧条件下制备的微生物悬液可促进专性厌氧菌定植增殖、抑制致病菌生长(64)。
此外,氢纳米气泡水具有强还原性,可有效清除活性氧与活性氮(65)。
基于上述特性,我们提出假设:氢纳米气泡水可同时促进移植微生物悬液中专性厌氧菌定植增殖,并抑制致病菌生长。
本研究结果提示:采用氢纳米气泡水在厌氧条件下制备的微生物悬液进行FMT,可促进短链脂肪酸产生、降低肠道pH、提升拟杆菌属等有益菌丰度、抑制致病菌生长。这些变化可改善大脑神经递质失衡,助力ASD核心症状减轻,支持“氢纳米气泡水FMT对肠道菌群组成与宿主生理具有有益作用”的假说。
此外,本临床试验严格按照药品GMP标准对SHIN‑1进行质量控制。
为维持SHIN‑1菌群组成稳定(质量核心要素之一)并保证移植结果可重复性,本研究使用同一供体粪便制备的SHIN‑1。
采用上述质量可控的SHIN‑1开展为期30周的临床研究,30例受试者未发生任何不良事件。
为广泛推广该新型FMT,需建立利用多供体粪便制备菌群组成比例稳定的供体菌液方法。目前本团队正开展相关供体菌制备研究,并计划采用该新型FMT开展后续临床试验。
5. 局限性
本研究存在若干局限性:
第一,本研究为无随机对照组的自身前后对照研究,无法完全排除安慰剂效应、均值回归或自然发育轨迹的影响;但改善幅度、持续性,结合客观眼动与微生物组数据,不支持单纯非特异性效应解释。
第二,样本量偏小(n=30),限制亚组分析(如胃肠道症状组vs无胃肠道症状组、年龄、性别)的统计学效能。
第三,仅使用单一供体:虽提升标准化程度,但限制外推性,且无法评估供体特异性效应。
第四,尽管评估了多个临床领域,但未纳入直接认知或学业表现指标,而此类指标对理解功能结局具有重要意义。
第五,微生物组分析虽证实整体重构,但尚未明确精准的疗效微生物“特征”,需进一步开展宏基因组与代谢组分析。
最后,所有受试者均在日本招募,文化或医疗体系差异可能影响对其他人群的外推性;但肠‑脑轴生物学机制在不同人群中大概率具有普遍性。
6. 未来方向
未来研究应优先开展:
1. 随机、安慰剂对照试验,对比SHIN‑1与标准治疗及/或传统FMT。
2. 剂量‑反应与时序研究,确定最佳方案、加强剂量及疗效超过1年的持久性。
3. 基于胃肠道表型、基线微生物组组成、临床特征的分层分析,明确疗效预测因子。
4. 机制研究:整合宏基因组、代谢组(如短链脂肪酸、胆汁酸)、免疫标志物与神经影像学,阐明菌群变化关联脑功能的通路。
5. 在阐明氢纳米气泡核心作用基础上,通过SHIN‑1给药前及给药期间单独额外给予氢纳米气泡水,开发更高效FMT方法。
6. 纵向发育随访(含认知、适应能力、教育结局),评估早期菌群靶向干预能否改变ASD长期发育轨迹。
若研究结果可被重复与拓展,SHIN‑1及相关氢纳米气泡FMT技术或可为神经发育障碍建立一类新型微生物治疗药物。
7. 结论
本项采用含氢纳米气泡水粪便微生物制剂(SHIN‑1) 的新型FMT疗法,可改善ASD核心症状与共病症状。
该疗法无需抗生素、无需肠道清洁,且移植菌量低于传统FMT,有望成为可持续、安全、患者负担更低的突破性治疗手段。
基于本临床试验获得的新发现,团队期望未来开展双盲临床试验。
转载本文请联系原作者获取授权,同时请注明本文来自孙学军科学网博客。
链接地址:https://wap.sciencenet.cn/blog-41174-1527692.html?mobile=1
收藏

