氢气吸入治疗阿尔茨海默病实验【韩国】
摘要
阿尔茨海默病(AD)是一种进行性神经退行性疾病,β‑淀粉样蛋白(Aβ)沉积、氧化应激(OS)与慢性炎症共同驱动突触功能障碍与认知衰退。分子氢(H₂)因具有选择性抗氧化与抗炎特性,成为潜在神经保护气体,但其在淀粉样蛋白介导病理中的作用机制尚未完全阐明。本研究将携带人源淀粉样前体蛋白(APP)与早老素‑1(PSEN1)突变的5xFAD转基因小鼠及同龄C57BL/6野生型小鼠,以2% H₂吸入干预,每日1小时,持续4周。
结果显示:H₂吸入可降低海马体活性氧(ROS)水平、提高全身过氧化氢酶活性、提升海马ATP含量;在血清中,H₂降低肿瘤坏死因子‑α(TNF‑α)与白介素‑1β(IL‑1β),恢复白介素‑10(IL‑10)水平,并部分纠正白介素‑13(IL‑13),使外周环境向低促炎表型转变;在海马体中,H₂上调核因子E2相关因子2(NRF2)、抑制核因子κB(NF‑κB)激活、降低BAX/BCL‑2比值、维持神经元核蛋白(NEUN)表达,并减少海马Aβ₄₂负荷。
综上,H₂吸入通过恢复氧化还原稳态、抑制炎症、改善线粒体功能、减少Aβ沉积,对5xFAD小鼠发挥多维度神经保护作用。
1 引言
阿尔茨海默病是一种以认知衰退与行为障碍为特征的进行性神经退行性疾病,核心病理特征包括:细胞外Aβ沉积、细胞内由过度磷酸化tau蛋白构成的神经原纤维缠结,以及广泛的突触功能障碍与神经元丢失。流行病学显示,AD占全球痴呆病例的60%–80%。随着人口老龄化加剧,痴呆发病率持续攀升,预计到2050年患者将达1.315亿,构成严峻公共卫生挑战。
尽管针对Aβ与tau病理已开展数十年研究,尚无疾病修饰疗法展现持续临床疗效,反映AD发病机制的复杂性与异质性。
越来越多证据表明,线粒体功能障碍、氧化应激、慢性神经炎症协同驱动AD神经退行性变。AD脑内线粒体氧化磷酸化受损、电子传递链不稳定,导致ROS过量生成、ATP合成减少,无法满足神经元代谢需求。过量ROS损伤线粒体DNA、膜脂质与蛋白质,破坏线粒体膜电位,促进线粒体通透性转换孔开放,共同降低细胞对Aβ毒性的耐受度。
生理状态下,NRF2通路通过诱导谷胱甘肽过氧化物酶(GPX)、过氧化氢酶、血红素氧合酶‑1(HO‑1)等解毒与抗氧化酶,维持胞内氧化还原平衡。而在AD中,持续氧化应激与Aβ介导的NRF2信号抑制,削弱内源性抗氧化防御,使神经元在慢性氧化损伤下易发生功能异常与凋亡。
受损线粒体释放损伤相关分子模式(DAMPs),包括线粒体DNA片段与心磷脂,激活 toll 样受体(TLRs)、cGAS‑STING通路与NLRP3炎症小体等天然免疫通路,导致小胶质细胞持续激活,表现为NF‑κB持续信号活化与IL‑1β、IL‑6、TNF‑α分泌增加,进一步加剧突触丢失与神经元死亡。
目前获批的AD药物主要通过调节神经递质系统对症缓解,如乙酰胆碱酯酶抑制剂(多奈哌齐、加兰他敏、卡巴拉汀)与NMDA受体拮抗剂美金刚。近年疾病修饰疗法进展聚焦于靶向核心病理标志物的抗Aβ单克隆抗体(如仑卡奈单抗、多奈单抗),可促进小胶质细胞清除Aβ斑块,使早期AD患者认知与功能衰退降低约30%;同时也有靶向tau病理的聚集抑制剂与免疫疗法。
但AD发病的多因素性提示,仅靶向蛋白聚集不足以起效。全基因组关联研究已鉴定出APOE、TREM2、CD33等免疫相关易感位点,调控小胶质细胞功能与炎症反应,因此靶向炎症与氧化通路成为极具前景的互补治疗策略。
分子氢(H₂)是一种理化性质独特、安全性良好的小分子气体,作为神经退行性疾病多靶点潜在治疗剂备受关注。与无差别清除ROS的传统抗氧化剂不同,H₂选择性中和羟基自由基(·OH)与过氧亚硝酸盐(ONOO⁻)等高细胞毒性物质,同时保留参与生理信号的超氧阴离子与过氧化氢。因其分子极小且兼具两亲性,H₂可快速穿透生物膜(包括血脑屏障),高效分布于胞内并进入线粒体。
迄今已有超2000篇科学文献(体外、动物、人体研究)探索H₂的治疗潜力。大量临床前研究证实,H₂可抑制病理性ROS过量生成、稳定线粒体膜电位、促进线粒体自噬、激活NRF2/ARE通路,增强下游抗氧化酶表达。除抗氧化外,H₂还具有免疫调节活性:通过抑制线粒体ROS,阻断NF‑κB激活与NLRP3炎症小体组装,减少促炎介质产生。
在AD相关模型中,H₂可改善认知缺陷、降低脑内脂质过氧化、减少炎症因子表达,提示其可同时缓解氧化应激与神经炎症。临床观察也支持其全身保护作用,例如H₂吸入可减轻放疗相关骨髓损伤、保护外周白细胞、缓解放疗所致骨髓抑制;本团队既往研究也表明H₂可减少气道炎症细胞浸润,调节外周免疫应答、维持免疫稳态。
药代动力学上,H₂为惰性、高扩散性气体,不被酶代谢,快速溶于体液、经循环分布,最终通过呼气排出。因其分子小且非极性,可轻易进入线粒体,抑制线粒体ROS过量生成,维持线粒体膜电位与呼吸功能,稳定电子传递链、减轻ROS所致线粒体损伤,从而维持线粒体能量稳态。
由于线粒体ROS是氧化还原敏感炎症通路的上游调控因子,H₂对线粒体氧化还原平衡的调节可影响下游细胞因子产生。基于此,本研究选取TNF‑α、IL‑1β、IL‑6作为ROS依赖性炎症信号的代表性促炎因子,IL‑10作为关键抗炎介质,反映免疫反向调节。既往体内研究显示H₂可降低TNF‑α、IL‑1β、IL‑6,部分情况下升高IL‑10,提示H₂调节炎症因子谱而非非特异性抑制。
为在体内验证上述机制,本研究采用5xFAD转基因小鼠模型,评估H₂吸入对氧化应激指标、线粒体能量代谢、Aβ负荷与炎症谱的影响,旨在阐明H₂在淀粉样蛋白相关神经退行性变中协同抗氧化与抗炎的分子机制,评估其作为AD多靶点干预手段的可行性,为临床转化提供实验依据。
---
2 材料与方法
2.1 实验动物与氢气吸入方案
所有动物饲养与实验均符合延世大学原州医学院动物伦理委员会规定(伦理批准号:YWC‑250728‑1,批准日期:2025年8月4日)。选用2–2.5月龄雌雄小鼠,包括携带APP与PSEN1突变的5xFAD转基因小鼠与C57BL/6野生型(WT)小鼠。半合子5xFAD小鼠由转基因5xFAD与F1代C57BL/6交配获得,PCR鉴定基因型。
小鼠分4组(每组n=10,性别均衡:4雄6雌):WT‑Veh(野生型对照)、WT‑H₂(野生型+H₂)、5xFAD‑Veh(模型对照)、5xFAD‑H₂(模型+H₂)。H₂干预组采用2% H₂(混合气体:20.6% O₂、77.4% N₂),通过Hueprogen制氢装置在密闭暴露舱内每日吸入1小时,连续4周;对照组给予相同环境与处理,仅通入空气。2% H₂浓度与4周干预方案基于既往体内研究的安全性与有效性确定。
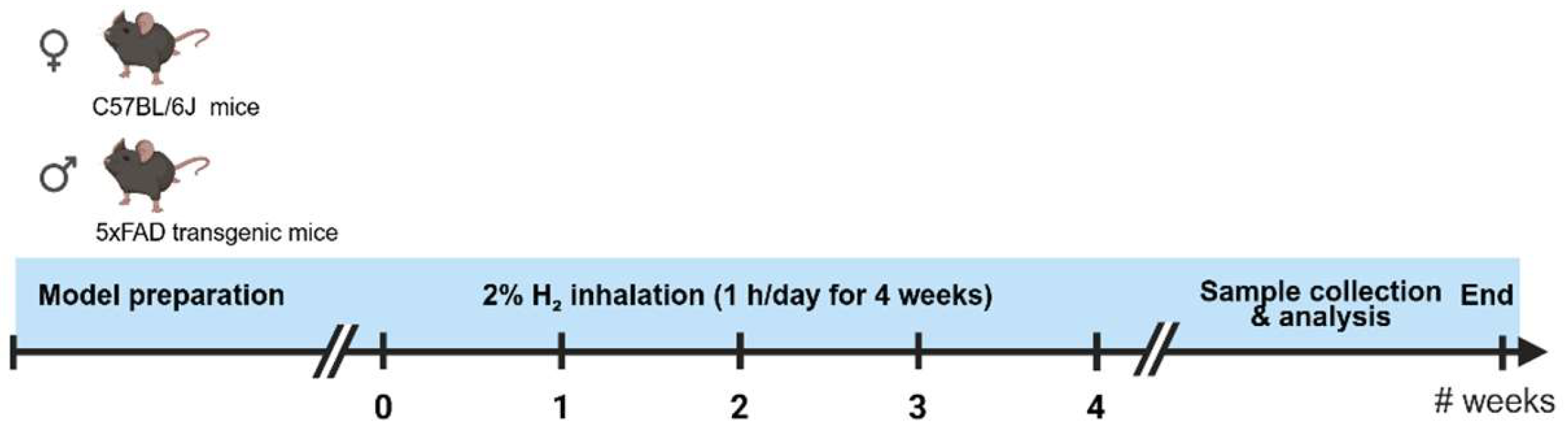
图1 实验设计
2.2 组织采集与样本制备
干预结束后,小鼠深度麻醉后CO₂安乐死,眼眶取血,离心分离血清,−80℃保存。快速取脑,冰上分离海马,液氮速冻后低温保存。海马裂解液总蛋白浓度采用BCA试剂盒测定,统一校准至2 mg/mL。
2.3 外周血白细胞计数
EDTA抗凝管取血,自动混匀5分钟,采用Hemavet HV950 FS全自动血液分析仪测定总白细胞(WBC)及中性粒细胞、淋巴细胞、单核细胞、嗜酸性粒细胞计数。
2.4 氧化应激指标与抗氧化酶活性检测
海马组织ROS采用DCF‑DA荧光法检测;血清NO采用Griess试剂法;血清过氧化氢酶活性采用过氧化氢酶活性试剂盒;GPX活性采用谷胱甘肽过氧化物酶试剂盒,按说明书操作。
2.5 细胞因子谱分析
采用多重液相芯片法检测血清TNF‑α、IL‑1β、IL‑6、GM‑CSF、IL‑10、IL‑13,Luminex平台读取荧光信号,标准曲线定量。
2.6 海马蛋白Western blot分析
RIPA裂解液提取蛋白,BCA定量。每组10只小鼠样本按蛋白浓度等比例混合为一组混合样,上样量10 μg/孔,SDS‑PAGE分离,转PVDF膜。一抗:NRF2、HO‑1、NF‑κB p65、IκBα、BAX、BCL‑2、NEUN、β‑actin;二抗为HRP标记抗兔抗体。ECL显影,ImageJ定量,每组技术重复3次,取均值统计。
2.7 ELISA定量海马Aβ₄₀与Aβ₄₂
采用ELISA试剂盒检测海马Aβ₄₀、Aβ₄₂,BCA校准蛋白浓度,450 nm吸光度计算浓度。
2.8 海马ATP水平测定
采用ATP试剂盒检测,样本去蛋白处理,450 nm吸光度定量,以nmol ATP/mg蛋白表示。
2.9 统计学分析
采用GraphPad Prism 10.1.2,单因素方差分析(ANOVA)+ Tukey事后检验,p<0.05为差异具有统计学意义,数据以`均值±标准差(Mean±SD)`表示。
---
3. 结果
3.1 氢气对外周血白细胞计数的影响
为明确5xFAD基因型与氢气吸入是否改变全身免疫状态,本研究分析了各组外周血白细胞总数及分类计数(图2)。各组间白细胞总数无显著差异。但与野生型对照组(WT‑Veh)、野生型氢气组(WT‑H₂)及5xFAD氢气组(5xFAD‑H₂)相比,5xFAD对照组(5xFAD‑Veh)小鼠白细胞总数呈轻度上升趋势,主要源于淋巴细胞计数略高,而中性粒细胞、单核细胞及嗜酸性粒细胞计数在各组间基本一致。
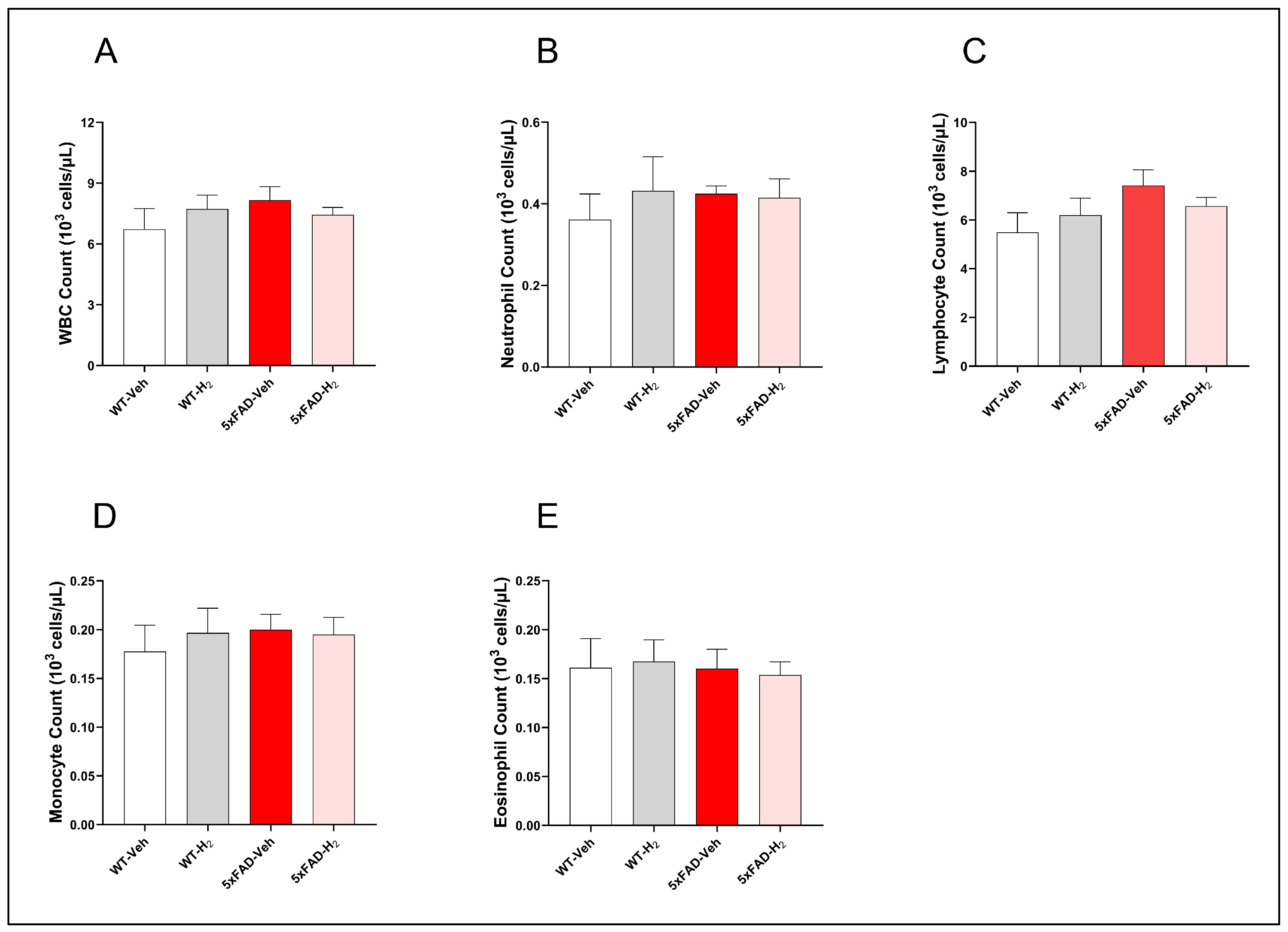
图2 野生型对照组(WT‑Veh)、野生型氢气组(WT‑H₂)、5xFAD对照组(5xFAD‑Veh)及5xFAD氢气组(5xFAD‑H₂)小鼠外周血白细胞分布情况(每组n=10)。(A) 白细胞总数;(B) 中性粒细胞数;(C) 淋巴细胞数;(D) 单核细胞数;(E) 嗜酸性粒细胞数。数据以平均值±标准差表示。
3.2 氢气对氧化应激指标及抗氧化酶活性的影响
为评估5xFAD小鼠的氧化还原改变及氢气的调控作用,检测了海马组织活性氧(ROS)水平及血清氧化应激相关指标。与野生型对照组相比,5xFAD对照组小鼠海马ROS水平显著升高(p<0.01),而氢气吸入可使5xFAD氢气组该升高显著缓解(p<0.05)(图3A)。5xFAD对照组血清一氧化氮(NO)浓度呈轻度上升趋势,但各组间无统计学差异(图3B)。与之相反,5xFAD氢气组血清过氧化氢酶活性较野生型对照组(p<0.01)及5xFAD对照组(p<0.05)显著升高,提示氢气可增强酶促抗氧化能力(图3C)。各组间血清谷胱甘肽过氧化物酶(GPX)活性无显著差异(图3D)。
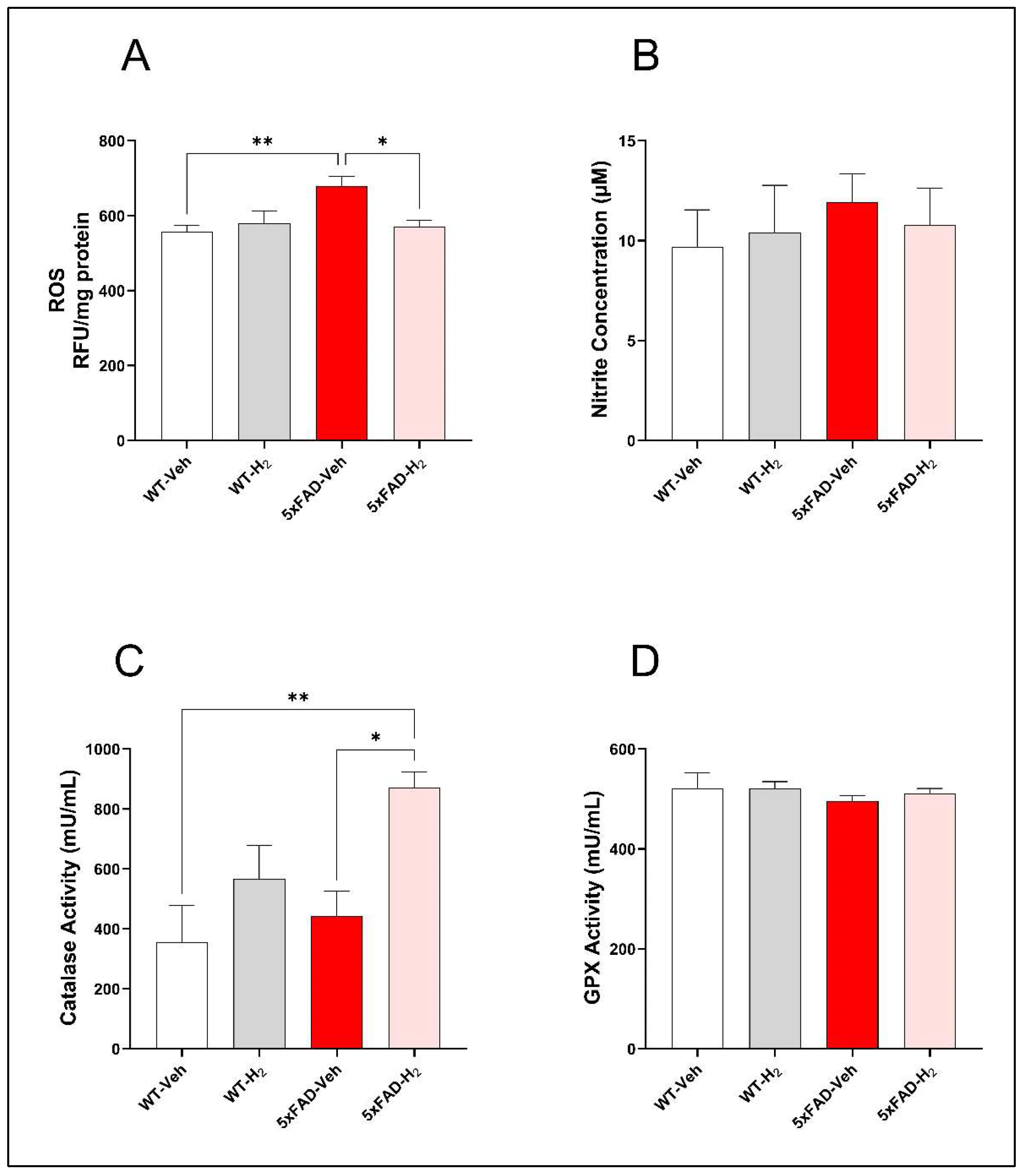
图3 各组小鼠氧化应激指标及抗氧化酶活性(每组n=10)。(A) 海马ROS水平;(B) 血清NO浓度;(C) 血清过氧化氢酶活性;(D) 血清GPX活性。数据以平均值±标准差表示,*p<0.05,**p<0.01。
3.3 氢气对血清细胞因子谱的影响
为评估全身炎症变化及氢气干预效果,检测了血清中肿瘤坏死因子‑α(TNF‑α)、白介素‑1β(IL‑1β)、白介素‑6(IL‑6)、粒细胞‑巨噬细胞集落刺激因子(GM‑CSF)、白介素‑10(IL‑10)及白介素‑13(IL‑13)浓度(图4)。与野生型对照组相比,5xFAD对照组促炎因子TNF‑α与IL‑1β水平显著升高(均p<0.01)。氢气吸入后,5xFAD氢气组上述细胞因子恢复至野生型对照组水平,且较5xFAD对照组显著降低(TNF‑α:p<0.01;IL‑1β:p<0.05)(图4A、B)。IL‑6与GM‑CSF在各组间无显著差异,尽管二者在5xFAD对照组中均呈轻度升高(图4C、D)。与之相对,抗炎因子IL‑10在5xFAD对照组中较野生型对照组显著降低(p<0.05),氢气吸入可使其恢复(p<0.05)(图4E)。IL‑13在5xFAD对照组中同样降低(与野生型对照组相比p<0.05),氢气干预可部分缓解该下降,但未达统计学差异(图4F)。
总体而言,上述结果表明氢气吸入可使5xFAD小鼠外周细胞因子谱向低促炎、以IL‑10为主导的状态转变。
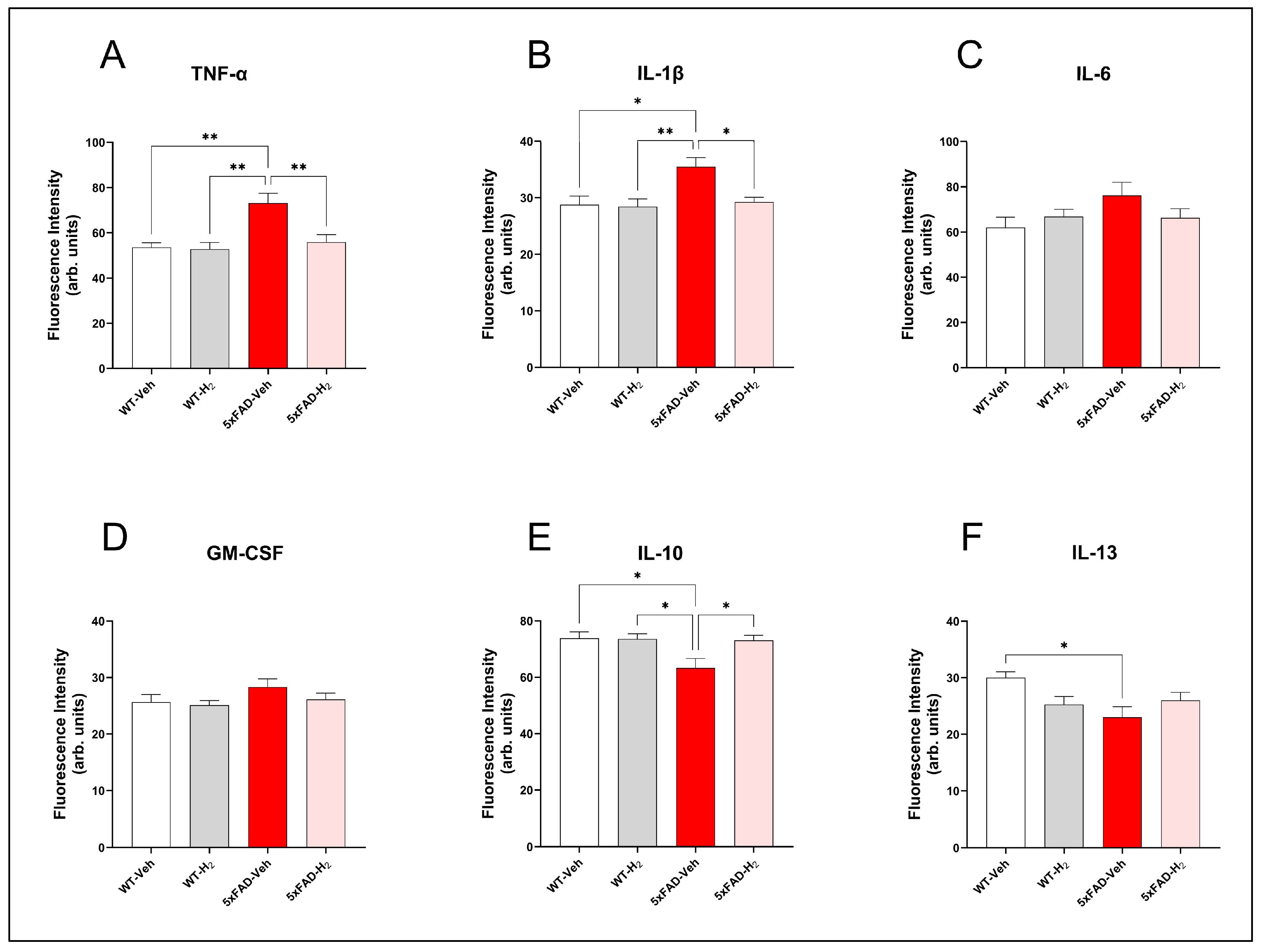
图4 各组小鼠血清细胞因子谱(每组n=10)。(A) TNF‑α;(B) IL‑1β;(C) IL‑6;(D) GM‑CSF;(E) IL‑10;(F) IL‑13。数据以平均值±标准差表示,*p<0.05,**p<0.01。
3.4 氢气对海马组织蛋白表达的影响(Western Blot)
为评估氢气对5xFAD小鼠海马氧化应激、炎症信号及神经元完整性的影响,采用蛋白免疫印迹法检测NRF2、HO‑1、NF‑κB、IκBα、BAX、BCL‑2及NEUN的表达水平(图5)。与野生型对照组相比,5xFAD对照组小鼠海马HO‑1表达显著降低(p<0.05)。氢气吸入可使5xFAD氢气组NRF2水平较5xFAD对照组显著升高(p<0.05),同时HO‑1表达呈同步上升趋势,与NRF2/HO‑1抗氧化通路激活一致(图5A–C)。
在炎症信号方面,5xFAD对照组NF‑κB表达较野生型对照组(p<0.05)及5xFAD氢气组(p<0.01)显著升高,并伴随IκBα降低(p<0.05)。氢气吸入可抑制5xFAD氢气组NF‑κB的上调,并部分恢复IκBα水平(图5A、D、E),提示氢气可抑制海马NF‑κB信号通路。
凋亡及神经元完整性标志物进一步支持氢气介导的神经保护作用。与野生型氢气组相比,5xFAD对照组BAX表达升高(p<0.05)、BCL‑2表达降低;而氢气干预后,5xFAD氢气组BAX降低、BCL‑2升高,BAX/BCL‑2比值显著降低(p<0.05)(图5A、G–I)。NEUN表达在5xFAD对照组中呈下降趋势,氢气吸入可使5xFAD氢气组NEUN水平显著升高(p<0.01),与海马神经元完整性得以维持一致(图5F)。
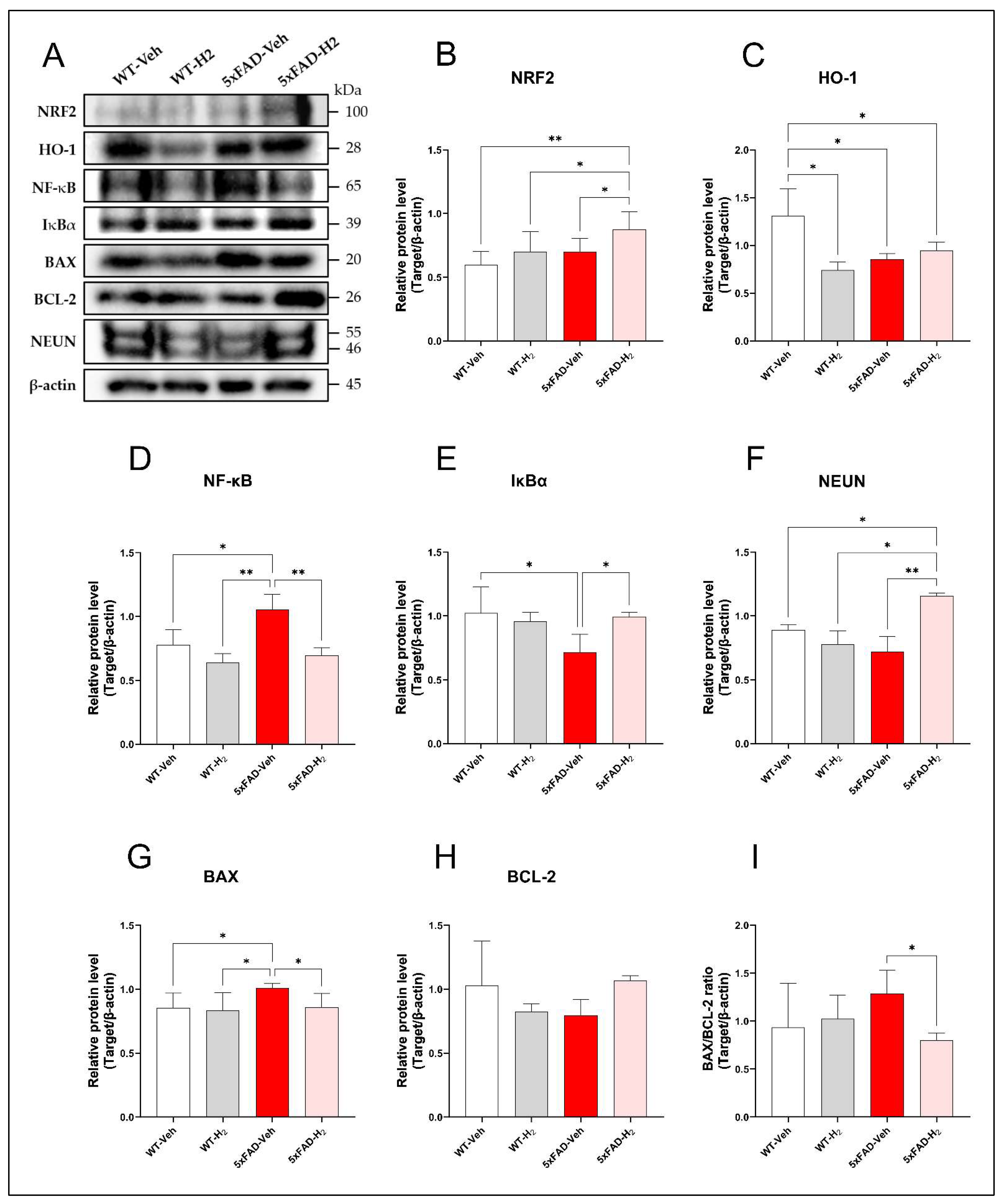
图5 各组小鼠海马组织蛋白表达谱(每组n=10)。(A) NRF2、HO‑1、NF‑κB、IκBα、BAX、BCL‑2、NEUN及β‑actin代表性蛋白条带;(B) NRF2定量;(C) HO‑1定量;(D) NF‑κB定量;(E) IκBα定量;(F) NEUN定量;(G) BAX定量;(H) BCL‑2定量;(I) BAX/BCL‑2比值。数据以平均值±标准差表示,*p<0.05,**p<0.01。
3.5 氢气对海马Aβ40与Aβ42水平的影响
以海马Aβ40与Aβ42浓度作为局部淀粉样蛋白负荷指标进行定量。与5xFAD模型强淀粉样变表型一致,5xFAD对照组Aβ40水平较野生型对照组显著升高(p<0.05)。氢气吸入后,5xFAD氢气组Aβ40水平较5xFAD对照组呈下降趋势,但未达统计学差异(图6A)。Aβ42呈现相似但更显著的变化模式:5xFAD对照组较野生型对照组显著升高(p<0.01);而氢气干预后,5xFAD氢气组Aβ42恢复至野生型水平,且较5xFAD对照组显著降低(p<0.05),提示氢气吸入可抑制更易聚集的Aβ42亚型在海马中的蓄积(图6B)。
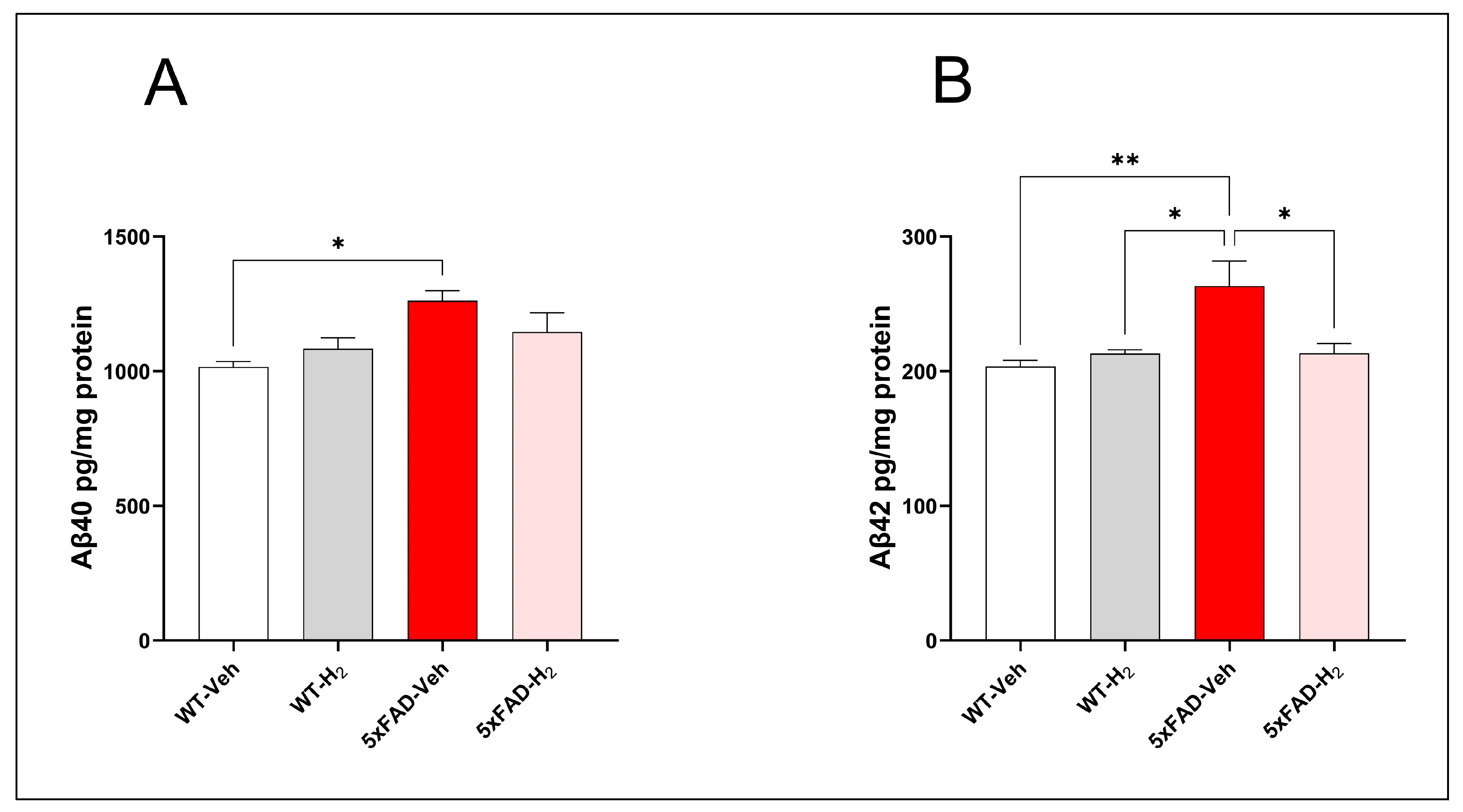
图6 各组小鼠海马Aβ水平(每组n=10)。(A) 海马Aβ40浓度;(B) 海马Aβ42浓度。数据以平均值±标准差表示,*p<0.05,p<0.01。
3.6 氢气对海马ATP水平的影响
以海马ATP水平作为线粒体能量代谢能力指标进行定量。各组间ATP水平存在显著差异,提示基因型与干预方式可影响线粒体能量代谢(图7)。与野生型对照组相比,野生型氢气组海马ATP水平显著升高(p<0.05),提示生理状态下氢气可增强线粒体能量代谢能力。与之相反,5xFAD对照组ATP水平较野生型氢气组降低,与淀粉样蛋白负荷动物线粒体功能受损一致。值得注意的是,氢气干预后,5xFAD氢气组ATP水平较5xFAD对照组显著升高(p<0.05),并部分恢复至野生型氢气组水平,提示氢气可缓解淀粉样蛋白相关线粒体功能障碍,部分恢复细胞能量状态。
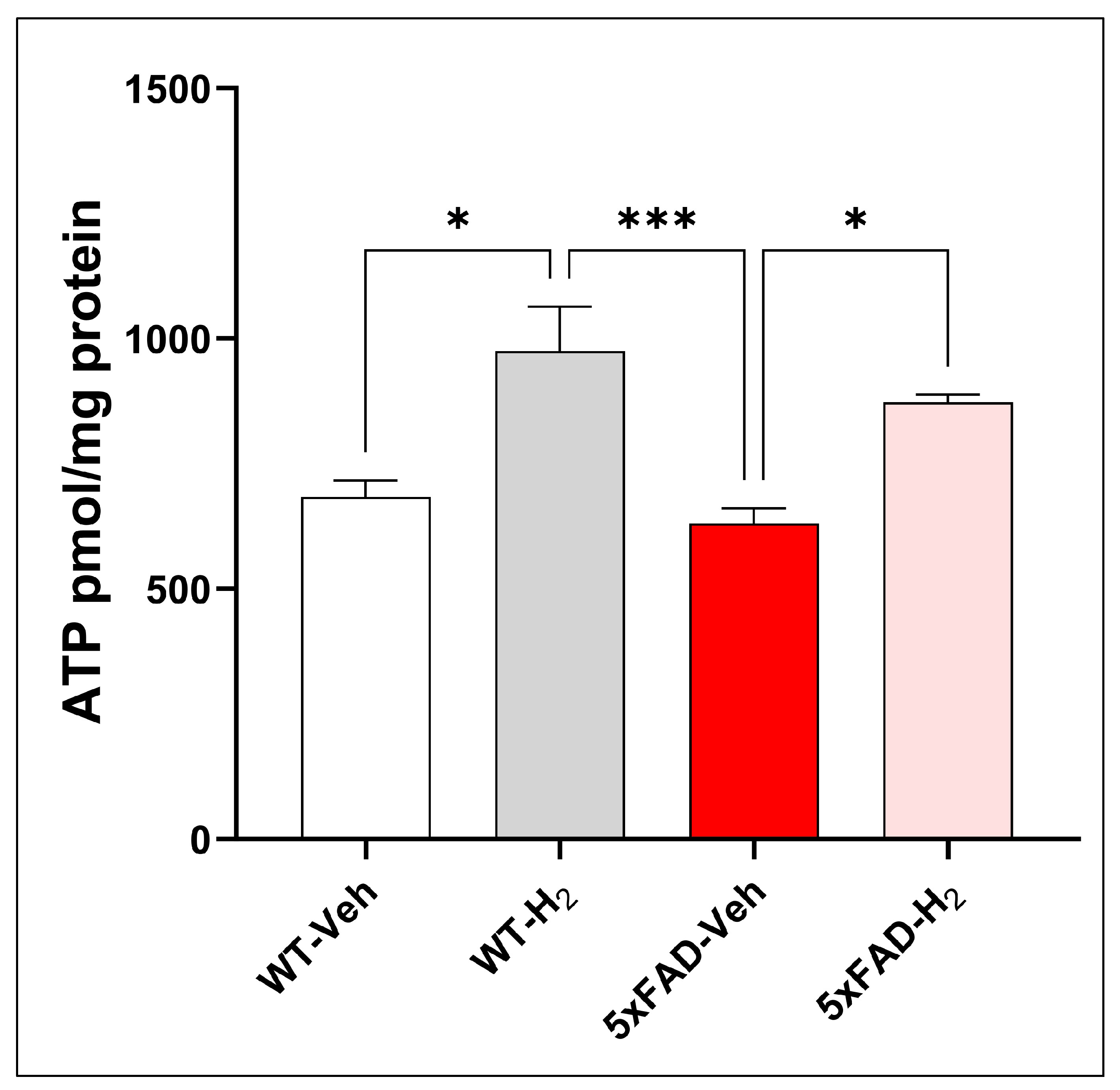
图7 各组小鼠海马ATP水平(每组n=10)。数据以平均值±标准差表示,*p<0.05,***p<0.001。
4. 讨论
本研究证实:2% H₂每日吸入1小时,持续4周,可通过调控氧化还原稳态、炎症信号、线粒体能量代谢、淀粉样蛋白病理,对5xFAD小鼠发挥全面神经保护作用,显著降低海马氧化应激与Aβ₄₂沉积,维持线粒体ATP生成与神经元完整性。
H₂对Aβ₄₂的选择性降低、能量代谢改善与神经元保护,表明其可缓解淀粉样生成与线粒体功能障碍的上游驱动因素,实现结构与功能神经保护;同时氧化还原平衡与炎症谱的协同改善,提示H₂可打断促进Aβ沉积与突触功能障碍的神经免疫‑代谢病理性交互。
5xFAD模型早期即出现显著Aβ沉积,伴随线粒体功能障碍与氧化应激,共同导致突触损伤与神经元丢失。氧化应激是AD神经退行性变的关键驱动因素,Nrf2/HO‑1通路是细胞氧化还原稳态核心调控轴,其功能异常参与AD发病。既往研究显示H₂可选择性中和·OH与ONOO⁻,保护细胞免受氧化损伤;本研究中5xFAD模型海马ROS显著升高,H₂可缓解氧化应激并提高过氧化氢酶活性,同时上调NRF2、伴随HO‑1升高,支持激活NRF2介导的抗氧化应答。
氧化应激与炎症在AD中紧密关联,氧化还原失衡可放大炎症信号。本研究显示5xFAD模型呈现外周促炎状态(TNF‑α、IL‑1β升高,IL‑10、IL‑13降低),H₂可逆转该失衡:降低TNF‑α、IL‑1β,恢复IL‑10,部分纠正IL‑13,重建外周免疫稳态。同时海马NF‑κB激活、IκBα降低,H₂可抑制NF‑κB、恢复IκBα,提示H₂协同外周与中枢抗炎,可能通过减轻线粒体ROS驱动的免疫激活,营造调节性免疫环境。
在淀粉样病理方面,H₂显著降低Aβ₄₂(毒性更强、更易聚集),对Aβ₄₀影响较弱。机制上,氧化应激与神经炎症可通过影响APP加工、γ‑分泌酶活性与清除通路,促进Aβ生成与聚集;H₂通过抑制ROS与NF‑κB,可间接限制淀粉样生成、增强Aβ清除;同时TNF‑α、IL‑1β降低与IL‑10恢复,可改善小胶质细胞吞噬能力,促进Aβ清除。
线粒体功能障碍是AD另一核心病理特征,导致神经元损伤与突触衰竭。H₂可显著提升海马ATP水平,在生理与AD模型中均改善线粒体能量代谢,稳定线粒体膜电位、调节电子传递链、抑制复合物I处超氧过量生成。同时H₂降低BAX/BCL‑2比值、恢复NEUN,抑制促凋亡信号、保护神经元群,结合NRF2激活与ATP恢复,提示H₂可调控淀粉样病理下线粒体依赖性凋亡易感性。
本研究存在若干局限:
1. 仅检测生化与分子指标,未直接评估学习认知功能,未来需加入水迷宫、Y迷宫、新物体识别等行为学实验;
2. Western blot采用组内混合样本,无法反映个体差异,后续需单样本分析;
3. 仅采用单一H₂浓度与干预时长(2%,1 h/d×4周),需剂量‑效应与时间梯度研究确定最优参数;
4. 下游分子通路与药理潜力仍需深入阐释。
---
5 结论
本研究表明,5xFAD小鼠吸入H₂可:
- 减轻氧化应激,激活NRF2/ARE抗氧化通路;
- 抑制全身与海马炎症,阻断NF‑κB信号;
- 增强线粒体ATP生成,改善能量代谢;
- 降低海马Aβ₄₂负荷,保护神经元完整性。
H₂安全性良好,可同时靶向AD发病的多条汇聚通路,是极具前景的疾病修饰与预防辅助手段。未来需结合行为学、纵向成像与通路靶向干预,验证保护效应并明确H₂在AD综合治疗体系中的应用方式。
转载本文请联系原作者获取授权,同时请注明本文来自孙学军科学网博客。
链接地址:https://wap.sciencenet.cn/blog-41174-1527552.html?mobile=1
收藏

