 精选
精选
博主本人对氧化和还原的看法
抗氧化,促氧化,都是度人。氧化有害有利其实是难以说清楚的。氧化是需氧生物生存的基础,没有氧化过程,就无法有效充分获得化学能,我们熟悉的氧化磷酸化就是氧化电子获得能量最典型的代表。因此氧化是生命核心过程,没有氧化生命就不可能存在。既然如此,氧化就没有问题吗?当然有,重要的过程一定存在瑕疵,瑕疵表现出来就是一种伤害。氧化损伤就是一种典型的损伤现象。氧化损伤可以说是氧化这一个重要生物过程的一个瑕疵。氧化损伤有时候又称为氧化应激,或者氧化还原平衡,所以如此,是因为氧化损伤这种说法存在误导。其实有时候损伤也是一种生理表现,蛋白质被氧化或氧化态可能是其最理想的功能状态。例如半胱氨酸被氧化形成二硫键,是胰岛素等重要蛋白质结构的基础,如果过于还原,则意味着结构破坏。这样的氧化就是功能的表现。生物系统是进化日趋完善理想的复杂系统,氧化或还原是生命基本过程,不能简单对一种重要过程用有害有利进行认识,只能用重要了描述。氧化是一种重要生理过程,氧化应激是一种重要生理表现,氧化过度或不足可能会带来细胞功能紊乱,可能表现为损伤或疾病。但是由于生物体本身属于还原底物为主,许多损伤过程表现为被氧化破坏,因此氧化损伤是更常见的表现形式。还原如果严重,也同样可以产生伤害,这是必然的。
编辑总结
鉴于抗氧化剂可能具有促进癌症的作用的新证据,Swamynathan等人测试了潜在的促氧化干预措施(参见Pannia和Dowling的观点文章)。特别是,作者关注了维生素K的水溶性前体物质——亚硫酸钠甲萘醌。正如作者预期的那样,这种甲萘醌衍生物抑制了前列腺癌的生长。研究人员随后研究了其作用机制,并确定了激酶VPS34(磷脂酰肌醇3-激酶催化亚单位类型3)作为其靶标。幸运的是,他们意识到一种致命的遗传性肌肉疾病——X连锁肌管肌病也与VPS34活性相对过剩有关,这是因为其拮抗剂的缺失,而饮食中补充甲萘醌在这种遗传性疾病的小鼠模型中被证明是有益的。——Yevgeniya Nusinovich
结构化摘要
引言
前列腺癌(PC)是男性中最常诊断的癌症,预计2024年美国将有超过299,000例新病例。这些男性中的大多数将呈现缓慢生长的疾病,这可能会转变为抵抗所有可用治疗选项的危及生命的PC。因此,人们非常感兴趣于定义明智的生活方式、饮食和补充选择,这些选择可以减缓疾病进展。这催生了大规模的人体试验,包括一项关于膳食抗氧化剂益处的试验:SELECT试验(硒和维生素E癌症预防试验),该试验对35,533名健康男性进行了10年以上的跟踪。出乎意料的是,SELECT显示,服用抗氧化维生素E补充剂的男性患PC的风险显著增加。
理由
抗氧化维生素E补充剂促进PC的效果立即引发了一个问题,即相反地,促氧化补充剂是否可以帮助预防这种疾病。基因工程改造的小鼠(GEM)PC模型提供了一个提出这个问题的平台。具体来说,我们使用了RapidCaP GEM模型,它让我们能够确定前列腺中的癌症如何以及多快进展为转移形式。
结果
我们用促氧化剂甲萘醌补充剂[亚硫酸钠甲萘醌(MSB)]治疗RapidCaP动物,这是哺乳动物维生素K的前体,它在消费绿叶中的植物维生素K后存在于循环中。每日在饮用水中补充MSB抑制了PC进展,产生了持久的响应。系统分析细胞死亡途径揭示了MSB通过一种我们提议称为三重凋亡的独特氧化细胞死亡机制杀死癌细胞。我们使用全基因组CRISPR筛选来了解背后的生物学原理,发现MSB耗尽早期内体(EE)膜脂质磷脂酰肌醇3-磷酸[PI(3)P]。PI(3)P定义了EE区室,允许派生的囊泡返回质膜或进入溶酶体降解系统。视频显微镜显示,三重凋亡的特征是积累大的PI(3)P阴性、去识别的内体,随后是细胞起泡和质膜破裂。我们发现MSB直接氧化III类PI 3-激酶VPS34上的关键半胱氨酸,从而失活产生PI(3)P的酶。值得注意的是,用额外的还原剂补充细胞完全消除了由MSB引起的细胞死亡。甲萘醌抑制PI(3)P产生的能力促使我们测试它是否可以抑制一种致命的遗传性疾病:X连锁肌管肌病。这种无法治愈的疾病是由MTM1基因的遗传突变引起的。MTM1是直接拮抗PI 3-激酶VPS34的磷酸酶。因此,患有这种疾病的男孩遭受未对抗的PI(3)P产生,导致肌肉构建失败。Mtm1敲除小鼠重现了最严重的表型,即婴儿期致死。在饮用水中补充MSB使这些小鼠的总体生存期加倍,达到2个月的中位数。治疗还改善了动物的体重增长和肌肉组织学。
结论
我们的结果建议,饮食中的甲萘醌可以形成多种疾病设置下新治疗方法的基础。这是因为MSB是PI 3-激酶VPS34的氧化拮抗剂,该酶产生磷脂PI(3)P。在PC细胞中,氧化应激降低了PI(3)P,导致细胞通过三重凋亡死亡。我们从数据推断,正常细胞有足够的还原力储备来抵御这种伤害。在肌管肌病中,甲萘醌可能抑制未对抗的VPS34激酶活性,并将PI3P带回可以改善肌肉发育的水平。总的来说,我们的发现有助于理解促氧化剂选择性的新兴认识,并展示了如何定义它们影响的路径可以为意外的治疗机会提供基础。
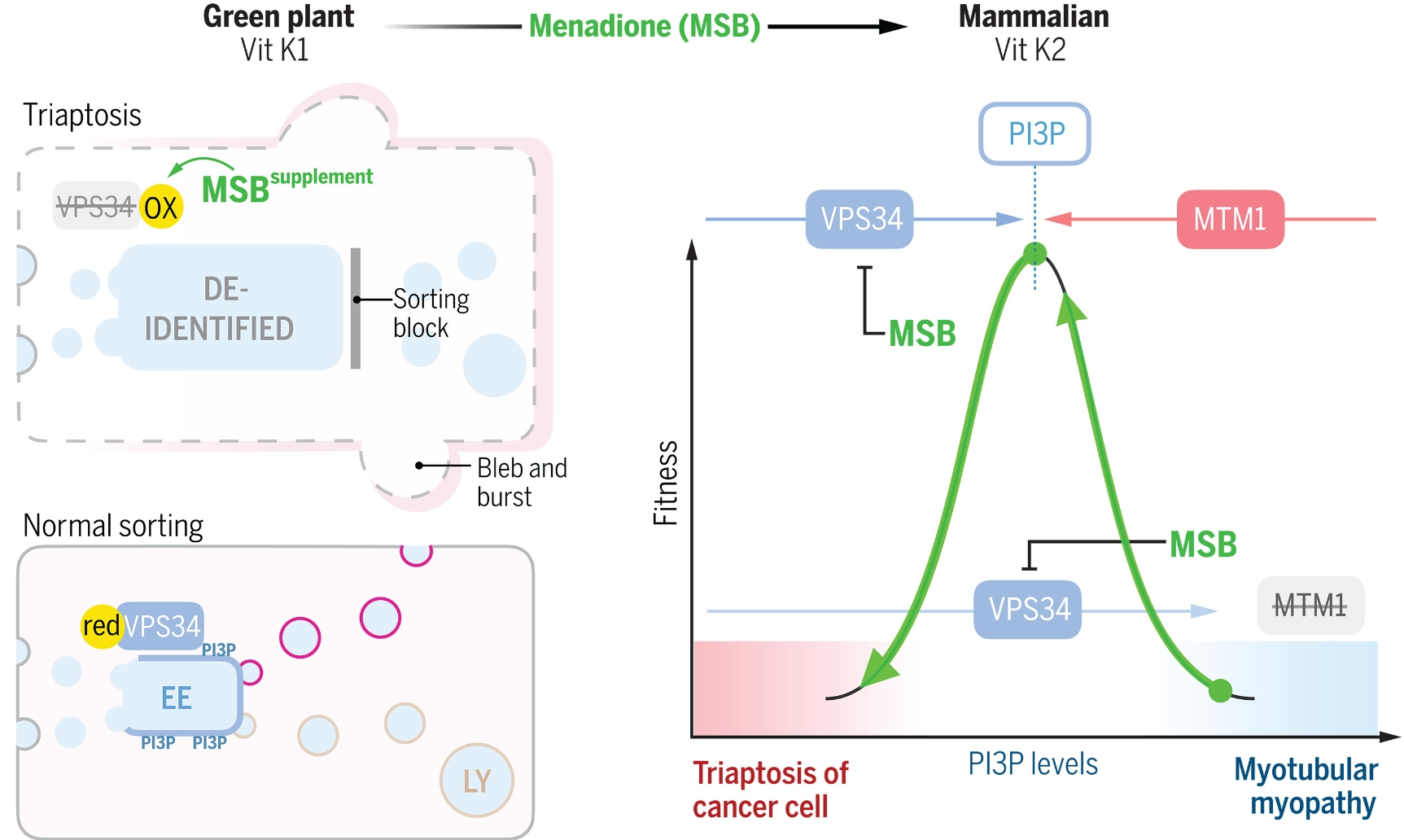
膳食促氧化剂治疗使用维生素K前体
(顶部)绿色植物食品是维生素K(Vit K1)的主要来源,哺乳动物将其转化为Vit K2。中间产物是甲萘醌,可以补充到饮食中(MSB)。(左侧)MSB氧化VPS34激酶。这导致三重凋亡,一种基于PI3P耗尽的独特细胞死亡机制,它使EE区室去识别化。LY,溶酶体降解系统。(右侧)利用MSB减少PI3P在两种疾病设置中的治疗概念。
摘要
服用抗氧化维生素E补充剂的男性患前列腺癌(PC)的风险增加。然而,促氧化剂是否能够预防PC尚不清楚。在本研究中,我们展示了促氧化剂维生素K前体[亚硫酸钠甲萘醌(MSB)]在小鼠中抑制了PC进展,通过氧化细胞死亡杀死细胞:MSB通过氧化关键半胱氨酸拮抗必需的III类磷脂酰肌醇(PI)3-激酶VPS34——内体身份和分拣的调节器,指向分拣过程中的一个氧化还原检查点。在由MTM1缺失驱动的肌管肌病模型中测试MSB——VPS34的磷酸酶拮抗剂,我们展示了饮食中的MSB改善了肌肉组织学和功能,并延长了寿命。这些发现增强了我们对促氧化剂选择性的理解,并展示了如何定义它们影响的路径可以带来意想不到的治疗机会。
转载本文请联系原作者获取授权,同时请注明本文来自孙学军科学网博客。
链接地址:https://wap.sciencenet.cn/blog-41174-1456994.html?mobile=1
收藏

