骨质疏松症是一种以骨量减少和骨骼微结构破坏为特征的疾病,严重威胁着人们的骨骼健康。随着社会老龄化的加速,这一问题愈发凸显。然而,当前用于预防或治疗骨质疏松的药物种类有限,主要原因是骨质疏松的发病机制和药物靶点尚未完全明晰。成骨细胞在维持骨骼稳态中扮演着关键角色,其功能受损是骨质疏松症发病的主要因素之一。氧化应激在绝经后骨质疏松症中起着关键作用,但其对成骨细胞的影响尚未被充分揭示。对此,能够有效保护细胞免受氧化应激、改善骨质疏松症的天然产物亟待开发。
近日,本实验室何蓉蓉教授/李怡芳教授等人在Nature Communications. 2025 Jan 17;16(1)上发表题为“Regulation of enzymatic lipid peroxidation in osteoblasts protects against postmenopausal osteoporosis”的研究文章,为这一领域带来了新的突破。该研究不仅揭示了磷脂过氧化与骨质疏松症之间的联系,同时发现天然产物6-和8-姜酚通过激活GPX4发挥抗骨质疏松作用的新机制,为开发新型抗骨质疏松疗法提供了有力的科学依据。
骨质疏松症的发病机制涉及多种因素,其中氧化应激被认为是关键因素之一。氧化应激会导致细胞内活性氧(ROS)水平升高,进而引发脂质过氧化等一系列细胞损伤反应。该研究在探讨磷脂过氧化与骨质疏松症之间的联系时发现,随着年龄增长,股骨组织中4-HNE(磷脂过氧化的关键终产物)含量逐渐升高。同样,卵巢切除(OVX)小鼠和老年小鼠的股骨和胫骨中,也观察到4-HNE水平的上升,表明磷脂过氧化与骨质疏松症的进展密切相关。进一步的实验发现,4-HNE在成骨细胞中积累尤为显著。这一现象提示,骨质疏松性骨中的成骨细胞受到了磷脂过氧化的不利影响。成骨细胞是维持骨骼稳态的关键细胞类型,其功能受损会导致骨形成减少,从而加剧骨质疏松症的发展。为了深入研究磷脂过氧化在骨质疏松症中的作用,研究通过LC-MS技术对磷脂的含量进行分析。结果显示,OVX小鼠骨组织中氧化磷脂(oxPLs)的oxPLs水平显著增加。这一发现提示,中和oxPLs有望缓解老年性骨质疏松症。为了验证这一假设,实验利用OVX手术小鼠灌胃给予维生素E。结果显示,维生素E对磷脂过氧化的抑制能够显著防止OVX诱导的骨质流失,从而证实了磷脂过氧化在骨质疏松症中的重要作用。
磷脂过氧化受到多种关键酶的调控,其中谷胱甘肽过氧化物酶4(GPX4)是能够还原磷脂过氧化物的酶。研究发现,GPX4在OVX小鼠、老年小鼠以及老年患者的骨组织中表达显著下调,提示GPX4缺乏与骨质疏松症中磷脂过氧化物积累之间存在潜在联系。免疫荧光实验进一步证实了GPX4在骨质疏松性骨组织内成骨细胞中的特异性下调。
鉴于在雌激素缺陷的患者和小鼠中观察到GPX4表达下调,实验通过深入探究了雌激素介导的GPX4激活机制。结果发现,雌激素通过雌激素受体β(ERβ)调节GPX4转录。通过双荧光素酶报告基因测定和染色质免疫沉淀(ChIP)实验,研究结果揭示了ERβ能够直接结合GPX4启动子区的E-box元件,从而激活GPX4转录。这一发现为理解雌激素在骨质疏松症中的作用机制提供了新的视角。
为了明确GPX4在成骨细胞分化和骨质疏松症中的作用,构建了成骨细胞特异性GPX4敲除小鼠(Gpx4OBs−/−)。实验结果显示,实验小鼠的骨量显著降低,成骨细胞数量也明显减少。此外,通过使用GPX4抑制剂RSL3,发现其诱导的骨组织磷脂过氧化导致了严重的骨质流失,并显著抑制了骨形成相关基因和蛋白的表达。这些结果提示GPX4在维持成骨细胞功能和骨稳态中的重要作用。
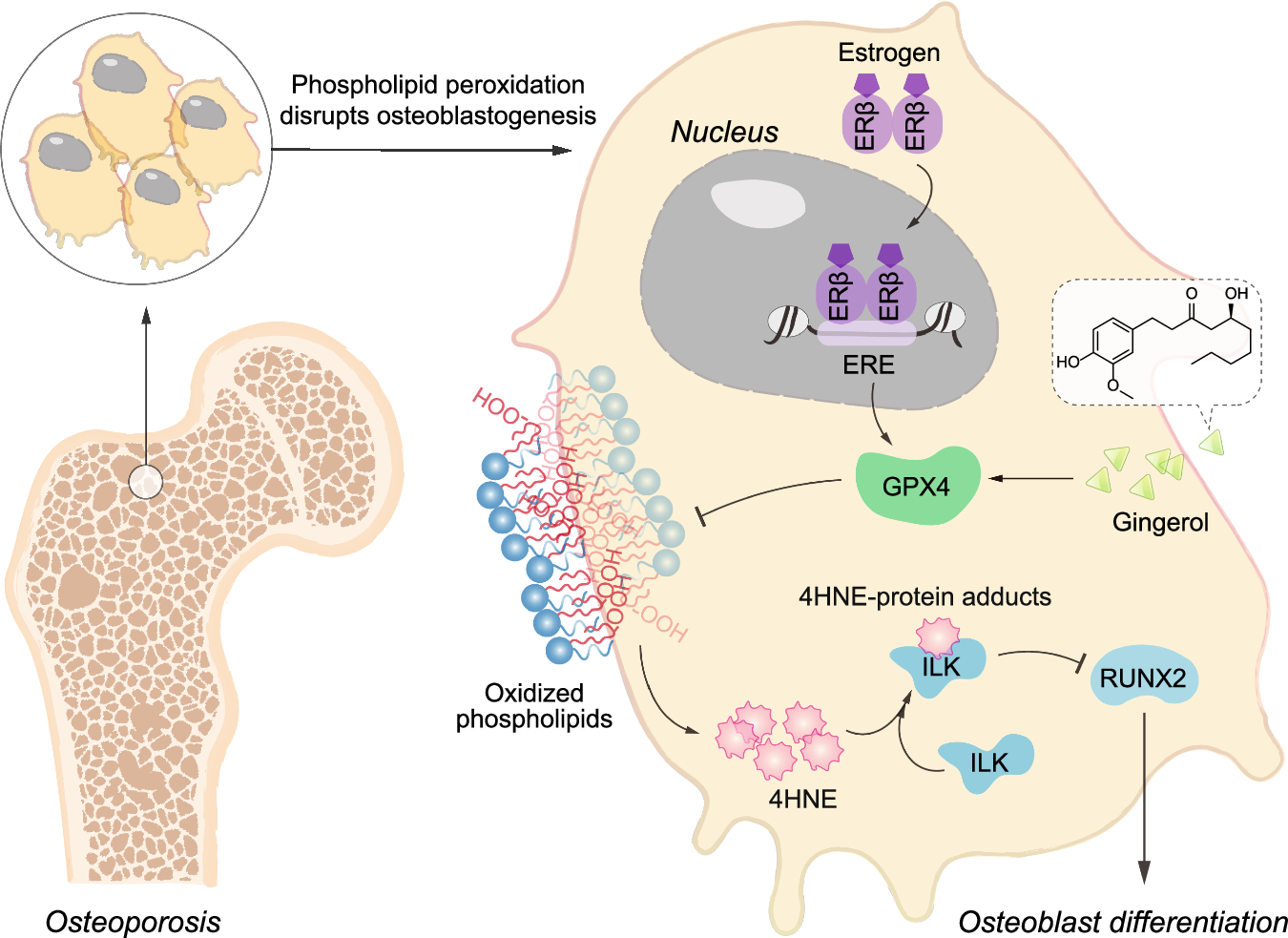
脂质过氧化会生成4-HNE,一种高反应性的亲电化合物,能够与蛋白质中的赖氨酸、组氨酸和半胱氨酸残基形成共价加合物。研究人员在老年患者和OVX小鼠的骨组织中观察到4-HNE结合蛋白的积累。当使用磷脂过氧化抑制剂Fer-1处理时,4-HNE蛋白偶联物的水平降低,同时减轻了RSL3对成骨细胞分化和矿化的抑制。这些发现揭示了磷脂过氧化介导的4-HNE蛋白修饰在骨形成中的抑制作用。为了确定受4-HNE修饰的参与骨形成的蛋白,研究人员执行了基于LC-MS的蛋白质组学分析。结果表明,在GPX4抑制组中,4-HNE修饰的ILK显著升高,并通过共免疫沉淀(Co-IP)和免疫荧光共定位实验得到了验证。4-HNE修饰的蛋白质可能会改变其活性或稳定性。研究发现,磷脂过氧化衍生的4-HNE修饰ILK,促进其泛素化依赖性降解,进而抑制RUNX2和OSX的表达,最终破坏了骨形成。
在确认GPX4在骨质疏松症中的关键作用后,利用天然产物库靶向GPX4变构位点进行分子对接,初步筛选出评分最高的15种化合物。其中,三种生姜来源的酚类化合物——6-、8-和10-姜酚,对RSL3诱导的细胞死亡表现出显著的抑制作用。通过分子对接、细胞热位移分析(CETSA)和微量热泳动(MST)实验,研究人员证实6-姜酚和8-姜酚能够与GPX4蛋白结合,增强GPX4活性。在体内实验中,6-姜酚和8-姜酚对OVX诱导的骨质疏松症具有显著的保护作用,能够显著降低磷脂过氧化衍生的终产物水平。这些体内和体外研究结果确定了6-姜酚和8-姜酚作为GPX4的天然变构激活剂,并展示了抗骨质疏松治疗中的潜力。
这项研究揭示了GPX4在维持骨形成中的重要作用。GPX4的缺乏会加剧骨质流失,破坏骨形成,从而导致骨质疏松症的发生。此外,研究还确定了6-姜酚和8-姜酚作为GPX4的新型变构激活剂,并在体内和体外模型中证实了它们的抗骨质疏松作用。这些发现不仅为磷脂过氧化在成骨功能障碍中的作用提供了重要见解,还强调了靶向GPX4治疗骨质疏松症的潜在价值,为未来开发新的抗骨质疏松疗法提供了有力的科学依据。
随着对骨质疏松症发病机制的深入研究,尤其是对氧化应激和磷脂过氧化在其中作用的揭示,未来有望开发出更多基于天然产物的新型治疗策略。6-姜酚和8-姜酚作为天然的GPX4激活剂,具有广阔的应用前景。它们不仅能够通过激活GPX4抑制脂质过氧化,还能通过多种机制保护成骨细胞免受氧化应激的损伤,促进骨形成。这一研究为抗骨质疏松治疗提供了新的思路和方向,也为天然产物在疾病治疗中的应用提供了新的范例。
转载本文请联系原作者获取授权,同时请注明本文来自栗原博科学网博客。
链接地址:https://wap.sciencenet.cn/blog-39778-1469778.html?mobile=1
收藏

