博文
Phenomics | 复旦大学/上海交大医学院等团队揭示饮食、菌群与龋齿在青少年中的互作机制
|
近日,《表型组学(英文)》(Phenomics)在线发表了由复旦大学生命科学学院/人类表型组研究院郑琰团队与上海交通大学医学院附属第九人民医院杨驰、邹多宏团队合作完成的题为“Associations Between Dietary Habits, Oral Microbiota, and Dental Caries in Adolescents”的研究论文。
该研究聚焦于青少年群体,通过对421名青少年的综合分析,深入探讨了饮食习惯、口腔微生物菌群与龋齿之间的复杂关系。研究不仅识别出与龋齿显著相关的关键菌群,并通过中介分析揭示某些菌属可能部分中介饮食与龋齿的联系,为理解饮食如何影响牙齿健康提供了新的潜在机制,并可能为龋齿的预防和管理带来新的思路。
文末点击“阅读原文”可在线阅读文章。

扫描二维码 | 下载PDF原文
论文DOI链接:
https://doi.org/10.1007/s43657-024-00208-3
论文引用格式:
Yue, H., Shen, P., Huang, Q. et al. Associations Between Dietary Habits, Oral Microbiota, and Dental Caries in Adolescents. Phenomics (2025). https://doi.org/10.1007/s43657-024-00208-3
研究背景
龋齿是全球范围内最普遍的慢性疾病之一,在青少年群体中具有较高的患病率。过量摄入含糖食品是公认的致龋关键风险因素。近年来,“生态学假说”认为龋齿的发生源于口腔微生物群落的生态失调(dysbiosis),而非单一病原体的作用。青少年期不仅是饮食习惯形成的关键期 ,其口腔微生物组也因永久牙列形成和生活方式转变而处于动态变化中。相较于成人和学龄前儿童,针对这一特殊群体的研究相对匮乏,导致饮食通过调节菌群介导龋齿发生的生物学机制尚不明确。因此,本研究旨在系统探究青少年口腔微生物在饮食习惯与龋齿关联中所扮演的角色,以期揭示潜在的致病机制,并为该年龄段的龋齿防治提供新见解。
研究结果
1,口腔微生物组成与龋齿显著相关
研究对421名青少年进行口腔检查和唾液微生物测序,发现龋齿组与无龋齿组的微生物组成存在显著差异。这一差异在外部580名成人人群中得到验证,证实了口腔菌群的宏观变化与龋齿状态密切相关。
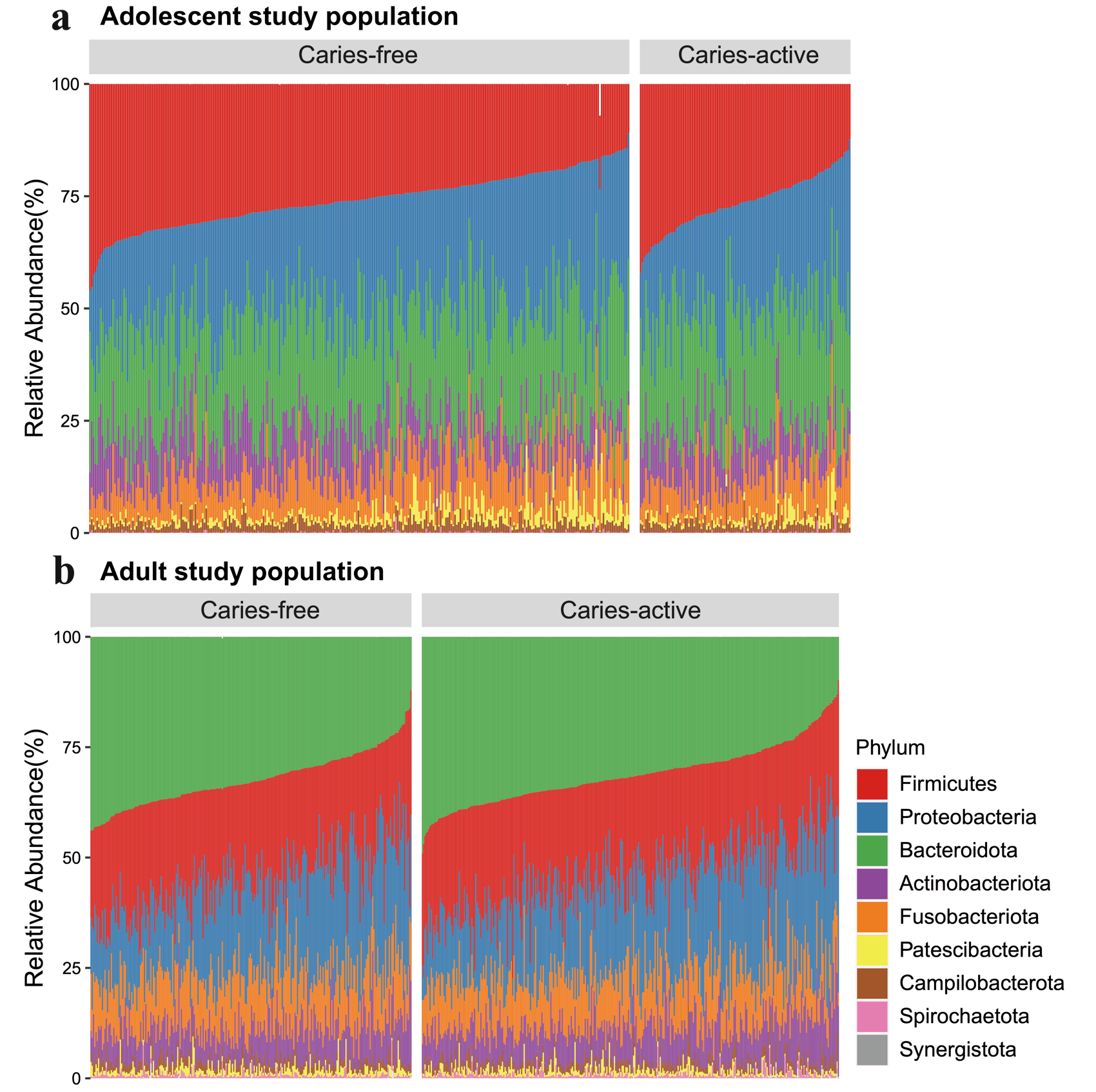
图1 龋齿组与无龋齿组口腔细菌菌门水平分布
2,与龋齿状态显著相关的差异丰度菌属与功能通路
使用多变量关联分析,研究鉴定出19个与龋齿相关的菌属。其中,7个菌属在龋齿组富集,例如之前研究已发现与龋齿进展相关的Prevotella(普雷沃氏菌属)和Veillonella(韦荣球菌属)。同时,有12个菌属在龋齿组中丰度更低(耗竭),暗示它们可能扮演着维持口腔健康的“有益菌”角色。功能预测显示102个通路与龋齿相关,包括氨基酸代谢通路(如精氨酸生物合成)在无龋齿组富集,核苷酸和辅因子生物合成通路在龋齿组升高。

图2 龋齿相关微生物功能通路的分类与相关分析
3,关键菌群与饮食习惯紧密关联并发挥中介作用
研究进一步发现,这些与龋齿相关的关键菌群的丰度与参与者的具体饮食习惯有关。例如,含糖食品和饮料的高频率摄入与龋齿富集菌属的丰度呈正相关。
中介效应结果显示,饮食习惯并非直接导致龋齿,而是通过调节特定的口腔微生物群落,进而介导了龋齿的发生过程。具体来说,含糖食品(如糖果和巧克力)与龋齿的关联,部分是通过Staphylococcus菌属介导的;而偏好较软食物的饮食习惯与龋齿的关联,则是由另Paludibacteraceae F0058菌属所介导。
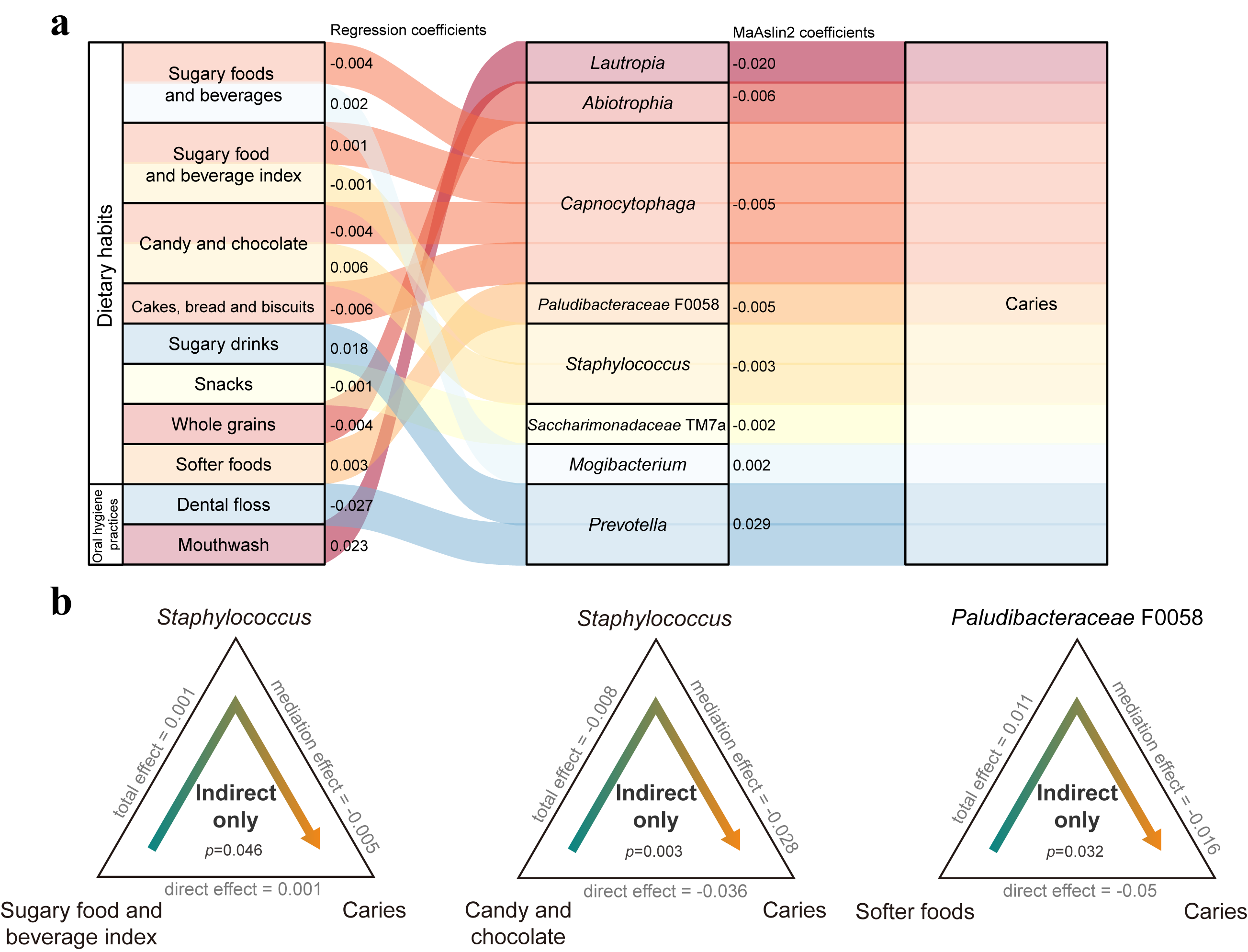
图3 中介分析示意图
研究结论
本研究系统地描绘了青少年群体中饮食习惯、口腔微生物和龋齿之间的复杂相互关系。本研究揭示了青少年口腔微生物组在饮食习惯与龋齿间的关键作用,鉴定出潜在的中介菌属,并强调了微生物功能通路在龋齿发生发展中的差异性作用。这些发现为靶向微生物的龋齿预防策略(如饮食干预或益生菌应用)提供了依据,并突显青少年期口腔健康管理的必要性。未来需通过纵向研究和鸟枪法宏基因组测序进一步验证因果关系,以扩展到更广泛人群。
Abstract
Suboptimal dietary habits, such as excessive consumption of sugary foods and beverages, have been associated with a higher risk of dental caries. While known cariogenic species enrichment in the oral microbiome correlating with dental caries, the complex interactions between dietary habits, the oral microbiota, and dental caries among adolescents remain underexplored. Here, we examined the comprehensive associations between dietary habits, oral microbiota, and dental caries among 421 adolescents (mean age: 12.9 years, 28% having dental caries). The dietary data were collected via a food frequency questionnaire, dental health was examined by a skilled dentist, and the saliva microbiota was profiled by 16S ribosomal RNA sequencing. Significant difference in the oral microbial composition was observed between participants with and without dental caries (p-value < 0.05), which was replicated in an external adult population (n = 580). The relative abundances of 19 genera were associated with dental caries in adolescents independent of gender (all FDR-adjusted p-values < 0.20). For example, dental caries was linked with a higher abundance of Prevotella and Veillonella, both of which were also enriched in higher consumer of sugary food and beverage. In mediation analysis, certain caries-related genera, including Staphylococcus and Paludibacteraceae F0058, might partially mediate the associations between dietary habits and dental caries (p-mediation < 0.05). This research highlighted the role of oral microbiota in the association between dietary intakes and dental caries and may explain the potential mechanisms by which diet affects dental caries.
作者简介
通讯作者

郑琰,现任复旦大学生命科学学院研究员,博士生导师。国家“万人计划”青年拔尖人才,上海高校特聘教授(东方学者),入选“全球前2%顶尖科学家榜单”(2023、2024)。近年来,共计主持人才项目6项和科研项目4项(国家自然科学基金2项,国家重点研发计划2项)。担任Molecular Genetics and Genomics杂志副主编,先后发表SCI文章100余篇,其中以重要作者身份在JAMA、Nature Reviews Endocrinology、BMJ、Diabetes Care、Natl Sci Rev等杂志上发表文章67篇。连续多年被评为中国高被引学者并受到国内外媒体报道。主要从事肥胖相关代谢病的人群流行病学因素,尤其是利用代谢组及微生物组学大数据,发现肥胖相关疾病的新型生物标志物,探索饮食影响健康的代谢中介机制。
通讯作者

杨驰,上海交通大学特聘教授,主任医师,博士生导师,国务院特殊津贴专家。上海交通大学医学院附属第九人民医院口腔外科学科带头人,国家口腔疾病临床医学研究中心主任,国家口腔医学中心主任。中华口腔医学会口腔颌面外科专委会主任委员、颞下颌关节病学及牙合学专委会候任主任委员,美国、欧洲颞下颌关节外科医师学会国际委员。获国家科技进步奖获国家科技进步奖二等奖,上海市科技进步一等奖,教育部科技进步二等奖等国家、省部级奖励13项。主持和参与包括863计划子课题、科技部重点研发计划子课题、国家自然科学基金在内的国家级和省部级课题30余项,发表论文411篇(含SCI收录182篇),共被他引2209次,近5年连续入选爱思唯尔高被引学者。成果获批专利175件(含发明专利39件,国际专利6件),16项共111件专利转化,合同金额1亿1325万元,取得注册证13个(含Ⅲ类证3个)。
通讯作者

邹多宏,上海交通大学医学院附属第九人民医院口腔外科(牙种植专科/老年口腔种植专科)副主任医师,口腔种植专业临床医学博士,博士后,教授、研究员,博士生导师,美国密歇根大学牙学院高级访问学者。获上海市卫生健康学科带头人、上海市杰出青年医学人才及安徽省杰出青年基金培养计划。主持国家及省部级课题15项,以第一/通讯作者发表SCI论文86篇。获上海医学科技奖青年奖、教育部科学技术进步奖二等奖1项及第五届中国医疗器械创新创业大赛二等奖。中华口腔医学会牙及牙槽外科专业委员会副主任委员及上海市主任委员,中华口腔医学会口腔种植专业委员会委员及上海市的常务委员。主要研究方向:老年口腔种植、牙槽骨重度缺损修复与重建及整合牙槽学研究。
第一作者

岳海岩,复旦大学人类表型组研究院硕士生,导师为郑琰研究员,主要研究方向为口腔和肠道微生物与疾病的关联研究。
第一作者

沈佩,副主任医师,博士研究生学历,临床主攻关节-正畸-正颌联合治疗。科研主要方向为髁突吸收发生发展的机制以及软骨干细胞在诱导分化、疾病进展及再生修复等方面的机理。以第一及通讯作者发表SCI论文30余篇(JCR Q1区文章占80%以上),主持及参与国家自然科学基金项目6项(以项目负责人身份主持2项),以及科技部重点研发项目、上海市高峰高原青年人才项目和上海交通大学医学院博士创新基金等项目,并负责多项RCT及专病队列研究。
第一作者

黄秋敏,复旦大学人类表型组研究院博士研究生,主要开展膳食营养与口腔、肠道微生物关联的研究,以第一作者或共同第一作者将研究成果发表于Nutrients、ERJ Open Res 和BMC Microbiol等期刊。博士期间在2022年肠道大会之循证营养会议上报告,获得国家奖学金、复旦大学优秀学生等荣誉。
https://wap.sciencenet.cn/blog-3558836-1503971.html
上一篇:祝贺 | Phenomics主编金力院士被授予“上海科技期刊杰出科技人物”
下一篇:Phenomics | 上海体育大学王茹教授团队基于9种机器学习方法构建游泳人才天赋预测模型
全部作者的其他最新博文
- • Phenomics | 《表型组学(英文)》2025 年第五期文章合集
- • 征文通知|第二十八届中国科协年会专题论坛——生命组学大数据与人工智能的交叉融合专题论坛
- • Phenomics | 中山大学肿瘤防治中心曾木圣院士团队发表综述:肿瘤诊疗新靶点,整合素α6靶向技术引领精准医疗新时代
- • Phenomics | 上海交通大学医学院张孝勇教授团队开发磁共振成像降噪新方法,有潜力改善脑小血管病的诊断效能
- • Phenomics | 复旦大学倪挺教授团队揭示基因内含子多聚腺苷酸化调控细胞衰老新机制
- • Phenomics | 加拿大阿尔伯塔大学和复旦大学联合开发基于文本、音频和视频的多模态抑郁症检测与评估方法