博文
东华大学张国军研究员/刘吉轩副研究员及赛迈科吴厚政博士团队对高熵电池正极材料的全新综述
||
原文出自 Journal of Advanced Ceramics (先进陶瓷) 期刊
Cite this article:
https://doi.org/10.26599/JAC.2024.9220913
1、研究背景
新能源汽车与储能产业协同发展已成为减少碳排放的必然。正极材料是决定动力电池能量密度和成本的关键材料,而目前开发和应用的正极材料还不能满足高比容量、低成本、安全、稳定性好的要求。高熵材料是由多个主元素以等摩尔或近等摩尔比组成的一种新型单相材料。多元素之间的相互作用可以在提高材料综合性能方面发挥重要作用,有望解决电池材料在实际应用中的局限性。
2、文章亮点
东华大学功能材料研究中心张国军研究员/刘吉轩副研究员及赛迈科吴厚政博士团队对目前动力电池正极材料的研究现状进行了综述。首先概述了锂离子电池和钠离子电池正极材料的发展历程、应用前景和面临的挑战。在此基础上,系统阐述了当前正极材料的改性策略和不足之处,包括工艺优化、元素掺杂、表面涂层和结构设计。并且回顾了高熵电池材料的设计概念,总结现有的研究成果和存在的问题,强调高熵效应对电化学性能的重要作用。最后,展望了可充电动力电池正极材料的未来发展方向,畅想了高熵电池材料在能源领域的功能应用。
3、研究结果及结论
目前,已成功开发并广泛商业化的锂离子电池正极材料主要有四类:锂钴氧化物(LCO)、锂锰氧化物(LMO)、磷酸铁锂(LFP)以及锂镍钴锰氧化物(NCM)和锂镍钴铝氧化物(NCA)等三元材料。图1总结了上述材料存在的商业化问题。
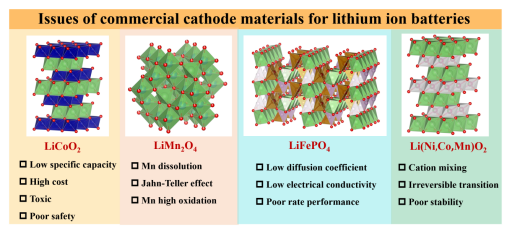
图1 锂离子电池商用正极材料面临的问题
商业化发展的锂离子电池正极材料中,LiCoO2的实际可逆容量较低,且Co具有高毒性、资源稀缺、价格昂贵。LiMn2O4由于Jahn-Teller效应、Mn3+的溶解和电解液的分解,导致容量衰减严重,循环性能下降。LiFePO4体相Li+扩散系数低,低温性能差,理论容量相对较低。尽管三元材料NCM和NCA具有较高的比容量和优良的循环寿命,但存在电压平台低和元素含量控制困难的问题。
新能源汽车的快速发展对电池的需求大幅上升,锂资源短缺的瓶颈逐渐显现,成本较高限制了锂离子电池的大规模应用。钠离子电池体系由于具有资源丰富、价格低廉、环境友好,以及与锂离子电池相近的电化学性质,在电池领域得到越来越广泛的关注。目前,研究最多的钠离子电池正极材料主要有过渡金属氧化物,聚阴离子化合物以及普鲁士蓝/白化合物。过渡金属氧化物可分为层状和隧道状两种。当钠含量较高时,一般以层状结构为主,MO2层和Na层交替排布,钠离子位于层间。当钠含量较低时(x<0.5),主要以隧道结构的氧化物为主。后者因初始钠含量过低,导致首周充电比容量较低,限制了它在实际中的应用。层状氧化物主要分为O2、O3、P2、P3型,其中“O”或“P”表示钠离子在八面体或棱镜中的位置,数字表示不同氧化层的重复排列单元。其中,O3和P2是钠离子电池层状正极材料中最常见的两种结构。O3相正极材料具有较高的初始Na含量,能够脱出更多的钠离子,具有较高的容量,但在高电压时难以稳定结构,可逆性差;P2相正极材料具有较大的Na层间距,能够提升钠离子的传输速率和保持层状结构的完整性,具有优异的倍率性能和循环性能,但由于Na含量不足而显示出较低的电荷容量,当与阳极电极匹配组装全电池时,其有效比容量不能得到充分利用,需要进行预钠化(图2)。
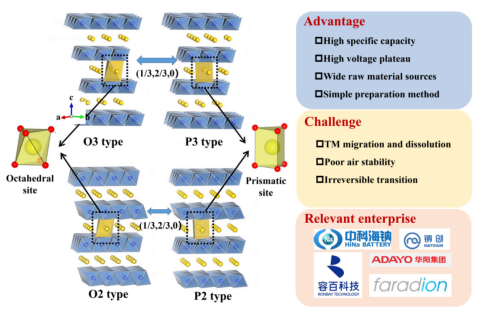
图2层状氧化物钠离子电池正极材料的晶体结构与市场化情况
聚阴离子型化合物由聚阴离子多面体和过渡金属离子多面体通过强共价键连接成,具有坚固且开放的三维网络结构,热稳定性和电化学稳定性最高,因此,在循环寿命方面表现最优。不足之处是成本高、能量密度低、倍率性能差(图3)。
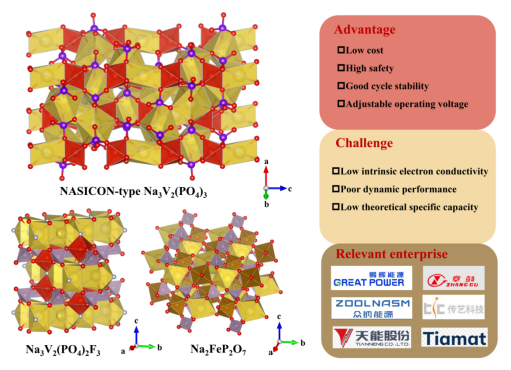
图3聚阴离子钠离子电池正极材料的晶体结构与市场化情况
普鲁士蓝类化合物是一种具有三维网状结构的配位聚合物,具有较大的隧道结构,可允许钠离子自由嵌入和脱嵌。同时,其能量密度高,且核心材料为Fe和Mn,成本相对较低。但由于化合物中Fe(CN)6空位和H2O的存在,导致倍率性能差、循环不稳定、库伦效率低(≤90%)等问题,此外,普鲁士蓝类化合物的热稳定性差,与水反应会生成有毒的HCN,存在安全性和环境处理难题(图4)。
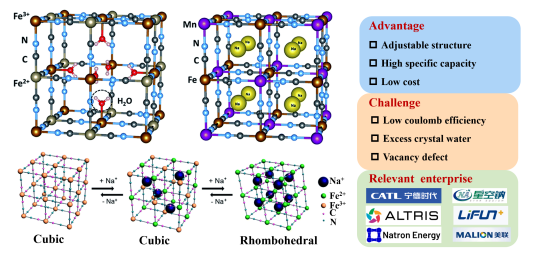
图4普鲁士蓝类合物钠离子电池正极材料的晶体结构与市场化情况
为了改善上述正极材料存在的问题,科研人员不断探索各种改善策略。迄今为止,改善其电化学性能的策略主要包括优化合成工艺、结构设计、表面包覆与元素掺杂等(图5)。优化合成工艺常被用于修饰聚阴离子型化合物和普鲁士蓝类似物正极材料,以减少有害杂质、空位和结晶水的形成。然而,这些方法由于其复杂性、低产量和有限的工业潜力而不常用。结构设计策略旨在通过增加电解质与电极材料之间的接触面积,缩短锂/钠离子的扩散路径,减缓材料在充放电过程中的体积变化来改善正极材料的电化学动力学和稳定性。然而精确地调节所制备的正极材料的形态和关键性能往往是具有挑战性的。表面包覆通常采用碳材料、金属氧化物和导电聚合物等作为保护层涂覆在电极材料表面,以提高电子/离子电导率,抑制表面副反应的发生,稳定结构。然而,涂层的厚度和不均匀性会增加离子传递阻抗,降低电池材料的倍率性能。元素掺杂是目前应用最广泛的电池正极材料改性策略,它通常可以实现以下功能:(1)提高材料的电子导电性和离子迁移率;(2)提高平均工作电压,激活阴离子氧化还原反应,从而提高材料比容量;(3)减缓离子嵌入/脱出过程中的晶格应变,提高材料的循环稳定性。然而,掺杂量和掺杂机制需要进一步深入研究。
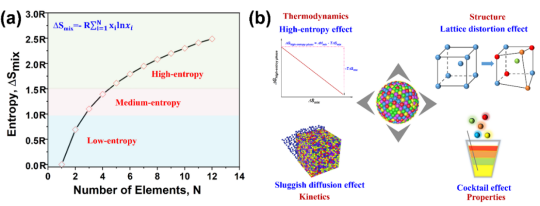
图5当前正极材料优化策略及特点
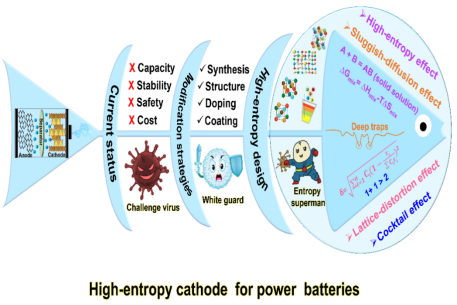
高熵材料(High-entropy materials,HEMs)是一类由多元素组成的新型材料。通过组合多个主要元素,可以实现最佳熵配置,从而提高性能。高熵氧化物(HEOs)具有较高的离子电导率,并且过渡金属高熵氧化物具有较高的理论比容量。此外,元素组成的近等摩尔比解决了材料成本降低和可持续性的问题。与传统电池正极材料相比,高熵电池正极材料的主要优点是其长期性能的提高。这主要归功于四大高熵效应:(1)高熵效应:根据Gibbs-Helmholtz方程,ΔGmix = ΔHmix - TΔSmix,其中ΔGmix、ΔHmix、ΔSmix分别代表固溶反应自由能变化、固溶反应焓变、固溶反应熵变(按混合熵计算),T为反应温度。高熵策略可以增加体系中的构型熵,从而提高ΔSmix的值,促进单相固溶体的形成并提高其稳定性。这为电池材料在更高温度下形成单相提供了可能性,克服了焓的能量障碍。(2)迟滞扩散效应:与传统材料相比,高熵材料表现出多个离子的缓慢扩散,从而抑制了相关的相变。晶体位置之间相邻原子排列的差异可能会增加这些位置之间扩散的迁移障碍,从而减少不必要的迁移。这可以形成更稳定的晶体结构和抑制晶间裂纹。(3)晶格畸变效应:不同离子大小和半径的元素在空间排列上的不对称性可能导致晶格畸变,从而影响电池材料中带电离子(如Li+和Na+)的行为。这反过来又影响了高熵电池正极材料的性能,包括导电性、导热性和机械强度。此外,高度扭曲的结构会在晶格中产生缺陷,促进电子、Li+和Na+的迁移。(4)鸡尾酒效应:在高熵电池材料中,电化学性能取决于单个掺杂元素的平均特性和元素之间的相互作用。因此,调整不同组分的种类和含量可以调节高熵电池正极材料的综合性能。这将降低电池材料的成本,增加相和结构的稳定性,抑制不必要的离子迁移,并调整电学、热学和机械性能,从而获得高性能的正极材料。

图7高熵材料的定义及高熵效应
表格1系统总结归纳了高熵正极材料在LIBs/SIBs的应用。通过分析可知,组成高熵正极材料的各主要元素起到了不用的作用,例如,Ni2+、Cu2+、Fe3+和Co3+具有电化学活性,为材料提供容量;Zn2+、Zr4+、Mn4+、Mg2+和Ti4+具有稳定结构和抑制相变的作用;Cu2+、Fe3+、Sn4+、Sb5+有助于提高平均电压;Li+, Mg2+, Zn2+可以触发阴离子的氧化还原,导致正极材料的电压范围和容量增加。这些过渡金属元素协同提高电池正极材料的整体电化学性能。
Materials | Electrochemical performance | ||||
Voltage | IDSC (mAh g-1 ) | ICE (%) | Capacity retention (%) | Ref. | |
(Lix(Co0.2Cu0.2Mg0.2Ni0.2Zn0.2)OFx) | 2-4.5V | 161 (0.1C) | ~88 | ~62.5 (0.1C, 150 th) | [234] |
LiNa(NiCoMnAlFe)1O2 | 3-4.5V | 75 (0.1C) | ~ | ~83 (0.1C, 20 th) | [239] |
Li1.3Mn2+0.1Co2+0.1Mn3+0.1Cr3+0.1Ti0.1Nb0.2O1.7F0.3 | 1.4-4.7V | 307 (20 mA g-1) | ~ | 84 (20 th) | [240] |
LiNi0.2Mn0.2Co0.2Fe0.2Ti0.2O2 | 1.2-4.4V | 160 | ~ | ~53 (50 th) | [235] |
LiNi0.8Mn0.13Ti0.02Mg0.02Nb0.01Mo0.02O2 | 2.5-4.3V | 210.1 (C/3) | 94 | ~98.5 (C/3, 100 th) | [236] |
LiNi0.8Mn0.1 Co0.1O2 | 208.2 (C/3) | 82 | 87.1 (C/3, 100 th) | ||
Li1.0(Li0.15Mn0.50Ni0.15Co0.10Fe0.025Cu0.025Al0.025Mg0.025)O2 | 2.1-4.8V | ~300 (0.1C) | 85 | >93 (0.1C, 100 th) | [231] |
Li1.20Mn0.54Ni0.13Co0.13O2 | ~280 (0.1C) | ~ | >51 (0.1C, 100 th) | ||
Li1.25Ni2+0.1Co2+0.1Mn3+0.1Cr3+0.1Ti0.2Nb0.15O1.8F0.2 | 1.5-4.8V | 277.6 (20 mA g-1) | ~ | 87.1 (30 th) | [233] |
NaNi0.12Cu0.12Mg0.12Fe0.15Co0.15Mn0.1Ti0.1Sn0.1Sb0.04O2 | 2.0-3.9V | ~110 (0.1C) | ~89 | ~83 (3C, 500 th) | [265] |
Na2/3Li1/6Fe1/6Co1/6Ni1/6Mn1/3O2 | 2.0-4.5V | 171.2 (0.1C) | ~ | ~89.3 (1C, 90 th) | [266] |
Na1.26Mn0.4Fe0.15Ni0.15Cu0.15Co0.15[Fe(CN)6] | 2.0-4.2V | 120 (0.01A g-1) | 94.9 | 90 (0.1A g-1, 200 th) | [262] |
LEM-HCF | ~120 (0.01A g-1) | 90.7 | 80 (0.1A g-1, 200 th) | ||
NaCu0.1Ni0.3Fe0.2Mn0.2Ti0.2O2 | 2-3.9V | 130 (0.1C) | ~100 | 87 (0.1C, 100 th) | [256] |
NaNi0.25Mg0.05Cu0.1Fe0.2Mn0.2Ti0.1Sn0.1O2 | 2-4V | 130.8 (0.1C) | 91 | 75 (1C, 500 th) | [257] |
NaNi0.4Fe0.2Mn0.4O2 | 135.6 (0.1C) | 87 | 38 (1C, 500 th) | ||
Na3VAl0.2Cr0.2Fe0.2In0.2Ga0.2(PO4)3 | 2.5-4.4V | 102 (0.1C) | 90 | 99.18 (10C, 1000 th) | [259] |
Na3VAl(PO4)3 | 88 (0.1C) | 71 | 96.2 (10C, 1000 th) | ||
Na3VCr(PO4)3 | 81 (0.1C) | 70 | 91.13 (10C, 1000 th) | ||
Na3V1.9(Ca,Mg,Al,Cr,Mn)0.1(PO4)2F3 | 2.0-4.5V | 118.5 (0.1C) | ~ | 90.2 (0.5C, 400 th) | [260] |
Na3V2(PO4)2F3 | 107.4 (0.1C) | ~ | 58.6 (0.5C, 400 th) | ||
Na0.95Li0.06Ni0.25Cu0.05Fe0.15Mn0.49O2 | 2.8-4.2V | 141 (0.2C) | 98.2 | >85 (0.2C, 1000 th) | [208] |
NaFe0.2Cu0.1Ni0.2Mn0.3Ti0.2O2 | 2.0-4.1V | 121 (0.1C) | 90 | ~83.8 (2C, 200 th) | [267] |
NaNi0.3Cu0.1Fe0.2Mn0.2Ti0.2O2 | 2.0-4.0V | 123.6 (0.1C) | ~ | 90.05 (0.1C, 50 th) | [268] |
NaNi0.4Fe0.2Mn0.2Ti0.2O2 | 129.1 (0.1C) | ~ | 74.83 (0.1C, 50 th) | ||
NaNi0.1Mn0.15Co0.2Cu0.1Fe0.1Li0.1Ti0.15Sn0.1O2 | 2.0-4.1V | 115 (10 mA g-1) | ~ | 82.7 (160 mA g-1, 1000 th) | [269] |
NaNi0.5Mn0.5O2 | 117.1 (10 mA g-1) | ~ | 0 (160 mA g-1, 400 th) | ||
Na0.85Li0.05Ni0.25Cu0.025Mg0.025Fe0.05Al0.05Mn0.5Ti0.05O2 | 2.0-4.1V | 122 (0.2C) | 95.4 | 89 (10C, 1000 th) | [258] |
S-HE | 120 (0.2C) | 83.1 | 82.8 (10C, 1000 th) | ||
Na0.7Mn0.4Ni0.3Cu0.1Fe0.1Ti0.1O1.95F0.1 | 2.0-4.3V | 133.5 (20 mA g-1) | 97.6 | 99.5 (200 th) | [270] |
Notes: Initial discharge specific capacity (IDSC), initial Coulombic efficiency (ICE)
尽管高熵电池材料在成本、安全性和循环寿命方面都有很好的应用前景,但目前还处于早期阶段。并且多种过渡金属的引入增加了材料的复杂性,目前还没有系统的理论来解释高熵电池材料的储存机制。此外,许多高熵材料的电化学性能在现阶段仍有很大的提升空间。因此,基于高熵策略设计的电池正极材料是机遇与挑战并存的。未来高熵电池材料的发展可以从以下几个方面考虑:(1)计算辅助设计。(2)开发特定合成方法。(3)结合先进的表征技术阐明高熵电化学机理。(4)建立高通量数据库。
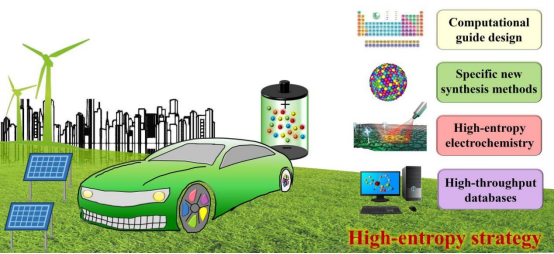
图8高熵电池材料的未来发展方向
4、作者及研究团队简介

第一作者:黄丽萍,东华大学材料科学与工程学院博士研究生,主要研究方向为钠离子电池正极。

第二作者:朱婧婷,博士,东华大学/赛迈科先进材料股份有限公司联合招收博士后。

通讯作者:刘吉轩,博士,博士生导师,东华大学功能材料研究中心副研究员,中国硅酸盐学会特陶分会理事。主要从事高熵陶瓷、超高温陶瓷、核能陶瓷方向的基础研究工作,发表学术论文80篇。

通讯作者:吴厚政,博士,现任赛迈科先进材料股份有限公司首席技术官、副总经理,担任中国核学会核石墨及碳材料测试与应用分会高级顾问。

通讯作者:张国军,博士,博士生导师,东华大学功能材料研究中心研究员,世界陶瓷科学院院士,中国硅酸盐学会特陶分会理事。长期从事非氧化物陶瓷的制备科学、微结构调控与性能表征研究,发表学术论文200余篇。
Journal of Advanced Ceramics (先进陶瓷)期刊简介
期刊中文网页:http://www.ccs-cicc.com/index.html
期刊英文网页:https://www.sciopen.com/journal/2226-4108
https://wap.sciencenet.cn/blog-3534092-1435978.html
上一篇:昆明理工大学葛振华课题组:通过天然矿物原位相分离增强硫化铜热电和机械性能
下一篇:中国科学院上海硅酸盐研究所李江团队:Y取代对(Tb1-xYx)3Al5O12磁光陶瓷微观结构、磁光性能与热学性能的影响
