博文
Biology:“口-肠轴” 宿主机制的新发现——HGF加重牙周炎相关肠道损伤和菌群紊乱
||
文章导读
牙周炎是一种由口腔微生态失衡引发的慢性炎症性疾病[1]。研究表明,牙周炎不仅局限于口腔局部组织损伤,还可能与多种全身性疾病密切相关,包括糖尿病、肝脏损伤和阿尔茨海默病等[1, 2]。然而,牙周炎与系统性疾病之间的关联机制尚不明确。
近年来,“口-肠轴”概念逐渐引起关注,指的是口腔疾病可能通过干扰肠道稳态进而影响全身健康的潜在通路。该理论认为,来源于口腔的致病菌 (如牙龈卟啉单胞菌) 可迁移至远端肠道,重塑肠道菌群结构,损害肠道屏障功能,进而诱导“肠漏”表型。这种屏障破坏使得肠道内源性病原体及其代谢产物进入循环系统,可能成为牙周炎与多种系统性疾病之间的桥梁[3-5]。
然而,当前研究多集中于口腔微生物的易位对“口-肠轴”的影响,对其中的宿主因子探索不足。肝细胞生长因子 (Hepatocyte Growth Factor, HGF) 是一种多功能细胞因子,在上皮和内皮细胞的增殖、迁移、形态发生、炎症反应和肿瘤发生发展等方面具有广泛作用[6-8]。临床研究发现,牙周炎患者的龈沟液中HGF水平显著升高,且其浓度与疾病严重程度呈正相关[9, 10]。近期,广州医科大学口腔医学院王新红教授团队发现HGF加剧牙周炎的炎症反应和骨破坏[7],提示HGF可能是作为影响“口-肠轴”的潜在候选因子。
基于此,该团队进一步在Biology期刊发表了相关研究,探讨HGF在牙周炎相关肠道损伤中的作用。该研究基于结扎诱导的牙周炎模型,使用HGF过表达基因小鼠,系统分析了HGF对肠道机械屏障、免疫屏障和微生物屏障的影响。研究结果揭示了HGF表达水平与肠道菌群失调及屏障破坏之间的密切关联,提出HGF可能通过影响“口-肠轴”,从而成为连接牙周炎与系统性疾病的新型关键介质。
研究内容及结果
1. HGF增加牙周炎期间的肠道通透性并促进肠道屏障损伤
在牙周炎背景下,HGF可显著加剧肠道通透性和屏障功能障碍。具体表现为血清中LPS和D-乳酸水平的进一步升高,提示肠道内毒素和代谢产物的系统性渗漏加重。同时,HGF导致肠绒毛结构破坏程度加深,包括绒毛高度降低、隐窝深度增加以及绒毛高度与隐窝深度比值下降。免疫组织化学结果显示,HGF进一步抑制了紧密连接蛋白occludin的表达,而对ZO-1的表达影响不显著。此外,HGF还促使免疫相关蛋白NOD2在肠道中的表达上调。上述结果提示,HGF可能通过影响肠道机械屏障和免疫屏障,从而在“口-肠轴”失衡中发挥关键作用 (图1, 2)。
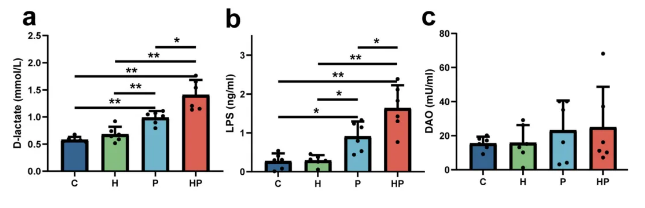
图1. HGF对血清DAO、D-乳酸、内毒素的影响
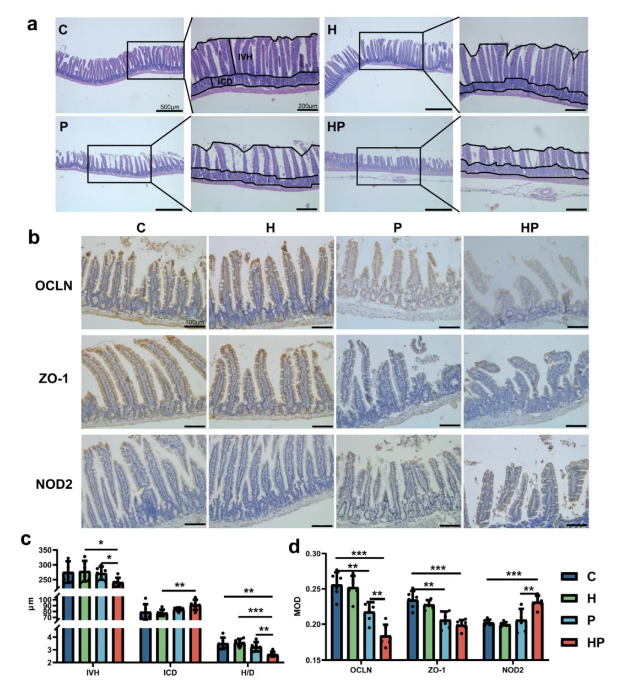
图2. HGF对肠道黏膜形态以及OCLN、ZO-1和NOD2的影响
2. HGF改变了小鼠肠道菌群的多样性
本研究通过分析包括sobs、Chao1、ACE、Coverage、Shannon和Simpson在内的多种 α 多样性指数,揭示了肠道菌群在不同处理条件下存在显著差异。结果显示,牙周炎显著改变了上述所有α多样性指标,而在牙周炎背景下,HGF表达进一步显著提高了sobs、Chao1和ACE指数,提示菌群丰富度的增强。此外,β多样性分析显示,不同处理组之间肠道菌群结构显著分离 (R² = 0.6211,p = 0.001),提示群落组成发生明显变化。有趣的是,无论是否伴随牙周炎,HGF均可使影响了肠道菌群的β多样性,提示HGF本身就具备塑造肠道微生态结构的作用 (图3)。
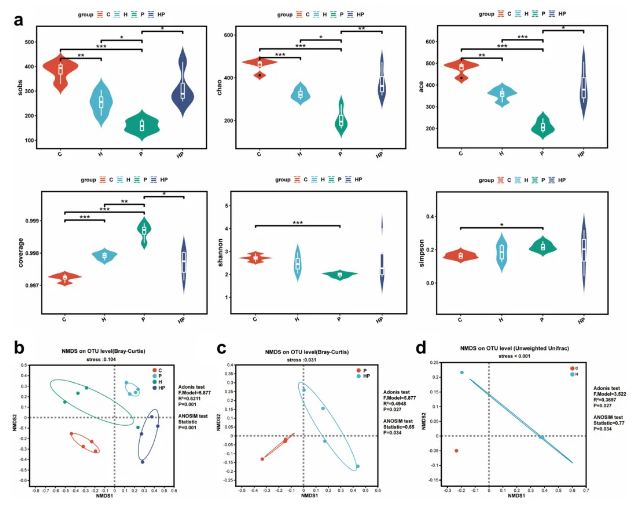
图3. HGF对肠道菌群α多样性和β多样性的影响
3.HGF促进牙周炎相关的菌群紊乱
在牙周炎背景下,HGF提高了肠道中促炎菌群的丰度,包括Streptococcus、Ruminococcaceae、Prevotellaceae_UCG-001以及Desulfovibrio fairfieldensis。值得注意的是,HGF还促进了牙周炎相关致病菌 (如Desulfovibrio) 在肠道菌群中的富集 (图4)。
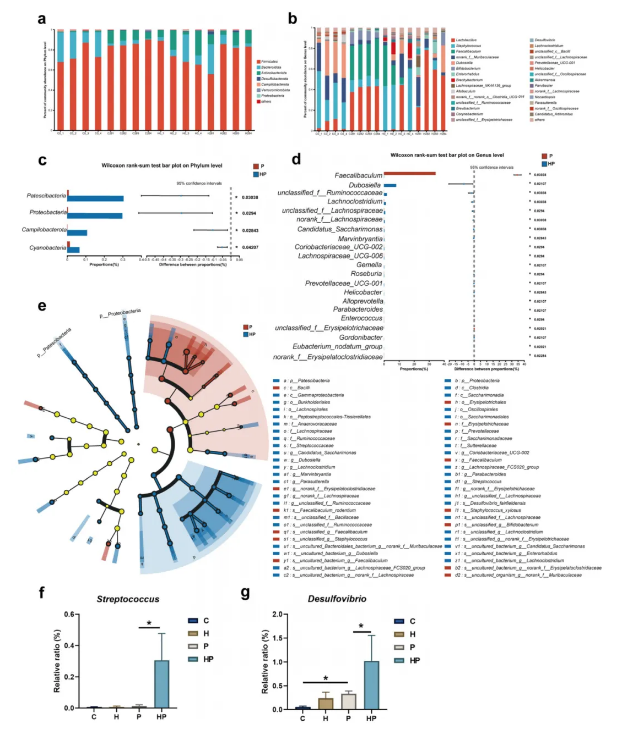
图4. HGF对肠道菌群组成的影响
微生物网络分析显示,在HGF高表达的牙周炎小鼠中,促炎菌群包括g_Prevotellaceae_UCG-001、g_Bacteroides、Alistipes和g_NK4A214_group 作为核心微生物组成分与其他物种相互作用 (图5)。
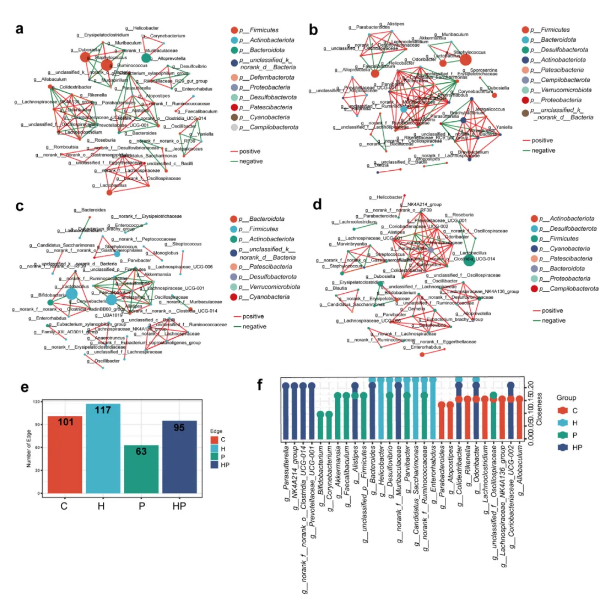
图5. HGF对微生物网络结构的影响
PICRUSt2功能预测分析表明,牙周炎状态下,HGF显著改变了肠道菌群的功能组成,尤其是与代谢相关的功能路径。MetaCyc分析显示,HGF显著上调了与肽聚糖、磷脂和核苷酸合成相关的代谢途径,可能有助于特定菌群的快速扩增。此外,参与O抗原生物合成的代谢途径也在HGF表达升高条件下显著富集,该代谢产物是LPS的关键组成部分,与我们观察到的血清LPS水平升高一致 (图6)。综上所述, HGF整体上进一步破坏了肠道微生态的结构和功能,增强了促炎微生物的稳态主导作用,从而加剧肠道损伤。
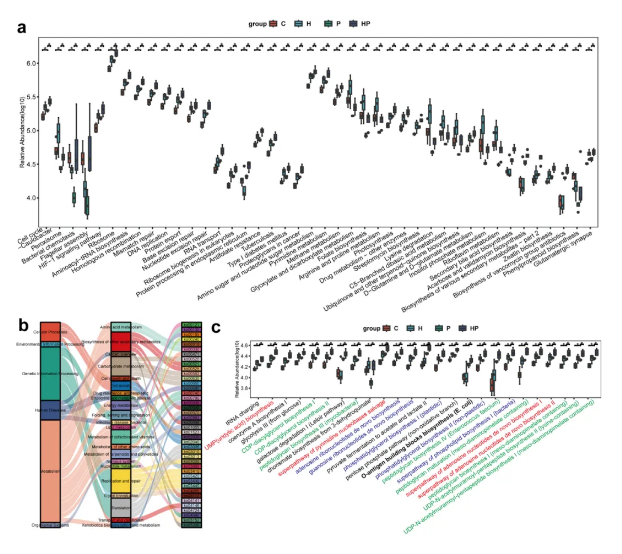
图6. HGF对肠道菌群功能的影响
研究总结
本研究发现,HGF 可能作为一种关键宿主因子,参与调控牙周炎相关“口-肠轴”失衡。在HGF过表达小鼠中,肠道的机械屏障、免疫屏障及微生态屏障均受到明显破坏,最终表现为“肠漏”表型,这一表型被认为是“口-肠轴”失调的重要特征。这一发现揭示了牙周炎不仅通过口腔菌群的移位影响肠道,还可能通过宿主因子,如HGF,放大肠道屏障的脆弱性,进而影响全身健康。因此,HGF可能在口腔-肠道-全身之间的病理链条中起到关键桥梁作用。
未来研究应进一步采用粪菌移植等方法验证HGF在牙周炎介导的肠道屏障破坏中的因果关系,并深入探讨HGF诱导的肠道渗漏如何驱动多器官功能障碍的发生机制,从而为牙周炎相关全身性并发症的精准干预提供新的理论依据和治疗靶点。
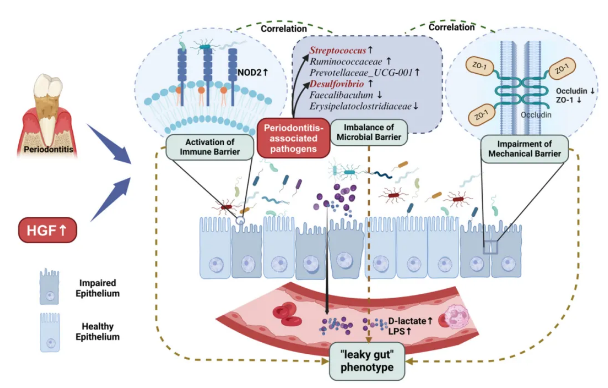
图7. HGF 对牙周炎小鼠肠道通透性和肠道屏障 (机械屏障、免疫屏障和微生物屏障) 的影响。
本研究的通讯作者是来自广州医科大学口腔医学院的王新红教授,第一作者为来自广州医科大学口腔医学院的陈圳,该论文的发表受到了广州市科学技术局的资助。
原文出自 Biology 期刊:https://www.mdpi.com/3296240
期刊主页:https://www.mdpi.com/journal/biology
Biology 期刊介绍
主编:
Jukka Finne, University of Helsinki, Finland; Andrés Moya, University of Valencia and CSIC, Spain
期刊主要涵盖细胞生物学、发育生物学、进化生物学、生物化学与分子生物学、微生物学等所有生物领域。期刊被 Scopus、SCIE (Web of Science)、PubMed 等重要数据库收录。
2024 Impact Factor:3.5 (JCR Q1*)
2024 CiteScore:7.4 (Q1**)
Time to First Decision:17.4 Days
Acceptance to Publication:2.5 Days
* JCR Q1 at "Biology"
** CiteScore Q1 at "General Agricultural and Biological Sciences"


https://wap.sciencenet.cn/blog-3516770-1502631.html
上一篇:聚焦水文科学——Hydrology
下一篇:Animals 吉林农业大学车东升教授创建特刊:营养——提升猪健康与产能的关键