博文
Metabolites 探索自闭症代谢重编程新机制:脂多糖诱导的维生素转运抑制与治疗前景
||
文章导读
自闭症谱系障碍 (ASD) 作为一种复杂的神经发育疾病,其发病机制一直是神经科学领域的研究热点。德国图宾根大学的Albion Dervishi 博士近期在 Metabolites 发表了一篇论文,该研究创新性地提出了微生物脂多糖 (LPS) 通过抑制维生素转运蛋白功能而触发大脑代谢重编程的系统假说,为ASD的病理机制和治疗策略开辟了新的研究方向。

图形摘要
研究过程与结果
过去的ASD研究主要聚焦于神经回路异常和遗传变异,然而越来越多的证据表明全身性代谢异常在疾病发生发展中起着关键作用。ASD患者普遍表现出线粒体功能障碍、氧化应激、氨基酸代谢失衡等代谢异常特征。研究团队注意到,这些代谢异常与ASD患者体内升高的脂多糖 (LPS) 水平可能存在重要关联。LPS作为革兰氏阴性菌细胞壁成分,不仅具有强效促炎作用,还能穿过肠道和血脑屏障影响中枢神经系统功能。
研究团队采用创新的“个性化代谢边缘图谱”(PM³) 系统生物学模型,对12例ASD患者和12例健康对照者的前额叶皮质样本进行了深入分析。这一模型突破了传统单基因分析的局限,通过整合158个与能量代谢、氧化还原平衡等相关的基因数据,结合无监督机器学习算法,成功捕捉到了代谢通路中细微但协调的转录变化。研究结果显示,ASD患者大脑中多种维生素转运蛋白的转录水平显著下调,其中钠依赖性多种维生素转运蛋白 (SLC5A6) 下调4.5%,硫胺素转运蛋白 (SLC19A2) 下调3.5%。这些关键转运蛋白的功能抑制可能导致细胞内生物素、硫胺素等辅因子供应不足,进而影响依赖这些辅因子的酶活性。
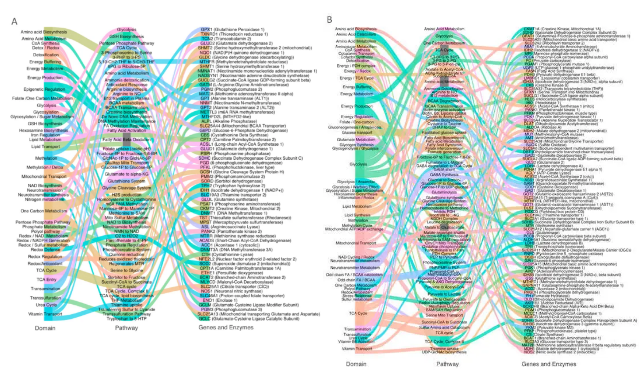
图1. (A) ASD皮质中上调的基因。(B) ASD皮质中下调的基因。
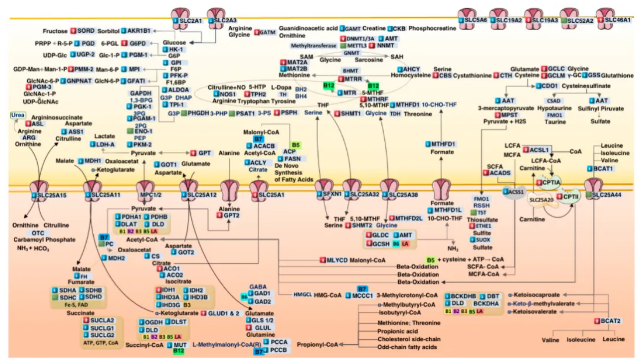
图2. 自闭症代谢功能障碍的系统模型。
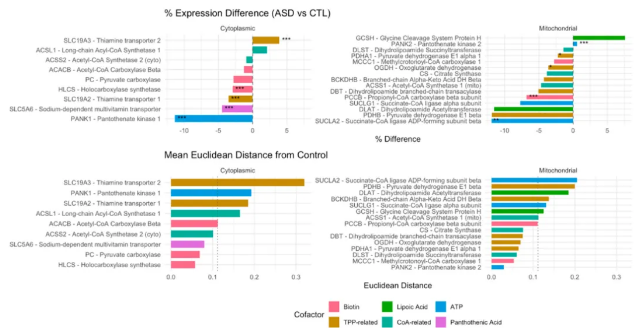
图3. 自闭症中辅因子依赖性转录组易感性。
随着研究的深入,研究团队进一步发现了ASD患者大脑中更为广泛的代谢紊乱。患者线粒体能量代谢相关基因普遍下调,包括丙酮酸脱氢酶复合物、异柠檬酸脱氢酶等TCA循环关键酶,这种抑制可能导致ATP生成减少和氧化还原失衡。与此同时,研究观察到糖酵解关键酶的转录水平降低,而磷酸戊糖途径和硫代谢相关基因上调,反映出ASD患者大脑在面对能量短缺和氧化应激时的适应性改变。
基于这些发现,研究团队提出了LPS驱动代谢紊乱的机制模型。LPS可能通过激活TLR4/NF-κB信号通路下调转运蛋白表达,或通过蛋白激酶A等途径破坏转运蛋白的膜定位,从而限制辅因子的细胞内供应。这种转运抑制引发的辅因子缺乏又会进一步导致依赖这些辅因子的酶活性降低,形成线粒体功能障碍和氧化应激的恶性循环。
这项研究的重要意义在于为ASD的精准治疗提供了潜在的新靶点。营养干预如补充生物素、硫胺素等辅因子或能部分缓解转运抑制导致的代谢缺陷;微生物组调控策略或能通过减少肠道LPS产生间接改善大脑代谢状态;而针对转运蛋白的靶向治疗则可能成为更具特异性的干预手段。当然,这些治疗设想还需要进一步的实验验证和临床研究。
值得注意的是,这项研究也存在一些局限性。由于数据来源于死后脑组织,无法直接建立LPS水平与基因表达的因果关系;实际辅因子浓度和酶活性的缺失也需要后续研究补充。未来的研究方向需结合多组学分析、建立LPS动物模型以及开展临床干预试验,以全面验证这一创新性假说。
研究总结
本研究通过系统生物学方法,首次将微生物组、维生素转运和大脑代谢重编程有机联系起来,为理解ASD的复杂机制提供了全新的理论框架。这一突破不仅丰富了ASD的基础研究,更重要的是为开发靶向代谢的治疗策略奠定了科学基础。随着后续研究的深入,这一假说有望转化为具有临床应用价值的诊疗方案,为ASD患者带来新的治疗希望。该研究也启发我们,在神经发育疾病的研究中,需要更多地关注系统层面的代谢调控网络,才能更全面地理解疾病的本质并开发有效的干预措施。
阅读英文原文:https://www.mdpi.com/3356290
期刊主页:https://www.mdpi.com/journal/metabolites
Metabolites 期刊介绍
主编:Amedeo Lonardo , Azienda Ospedaliero-Universitaria, Italy
期刊内容涵盖代谢组学、代谢生物化学、计算和系统生物学、生物技术和医学领域相关的代谢物以及代谢方面的研究。
2024 Impact Factor:3.7
2024 CiteScore:6.9
Time to First Decision:14.4 Days
Acceptance to Publication:3.6 Days


https://wap.sciencenet.cn/blog-3516770-1496098.html
上一篇:Microorganisms:石河子大学高飞飞博士创建特刊——果酒发酵与微生物群落
下一篇:Publications:北京工业大学梁国强博士、张硕博士合作创建特刊——AI时代的科学计量和影响力评价