一种由KRAS基因突变驱动的胰腺导管腺癌(PDAC)和结直肠癌(CRC)中能激活T细胞活性的新型癌症疫苗,在早期测试中显示出潜力。这款由 Elicio Therapeutics 公司研发的研究性疫苗ELI-002,旨在训练免疫系统识别并攻击携带突变型 KRAS 基因的肿瘤细胞。约93%的胰腺导管腺癌和50%的结直肠癌患者体内都存在这种基因突变。
尽管该疫苗目前仅处于1期临床试验阶段,但在接受标准局部区域治疗后仍存在微量KRAS 突变残留病灶的患者中,超80%在接种后产生了强烈的T细胞应答。美国UCLA的研究团队本月在(Nature Medicine)杂志发表的研究称,这种强烈的T细胞免疫应答与更长的无复发生存期和总生存期相关。
KRAS是人类肿瘤中最常见的驱动突变基因之一,在93%的胰腺导管腺癌(PDAC)和 50%的结直肠癌(CRC)中存在突变(主要为 G12D、G12R 等亚型)。尽管手术、化疗等标准局部区域治疗可清除可见病灶,但PDAC患者术后复发率仍居高不下。 微量残留病灶(MRD) 阳性(循环肿瘤DNA-ctDNA或血清肿瘤标志物 CA19-9/CEA 检测确认)患者的传统中位数 RFS仅5.0-6.37个月,中位数总生存期(OS)约17个月,且复发后治疗多为姑息性,5 年生存率仅 23.3%。
传统疫苗的局限性与 ELI-002 2P 的创新
KRAS突变作为 “公享新抗原”,因发生率高、是理想的免疫治疗靶点。但传统肽疫苗(分子量 < 20 kDa)难以在淋巴结聚集,而淋巴结是抗原提呈细胞激活适应性免疫(T 细胞应答)的关键场所。ELI-002 2P 通过 “两亲性修饰”(结合白蛋白亲和脂质基团)解决这一问题:可借助内源性白蛋白(约 65 kDa)的淋巴运输功能,从外周注射部位靶向到达淋巴结,同时包含mKRAS(G12D、G12R)两亲性肽抗原和两亲性佐剂 CpG-7909,可同时激活 CD4⁺辅助T细胞和CD8⁺细胞毒性T细胞。
本研究显示AMPLIFY-201试验的长期随访结果,验证ELI-002 2P在MRD阳性 PDAC/CRC 患者中的临床价值。能有一种疫苗在KRAS驱动型肿瘤中激活T细胞活性,这个结果潜力很大。因为这类肿瘤通常属于‘冷肿瘤’(即肿瘤微环境中免疫细胞浸润少、免疫活性低),因此迫切需要能为这类患者激活免疫应答反应的疗法。目前这项研究数据仍处于初步阶段,研究设计的样本量尚不足以对疗效进行量化判断。
1 期试验的关键结果:84%患者产生特异性T细胞应答,在这项(AMPLIFY-201)的1期研究中,20名胰腺导管腺癌和5名结直肠癌患者(均在手术和化疗后仍存在微量残留病灶)接受了ELI-002 多肽疫苗治疗,剂量分别为0.1毫克、0.5毫克、2.5毫克、5毫克和10毫克。研究人员确定了一个T细胞应答阈值:在基线水平上增加9.17倍,这一阈值能有效区分预后较好(17人,占68%)和预后较差(8人,占32%)的患者。
总体而言,25名患者中有21人(84%)产生了针对突变型KRAS的特异性T细胞应答,其中接受两种最高剂量(5毫克、10毫克)治疗的6名患者全部产生应答;此外,71% 的患者同时激活了CD4⁺和CD8⁺T细胞。研究发现,CD4⁺和CD8⁺T 细胞的共同激活与肿瘤标志物的整体应答反应显著相关。
通过“生物标志物分析”发现,21名患者(84%)出现肿瘤生物标志物应答(至少有一类ctDNA,或CA19-9,或CEA出现了符合试验标准的“减少”或“完全清除”),其中6人(3名胰腺导管腺癌患者、3名结直肠癌患者)实现肿瘤生物标志物的完全清除。
在中位数随访时间延长至19.7个月时,患者的中位数无复发生存期为16.3个月,中位总生存期为28.9个月。在达标T细胞应答阈值的患者,其中位数总生存期尚未达到(即随访期内仍有较多患者存活,至少有超过50%仍未发现有肿瘤复发/进展,且仍存活,达到“中位数”需要50%患者发生上述事件;若超过50%患者始终未出现这些情况,则记录中位数总生存期尚未达到”。
研究中也补充了支持数据:达标阈值的17例患者中,65%(11例)“无影像学的疾病进展”,其中5例甚至未接受后续治疗仍无复发,说明该组患者的无复发时间远超当前19.7个月的随访期,是预后良好的明确信号。
文章中同时提到 “未达到T细胞应答阈值患者(8例)的中位数影像学无复发率(RFS)为 3.02个月”,50%患者在3.02个月内就出现影像学的复发/进展,且所有患者最终均疾病进展;达标组(17例):超过50%患者随访19.7个月仍无复发/进展,直接体现了“T细胞应答达标”对延长无复发时间的显著作用,也印证了疫苗通过激活有效免疫应答,确实能延缓甚至阻止肿瘤复发。
总体来看,17名T细胞应答阈值达标(也就是T细胞对肿瘤细胞产生了免疫排斥反应)的患者中,11人未出现影像学进展;而8名未达标者(T细胞对肿瘤细胞没产生免疫排斥反应)的患者均出现影像学进展,其中7人已死亡。
此外,研究还发现67%的患者体内,免疫系统还将攻击范围扩大到了疫苗中未包含的其他肿瘤特异性抗原,这一现象或可能进一步扩大疫苗的保护范围。
临床疫苗接种技术细节:
一、疫苗接种程序
两亲性疫苗的接种程序以ELI-002 2P(1 期 AMPLIFY-201试验,2P配方,覆盖2种KRAS突变)为核心参考,后续7P 配方在其基础上优化:
1. ELI-002 2P(1 期试验)的标准程序
分三阶段给药,总周期含随访
诱导免疫期:8周内完成6剂皮下注射,目的是快速激活免疫系统对mKRAS的特异性识别。
抗原剂量固定:含 mKRAS G12D和G12R突变的两亲性肽(Amph-肽)各0.7mg,总肽剂量1.4mg;
佐剂剂量递增:两亲性佐剂 Amph-CpG-7909分5个剂量组(0.1mg、0.5mg、2.5mg、5.0mg、10.0mg),通过剂量递增验证安全性和最佳应答剂量(最终确定10.0mg为后续试验的参考剂量)。
观察期:诱导期结束后,进入3个月“无给药观察期”,监测患者免疫应答稳定性和肿瘤标志物变化(如 ctDNA、CA19-9/CEA)。
加强免疫期:观察期后,4周内完成4剂皮下注射,剂量与诱导期最终耐受剂量一致(如 10.0mg 佐剂组维持该剂量),目的是巩固免疫记忆、延长T细胞应答持续时间。
长期随访:首次接种后随访最长2年,定期检测免疫应答(T细胞活性)、影像学(肿瘤复发情况)和生存状态(OS/RFS)。
患者入组后的接种前提
仅针对术后MRD阳性患者(即标准手术+化疗/放疗后,影像学无可见肿瘤,但 ctDNA 阳性或血清 CA19-9/CEA升高),且需在术前治疗(如化疗、放疗)结束后,身体恢复至无明显并发症(如血常规、肝肾功能达标)再开始接种。
2. ELI-002 7P(后续试验)的程序调整
7P 配方(覆盖7种KRAS突变)在2P基础上优化给药频率,以适应更广人群:
诱导期:调整为“每周1次皮下注射”
加强期:改为“每两周1次皮下注射”,减少患者就医频率,同时维持免疫记忆;
剂量设计:肽剂量提升(如 4.9mg,为 2P 的 3.5 倍),佐剂固定为 10.0mg(基于 2P的安全数据,无需再递增),目前在135例胰腺癌患者的2期试验中验证(NCT05726864)。
目前,Elicio Therapeutics公司正针对135名KRAS驱动型胰腺导管腺癌患者,测试 ELI-002的7肽配方(ELI-002 7P),预计今年晚些时候公布无病生存期的中期数据。尽管现有研究结果具有潜力,但仍处于初步阶段。
两亲性分子疫苗制备原理
给抗原(Amph-肽)和佐剂(Amph-CpG) 均连接 “脂质分子”,形成 “两亲性分子”(一端亲水、一端亲脂);亲脂端可非共价结合体内内源性白蛋白(分子量~65kDa),使疫苗复合体从“小分子(<20kDa,易被血液清除)”变为“中大分子(~65kDa)”,优先通过淋巴管道运输至淋巴结(免疫系统激活T细胞的“核心器官”),避免在血液中稀释或被肝脏快速代谢。
肽抗原的结构设计
18-mer长肽+重叠短肽(OLP):2P配方的抗原为18个氨基酸的长肽(G12D、G12R 各1条),每个长肽搭配9-mer和10-mer的重叠短肽;
目的:18-mer长肽可被HLA-II类分子(提呈12-20mer肽)识别,激活CD4⁺辅助T细胞;短肽可被HLA-I类分子(提呈 8-10mer 肽)识别,激活 CD8⁺杀伤 T 细胞,实现CD4⁺/CD8⁺ T细胞激活”。
7P 配方的抗原在2P 基础上的扩展,新增 G12V、G12A、G12C、G12S、G13D 突变的 18-mer肽,共7条肽链,覆盖90%以上的KRAS 突变类型,适配更多HLA型别(如 HLA-A02:01、HLA-DRB104:01),使适用人群从“仅 G12D/R 突变患者”扩展至“25%的实体瘤患者”。
许多患者都存在KRAS突变,因此一款‘现成可用’(off-the-shelf,无需个性化定制)的疫苗可能让大量患者受益。它省去了定制个性化疫苗所需的成本和时间。不过,研究人员对这项进展,持非常谨慎的态度,认为现在就明确这款疫苗能否预防‘手术已清除所有病灶患者’的癌症复发,还为时过早,仍需开展更大规模的研究。这项工作实际上仅表明,该疫苗能诱导产生针对突变型KRAS的多功能CD4⁺和CD8⁺T 细胞免疫应答。“尽管1期研究中观察到的免疫信号和临床信号具有潜力和希望,且所呈现的科学数据具有可靠性,但这些发现尚未证实疫苗的疗效,需要更大规模的2期或3期试验中加以证实”。
乐观的预期是,ELI-002 2P疫苗在胰腺癌治疗中的生存数据,无论全队列还是T细胞应答达标患者,均显著优于普通治疗水平:全队列OS提升70%、RFS提升2-3倍,达标患者更是实现“随访19.7个月未达中位数生存时间”(传统治疗此时多数患者已复发/死亡)。这种差异的核心应该是疫苗突破了胰腺癌“冷肿瘤”和“KRAS不可靶向”的瓶颈,为胰腺癌治疗提供了“从‘清除病灶’到‘激活免疫防复发’”的新范式,即便存在1期试验的局限性,其对高危患者的生存改善幅度,仍超过当前普通治疗的天花板。
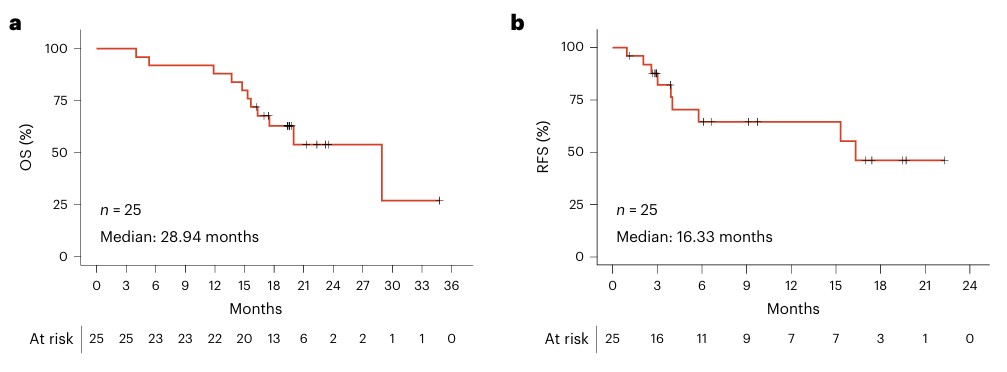
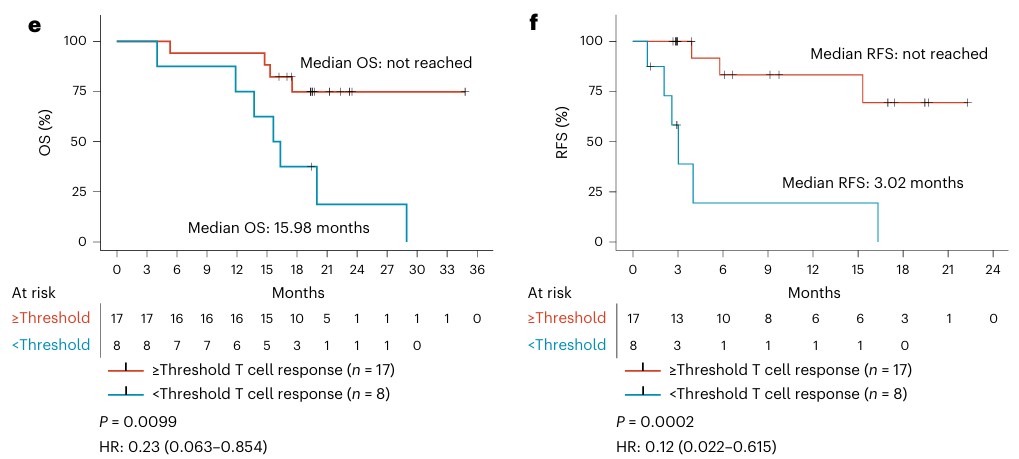
mKRAS特异性T细胞应答与肿瘤标志物应答与患者OS和RFS的相关性
Lymph node-targeted, mKRAS-specific amphiphile vaccine in pancreatic and colorectal cancer: phase 1 AMPLIFY-201 trial final results.
Nature Medicine. 11 Aug 2025
转载本文请联系原作者获取授权,同时请注明本文来自阎影科学网博客。
链接地址:https://wap.sciencenet.cn/blog-3302154-1498937.html?mobile=1
收藏

