精选
精选
肥胖症中导致代谢性疾病的原因是什么?
诸平
据德国莱比锡大学(Leipzig University)2025年2月11日提供的消息,肥胖症中导致代谢性疾病的原因是什么?(What are the causes of metabolic diseases in obesity?)以及来自医学界:肥胖症中代谢性疾病的原因调查(From the world of medicine: Causes of metabolic diseases in obesity investigated)2篇报道,现介绍如下,仅供参考。
体重和身体质量指数(body mass index简称BMI)本身不足以说明一个人是否会患上代谢紊乱。一项新的脂肪组织细胞图谱现在可以帮助解释为什么有些超重的人保持健康,而有些人则不然。该研究结果由德国莱比锡大学医学中心(University of Leipzig Medical Center, Leipzig, Germany)牵头,与来自瑞士、美国、德国的研究人员合作完成,已经在《细胞代谢》(Cell Metabolism)杂志发表——Isabel Reinisch, Adhideb Ghosh, Falko Noé, Wenfei Sun, Hua Dong, Peter Leary, Arne Dietrich, Anne Hoffmann, Matthias Blüher, Christian Wolfrum. Unveiling adipose populations linked to metabolic health in obesity. Cell Metabolism, 2024 Dec 11: S1550-4131(24)00452-2. DOI: 10.1016/j.cmet.2024.11.006. https://pubmed.ncbi.nlm.nih.gov/39694039/
参与此项研究的除了来自德国莱比锡大学(Medical Department III-Endocrinology, Nephrology, Rheumatology, University of Leipzig Medical Center, Leipzig, Germany)的研究人员之外,还有来自瑞士苏黎世联邦理工学院(Institute of Food, Nutrition and Health, ETH Zurich, Schwerzenbach, Switzerland)、 瑞士苏黎世联邦理工学院和苏黎世大学合办的苏黎世功能基因组学中心(Functional Genomics Center Zurich, ETH Zurich and University of Zurich, Zurich, Switzerland)、美国斯坦福大学(Department of Bioengineering, Stanford University, Stanford, CA, USA; Stem Cell Bio Regenerative Med Institute, Stanford University, Stanford, CA, USA)、德国莱比锡大学医院(Department of Visceral, Transplant, Thoracic and Vascular Surgery, University Hospital of Leipzig, Leipzig, Germany)以及德国莱比锡大学和莱比锡大学医院的亥姆霍兹慕尼黑中心的亥姆霍兹代谢、肥胖和血管研究所{Helmholtz Institute for Metabolic, Obesity and Vascular Research (HI-MAG) of the Helmholtz Zentrum München at the University of Leipzig and University Hospital Leipzig, Leipzig, Germany}的研究人员。超重的人患糖尿病、高血压或高胆固醇的风险更大,但并不是所有超重的人都会患上这些代谢疾病——大约1/4的人是健康的。科学家们正试图找出为什么有些超重的人会生病,而有些人却不会。来自瑞士苏黎世(Zurich, Switzerland)、德国莱比锡(Leipzig, Germany)以及美国斯坦福大学的一项综合研究为这一观点提供了重要依据:研究人员编制了一份详细的图谱,其中包含了健康和患病的超重人群、他们的脂肪组织和组织细胞中的基因活性的数据。
研究人员从莱比锡大学医学中心(University of Leipzig Medical Center, Leipzig, Germany)的莱比锡肥胖生物银行(Leipzig Obesity BioBank)和德国亥姆霍兹代谢、肥胖和血管研究所(Helmholtz Institute for Metabolism, Obesity and Vascular Research简称HI-MAG)收集了大量来自严重超重人群的活组织检查数据。德国莱比锡大学的科学家收集了这些活组织切片。
它们来自接受过外科手术的超重患者,并同意为研究目的采集脂肪组织样本。该研究的联合负责人、莱比锡大学临床肥胖研究教授马蒂亚斯·布吕赫(Matthias Blüher)解释说:“这些数据还包含了大量关于测试对象健康的医学信息。”这些组织样本来自患有或不患有代谢疾病的严重超重人群,从而可以对健康和病态肥胖人群进行比较。在70名志愿者的样本中,研究人员逐个细胞检查哪些基因是活跃的,以及如何活跃。他们分析了两种类型的脂肪组织:皮下组织和内脏组织。科学和医学认为,位于腹腔深处并包围内脏器官的内脏脂肪是代谢性疾病的主要原因。另一方面,专家通常认为,直接躺在皮肤下面的脂肪问题较少。腹腔脂肪组织有明显变化(Significant changes in fatty tissue in the abdominal cavity)
正如研究人员能够证明的那样,患有代谢性疾病的人内脏脂肪组织中的细胞在功能上发生了严重改变。几乎这种组织中的每一种细胞类型都受到这种重组的影响。例如,基因分析表明,病人的脂肪细胞也不再能够燃烧脂肪。相反,它们产生了更多触发免疫反应的免疫信使物质,从而可能促进代谢性疾病。
Fig. 2 Matthias Blüher Photo: Christian Hüller / Leipzig University
研究人员还发现,在间皮细胞(mesothelial cells)的数量和功能上存在非常明显的差异:健康的超重人群内脏脂肪中间皮细胞的比例要高得多,而且这些细胞在内脏脂肪中的功能更灵活:在健康人群中,它们可以切换到一种干细胞模式,从而转化为另一种细胞类型,例如转化为脂肪细胞。最后,科学家们还发现了男女之间的差异:某种类型的祖细胞只存在于女性的内脏脂肪中。
寻找新的生物标志物(Finding new biomarkers)
超重人群基因活性的新图谱描述了脂肪组织中细胞类型的组成及其功能。“然而,我们不能说这些差异是否是一个人代谢健康的原因,或者相反,是否是代谢性疾病导致了这些差异,”马蒂亚斯·布吕赫说。相反,科学家们将他们的工作视为进一步研究的基础。他们将所有数据发布在一个免费访问的网络应用程序中,以便其他研究人员可以使用它。
特别是,现在可以发现新的标记物,可以对患代谢性疾病的发展风险作出表述。这些也有助于改善代谢性疾病的治疗。例如,有一类新的药物可以抑制食欲,促进胰腺中的胰岛素分泌。
然而,这些药物供不应求。“从我们的数据中提取的生物标志物可以帮助识别那些最需要这种治疗的患者,”马蒂亚斯·布吕赫说。
除了传统的新闻稿外,莱比锡大学还以短新闻的形式提供有关肥胖与代谢性疾病的信息,现介绍另一篇报道:来自医学界:调查肥胖患者代谢性疾病的原因(From the world of medicine: Causes of metabolic diseases in obesity investigated)。这是关于莱比锡大学医学院的两篇高级研究论文之一。
肌肉更有力量:研究人员发现了男性性激素的新机制(More strength in the muscles: Researchers discover new mechanism for male sex hormone)
德国莱比锡大学医学院和中国山东大学(Shandong University in China)的研究人员发现了一种新的机制,通过这种机制,对肌肉和骨骼功能至关重要的男性性激素可以发挥作用。基于这些发现,可以开发出副作用更小的新药,例如用于增强行动不便患者的肌肉。研究人员的相关研究结果于2025年1月23日已经在《细胞》(Cell)杂志网站发表——Zhao Yang, Yu-Qi Ping, Ming-Wei Wang, Chao Zhang, Shu-Hua Zhou, Yue-Tong Xi, Kong-Kai Zhu, Wei Ding, Qi-Yue Zhang, Zhi-Chen Song, Ru-Jia Zhao, Zi-Lu He, Meng-Xin Wang, Lei Qi, Christian Ullmann, Albert Ricken, Torsten Schöneberg, Zhen-Ji Gan, Xiao Yu, Peng Xiao, Fan Yi, Ines Liebscher, Jin-Peng Sun. Identification, structure, and agonist design of an androgen membrane receptor. Cell, 2025 Jan 23: S0092-8674(25)00035-2. DOI: 10.1016/j.cell.2025.01.006. https://pubmed.ncbi.nlm.nih.gov/39884271/
参与此项研究的有来自中国济南山东大学(Key Laboratory Experimental Teratology of the Ministry of Education, New Cornerstone Science Laboratory, Department of Biochemistry and Molecular Biology, School of Basic Medical Sciences, and Advanced Medical Research Institute, NHC Key Laboratory of Otorhinolaryngology, Qilu hospital, Cheeloo College of Medicine, Shandong University, Jinan, China; Department of Clinical Laboratory, The Second Hospital, Cheeloo College of Medicine, Shandong University, Jinan, China; Department of Physiology, School of Basic Medical Sciences, Cheeloo College of Medicine, Shandong University, Jinan, China; Biomedical Research Center for Structural Analysis, Shandong University, Jinan, Shandong, China; Key Laboratory of Infection and Immunity of Shandong Province, Department of Pharmacology, School of Basic Medical Sciences, Shandong University, Jinan, China)、山东第一医科大学和山东医学科学院的医学科技创新中心(Medical Science and Technology Innovation Center, Shandong First Medical University & Shandong Academy of Medical Sciences, Jinan, China)、中国科学院物理研究所(Laboratory of Soft Matter Physics, Institute of Physics, Chinese Academy of Sciences, Beijing, China)、德国莱比锡大学(Rudolf Schönheimer Institute of Biochemistry, Medical Faculty, Leipzig University, Leipzig, Germany; Institute of Anatomy, Medical Faculty, Leipzig University, Leipzig, Germany)、中国南京大学(Medical School of Nanjing University, Nanjing University, Nanjing, China)以及中国北京大学(Department of Physiology and Pathophysiology, School of Basic Medical Sciences, State Key Laboratory of Vascular Homeostasis and Remodeling, Beijing Key Laboratory of Cardiovascular Receptors Research, Peking University, Beijing, China)的研究人员。
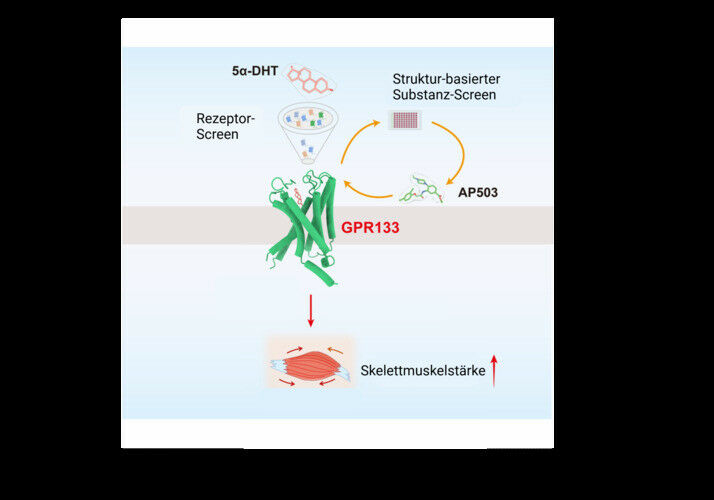
在这项国际研究中,科学家们能够证明粘附G蛋白偶联受体(adhesion G protein-coupled receptors)之一GPR133被雄激素类固醇激素——5α-二氢睾酮(androgenic steroid hormone 5α-DHT)激活。“除此之外,这种激活可以增加骨骼肌的收缩力,我们的研究还使用了一种新开发的,这种受体的有效激活剂来专门触发这种效果,”莱比锡大学信号转导教授,该研究的联合负责人伊内斯·利布舍尔(Ines Liebscher)说。
脂肪组织之间的差异,甚至在男性和女性之间(Differences between fatty tissues, even in men and women)
超重的人患糖尿病、高血压或高胆固醇的风险更大,但并不是所有超重的人都会患上这些代谢疾病——大约1/4的人是健康的。科学家们正试图找出为什么有些超重的人会生病,而有些人却不会。来自瑞士苏黎世和德国莱比锡的一项综合研究为这一观点提供了重要依据:研究人员编制了一份详细的图谱,其中包含了健康和患病的超重人群、他们的脂肪组织和组织细胞中的基因活性的数据。
研究人员从莱比锡大学医学院的莱比锡肥胖生物银行(Leipzig Obesity BioBank of Leipzig University Medicine)和亥姆霍兹代谢、肥胖和血管研究所(Helmholtz Institute for Metabolism, Obesity and Vascular Research简称HI-MAG)收集了大量来自严重超重人群的活组织检查数据。莱比锡大学的科学家收集了这些活组织切片。它们来自接受过外科手术的超重患者,并同意为研究目的采集脂肪组织样本。该研究的联合负责人、莱比锡大学临床肥胖研究教授马蒂亚斯·布吕赫(Matthias Blüher)解释说:“这些数据还包含了大量关于测试对象健康的医学信息。”
上述介绍仅供参考,欲了解更多信息敬请注意浏览原文和相关报道。
Abstract (Cell Metab, 2024 Dec 11, DOI: 10.1016/j.cmet.2024.11.006)
Precision medicine is still not considered as a standard of care in obesity treatment, despite a large heterogeneity in the metabolic phenotype of individuals with obesity. One of the strongest factors influencing the variability in metabolic disease risk is adipose tissue (AT) dysfunction; however, there is little understanding of the link between distinct cell populations, cell-type-specific transcriptional programs, and disease severity. Here, we generated a comprehensive cellular map of subcutaneous and visceral AT of individuals with metabolically healthy and unhealthy obesity. By combining single-nucleus RNA-sequencing data with bulk transcriptomics and clinical parameters, we identified that mesothelial cells, adipocytes, and adipocyte-progenitor cells exhibit the strongest correlation with metabolic disease. Furthermore, we uncovered cell-specific transcriptional programs, such as the transitioning of mesothelial cells to a mesenchymal phenotype, that are involved in uncoupling obesity from metabolic disease. Together, these findings provide valuable insights by revealing biological drivers of clinical endpoints.
Abstract(Cell, 2025 Jan 23. DOI: 10.1016/j.cell.2025.01.006)
Androgens, such as 5α-dihydrotestosterone (5α-DHT), regulate numerous functions by binding to nuclear androgen receptors (ARs) and potential unknown membrane receptors. Here, we report that the androgen 5α-DHT activates membrane receptor GPR133 in muscle cells, thereby increasing intracellular cyclic AMP (cAMP) levels and enhancing muscle strength. Further cryoelectron microscopy (cryo-EM) structural analysis of GPR133-Gs in complex with 5α-DHT or its derivative methenolone (MET) reveals the structural basis for androgen recognition. Notably, the presence of the "Φ(F/L)2.64-F3.40-W6.53" and the "F7.42××N/D7.46" motifs, which recognize the hydrophobic steroid core and polar groups, respectively, are common in adhesion GPCRs (aGPCRs), suggesting that many aGPCRs may recognize different steroid hormones. Finally, we exploited in silico screening methods to identify a small molecule, AP503, which activates GPR133 and separates the beneficial muscle-strengthening effects from side effects mediated by AR. Thus, GPR133 represents an androgen membrane receptor that contributes to normal androgen physiology and has important therapeutic potentials.
转载本文请联系原作者获取授权,同时请注明本文来自诸平科学网博客。
链接地址:https://wap.sciencenet.cn/blog-212210-1472721.html?mobile=1
收藏