博文
[转载]355.流浪犬对狂犬病疫苗的免疫反应评估
|||
流浪犬对狂犬病疫苗的免疫反应评估
摘要
狂犬病是一种致命的脑脊髓炎,主要通过患狂犬病的犬咬伤传播给人类和其他动物。因此,疫苗接种计划正在制定,以控制狂犬病的犬。尽管流浪犬已经在为控制疾病而启动的各种计划下接种了多年疫苗,但这些计划的有效性只能通过评估这些犬的免疫力来确定。有鉴于此,印度班加卢鲁市市政公司进行了一项研究,以评估正在进行的大规模犬类疫苗接种(MDV)计划的有效性。通过快速荧光灶抑制试验(RFFIT)和内部定量间接酶联免疫吸附试验(iELISA)检测体液反应,并通过干扰素-γ(IFN–γ)ELISA检测细胞反应,对来自8个区26个点的接种流浪犬的全血和血清样本(n = 260)进行了检测。如通过0.5 IU/mL血清的截止值所确定的,来自接种过的犬的71%和87%的样品显示了足够水平的抗体,推测分别通过RFFIT和iELISA提供保护。该方法的敏感性和特异性分别为100%和63.3%。IFN–γELISA显示50%的样本有足够的细胞反应。发现定量iELISA在MDV项目的大规模血清监测中是有用的,以帮助消除犬介导的狂犬病。
关键词:
1.介绍
狂犬病是一种急性病毒性脑脊髓炎,由狂犬病病毒属于家庭的弹状病毒科。这是一种中枢神经系统(CNS)疾病,通常在被感染的动物咬伤人或其他动物时传播。当被感染动物的唾液与被咬动物或人的眼睛、嘴巴或鼻子接触时,病毒通过唾液传播。进行性脑炎在感染后数天或数月开始,并以受感染个体或动物的死亡而结束,通常在症状发作后30天内。[2].病死率(CFR)接近100%,是已知传染病中最高的。狂犬病没有特效疗法;但是,通过适当的疫苗接种是可以预防的。
犬是亚洲狂犬病最重要的宿主。世界卫生组织(WHO)估计,每年有59,000人死于由犬传播的狂犬病,其中大多数发生在亚洲(59.6%)和非洲(36.4%) 。狂犬病在印度的发病率特别高,每年有多达20,000人死亡。人类感染的主要来源(超过96%的病例)是未接种疫苗的自由放养的流浪犬群。考虑到这种疾病的严重性及其流行性,特别是在非洲和亚洲大陆,包括联合国粮食及农业组织(FAO)、世界动物卫生组织(WOAH)、世卫组织以及全球狂犬病控制联盟在内的三方联盟发起了“2030年前消灭狂犬病:到2030年结束由犬传播的狂犬病造成的人类死亡的全球战略计划”。
人类狂犬病的消除取决于犬狂犬病的消除。这可以通过暴露患者的暴露后预防(PEP)、高危人群的暴露前预防(PrEP)、控制动物宿主的感染以及管理流浪犬群来实现.大规模犬类疫苗接种(MDV)运动预计将有助于提高散养犬类的群体免疫水平,并防止人类暴露于狂犬病病毒。
鉴于该疾病在印度的严重性和控制该疾病的需要,印度政府(GOI)国家疾病控制中心(NCDC)于2021年9月28日启动了消除狂犬病国家行动计划。该行动计划侧重于预防和控制狂犬病的战略,以实现到2030年消除犬传播的狂犬病。在NAPRE启动之前,几个印度城市已经开始实施动物节育和抗狂犬病疫苗接种(ABC-ARV)计划,目的是通过采用人道的方法减少犬的数量,从而减少狂犬病病例的数量。然而,由于各种原因,缺乏持续的努力。另一方面,为适应地区条件,允许印度各邦制定自己的行动计划,即《消除狂犬病邦行动计划》。策略包括犬的数量调查和管理以及MDV。此外,抗狂犬病疫苗接种计划的有效性也需要通过监测疫苗接种后引发的抗体来评估。
印度的大都市,包括孟加拉鲁鲁,有大量的流浪犬。为了控制这些流浪犬的数量,几个非政府组织(NGO)遵循了“捕捉-绝育-接种-释放”( CNVR ),作为ABC-ARV在Bengaluru的项目的一部分,以减少街头犬的威胁和减少犬咬伤的病例。2019年9月,本加卢鲁市市政公司[bru hat Bengal uru Mahanagara Palike(BBMP)]在本加卢鲁兽医学院、世界兽医服务(WVS)印度公司、狂犬病任务和非政府组织的支持下,通过使用WVS开发的收集散养犬数据的网络应用程序,对其管辖范围内的流浪犬种群进行了系统调查。因此,在本加卢鲁市估计有310,000只自由漫步的犬。根据这项调查,2020年9月,BBMP在Rajarajeshwari Nagar(BBMP 8个区之一)启动了大规模犬类疫苗接种(MDV ),作为试点研究。此后,从2021年起,除了在传教会狂犬病小组的支持下控制流浪犬狂犬病的ABC-ARV计划之外,MDV计划扩展到所有地区。
为了在群体中获得群体免疫的流行病学基线,70%的犬应该成功接种狂犬病疫苗。为了了解由BBMP发起的MDV计划的有效性,我们对来自BBMP所有八个区的流浪犬的血液样本进行了筛查,并使用快速荧光灶抑制试验(RFFIT)研究了免疫反应在狂犬病准备中的作用,并将其与内部间接酶联免疫吸附试验(iELISA)进行了比较。干扰素-γ(IFN-γ)试验也用于评估接种犬的细胞介导免疫(CMI)反应。本研究的目的是评估在BBMP特定地区通过接种疫苗获得足够免疫应答(≥0.5 IU/mL)以预防狂犬病的犬的百分比,以检查MDV的效力。
2.材料和方法
2.1.学习区
流浪犬群的血液样品从孟加拉鲁鲁市市政公司(BBMP)的所有8个区域收集。
2.2.样品
2.2.1.机构动物伦理委员会的批准
取样工作是在获得本加卢鲁赫巴尔克瓦夫苏兽医学院机构动物伦理委员会(IAEC)的批准(编号:VCH/IAEC/2021/27)后开始的。
2.2.2.抽样
总样本量的选择基于Cochran公式,假设所有接种过疫苗的动物中有25%受到保护。由于人力、IFN-γ检测试剂盒的预算和后勤限制,仅使用了25%,但是应用了95%的置信区间。因此,估计样本量为288。
2.2.3.样品
血样分成两份,一份用于血清分离,另一份(3-4mL)含EDTA。血清样本储存在20℃下,以供进一步分析。
根据统计数据,从本加鲁鲁市政公司八个区的三个接种点收集了288份样本。在我们的抽样调查中,MDV仅在两个点中没有实施,尽管ABC-ARV自2007年以来一直在这些点中实施。因此,除了288个样本之外,还从这两个点收集了20个样本(每个点10个样本)来评估它们的免疫状态。然而,240个样本可用于分析,因为48个样本不足/不适合(表1)。总共分析了来自八个BBMP区的26个点的260份样本(其中24个点实施了MDV,2个点未实施MDV,但ABC-ARV正在实施)。
2.3.细胞和病毒
将狂犬病病毒的BHK-21细胞和攻击病毒标准(CVS-11)株用于RFFIT。可从KVAFSU-CVA狂犬病诊断实验室获得的BHK-21细胞在含有10%胎牛血清(FBS)和抗生素的Dulbecco改良Eagle培养基(DMEM)中繁殖。用于RFFIT的滴定的CVS-11狂犬病病毒株(RABV)从孟加拉鲁鲁的国家精神健康和神经科学研究所(NIMHANS)获得。
2.4.快速荧光灶抑制试验
对于RFFIT,以前标准化的协议被使用。将血清加热至56℃30分钟以灭活补体,并在平底96孔微量滴定板中连续稀释(Nunc MaxiSorp平底,Thermo Fisher Scientific,Waltham,MA,USA)。随后,将100 TCID50狂犬病病毒加入除细胞对照之外的所有孔中,并在37℃孵育90分钟。然后,将25,000–30,000个BHK-21细胞/孔接种到所有孔中,并在5% CO2中于37℃孵育48小时孵化器。在不干扰单层的情况下,将培养基从平板中倒出,用70%冷冻丙酮在20℃下固定细胞30分钟。将固定的细胞与1:5稀释的荧光素标记的抗RABV核蛋白抗体(Fujirebio Diagnostics,Devault,Malvern,PA,USA)在37℃下孵育1小时。使用荧光显微镜检查平板。抗狂犬病病毒中和抗体(VNA)的效价通过与世卫组织参考血清进行比较进行评估。显示RABV完全中和的血清的最高稀释度被认为是VNA滴度。0.5 IU/mL血清的VNA滴度被认为反映了足够的免疫反应。滴度是根据下面的公式估算的。
滴度(IU/mL) = (显示完全中和的试验血清的最高稀释度 × 参考血清滴度)/参考血清显示完全中和的最高稀释度
2.5.间接酶联免疫吸附试验
内部iELISA是使用杆状病毒表达的RABV糖蛋白开发的。以500 ng/100 μL/孔的浓度包被抗原,并在4℃下孵育过夜。丢弃孔中的内容物,用pH 7.2的磷酸盐缓冲盐水(PBS)洗涤平板两次。使用PBS中的3%牛血清白蛋白和0.05%吐温20 (PBST)在37℃下进行封闭2小时。用PBS洗涤三次后,加入在PBST的1% BSA中稀释的血清,并将板在37℃下孵育60分钟。对照包括系列稀释的阳性和阴性血清、结合物对照和空白孔。孵育后,用PBST洗涤平板两次,然后加入100 μL/孔的1∶20,000稀释的兔抗鸡IgG HRP结合物(适马-奥尔德里奇公司,圣路易斯,密苏里州,美国)。在37℃孵育60分钟并洗涤三次后,色原底物(OPD-H2O2),最后加入2.5 N HCl终止反应。在ELISA读数器中在492 nm处测量光密度(OD)。
将每个样品获得的OD值转换为阳性百分比(PP)值。使用以下公式计算每个样本读数的PP:
PP= (测试血清的OD × 100)/阳性对照的OD
在内部iELISA中,根据该实验室之前开展的工作,选择了57.1%的临界值(PP值)。简而言之,将所有对照PP值的平均值相对于相应的中和抗体滴度作图,并制成给出双曲线的图。根据该图,0.5 IU/mL的RFFIT对应于iELISA的57.1 PP值,因此将该值作为临界值,以确定iELISA中足够的免疫反应。
根据Thrusfield的统计公式,通过与RFFIT进行比较,确定内部iELISA的敏感性和特异性。
2.6.干扰素-γ酶联免疫吸附试验
将血样(1 mL)加入24孔组织培养板中,并使用5 μL灭活狂犬病抗原(可从KVAFSU-CVA狂犬病诊断实验室获得的Nobivac-R)进行刺激。将平板在37℃含5% CO2的增湿室中孵育收集上清液并储存在20℃下用于进一步分析。
使用犬IFN-γ ELISA进行夹心ELISA基本的套件(美国Mabtech公司)。将在PBS (pH 7.4)中稀释至2 μg/mL的捕获抗体(mAb MT13)添加(100 μL/孔)到96孔平底Nunc Maxisorp平板中,并在4–8℃下孵育过夜。将平板清空,并添加200 μL/孔封闭缓冲液(0.1% BSA,PBST)。将平板在室温(RT)下孵育1小时,然后用PBST洗涤5次。以100 μL/孔添加在封闭缓冲液中稀释的样品和标准品。包括分析背景对照,即没有标准的孔,并且板在室温下孵育2小时。在用洗涤缓冲液洗涤5次后,以100 μL/孔加入在封闭缓冲液中稀释至0.5 μg/mL的检测抗体(mAb mt 166-生物素),并且在室温下进一步孵育1小时。板洗涤5次,并且以100μL/孔加入在封闭缓冲液中以1:1000稀释的链霉亲和素-HRP。将平板在室温下孵育1小时,洗涤,并以100μL/孔加入TMB底物(产品代码:3652-F10)。用0.2 M H2SO4终止反应,并且在ELISA读数器中在450 nm处测量光密度。
2.7.统计分析
通过与RFFIT进行比较,使用Spearman等级相关分析来评估iELISA的性能。使用Cohen的kappa统计来评估iELISA相对于RFFIT的强度。所有的统计分析都是在R studio(版本1.4.1103)的帮助下使用带有软件包ggplot2的R base pack 4.0.4进行的。
3.结果
通过评估狂犬病疫苗接种的免疫反应,对正在进行的MDV项目在孟加拉国流浪犬群中的有效性进行了评估。通过使用RFFIT和内部iELISA评估抗体滴度来研究体液免疫应答。使用市售的IFN-研究细胞介导的免疫反应γ检测试剂盒。
如RFFIT所证实的,171/240 (71%)只犬表现出足够的免疫反应(≥0.5 IU/mL),而来自未实施MDV的点的仅13/20 (65%)只犬表现出足够的免疫反应(表2)。除了南班加卢鲁、达萨拉哈里和RR Nagar以外,BBMP不同地区的响应充分性至少为70%。此外,充分答复率最高的是西本加卢鲁区的86.4%(66.7-95.3),最低的是RR Nagar区的53.7%(38.7-67.9)图2。
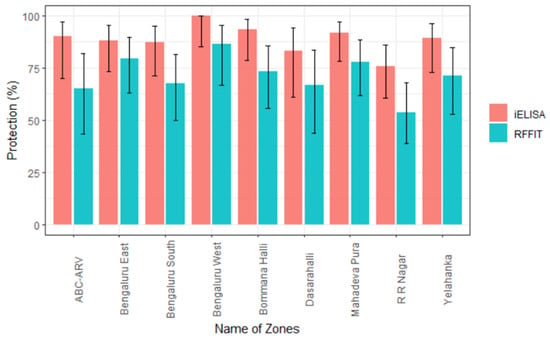
图2. RFFIT和iELISA观察到的充分免疫反应的分区比例(误差棒代表95% CI的范围)。显示足够免疫反应的犬的百分比表示为保护(%) onY-轴。BBMP地区的不同区域在X-轴。ABC-ARV开机X-安讯士指的是只有ABC-ARV正在实施,但MDV尚未实施的点。
在内部iELISA中,57.1%的临界值(PP值)是根据该实验室之前开展的工作选择的。因此,87% (209/240)的样本(表2)在接种疫苗的点中显示了足够的免疫应答(≥57.09 PP),在未实施MDV的两个点中90% (18/20)的样本也显示了足够的抗体滴度。表现出足够滴度的犬的比例在Bengaluru West最高,为100%(85.1–100),在Rajarajeshwari Nagar区最低,为75.6%(60.7–86.2)图2)。
表2.在接种过疫苗的狗中观察到的血清转化。
对于240个样本 | RFFIT | iELISA | ||
足够的免疫反应 | 免疫反应不足 | 足够的免疫反应 | 免疫反应不足 | |
样本数目 | 171 | 69 | 209 | 31 |
百分率 | 71% | 29% | 87% | 13% |
通过比较iELISA和RFFIT的结果,进一步评估了内部iELISA的性能。内部iELISA的敏感性和特异性分别为100%和63.3%(表3)。斯皮尔曼等级相关(ρ值= 0.463和p值< 0.05)表明测试之间存在一定的相关性,并且0.55的kappa值表明RFFIT和iELISA之间的适度一致(图3)。
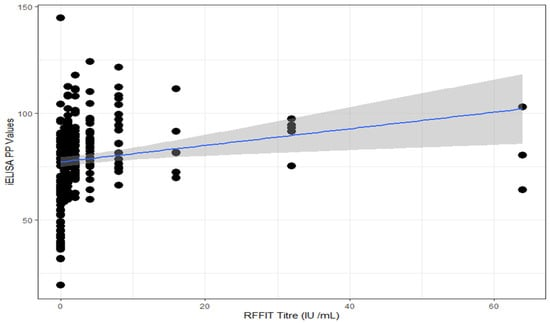
图3.描述RFFIT和iELISA之间相关性的散点图。阴影区域代表95%水平的置信区间。蓝线是相关性分析的回归线。
表3.iELISA敏感性和特异性的双边列联表。
试验 | RFFIT | 总数 | 灵敏度 | 特征 | Kappa值 | ||
阳性 | 阴性 | ||||||
G-protein iELISA | 积极的 | 189 | 38 | 227 | 100% | 63.3% | 0.55 |
否定的;消极的;负面的;负的 | 0 | 33 | 33 | ||||
总数 | 189 | 71 | 260 | ||||
IFN-γ ELISA用于评估细胞介导的免疫反应。犬的IFN-γ的正常范围是3 1 pg/mL16].在本研究中,IFN-γ浓度高于正常范围的样本被认为具有足够的CMI反应。在来自接种过疫苗的点的240只犬中,50% (120/240)来自BBMP的所有八个区(表4)显示了足够的CMI响应。有趣的是,在只有ABC-ARV正在进行,但没有实施MDV的点中,90% (18/20)的样本显示出足够的CMI反应。最高的86.4%(66.7–95.3)CMI反应在来自Bengaluru西区的样本中观察到(图4),来自Yelahanka区的样本显示14.3%(5.7-31.5)的CMI反应最少。
表4.在接种疫苗的狗中观察到细胞介导的免疫反应。
对于240个样本 | 充足的CMIR | CMIR不足 |
样本数目 | 120 | 120 |
百分率 | 50% | 50% |
此外,在来自接种过疫苗的点的样品中,38% (26/69)的RFFIT滴度不足(< 0.5 IU/mL)的犬显示出足够的CMI反应。此外,100% (7/7)来自未实施MDV且RFFIT滴度不足的点的犬显示出足够的CMI反应。
4.讨论
孟加拉鲁鲁市的流浪犬大规模疫苗接种于2021年启动,计划逐步覆盖八个区所有198个区的所有散养犬。为了评估疫苗接种的有效性,收集血清和血液以评估体液和CMI反应。
在RFFIT中,接种过疫苗的点中71%的犬表现出足够的免疫反应。这表明全市范围的MDV计划是有效的。有趣的是,来自没有实施MDV的点的犬的65%的血清样品也显示了足够的免疫反应。这可能归因于作为ABC-ARV项目一部分的既往疫苗接种(早于MDV的开始),因为疫苗接种后的狂犬病保护性免疫被认为可持续至少3年甚至更长时间。自2007年以来,ABC-ARV项目已在这两个点广泛实施。同样,斯里兰卡的一项研究报告称,在一剂疫苗接种后,60%的流浪犬携带RFFIT保护性抗体滴度。在这项研究中,他们给流浪犬和家犬接种疫苗,并在第0、30、180和360天采用RFFIT测试血清样本中抗狂犬病抗体的存在。在流浪犬中,在第0天具有足够抗体滴度的犬的百分比为1.6至6.4。然而,在一剂疫苗接种后,直到第180天,在> 70%的犬中观察到足够的免疫反应,但是到了第360天,显示足够滴度的动物的百分比下降到43–60%。他们得出结论,单剂抗狂犬病疫苗不足以维持一年的抗体滴度。在我们之前的研究中,2018年从孟加拉鲁鲁的北部和南部收集了样本,50%的流浪犬有足够的抗体,其滴度在北部为0.5至32 IU/mL,在南部为0.5-4 IU/mL。然而,这项研究是在MDV项目开始之前进行的。
在目前的研究中,在Bengaluru West,86.4%的流浪犬显示出足够的抗体水平,这可能归因于作为MDV一部分的有效疫苗接种覆盖率,以及在该地区持续开展的中航-ARV项目。这表明增加疫苗覆盖范围有助于犬群中更好的血清转化。
然而,我们观察到不同区域犬的血清转换有所不同。这可能归因于影响犬体液反应的许多因素,例如接种时的年龄、性别、犬的大小和品种、动物的营养状况、疫苗类型、接种次数、从接种到样品收集的时间间隔等。为评估与犬狂犬病免疫相关的因素而进行的研究表明,血清抗体水平与疫苗年龄、犬种群的遗传、疫苗接种次数、制造商、最近一次疫苗接种后的时间间隔和样本收集相关。印度尼西亚的一项研究调查了拥有和自由漫游的犬在接种狂犬病疫苗后的免疫反应,以及与接种疫苗后30天内抗体产生相关的因素。他们观察到,犬的疫苗接种史和良好的身体状况评分与第0天出现狂犬病抗体和第30天出现抗体显著相关。在目前的研究中,MDV项目使用了一种普通疫苗,因此,疫苗的类型和效力不可能是我们观察到的体液反应变化的主要原因,因为在某些地区,犬对疫苗接种有良好的反应。
WOAH建议在狂犬病控制框架下,即在大规模调查中,使用ELISA监测接种疫苗后的免疫状态。在目前的研究中,通过iELISA,来自接种疫苗点的87% (209/240)的犬具有足够的被认为是保护性的抗体,然而,在没有实施MDV的点中,90%的犬具有足够的抗体。这可能要归功于自2007年以来在这两个点持续开展的ABC-ARV计划。有趣的是,当通过iELISA测试时,在来自每个区域的超过70%的样本中观察到足够的免疫反应的存在。2022年的一项类似研究报告称,只有50%的犬具有足够的抗体滴度,孟加拉鲁鲁北区的犬的比例(66%)高于南区(40.5%)。该研究将低比例归因于一系列因素,包括缺乏持续的疫苗接种以及疫苗接种失败。结论是,大部分流浪犬将通过ABC-ARV计划持续的年度疫苗接种获得假定的保护状态,该计划于较早前启动。在印度昌迪加尔的另一项研究显示,只有1%的街头流浪犬具有必需的抗体水平,这是通过酶联免疫吸附试验检测出来的,而MDV并不是在印度昌迪加尔发起的。然而,自2004年以来,昌迪加尔开展了免费大规模免疫接种运动。因此,作者希望评估狂犬病项目的有效性,因此,流浪犬和拥有的犬都被取样并通过ELISA进行评估。令人惊讶的是,仅在1%的街道犬和16%的宠物犬中发现足够的抗狂犬病抗体滴度。在印度古吉拉特邦的一项研究中,通过ELISA测试,该比例为1.9%。
RFFIT等病毒中和试验繁琐复杂,不适合大规模血清流行病学监测研究。为了克服这一限制,已经开发了几种ELISA方案,用于使用单克隆抗体检测狂犬病病毒的抗体。ELISA具有几个优点,例如安全性(不需要处理活病毒)、简单的实验室要求(不需要细胞培养设备或荧光显微镜)、用户友好性、快速性和较少的技术要求。在VNT,劣质血清会导致细胞毒性,从而导致假阳性结果。对于这样的样品,间接ELISA已被证明与VNT一样敏感和特异;它也不需要很高的防护设施,并能快速产生结果。尽管ELISA不能直接与中和试验结果相比,但由于上述优点,抗糖蛋白抗体的检测和滴定可能是与RFFIT同等的选择方法。在狂犬病控制的框架内,VN和ELISAs是用于监测单个动物或接种后群体的免疫状态的推荐试验。为了在国际动物移动或贸易之前测量对疫苗接种的抗体反应,只有VN方法(FAVN试验和RFFIT)是可接受的。在目前的研究中,与RFFIT相比,iELISA的免疫反应成比例增加。对样本的分区评估表明,RFFIT和IELISA在Bengaluru West的响应最高(分别为86.4%和100%),而在毗邻的RR Nagar区的响应最低(分别为53.7%和75.6%)。与RFFIT相比,在iELISA中观察到的更高百分比可能归因于iELISA检测中和抗体以及甚至非中和抗体的能力,而RFFIT仅检测中和抗体。iELISA的敏感性和特异性分别为100%和63.3%。Kappa值为0.55,表明RFFIT和iELISA之间的一致性适中。
干扰素-γ是一种参与CMI反应的重要细胞因子,对巨噬细胞活化、T细胞增殖和分化以及参与抗原加工和呈递的蛋白质上调至关重要。它通过促进病毒感染细胞的溶解和清除以及抑制病毒基因表达和复制来发挥抗病毒作用。狂犬病感染中的CMI反应可能是保护动物免于狂犬病的重要机制,但是还没有很好的调查。当抗狂犬病病毒中和抗体(RVNA)滴度低于0.5 IU/mL时,研究犬的细胞反应的作用是重要的。在一项针对人类的研究中,观察到产生狂犬病毒特异性T细胞的IFN-γ数量与RVNA滴度呈正相关,并推断IFN-γ在预防狂犬病中具有重要作用。在本研究中,在实施和未实施MDV的点中,分别有50%和90%的犬样品中的IFN-γ水平高于正常范围,这表明在大部分犬中引发了必要的CMI反应。此外,在RFFIT滴度不足(< 0.5 IU/mL)的接种点中,38%的犬表现出足够水平的IFN-γ (≥3 1 pg/mL),令人惊讶的是,来自未实施MDV且RFFIT滴度不足(< 0.5 IU/mL)的点的犬100%表现出足够水平的IFN-γ。这可能归因于之前作为ABC-ARV项目的一部分进行的疫苗接种和T细胞记忆。
5.结论
犬只大规模接种狂犬病疫苗是阻断狂犬病自然传播的最合理策略。本研究旨在评估BBMP班加罗尔市市政公司正在实施的MDV项目的有效性。结果显示,在51%的犬群接种疫苗后,来自BBMP 8个区的260只犬中的71%对狂犬病有足够的免疫反应。因此,考虑到世卫组织的建议,可以认为进展良好,在该国,达到至少70%的覆盖率是预防或消除狂犬病的先决条件。这是一项初步研究,从BBMP每个区的选定点中抽取有限数量的样本进行研究。所有地区都需要对以前接种过疫苗的流浪犬群进行额外的大规模调查。我们的研究表明,在维持MDV项目的同时,应用更简单的检测,如内部iELISA,将为更好地实施狂犬病控制和消除项目铺平道路。需要在印度的其他城市开展类似的活动,以实现到2030年消除犬传播的狂犬病的目标。还需要进一步的研究来评估狂犬病疫苗所赋予的免疫持续时间;特别是细胞免疫的作用需要进一步探讨。
Prakash Rao VC, Ramakrishnaiah S, Isloor S, Doddamane R, Lakshman D, Maralavadi MSSR, Bhat A, Chandrashekar B, Natesan K, Kondabattula G, Hegde NR. Assessment of Immune Responses to Rabies Vaccination in Free-Ranging Dogs in Bengaluru, India. Vaccines (Basel). 2023 Apr 24;11(5):888. doi: 10.3390/vaccines11050888. PMID: 37242992; PMCID: PMC10224170.
https://wap.sciencenet.cn/blog-55647-1393744.html
上一篇:[转载]354.编码保守的非刺突抗原的T细胞定向疫苗BNT162b4保护动物免受严重的新型冠状病毒感染
下一篇:[转载]356.在斯里兰卡上市的兽用狂犬病疫苗的效力