博文
论平衡态热力学中热力学第一定律设计的三个缺陷
|
本文拟指出平衡态热力学中热力学第一定律设计的三个缺陷,供同行参考.
热力学第一定律
平衡态热力学认为热力学能变由热量、体积功及有效功(或称非体积功)三部分组成;相应的热力学第一
定律的微分表示式参见如下式(1):
dU=δQ+δWT+δW' (1)
式(1)中”Q“表示热量;“WT”表示体积功;“W' ”代表有效功.
2. 热量
平衡态热力学认为热量是由于温差所导致的系统与环境之间传递的一种能量形式,可记为:
δQ=cp·m·dT (2)
式(2)中“cp”为比定压热容,也称比热.
事实上,热力学过程中热量与温差并不存在必然关联. 例如①晶体发生相变;②恒温恒压(或恒容)条件下
发生的化学反应(或相变)均存在明显的热效应,但热力学过程恒温.
需指出温度差仅是热量的一种客观表现形式,并未揭示出热量现象的“熵”本质.
3. 体积功
平衡态热力学通常规定:热力学过程发生时,体积功是环境提供给系统的唯一形式功,可记为:
δWT=-pe·dV (3)
式(3)中“pe”代表外压.
事实上,封闭系统体积膨胀时,系统压强p大于外压pe;参见如下图1.
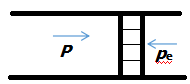
图1. 封闭系统体积膨胀示意图
图1左边为一封闭系统,气体压强为p;右边为环境,外压为pe.
依题,p>pe
封闭系统体积膨胀过程,▕ -p·dV ▕ >▕ -pe·dV ▕ ;即该过程系统实际付出的功要多于体积功,体积功
WT不应单独出现在式(1).
4. 有效功
平衡态热力学的有效功特指电功与表面功;通常情况下,平衡态热力学规定热力学过程的有效功均为0,
即:δW'=0.
此时式(1)可化简为:dU=δQ+δWT (4)
事实上,热力学有效功的存在形式往往不确定,并不专指电功与表面功;硬性规定有效功为0不合理.
例如:对于某原电池反应aA+bB=cC+dD,无论是否通过原电池实现,该反应的ΔrGm值总是客观存在.
为什么在原电池中ΔrGm称有效功,而在一般反应中相同数值的ΔrGm没有意义?
5. 结论
⑴温度差仅是热量的一种客观表现形式,并未揭示出热量现象的“熵”本质;
⑵热力学过程▕ -p·dV ▕ >▕ -pe·dV ▕ ,体积功WT不应单独出现在热力学第一定律表达式中;
⑶有效功的存在形式不确定,硬性规定热力学过程的有效功为0不合理.
https://wap.sciencenet.cn/blog-3474471-1404510.html
上一篇:热力学有效功与最大功
下一篇:热力学研究的方法论