博文
改造线粒体强化免疫治疗
|
改造线粒体强化免疫治疗
Mitochondrial metabolism and signaling direct dendritic cell function in antitumor immunity
编者概要
1型经典树突状细胞(cDC1s)可促进CD8⁺T细胞介导的抗肿瘤免疫应答。但在肿瘤微环境中,cDC1s会出现功能失常,且癌症中调控cDC1发挥正常功能与发生功能障碍的相关机制尚不明确。余等人研究证实,线粒体代谢状态与信号通路可调控cDC1的抗肿瘤免疫功能(详见莫利纳与哈尔达尔的观点评述)。线粒体蛋白OPA1缺失会抑制核呼吸因子1(NRF1)活性、破坏电子传递链完整性,进而造成cDC1线粒体生物能代谢与氧化还原平衡紊乱,削弱机体抑瘤能力。肿瘤进展过程中,OPA1-NRF1信号通路活性会持续下调;给荷瘤小鼠输注线粒体功能优良的cDC1,可增强抗肿瘤应答,与免疫疗法联用时效果尤为显著。综上,对cDC1进行代谢工程改造,有望成为癌症免疫治疗的全新作用机制。——普丽西拉·N·凯利
结构化摘要
引言
1型经典树突状细胞(cDC1s)是癌症免疫及免疫治疗中,细胞毒性CD8⁺T细胞产生应答的关键细胞。既往研究表明,体外实验中线粒体氧化磷酸化(OXPHOS)并非树突状细胞成熟的必需条件,且是人单核源性树突状细胞免疫耐受的典型特征;但线粒体代谢如何调控cDC1与CD8⁺T细胞的互作、进而影响抗肿瘤免疫,目前仍缺乏清晰认知。本研究发现,肿瘤内cDC1存在差异化线粒体状态;线粒体融合蛋白OPA1可通过调控线粒体能量代谢与氧化还原代谢,决定cDC1的抗肿瘤免疫效能。
研究依据
免疫治疗虽已广泛应用于癌症治疗,但仍有大量患者出现治疗耐药或病情复发。cDC1可通过调控CD8⁺T细胞的活化与功能,决定免疫检查点阻断疗法(ICB)的抗肿瘤效果与临床获益。然而,肿瘤微环境内的cDC1常面临代谢应激,细胞功能活性大幅下降。本研究旨在筛选可增强cDC1依赖性抗肿瘤应答的核心代谢调控因子,为通过代谢改造激活cDC1、提升抗癌疗效(尤其联合免疫检查点阻断疗法)提供潜在靶点。
研究结果
本研究在小鼠与人类肿瘤样本中均证实:肿瘤内cDC1存在两种差异化线粒体状态。一类为[TMRM/MG]高表达细胞,线粒体膜电位极化(以四甲基罗丹明甲酯高氯酸盐TMRM检测线粒体膜电位、线粒体绿探针MG检测线粒体质量,二者比值判定);另一类为[TMRM/MG]低表达细胞,线粒体发生去极化。线粒体极化的肿瘤内cDC1,激活CD8⁺T细胞应答的能力远强于线粒体去极化的cDC1。
通过无偏向筛选及实验验证,研究明确OPA1可调控肿瘤内cDC1的线粒体状态与形态。特异性敲除cDC1的OPA1后,肿瘤生长加快,CD8⁺T细胞抗肿瘤应答受损,本质是cDC1抗原呈递功能缺陷所致。
机制层面:OPA1可维持核呼吸因子1(NRF1)的活性与表达,保障cDC1线粒体氧化磷酸化正常运转;OPA1-NRF1通路介导的氧化磷酸化,能抑制自噬及溶酶体对主要组织相容性复合体I类分子(MHC-I)、抗原的降解。同时,OPA1维持电子传递链(ETC)正常运转,促进还原型辅酶NADH转化为氧化型辅酶NAD⁺,增强cDC1的免疫原性;而线粒体分裂蛋白DRP1可拮抗上述OPA1的保护作用。
肿瘤进展期间,肿瘤内cDC1持续出现线粒体功能衰退:[TMRM/MG]高表达细胞亚群减少、线粒体体积缩小,OPA1-NRF1信号通路活性逐步降低。向荷瘤小鼠瘤内输注负载肿瘤抗原、线粒体极化的cDC1,抑瘤效果显著优于输注线粒体去极化的cDC1;该方案与免疫检查点阻断疗法联用增效明显,大量联合治疗小鼠可实现肿瘤完全消退,且再次接种肿瘤时能产生持久的免疫记忆应答。
研究结论
本研究明确了cDC1的差异化线粒体状态,以及支撑其抗肿瘤免疫功能、保障免疫检查点阻断疗法长效应答的线粒体代谢信号调控网络。该成果为靶向激活cDC1、优化癌症免疫治疗提供了全新方向。
配图说明
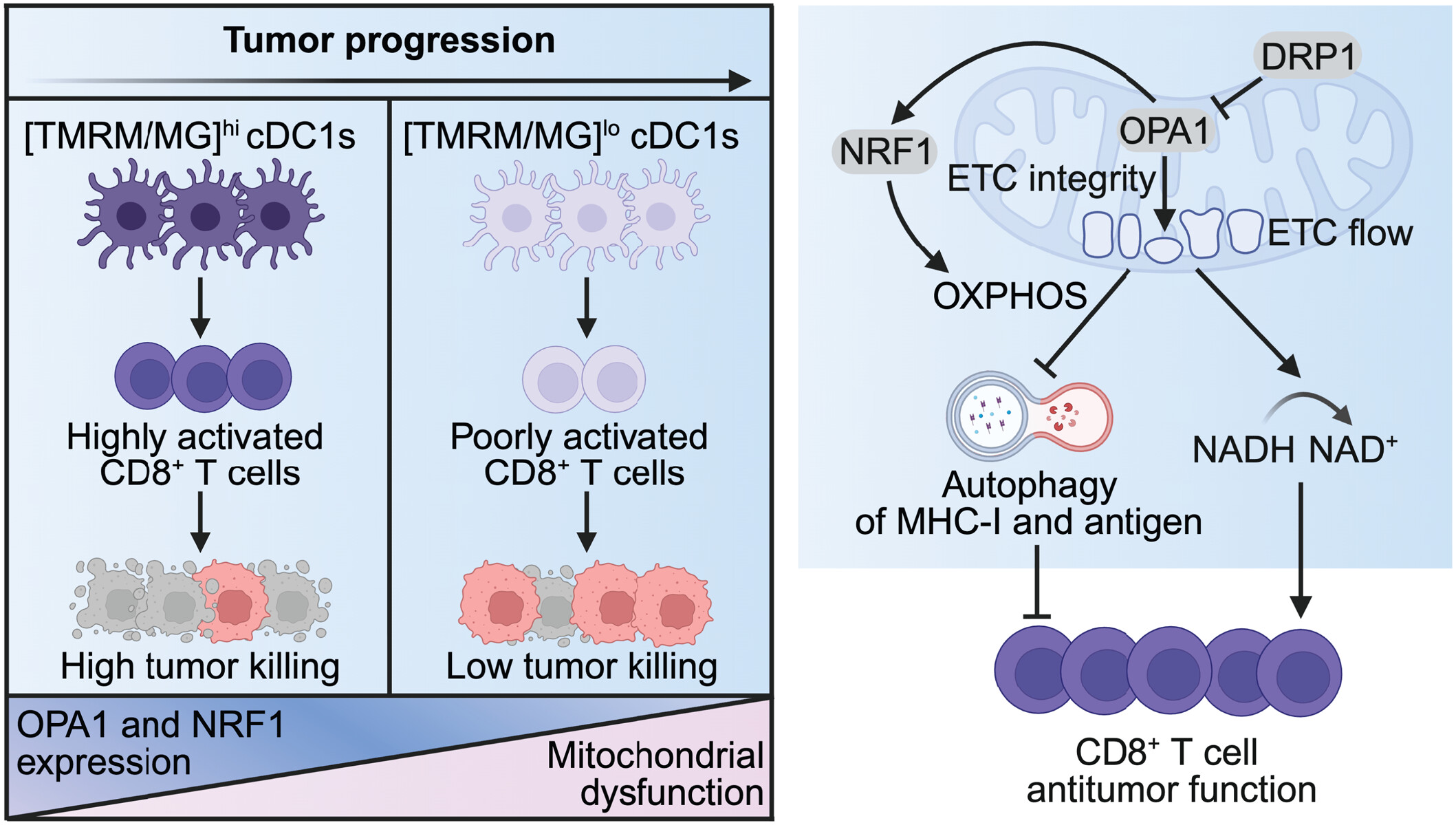
线粒体代谢与信号通路调控cDC1抗肿瘤应答
(左图)相较于[TMRM/MG]低表达cDC1,[TMRM/MG]高表达cDC1能更高效激活CD8⁺T细胞应答、抑制肿瘤生长;肿瘤进展中,肿瘤内cDC1会发生线粒体功能障碍,OPA1-NRF1信号通路活性下调。
(右图)OPA1-NRF1通路维持氧化磷酸化进程,抑制自噬与溶酶体降解MHC-I分子及抗原;OPA1保障电子传递链正常运转,平衡NAD⁺/NADH比值,增强cDC1免疫原性;线粒体分裂蛋白DRP1可拮抗以上作用。(配图由BioRender.com制作)
摘要全文
抗肿瘤免疫依赖1型经典树突状细胞(cDC1s),但cDC1如何在肿瘤微环境中维持正常功能活性,此前尚无定论。本研究证实:肿瘤内cDC1存在差异化线粒体状态,OPA1介导的线粒体能量代谢与氧化还原代谢,是决定cDC1抗肿瘤应答的核心因素。机制上,OPA1通过促进核呼吸因子1(NRF1)表达、维持电子传递链完整性,调控cDC1的抗原呈递与CD8⁺T细胞激活功能,保障线粒体能量供给稳定、维持NAD⁺/NADH氧化还原平衡。肿瘤进展过程中,肿瘤内cDC1的线粒体膜电位、线粒体体积逐步下降,OPA1-NRF1信号通路持续弱化。动物实验显示,瘤内输注线粒体极化的cDC1可发挥显著免疫治疗效果,与免疫检查点阻断疗法联用疗效更佳。综上,本研究证实线粒体代谢与相关信号通路可作为潜在靶点,用于激活cDC1功能、优化癌症免疫治疗方案。
https://wap.sciencenet.cn/blog-41174-1528693.html
上一篇:为何部分抗癌免疫细胞会在肿瘤内部丧失战斗力