 精选
精选
癫痫药跨界阿尔茨海默病
新研究揭示阿尔茨海默病早期分子事件关键环节,老药或可从源头阻断致病蛋白生成
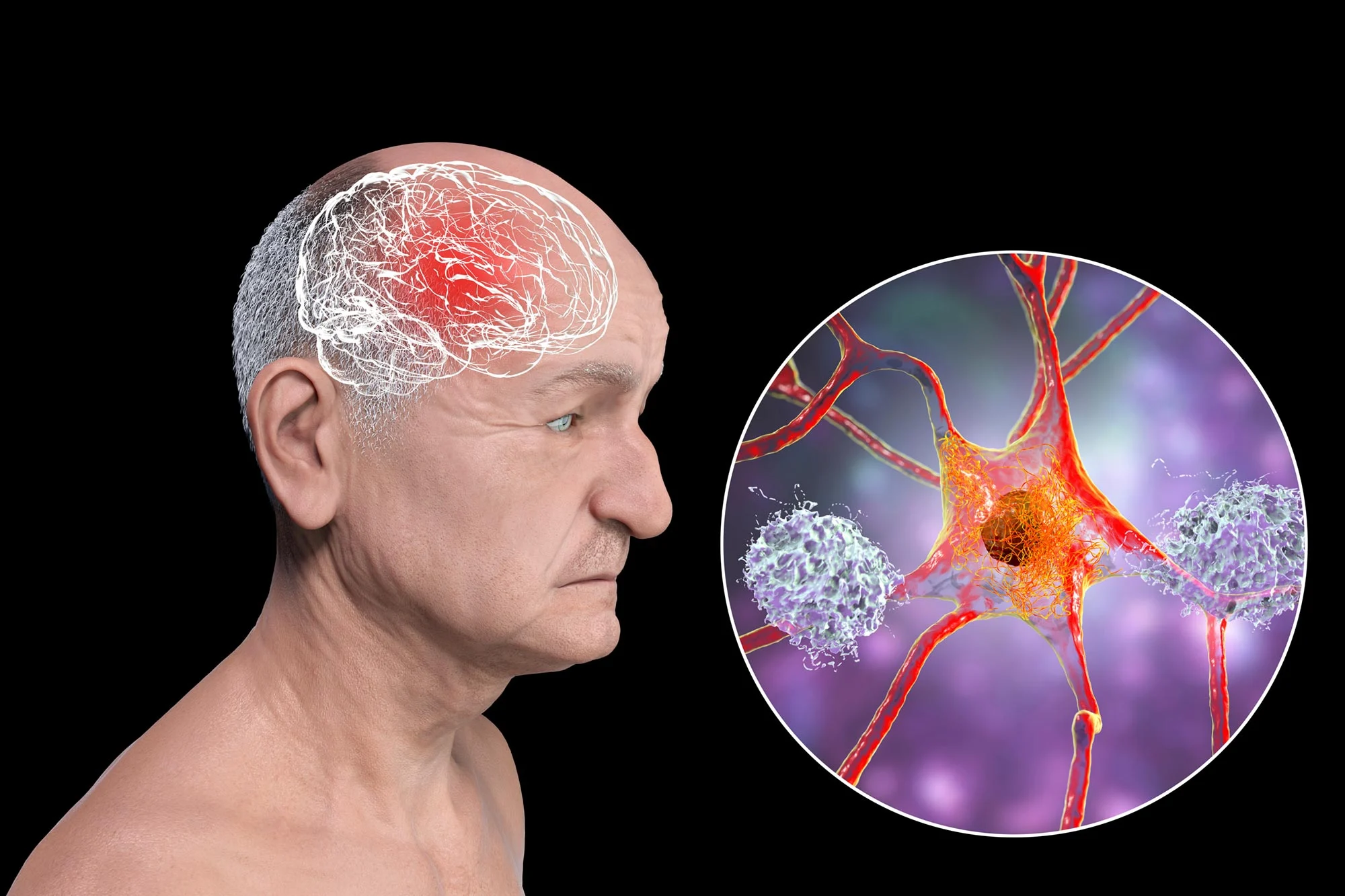
一项新研究发现了阿尔茨海默病早期分子事件中一个此前被忽视的关键步骤,明确了一种毒性极强的蛋白片段在神经元内的形成位置,以及如何阻断这一形成过程。
与现有聚焦于清除已形成斑块的治疗手段不同,左乙拉西坦的作用机制独树一帜——它能从源头上阻止毒性β淀粉样肽的生成。
数十年来,研究人员早已确认,阿尔茨海默病的特征是大脑中堆积毒性蛋白片段,但这些有害片段具体在何处、以何种方式产生,始终是未解之谜。
美国西北大学的科学家在这项新研究中,不仅确定了阿尔茨海默病患者体内这类毒性物质堆积的位置和时间,还发现了一种已获美国食品和药物管理局批准、价格低廉的药物,能在脑组织受损前阻断这一致病过程。
研究人员结合动物模型、实验室培养的人类神经元,以及阿尔茨海默病高风险人群的脑组织展开研究,重点关注了一种极具危害性的蛋白片段——β淀粉样蛋白42。他们发现,这种肽会在突触小泡内大量堆积,而突触小泡是神经元释放化学信号、实现相互通讯的微小囊状结构。
左乙拉西坦是一种应用数十年、临床处方量极大的抗癫痫药物,研究人员将其用于动物和人类神经元的实验后发现,该药物能有效抑制β淀粉样蛋白42的生成。通过阻止这种肽的产生,左乙拉西坦切断了最终导致β淀粉样斑块堆积的连锁反应。

研究通讯作者杰弗里·萨瓦斯与实验室成员交流
该研究的通讯作者、西北大学范伯格医学院行为神经学副教授杰弗里·萨瓦斯博士表示:“目前市面上的多款阿尔茨海默病药物,如仑卡奈单抗和多纳单抗,获批的适应症均为清除已形成的β淀粉样斑块,而我们则找到了能阻止β淀粉样蛋白42肽和相关斑块生成的全新机制。这项新发现不仅揭示了阿尔茨海默病的全新生物学特征,也为新的药物靶点开发打开了大门。”
该研究成果近期发表于《科学·转化医学》期刊。
抗癫痫药物跨界助力阿尔茨海默病防治
这一发现的核心与淀粉样前体蛋白(APP) 相关,该分子对大脑发育和突触(神经元间的连接结构)形成至关重要。当淀粉样前体蛋白发生异常加工时,会生成包括β淀粉样蛋白42在内的多种β淀粉样肽,而β淀粉样蛋白42与阿尔茨海默病的关联尤为密切。西北大学的研究人员发现,淀粉样前体蛋白在神经元内的转运方式,是决定β淀粉样蛋白42是否生成的关键因素。
FDA-Approved Seizure Drug May Stop Alzheimer’s Before It Starts
动画展示了神经元内突触小泡循环的过程,以及施用左乙拉西坦后,如何让淀粉样前体蛋白在细胞表面停留更长时间,从而使其偏离生成毒性β淀粉样蛋白42的通路。
突触小泡循环是一个持续进行的过程,支撑着人类的每一个想法、记忆、动作和感知,而左乙拉西坦的作用恰好发生在这一过程中。该药物会与一种名为SV2A的蛋白结合,这一相互作用会减缓神经元从细胞表面回收并循环利用突触小泡组件的步骤。通过延缓这一循环过程,左乙拉西坦能让淀粉样前体蛋白在神经元表面停留更久,进而使其偏离细胞内生成毒性β淀粉样蛋白42的通路。
萨瓦斯说:“在三四十岁乃至五十岁时,我们的大脑通常能引导蛋白质避开这些有害的代谢通路。但随着年龄增长,这种保护能力会逐渐减弱——这并非疾病的表现,而只是衰老的自然过程。但在阿尔茨海默病患者的大脑中,大量神经元的蛋白代谢会偏离正常轨道,β淀粉样蛋白42也因此开始生成。随后,tau蛋白缠结出现,神经细胞死亡,痴呆症状显现,神经炎症发生,到这个阶段就回天乏术了。”
药物干预需“极早开展”
萨瓦斯强调,要实现阿尔茨海默病的预防,必须进行极早期的干预。阿尔茨海默病高风险人群可能需要“极早”开始服用左乙拉西坦,甚至可能要在美国食品和药物管理局新批准的检测手段发现β淀粉样蛋白42水平轻度升高前20年就开始用药。
他表示:“一旦出现痴呆症状,再服用这款药物就毫无意义了,因为此时大脑已经发生了大量不可逆的改变,众多神经细胞也已死亡。”

杰弗里·萨瓦斯在实验室开展研究
研究通讯作者杰弗里·萨瓦斯指着电脑,与实验室成员探讨他们发表在《科学·转化医学》上的最新研究成果。
鉴于有效的干预窗口期极短,研究团队计划将研究重点放在遗传性阿尔茨海默病患者身上,包括唐氏综合征患者。尽管这类患者群体规模较小,但他们或将成为首批从这项研究衍生的预防策略中获益的人群。
挖掘现有人类临床数据,验证药物效果
由于左乙拉西坦已获美国食品和药物管理局批准,且被广泛用于癫痫治疗,研究人员着手分析现有医疗记录,寻找其对阿尔茨海默病病程影响的线索。他们利用美国国家阿尔茨海默病协调中心的数据,开展了相关性分析,对比了服用左乙拉西坦的患者、服用劳拉西泮的患者,以及服用其他抗癫痫药物或未服用抗癫痫药物的患者的预后情况。
分析结果显示,与其他组别相比,服用左乙拉西坦的阿尔茨海默病患者,从被诊断出认知衰退到死亡的时间出现了具有临床意义的延迟。
萨瓦斯表示:“尽管病程延缓的幅度有限,仅有数年时间,但这一分析结果证实,左乙拉西坦对减缓阿尔茨海默病的病理进展具有积极作用。”
唐氏综合征脑组织研究提供关键佐证
除了基因工程小鼠模型和培养的人类神经元实验,研究团队还分析了因意外或其他非相关原因、在二三十岁时离世的唐氏综合征患者的脑组织。萨瓦斯解释道,超过95%的唐氏综合征患者会在40岁左右患上恶性早发性阿尔茨海默病,原因是淀粉样前体蛋白的编码基因位于唐氏综合征患者体内多了一条的那条染色体上。
他说:“研究这些二三十岁离世的唐氏综合征患者的脑组织,我们可以确定他们最终都会患上阿尔茨海默病,这也为我们研究人类大脑中阿尔茨海默病的极早期变化提供了绝佳机会。”
研究人员在这些脑组织中,观察到了与萨瓦斯实验室此前在小鼠模型中发现的相同现象——突触前蛋白堆积。而这种早期堆积现象,发生在突触丢失和痴呆症状出现之前。
萨瓦斯指出:“这一阶段被我们及其他研究者称为阿尔茨海默病的‘悖论期’——在突触丢失、痴呆症状出现前,最先发生的变化是突触前蛋白的堆积。因此可以想象,如果在这些患者的青少年时期就开始施用左乙拉西坦,实际可能会产生预防性的治疗效果。”
萨瓦斯也坦言,左乙拉西坦并非“完美的药物”,该药物在体内的代谢清除速度相对较快。目前,他和同事正致力于研发该药物的改良版本,让新药能在体内保持更长时间的活性,更精准地靶向阻断β淀粉样斑块形成的作用机制。
转载本文请联系原作者获取授权,同时请注明本文来自孙学军科学网博客。
链接地址:https://wap.sciencenet.cn/blog-41174-1524040.html?mobile=1
收藏

