 精选
精选
利用细胞周期中受损检查点的抗癌化合物
许多致癌突变会破坏细胞生长与分裂之间周期中的关键检查点,导致E2F转录因子家族蛋白的活性不受调控。一组旨在直接阻断细胞周期关键调控因子(称为周期蛋白,cyclins)的化合物,能够抑制由E2F高活性驱动的癌症生长。
研究背景
许多癌症由抑癌基因(如RB1和TP53)的功能缺失突变驱动,这类癌症治疗难度较大。这些突变会破坏细胞周期中G1期(生长阶段)与S期(DNA合成阶段)之间的检查点,导致E2F转录因子家族蛋白的活性不受约束——而E2F的异常激活会驱动细胞失控增殖和肿瘤生长1。这种机制存在于多种癌症中,在小细胞肺癌(SCLC)中尤为常见:几乎所有小细胞肺癌患者都存在RB1和TP53基因缺失2。不过,E2F的过度激活也可能触发细胞凋亡(程序性死亡)3。
此前研究表明,周期蛋白(cyclin)可与E2F结合并抑制其活性⁴;若破坏这种周期蛋白-E2F相互作用,可能导致E2F过度激活,进而选择性杀伤G1-S检查点缺陷的肿瘤细胞⁵。然而,目前尚无法直接阻断周期蛋白与其底物的相互作用,且这种干预方式的潜在机制及可能的抗肿瘤效果仍不明确。
研究发现
我们研发了一类大环肽化合物,可阻断带有“RxL基序”的底物蛋白与周期蛋白的结合。我们将这类化合物命名为“周期蛋白RxL抑制剂”,并对其进行优化,以提高对特定周期蛋白的选择性及口服生物利用度。
靶向周期蛋白A(cyclin A)和周期蛋白B(cyclin B)的RxL抑制剂,可诱导E2F高活性癌细胞(包括大多数小细胞肺癌细胞系)发生凋亡。在移植了化疗耐药性小细胞肺癌患者肿瘤组织的小鼠模型中,口服周期蛋白A/B RxL抑制剂展现出显著的抗肿瘤活性。随后,我们结合细胞生物学、基因筛选及生物化学方法,阐明了这类周期蛋白RxL抑制剂杀伤E2F高活性癌细胞的具体机制。
诱导肿瘤细胞凋亡需同时抑制周期蛋白A和周期蛋白B:
- 阻断周期蛋白A会导致S期E2F活性升高,引发DNA损伤和复制应激;
- 基因筛选结果显示,周期蛋白A/B RxL抑制剂通过激活“纺锤体组装检查点(SAC)”触发细胞死亡——该检查点可暂停细胞分裂,直至染色体正确排列(图1a)。
有趣的是,这一效应的产生既需要周期蛋白B,也需要另一种名为CDK2的蛋白。意外的是,周期蛋白B RxL抑制剂会促进周期蛋白B与CDK2形成复合物——这一现象较为特殊,因为CDK2通常与其他周期蛋白结合(图1b)。该复合物可驱动纺锤体组装检查点激活并诱导细胞凋亡。
此外,周期蛋白B RxL抑制剂还能阻断周期蛋白B与MYT1(一种酶)的相互作用:MYT1与周期蛋白B结合后会降低周期蛋白B-CDK复合物的活性,而抑制剂通过解除这种抑制,释放周期蛋白B-CDK2的活性以促进凋亡——即这类抑制剂通过“增强而非抑制”周期蛋白B的活性发挥作用。
这些发现揭示了一种针对E2F高活性肿瘤的“两步式细胞死亡机制”。
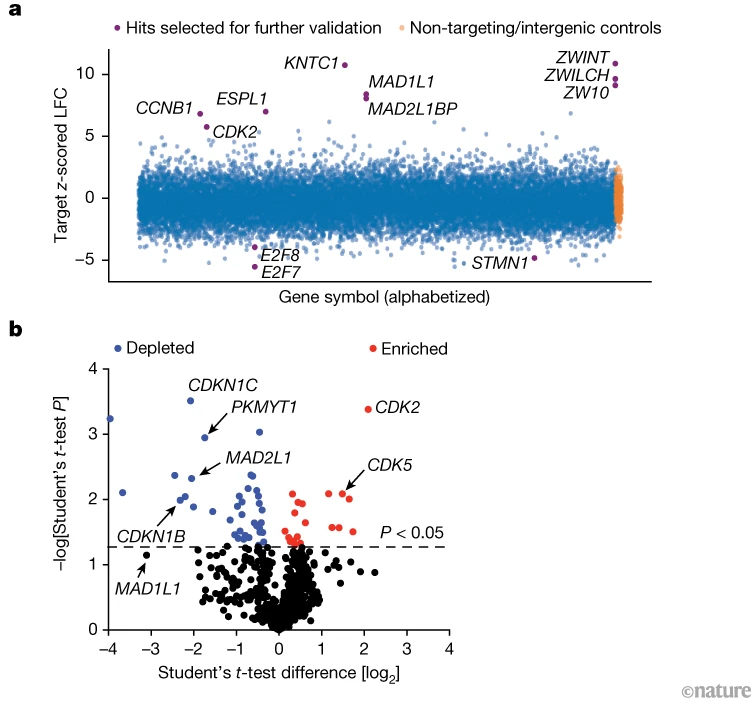
图1 | 细胞周期蛋白抑制剂通过细胞周期检查点依赖性机制诱导细胞死亡**
存在细胞周期检查点突变的小细胞肺癌(SCLC)细胞系,对新研发的周期蛋白A/B靶向化合物敏感。
a. 基因编辑筛选显示:从小细胞肺癌细胞系中敲除不同基因后,细胞对该化合物(相较于其无活性镜像异构体对照)的耐药性(y轴正值)和敏感性(y轴负值)发生变化。筛选中“显著命中”的基因在耐药性或敏感性上表现出统计学显著的对数转换倍数变化(LFC)。许多耐药相关基因参与确保细胞分裂过程中染色体的正确分离。
b. 与异构体对照处理相比,抑制剂处理后(蓝色标注)部分蛋白与周期蛋白B的结合减少,而另一些蛋白与周期蛋白B的结合增加(红色标注)。
研究意义
在尝试抑制周期蛋白-E2F相互作用的过程中,我们研发的周期蛋白抑制剂通过一种此前未被发现的机制杀伤E2F高活性癌细胞。尽管研究重点为小细胞肺癌,但我们发现,其他因遗传改变导致G1-S检查点破坏、进而引发E2F活性升高的癌症,同样对这类抑制剂敏感。
这些发现为G1-S检查点功能异常的癌症提供了一种更具普适性的治疗策略:E2F激活可作为“通路异常”的标志,同时提示这类癌症可能对该治疗方法敏感。目前,针对其中一种周期蛋白A/B RxL抑制剂(CID-078)的Ⅰ期临床试验已启动,受试者为患有G1-S检查点异常实体瘤的患者,包括小细胞肺癌和三阴性乳腺癌(详见临床试验网站clinicaltrials.gov,试验编号NCT06577987)。
尽管破坏周期蛋白B-MYT1相互作用可提高周期蛋白B-CDK的活性,但目前仍不清楚为何周期蛋白B会招募CDK2而非其常规结合伙伴CDK1。此外,虽然本研究为G1-S检查点缺陷癌症中使用这类抑制剂提供了临床前证据,但该策略的临床有效性和耐受性仍需临床试验结果验证。
未来,我们将通过临床试验进一步探索这一治疗方法,并深入研究这类化合物如何“劫持”细胞周期通路以杀伤癌细胞;同时,我们也在研究其他周期蛋白RxL抑制剂,以明确选择性阻断不同周期蛋白-底物相互作用对癌症生物学及治疗潜力的影响。
(作者:希尔帕·辛格(Shilpa Singh)、马修·G·奥瑟(Matthew G. Oser),任职于美国马萨诸塞州波士顿市丹娜-法伯癌症研究所。)
专家观点
这项出色的研究涵盖多个层面:从利用结构数据研发小分子化合物,到在细胞系和小鼠模型中测试抑制剂效果,再到阐明其作用机制。尽管研究聚焦于小细胞肺癌,但这类小分子化合物可能对多种肿瘤有效,尤其是E2F高活性肿瘤。除了转化医学层面的意义,该研究还揭示了与细胞周期进程基础机制相关的极具价值的新发现。
(评论者:朱利安·萨奇(Julien Sage),任职于美国加利福尼亚州斯坦福市斯坦福大学。)
研究背后的故事
2019年,我刚成立自己的实验室,致力于研究RB1缺陷型小细胞肺癌的治疗策略。当时,我与Circle制药公司建立了合作——该公司正研发针对RB1缺陷、E2F驱动型癌症的周期蛋白靶向大环肽化合物⁵。
Circle公司发现,同时抑制周期蛋白A和周期蛋白B可杀伤部分小细胞肺癌细胞系,但单独使用周期蛋白B RxL抑制剂无法杀伤细胞,因此其科研团队最初认为细胞毒性仅由阻断周期蛋白A介导。彼时,Circle公司还与本研究共同作者迪帕克·尼哈万(Deepak Nijhawan)的实验室有合作,我们两个学术实验室一致认为:周期蛋白A/B RxL抑制剂通过激活纺锤体组装检查点(SAC)杀伤细胞,且需同时阻断两种周期蛋白才能诱导细胞死亡。
后来,Circle公司研发出周期蛋白A选择性抑制剂,发现其无细胞毒性,这进一步证实“同时抑制两种周期蛋白”是诱导细胞死亡的必要条件。我们最初发现,细胞毒性的产生需要周期蛋白B和CDK2的参与,并推测CDK2的作用是通过其与周期蛋白A的常规相互作用实现的。数年后,我们才发现:破坏周期蛋白B与CDK2的相互作用会使细胞对周期蛋白A/B RxL抑制剂产生耐药性。这次合作是学术界与工业界协同创新的典型范例。
(讲述者:马修·G·奥瑟(M.G.O.))
编辑视角
本文的突出之处在于:一方面研发了可同时靶向周期蛋白A和周期蛋白B的大环肽化合物,并在G1-S检查点受损癌症的小鼠模型中证实其显著的抗肿瘤活性;另一方面,揭示了周期蛋白A/B抑制与纺锤体组装检查点之间的机制关联——正是这种关联最终驱动了肿瘤细胞死亡。
转载本文请联系原作者获取授权,同时请注明本文来自孙学军科学网博客。
链接地址:https://wap.sciencenet.cn/blog-41174-1498964.html?mobile=1
收藏

