 精选
精选
涡轮增压NK细胞在自身免疫性疾病治疗中展现前景
这种新疗法或为狼疮等自身免疫疾病提供比CAR-T细胞疗法更安全、更廉价的替代方案。
彩色扫描电子显微镜下,一个绿色的自然杀伤细胞呈圆形,表面“毛茸茸”的,背景为黑色。
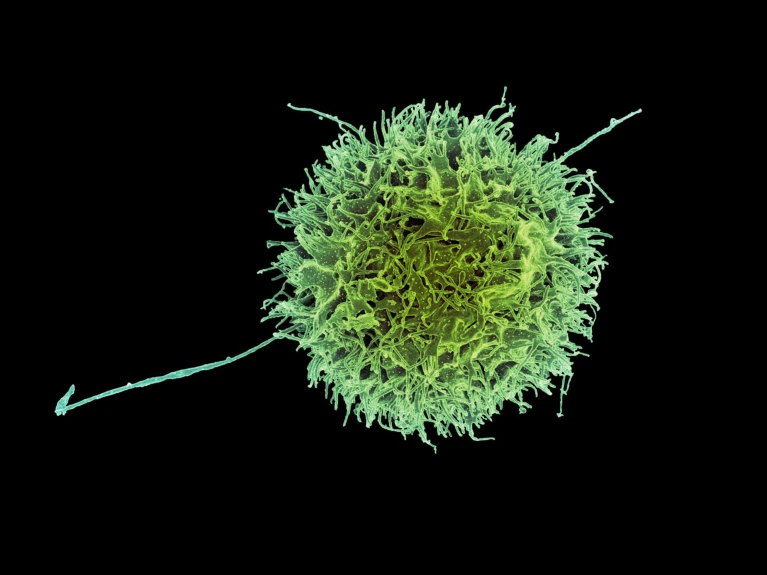
这种被称为自然杀伤细胞的免疫细胞(经人工染色)可通过生物工程改造,攻击产生危险抗体的细胞。图片来源:美国国家过敏和传染病研究所/美国国立卫生研究院/科学图片库
经过增强的“自然杀伤”细胞有望成为一种有效的手段,重置紊乱的免疫系统,从而缓解某些自身免疫性疾病。
两项小型临床试验的结果表明,研究人员可以对自然杀伤细胞——一种能摧毁受感染或病变细胞的免疫细胞——进行基因工程改造,以消灭那些产生针对人体自身组织抗体的异常细胞。这些“自身抗体”会损害组织,引发狼疮和系统性硬化症等自身免疫性疾病。
“自然杀伤细胞进化出了寻找并摧毁异常细胞的能力,”位于加利福尼亚州旧金山南部的生物技术公司Nkarta的总裁纳迪尔·马哈茂德说,“如果这种能力足够强大,能够推动免疫系统重置,那么就有可能重建一个健康、未受影响的免疫系统。”
其中一项试验的结果于6月在西班牙巴塞罗那举行的欧洲风湿病协会联盟(EULAR)会议上公布。另一项试验的结果则发表在《细胞》杂志上。
杀手细胞出现之前
这种方法源于癌症疗法,该疗法依赖另一种免疫细胞——T细胞,通过基因工程改造T细胞,使其能够识别并杀死肿瘤细胞。经过改造的细胞利用一种名为嵌合抗原受体(CAR)的蛋白质来识别目标,因此被称为CAR-T细胞。
CAR-T细胞可以使某些类型的血癌缓解期超过十年,并且在治疗某些自身免疫性疾病方面也显示出初步前景。但目前市面上的CAR-T细胞疗法价格昂贵,且制备过程复杂:每一次治疗都必须利用接受治疗者自身的T细胞来制备。
休斯顿德克萨斯大学MD安德森癌症中心研究细胞疗法的凯蒂·雷兹瓦尼说,这些因素意味着,目前在美国,可能从CAR-T细胞癌症疗法中受益的人当中,只有约四分之一能够获得这种治疗。“自身免疫性疾病患者的数量是癌症患者的五倍,”她说,“那么,我们怎么可能负担得起用这些昂贵的疗法来治疗自身免疫性疾病呢?”
然而,自然杀伤细胞可以从献血者身上获取,并进行基因改造以产生“CAR-NK”细胞,这些细胞可以冷冻起来,用于治疗多名患者。雷兹瓦尼说,她在MD安德森癌症中心的同事可以从一份脐带血捐赠中制备出数百剂CAR-NK细胞。
完美之选?
马哈茂德说,CAR-NK细胞的首批试验是在癌症治疗中进行的,早期结果喜忧参半。中国南京锐格 Therapeutics公司(一家正在研发CAR-NK细胞疗法的公司)的首席执行官 Max Qian钱马克说,一个可能的局限性是这些细胞的寿命比CAR-T细胞短。“如果肿瘤复发,就需要药物仍然存在于体内。”他说。
但细胞的短暂存在对于治疗自身免疫性疾病来说可能不是问题。钱马克补充说,用CAR-NK细胞进行短暂治疗可能足以消除自身抗体的产生,或者如果需要,患者可以接受多剂治疗。之后,免疫系统可以利用新产生的、未被触发产生自身抗体的抗体生成细胞群进行自我重建。
去年年底,Nkarta宣布将终止其CAR-NK细胞癌症疗法的研发工作,转而专注于自身免疫性疾病。“CAR-NK细胞疗法似乎是为自身免疫性疾病量身定制的,”马哈茂德说。
在上个月的EULAR会议上,锐格 Therapeutics及其合作者展示了27名接受CAR-NK细胞治疗自身免疫性疾病系统性红斑狼疮(可引起关节、肾脏、大脑和其他器官炎症)患者的数据。所有参与者在治疗后都有一定程度的改善。一些参与者在治疗后被随访了近两年,仍然处于缓解状态。
多靶点杀手
这些参与者接受的CAR-NK细胞靶向一种名为CD19的蛋白质,这种蛋白质由许多产生抗体的细胞所产生。但纽约哥伦比亚大学的风湿病学家安卡·阿斯卡纳西说,在某些自身免疫性疾病中,可能还需要靶向一组不产生CD19的长寿抗体生成细胞。
中国海军军医大学的风湿病学家徐沪济带领的研究团队采用了这种方法,治疗了一名患有自身免疫性疾病系统性硬化症的患者,这种疾病会导致过量瘢痕组织的产生,使皮肤、血管和其他组织硬化。
该团队设计了靶向CD19和另一种名为BCMA(由长寿抗体生成细胞产生)的蛋白质的CAR-NK细胞。研究人员在6月24日报告称,治疗后,该患者的自身抗体水平下降。
CAR-NK细胞似乎还逆转了患者组织的硬化,恢复了正常的皮肤和血管结构。
雷兹瓦尼说,这一发现特别值得关注,因为它带来了希望,即自身免疫性疾病造成的某些损害不仅可以预防,还可以逆转。“希望是存在的,”她说,“现在我们需要更多的数据。”
转载本文请联系原作者获取授权,同时请注明本文来自孙学军科学网博客。
链接地址:https://wap.sciencenet.cn/blog-41174-1492790.html?mobile=1
收藏

