既然是纤维材料,使用这种材料作为各种生物释放氢气的工具应该可行。
摘要:氢气(H₂)在治疗骨关节炎方面具有巨大潜力,但其快速扩散和短暂保留时间使其难以发挥稳定的治疗效果。本研究开发了一种短纤维注射材料,能够在现场持续生成氢气以消除活性氧物种(ROS),缓解氧化应激和炎症,并促进组织修复。我们通过湿化学剥离方法制备了具有高产氢效率的H-Si纳米片,并通过电纺技术将其与GelMA短纤维结合,实现了H-Si纳米片的现场递送和通过GelMA的封装和降解调节产氢速率,最终实现连续和受控的氢气供应以及对骨关节炎的稳定治疗效果。体外和体内实验证实了这种材料的安全性和有效性。结果显示,该材料能够在模拟生理环境中持续高效地产生氢气(100毫克材料可产生8.6%的氢气),有效消除细胞活性氧物种(ROS阳性率减少85.89%),减少细胞衰老和凋亡(细胞死亡率降低52%,SA-βgal表达减少78.3%),促进正常软骨细胞功能(Col II表达增加67.4%,Ki67表达增加87.5%),并改善大鼠的骨关节炎(OARSI评分增加216%)。本研究设计的现场氢气生成和控制系统为氢气局部稳定治疗骨关节炎提供了一种新方法。
研究意义:氢气(H₂)通过缓解氧化应激在治疗骨关节炎方面具有巨大潜力,但其快速扩散和短暂保留时间使其难以发挥稳定的治疗效果。本研究引入了一种创新的注射材料,结合了H-Si纳米片和GelMA短纤维来解决这一问题。通过使现场持续生成氢气,这种材料有效地消除了活性氧物种,减少了氧化应激和炎症,并促进了组织修复。体外和体内实验证明了其高产氢效率、安全性和治疗效果,为骨关节炎管理提供了一种有前景的新方法。
背景分析
骨关节炎(OA)是一种常见的慢性退行性关节疾病,其症状包括关节疼痛、肿胀、僵硬和活动受限[1]。随着人口老龄化趋势的加剧,OA已成为一个重大的全球健康问题,严重影响患者的生活质量和日常活动[2]。在OA的病理过程中,炎症反应的发生和发展起着关键作用[[3], [4], [5], [6]]。炎症的扩散导致关节组织持续降解,进一步加剧炎症,形成恶性循环,这是OA持续疼痛的主要原因之一[7]。在目前的OA治疗中,药物如非甾体抗炎药可以在一定程度上缓解疼痛症状,但在控制炎症方面效果不佳[3]。因此,寻找一种能够有效控制炎症、缓解疼痛并促进关节组织修复的新治疗方法具有重要的临床意义[8]。
氧化应激在OA的发病和进展中起重要作用,活性氧物种(ROS)是氧化应激的主要介质,包括超氧自由基(O2-)、羟基自由基(·OH)、过氧化氢(H2O2)等[9]。ROS可以直接损伤软骨细胞、滑膜细胞和骨细胞,导致细胞凋亡和死亡[[9], [10], [11], [12], [13]]。此外,ROS可以激活炎症信号通路,促进炎性因子的释放,加重关节炎症[[14], [15], [16]]。近年来,基于氢气的治疗策略引起了研究人员的广泛关注[[17], [18], [19], [20], [21]],包括其潜在的生物安全问题,如微生物群落的改变和长期暴露的影响[[22], [23], [24]]。氢气是一种具有还原性的生物活性气体,表现出多种生物学效应,如抗氧化、抗炎、促进细胞增殖和组织修复[[25], [26], [27]]。与超氧化物歧化酶模拟物(SOD模拟物)相比,一些SOD模拟物在较高浓度下可能表现出脱靶效应或毒性[28],生物相容性的氢气减少了不良免疫反应或炎症的风险,使其更适合重复或长期使用。因此,利用氢气消除活性氧物种以缓解炎症已成为治疗关节炎的一种新颖且有前景的方法。
然而,纯氢气气体存在快速扩散和短保留时间的缺点,不利于长期治疗效果[27]。为解决这些问题,开发一种能够在原位持续生成氢气的生物材料是必要的[17]。研究人员已合成了各种纳米材料,这些材料可以在相对条件下生成H2[[29], [30], [31]],其中You等人通过将CaSi2与浓盐酸反应并超声剥离合成了H-Si纳米片[27]。H-Si纳米片可以与水反应生成氢气,呈现出理想的释氢性能,这使得H-Si纳米片非常适合体内原位生成H2。此外,产物硅离子可以促进血管生成和软骨下骨形成,有利于修复关节软骨损伤。然而,类似于纯氢气气体,H-Si纳米片由于其快速的产氢速率而存在短效治疗持续时间的问题。因此,有必要将H-Si封装在响应性可降解材料中,以减缓其反应速率并控制氢气释放速率。甲基丙烯酸化明胶(GelMA)具有良好的生物相容性和促进细胞生长及组织再生的多重益处,常作为组织工程中的载体材料[[32], [33], [34]]。此外,GelMA可以在OA微环境中被基质金属蛋白酶降解,适合作为H-Si纳米片的载体[[35], [36], [37]]。治疗关节炎最常用的方法是将药物注入关节腔内。为实现H-Si的负载和H-Si/GelMA的可注射性,我们提出通过电纺制备H-Si纳米片和GelMA的复合纤维,并通过紫外线交联GelMA和使用均质器将其破碎成短纤维,从而平衡材料的可注射性和产氢速率[[42], [43], [44]]。
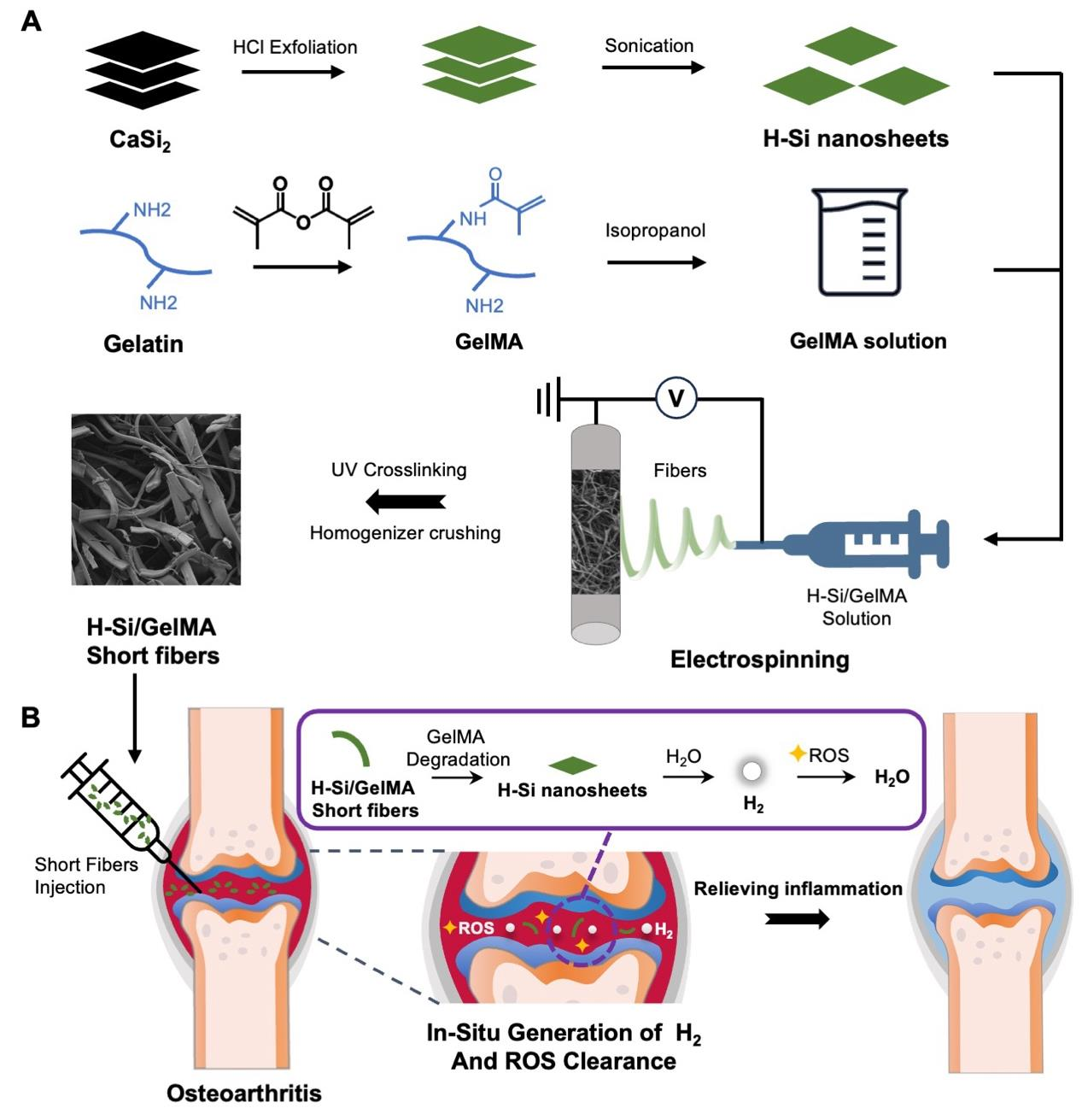
研究方法总结:考虑到关节炎抗氧化治疗的迫切需要以及氢气在抗氧化疗法中的显著价值,我们设计了一种基于无机H-Si纳米片和GelMA短纤维的释氢材料。具体来说,我们通过湿化学剥离制备了具有产氢性能的H-Si纳米片,同时制备甲基丙烯酸化明胶(GelMA)。然后,我们使用电纺将H-Si和GelMA混合,得到H-Si/GelMA纤维,随后通过紫外光交联GelMA并使用均质器将其破碎成H-Si/GelMA短纤维(图1A)。这种短纤维系统可以通过注射进入关节腔,降解后释放H-Si纳米片,后者进一步与水反应生成氢气。释放的氢气通过氧化还原反应在关节炎部位消除活性氧物种,从而缓解炎症并有效治疗骨关节炎(图1B)。
在这项研究中,我们探索了这种新型关节炎治疗材料的有效性和安全性。体外实验结果证实,这种复合材料具有高表面积和丰富的产氢性能,能够在模拟关节液环境中缓慢释放氢气。此外,体内实验表明,注射该材料后,释放的氢气有效改善了氧化应激,从而缓解炎症、促进组织修复并改善关节功能。通过对材料的释氢机制、生物相容性和治疗效果的深入研究,我们希望为骨关节炎患者提供更有效和个性化的治疗选择,为缓解这种疾病带来新的希望和可能性。
转载本文请联系原作者获取授权,同时请注明本文来自孙学军科学网博客。
链接地址:https://wap.sciencenet.cn/blog-41174-1452293.html?mobile=1
收藏

