 精选
精选
胰高血糖素样肽-1(GLP-1)是由肠道内分泌细胞在食物摄取后分泌的,并作为增糖激素增强依赖葡萄糖的胰岛素分泌。药理激活GLP-1受体(GLP-1R)减少了胰高血糖素的分泌(这会提高血糖)和胃排空速率,导致开发了用于治疗2型糖尿病(T2D)的GLP-1疗法。GLP-1R在几种胰腺岛细胞类型上表达,并在中枢神经系统的多个区域中表达。随后的研究揭示,外源性GLP-1给药通过动物和人类大脑中的GLP-1R激活抑制了食物摄入,导致体重减轻。几十年来使用GLP-1药物的经验,主要是如利拉鲁肽和司美格鲁肽这样的酰化肽,用于治疗肥胖症和T2D(1),揭示了它们还在控制血糖和体重之外具有多方面的作用,例如减少心脏和肾脏疾病。这些益处背后有几种潜在机制,如减少全身性炎症(2),这对未来的临床应用和药物开发具有重要意义。
首批获批的GLP-1药物,如艾塞那肽和利拉鲁肽,需要每天一次或两次给药,随后出现了如杜拉鲁肽、每周一次的艾塞那肽、司美格鲁肽和替尔泽帕肽[一种葡萄糖依赖性胰岛素促分泌多肽受体(GIPR)和GLP-1R共激动剂]等长效版本,适合每周给药一次。GLP-1疗法的一个主要非代谢益处在心血管系统变得明显。一系列临床前研究表明,GLP-1R激动剂保护缺血心肌并在缺血性心脏损伤后保留心脏功能,这些作用与控制血糖或减重无关(1)。在2型糖尿病患者中进行了八项不同的心血管结果试验,以及在肥胖患者中的一项试验。持续存在于循环中的长效GLP-1药物降低了2型糖尿病和/或肥胖患者的非致死性中风、非致死性心肌梗死和心血管死亡的发生率。随后的试验证明,对于心力衰竭且射血分数保持正常的患者,无论是否患有2型糖尿病,司美格鲁肽都有益(NCT04788511)。
这是如何发生的?GLP-1药物对心血管有益的间接作用包括降低血压、减少从肠道分泌的致动脉粥样硬化脂蛋白、更好地控制血糖和减重。然而,临床前研究证明,GLP-1在正常血压非糖尿病动物中保护缺血心脏的程度超过了减重所能达到的效果。此外,一种因对2型糖尿病患者降低血糖和体重效果一般而退出市场的长效GLP-1疗法,艾比格列肽,降低了主要不良心血管事件的发生率22%(NCT02465515)。
在机制上,小鼠与人类心脏中GLP-1R的分布不同,这挑战了利用临床前研究推断人类潜在机制的实用性。GLP-1疗法还减少了敏感小鼠模型中动脉粥样硬化的发展,目前正在外周动脉疾病患者中进行临床试验(NCT04560998)。将GLP-1R激活与减少动脉粥样硬化和/或改善血流联系起来的机制尚不清楚,但可能与减重无关,而是与减少炎症有关。有趣的是,在肥胖患者中观察到的司美格鲁肽的心脏保护效应在药物开始使用几个月内发展出来,这远远早于大多数试验参与者实现有意义的体重减轻。此外,在研究司美格鲁肽对肥胖患者影响的SELECT心血管结果试验(NCT03574597)中,减重的程度与药物减少心脏病发作、中风和心血管死亡的效果没有关联。尚未研究GLP-1药物是否对1型糖尿病患者或高风险中风或心肌梗死的非糖尿病患者具有心脏保护作用。
GLP-1药物的作用
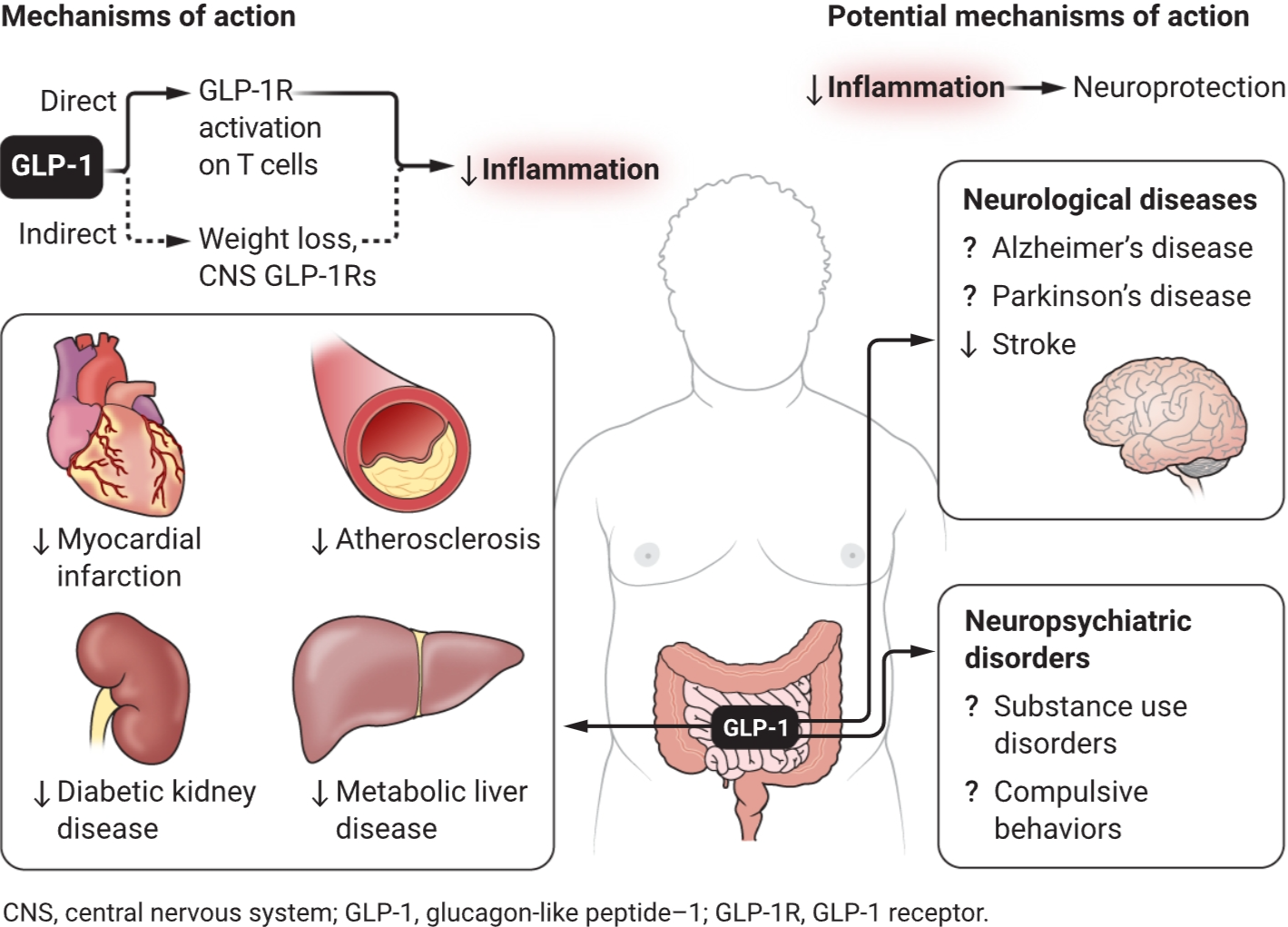
GLP-1通过直接和间接作用减少血糖和体重。GLP-1通过减重和神经GLP-1R激活间接减弱炎症,并通过在T细胞上的GLP-1R直接激活减弱炎症,同时通过靶向多个器官中的GLP-1R减少并发症。最初显示能减少血糖和体重,后续试验证明GLP-1药物减少了代谢疾病的心脏肾脏并发症。GLP-1药物目前正被探索用于广泛的神经和精神疾病。
临床试验和动物研究也支持GLP-1药物在治疗代谢性肝病患者中的作用,一项关于司美格鲁肽的第三阶段试验正在进行中(NCT04822181)。GLP-1R不由肝细胞表达,这挑战了我们理解GLP-1如何改善肝脏健康的方式。虽然体重减轻与减少肝脏脂肪变性和炎症有关,但临床前实验表明,少数群体的肝内GLP-1R表达细胞,主要是内皮细胞和T细胞(3),对代谢性肝病中GLP-1的治疗益处有贡献。有趣的是,司美格鲁肽在2型糖尿病患者中将肾脏疾病和心血管死亡的比率降低了24%(NCT03819153),而在动物模型的肾损伤中,GLP-1R信号的增加和减少分别改善或恶化了肾功能(4)。对GLP-1在肾脏作用机制的理解还不完整。尽管持续的GLP-1R激动剂逆转了糖尿病诱导的多种肾细胞类型中基因表达的失调,但GLP-1R在肾脏中的表达局限于啮齿动物和人类肾脏的一部分血管平滑肌细胞,而不是肾小球上皮细胞或管状细胞(5)。因此,GLP-1药物对肾脏的影响是否反映了直接的肾效应或来自肾外GLP-1R+细胞群的间接贡献仍不确定。
心脏、血管、肝脏和肾脏含有可能有助于器官保护的GLP-1R+细胞群体(5)。GLP-1R激动剂的另一个潜在的统一作用机制是减少炎症(见图)。小肠和大肠粘膜内的肠内分泌L细胞作为病原体传感器,对感染或无菌组织损伤作出反应,分泌GLP-1(6)。反过来,GLP-1在动物和人类中急性减少肠道和全身炎症。在免疫系统中,肠道上皮内淋巴细胞(IELs)和一些耗竭的T细胞是GLP-1R表达的主要细胞位点(7)。当通过激活T细胞,例如使用针对T细胞共受体CD3的抗体诱导炎症时,IEL GLP-1R对于转导GLP-1的局部和全身抗炎症作用是必需的(8)。然而,当通过多种Toll样受体(TLR)配体,如脂多糖(LPS)诱导炎症时,IEL GLP-1R对抗炎症作用不是必需的(2, 8)。出乎意料的是,减少TLR激活炎症的GLP-1全身抗炎症作用需要大脑中的GLP-1R信号传导,在神经元内(2)。此外,α1-肾上腺素能和δ及κ-阿片受体信号传导对于GLP-1药物的全身抗炎症作用的转导至关重要。大脑GLP-1R也是GLP-1药物减轻小鼠多发性败血症肺和髓系细胞全身炎症所必需的(2)。
GLP-1R信号的增加和减少分别减轻或加重了实验性脑损伤、中风或神经退行性疾病小鼠模型中的神经退行性和神经炎症程度(9, 10)。几项临床试验已检验了艾塞那肽在帕金森病患者中的治疗潜力,结果不一。一项更大的第三阶段试验正在检查每周一次的艾塞那肽在帕金森病中的潜在疗效(NCT04232969)。对真实世界医疗保健数据库和临床试验数据的审查将GLP-1药物的使用与2型糖尿病患者认知功能障碍率降低联系起来,两项第三阶段试验EVOKE(NCT04777396)和EVOKE Plus(NCT04777409)正在评估口服司美格鲁肽对有进行性认知功能障碍风险个体的影响(10)。
随着像司美格鲁肽和替尔泽帕肽这样更有效力的GLP-1药物的使用增加,这些药物在2型糖尿病或肥胖症患者中产生更大的血糖降低和更多减重效果,促使人们审查这些药物是否会改变多种中枢神经系统疾病的结果,包括抑郁症、强迫行为、过度饮酒或麻醉药品使用以及自杀意念。在SELECT心血管结果试验中,超过3年的暴露期间,在超重或肥胖且有心血管疾病史的人群中,随机分配至司美格鲁肽(n = 8803)与安慰剂(n = 8801)的精神病发病率没有差异(11)。在两个不同的大型医疗保健数据库的真实世界队列中分析超重或肥胖人群(无论有无2型糖尿病)的新发或复发自杀意念率时,与使用其他降糖或减肥药物的用户相比,接受司美格鲁肽治疗的个体自杀意念率较低。新发或复发自杀意念报告的危险比分别为0.27和0.44,反映了司美格鲁肽治疗个体中降低的比率(12)。此外,在TriNetx网络中的电子健康记录分析显示,相对于使用非GLP-1降糖或减肥药物的2型糖尿病和/或超重或肥胖人群,新发或复发的大麻使用障碍率较低(13)。
尽管关于使用GLP-1药物减少酒精使用的轶事报道很常见,但随机试验的结果仍不确定。接受度拉鲁肽治疗12周的个体,其主要目标是检查戒烟效果,报告称酒精消费量减少(14),而患有酒精使用障碍的人被随机分配到每周一次艾塞那肽治疗26周后,并没有减少重度饮酒天数的总数,尽管通过功能性磁共振成像确定,在大脑的隔区和腹侧纹状体区域显示出减弱的酒精线索反应性(15)。改善一系列依赖相关行为的轶事报道促使启动了多项随机对照试验,以确定GLP-1药物在这些疾病中是否具有治疗效用。
GLP-1药物在治疗2型糖尿病和肥胖症方面的成功促进了开发下一代疗法的兴趣,这些疗法比当前的GLP-1R激动剂更有效,能产生更大的体重减轻。替尔泽帕肽同时针对GIPR和GLP-1R,实现了前所未有的血糖控制和体重减轻(1)。与GLP-1类似,GIP也是一种对血糖生理控制重要的肠道肽,用长效GIPR激动剂药理激活GIPR也能在人类中产生体重减轻(NCT04586907)。由于GIP和GLP-1通过不同的受体发挥互补作用,同时激活两个受体提供了最大化代谢益处的机会,超越了仅针对一个受体的做法。临床开发中的其他GLP-1药物包括那些与GIPR拮抗剂、胰高血糖素受体或GLP-2R激动剂、或淀粉样肽受体激动剂结合的药物。目标是在保留或理想情况下增强当前GLP-1R激动剂的心脏肾脏和肝脏作用的同时,实现更大的体重减轻。这些新药物通常设计为用于肠胃外给药的肽,在某些情况下,开发为口服给药的小分子或肽制剂。
这些新兴组合如何改善2型糖尿病或肥胖症患者的预后,他们有发展心血管疾病、肾脏、肝脏或神经退行性疾病的风险?胰高血糖素、GIP和淀粉样肽的受体都在中枢神经系统内表达,但相对于GLP-1R激动剂而言,它们在神经保护方面的潜力了解得还很少。这些受体在人心中表达不高,它们改变GLP-1介导的心脏保护的可能性还没有被仔细审查。胰高血糖素受体在肝细胞和肾细胞中表达,现有数据表明胰高血糖素受体激活可能会带来额外的好处,或许能减少代谢性肝病和糖尿病肾病的发生率,超出仅用GLP-1可能达到的效果。尽管一种短效淀粉样肽类似物普兰林肽已在美国获批用于治疗糖尿病19年,但淀粉样肽受体主要在神经系统中表达,且没有确切的研究检查淀粉样肽受体激动剂是否改善长期健康结果。GLP-2类似物特度鲁肽已被用于治疗肠道衰竭十多年,GLP-2R激动剂可能改善肠道屏障功能并减少肝脏炎症。然而,对于2型糖尿病或肥胖症患者单独或与GLP-1R激动剂联合使用GLP-2R激动剂的临床经验有限。
GLP-1创新的首章集中在血糖控制上,后来是减重。随后的浪潮很可能会改善患有多种慢性疾病的患者的健康结果。数十种新分子正在临床中进行检验,其中一些可能会针对新的机制并在多种疾病中实现更大的益处,而不仅仅是更有效的血糖控制和减重。正在进行广泛的临床试验,其结果很可能支持扩大受益于GLP-1疗法的临床指示范围。因此,在GLP-1临床用于2型糖尿病近二十年和第一种GLP-1药物利拉鲁肽获批用于治疗肥胖症患者的减肥十年后,下一个十年可能会带来更大的进步,引入更强大的GLP-1药物同时扩大GLP-1治疗药物的用途,超越目前已确立的心脏代谢疾病。
转载本文请联系原作者获取授权,同时请注明本文来自孙学军科学网博客。
链接地址:https://wap.sciencenet.cn/blog-41174-1442879.html?mobile=1
收藏

