对抗生素耐药的致病细菌的出现通常归因于人和牲畜过度使用抗生素。但研究人员已经锁定了耐药性的另一个潜在驱动因素:抗抑郁药。通过研究实验室中生长的细菌,一个研究小组现在已经追踪了抗抑郁药如何引发耐药性。
“即使在接触几天后,细菌也会产生耐药性,不仅针对一种抗生素,而且针对多种抗生素,”资深作者Jianhua Guo说,他在澳大利亚布里斯班昆士兰大学水与环境生物技术中心工作。他说,这既有趣又可怕。
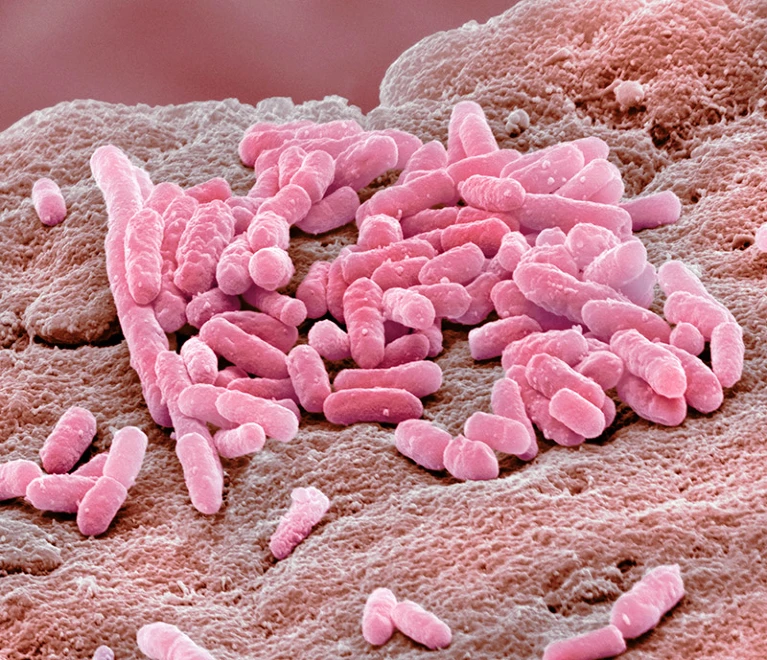
Antidepressants can induce mutation and enhance persistence toward multiple antibiotics | PNAS
Wang, Y. et al. Proc. Natl Acad. Sci. USA 120, e2208344120 (2023).
在全球范围内,抗生素耐药性是一个重大的公共卫生威胁。据估计,2019年有120万人直接死于此,预计这个数字还会攀升。
郭在2014年对非抗生素药物对抗生素耐药性的可能贡献产生了兴趣,因为他的实验室发现,家庭废水样本中循环的抗生素抗性基因比医院废水样本中更多的抗生素耐药基因,抗生素使用率更高。
郭的小组和其他团队还观察到,抗抑郁药 - 这是世界上最广泛的处方药之一 - 杀死或阻碍某些细菌的生长。郭解释说,它们引发“SOS反应”,触发细胞防御机制,从而使细菌更好地在随后的抗生素治疗中存活下来。
在2018年的一篇论文中,该小组报告说,大肠杆菌在暴露于氟西汀后对多种抗生素产生耐药性3,通常作为百忧解出售。最新的研究检查了来自6类此类药物的5种其他抗抑郁药和13种抗生素,并调查了大肠杆菌耐药性的发展情况。
在含氧良好的实验室条件下生长的细菌中,抗抑郁药使细胞产生活性氧:激活微生物防御机制的有毒分子。最突出的是,抗抑郁药通过使细菌产生活性氧激活了细菌的外排泵系统,这是一种通用的排出系统,许多细菌用它来消除各种分子,包括抗生素。这可能解释了细菌如何在没有特定抗性基因的情况下承受抗生素。
但大肠杆菌暴露于抗抑郁药也导致微生物突变率增加,以及随后各种抗性基因的选择。尽管在厌氧条件下生长的细菌中,活性氧水平要低得多,抗生素耐药性的发展要慢得多。
此外,至少一种抗抑郁药舍曲林促进了细菌细胞之间的基因转移,这一过程可以加速耐药性在人群中的传播。这种转移可能发生在不同类型的细菌之间,允许物种之间的抗性 - 包括从无害细菌到致病细菌。
英国剑桥大学研究微生物组-化学相互作用的Kiran Patil说,在过去五年中,人们越来越认识到,许多针对人体细胞的非抗生素药物也会影响细菌并导致抗生素耐药性。“这项研究的优势在于机制比较深入,”帕蒂尔说。
德国蒂宾根大学研究药物与微生物组之间相互作用的Lisa Maier说,要了解抗抑郁药如何驱动抗生素耐药性,研究人员需要确定药物在细菌中靶向的分子,并评估药物对更多临床相关细菌物种的影响。2018年,Maier和她的同事调查了835种不针对微生物的药物,发现24%抑制了至少一种人类肠道细菌的生长。4.
帕蒂尔和迈尔说,重要的是要收集证据来评估抗抑郁药对耐药性的真实影响,例如抗抑郁药是否正在推动抗生素耐药细菌的积累,特别是致病细菌,在人,动物或环境中。
尽管在废水中发现了大量的抗抑郁药,但报告的水平往往低于郭的小组在大肠杆菌中观察到显着影响的浓度。但是,在这项研究中具有强烈作用的一些抗抑郁药的浓度预计将在服用药物的人的大肠中达到。
Maier说,现在有几项研究将抗抑郁药和其他非抗生素药物与细菌的变化联系起来,初步研究已经给出了关于这些药物如何影响服用它们的人的微生物组的“初步提示”。
但是在健康的人类中,大肠杆菌主要存在于大肠中,那里的条件是厌氧的,这意味着论文中描述的过程可能不会以相同的速度在人身上发生,Maier说。未来的研究应该使用细菌生长条件来模拟抗抑郁药可能起作用的部位,Patil说。
郭说,他的实验室现在正在研究服用抗抑郁药的小鼠的微生物组。早期未发表的数据表明,这些药物可以改变动物的肠道微生物群并促进基因转移。
但郭和迈尔在这项研究的基础上警告人们不要停止服用抗抑郁药。“如果你有抑郁症,需要以最好的方式治疗。然后,细菌其次,“Maier说。
尽管研究人员和制药公司需要量化非抗生素药物对抗生素耐药性的贡献,但郭说。“非抗生素药物是一个我们不应该忽视的大问题,”他说。
转载本文请联系原作者获取授权,同时请注明本文来自孙学军科学网博客。
链接地址:https://wap.sciencenet.cn/blog-41174-1373307.html?mobile=1
收藏

