博文
盘点! 2025 年度∶ 那些 [666] 的科研大事 & 热点研究_MCE 中国
|
2025 年,生物医药领域迎来了一个高度密集的突破之年。基础研究持续"出圈",前沿技术加速走向临床,多个曾被认为"难以转化"的方向实现了实质性落地。
从诺贝尔奖聚焦免疫耐受,到基因编辑婴儿"定制治疗";从干细胞药物首次在中国获批,到异种移植刷新存活纪录;这一年,生物医药的底层逻辑正在发生清晰而深刻的变化。本文系统梳理 2025 年度生物医药领域的热点课题与科研大事记,以期呈现这一年真正值得被记录的科学进展!
Section.01
2025 年度:
生物医药风向标
诺贝尔生理学或医学奖
2025 年诺贝尔生理学或医学奖,颁给了调节性 T 细胞 (Regulatory T cells, Treg) 及免疫耐受机制的奠基性研究。这项研究回答了一个看似简单、却困扰医学数十年的问题:为什么免疫系统能攻击病原体,却通常不会"误伤"自己?科学家发现,Treg 并不是"被动存在",而是通过一整套精细的分子与细胞机制,主动抑制过度免疫反应,维持机体内环境稳定。这一发现的意义远不止基础研究:- 为自身免疫病 (类风湿关节炎、系统性红斑狼疮等) 提供理论根基
- 为器官移植免疫耐受提供新思路
- 也为肿瘤免疫治疗中"疗效与副作用的平衡"提供了关键解释
 图 1. 2025 年诺贝尔生理学或医学奖[1]。
图 1. 2025 年诺贝尔生理学或医学奖[1]。
国际医学大奖
如果说早期的精准医学更多停留在"概念提出"和"个案成功",那么 2025 年,一系列国际医学大奖所表彰的成果,则清晰地标志着—精准医学已经进入“长期、可重复、可验证”的成熟阶段。2025 年,多项国际权威医学奖项 (如 Lasker 系列奖项、国际临床医学奖等) 不再单纯奖励技术本身,而是将焦点放在一个核心问题上:这种精准干预,是否真正、持续地改变了患者的疾病进程?以囊性纤维化 (Cystic Fibrosis, CF) 为代表的研究成果,成为精准医学长期验证的典型范例。该疾病由 CFTR 基因突变导致,过去治疗只能缓解症状,无法改变疾病自然史。获奖研究团队从突变蛋白的折叠、转运与功能缺陷机制出发,开发出靶向不同突变类型的联合小分子治疗策略[2]。关键不在于"药物是否新",而在于:- 治疗效果在多年随访中持续存在;
- 患者肺功能、营养状态和生存期显著改善;
- 疾病从"致死性慢性病"转变为"可长期管理的疾病"。
这类成果,被国际医学界视为精准医学从成功案例走向标准范式的标志。
中国两院院士增选 (生物医药领域)
2025 年中国两院院士增选于 11 月 21 日公布结果,生物医药领域共 21 人当选,其中中国科学院生命科学和医学学部 13 人,成果覆盖自身免疫病、肿瘤、器官移植等领域,推动多项临床指南更新与技术转化;中国工程院医药卫生学部 8 人,聚焦 "卡脖子" 技术与临床转化,如徐瑞华牵头国产创新药临床研究,间接产生超百亿元价值。Section.02
基础研究热点
免疫调控与耐受机制
2025 年诺贝尔生理学或医学奖聚焦调节性 T 细胞 (Treg) 及 Foxp3 基因,系统阐明了外周免疫耐受的分子与细胞机制。这一成果回答了免疫学长期悬而未决的核心问题——免疫系统如何在防御外敌的同时避免攻击自身组织。该理论框架直接推动了自身免疫病、肿瘤免疫、器官移植等领域 50 余项临床试验的开展,成为近年来免疫医学最重要的基础突破之一。临床转化进展:- Treg 细胞疗法在 1 型糖尿病治疗中显示出长期效果,部分患者 12 年无需胰岛素治疗[3];
- 在 IPEX 综合征等罕见免疫疾病 中,基于 Treg 的治疗策略取得突破性疗效[4]。
免疫耐受研究,正从"机制阐释"迈向"治疗范式"。 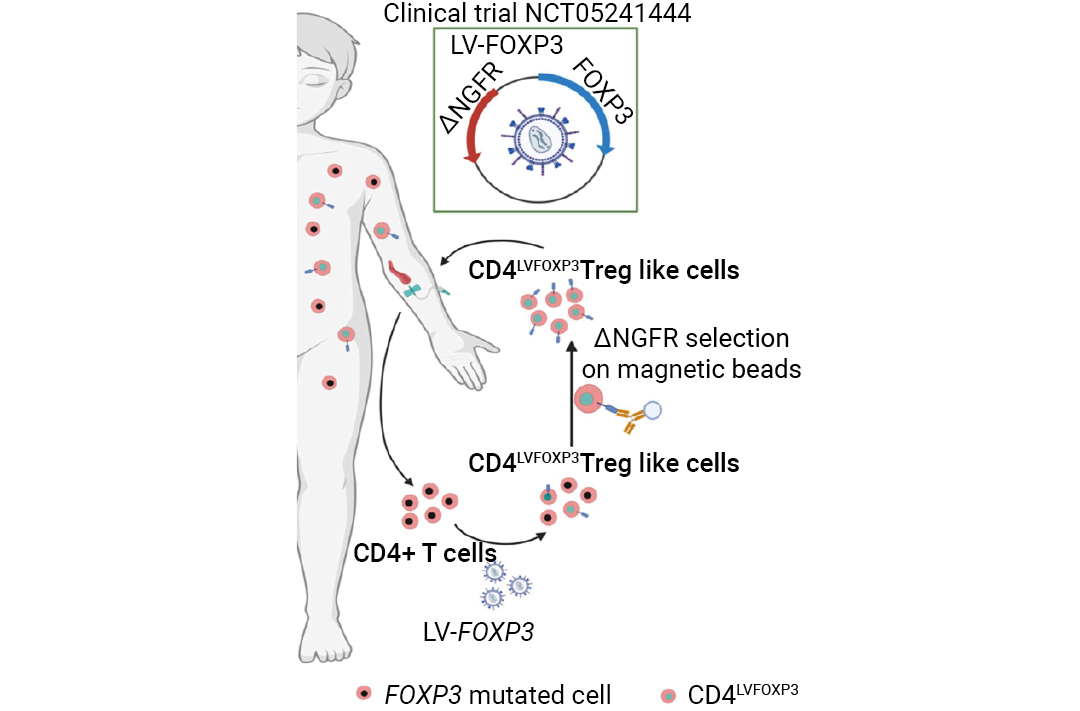 图 2. 自体慢病毒载体 LVFOXP3 CD4 T 细胞用于 IPEX 综合征的治疗[4]。
图 2. 自体慢病毒载体 LVFOXP3 CD4 T 细胞用于 IPEX 综合征的治疗[4]。
基因编辑技术升级
『体内精准编辑取得关键突破』
2025 年,基因编辑在体内应用的“尺寸瓶颈”被突破,实现 12.7 kb 外源 DNA 片段的"无疤痕精准插入",为严重心力衰竭等复杂疾病提供了新的治疗思路[5]。『罕见病治疗的里程碑案例』
美国费城儿童医院为一名 CPS1 缺乏症婴儿定制 CRISPR 碱基编辑疗法,仅 3 次输注 即使患儿摆脱生命危险并恢复正常饮食,成为"按患者定制基因治疗"的标志性事件[6]。『中国进展』
中国空军军医大学西京医院团队在陕西西安完成了亚洲首例基因编辑猪肾脏移植到终末期肾病患者的手术,这是全球第 5 例相关临床探索。术后移植肾开始发挥功能,患者血肌酐水平迅速恢复正常。2025 年 9 月官方报道显示,该移植猪肾在患者体内已正常工作超过 200 天,创造了亚洲异种肾移植存活时间的新纪录,这证明了移植器官的长期稳定性意义重大[7]。肿瘤疫苗与免疫治疗
『mRNA 个性化肿瘤疫苗』
BNT122 mRNA 个性化疫苗用于胰腺癌术后患者:
8 例免疫应答者 18 个月内无复发;随访 3.2 年,仍有 6 例患者保持无复发生存。这一结果为长期被视为“免疫冷肿瘤”的胰腺癌带来新的治疗希望[8]。
『冷肿瘤联合策略』
针对胰腺癌、卵巢癌等免疫反应弱的肿瘤类型,疫苗 + 免疫治疗的联合策略正在逐步激活抗肿瘤免疫反应,成为重要研究方向。『产业层面标志性事件』
三生制药 PD-1/VEGF 双抗授权辉瑞:首付款 12.5 亿美元 + 总里程碑金额 48 亿美元,刷新了中国创新药对外授权纪录,彰显了中国在肿瘤免疫领域的全球竞争力。干细胞与再生医学
『中国干细胞药物实现“零的突破”』
2025 年 6 月,中国首个干细胞药物—"艾米迈托赛注射液"开出首张处方,标志着干细胞治疗正式进入规范化临床应用阶段。『iPSC 临床转化里程碑』
京都大学公布全球首例 iPSC 衍生多巴胺能神经细胞移植治疗帕金森病的 2 年随访结果:未出现严重安全性问题;运动症状持续改善[9]。『脑修复领域进展』
干细胞移植在中风后脑损伤修复中显示出促进神经元再生、改善运动功能的潜力,为神经系统疾病治疗提供新路径[10]。异种移植与器官替代
『猪器官移植刷新纪录』
美国-基因编辑猪肾移植存活近 9 个月;中国-"四川造"基因编辑猪肾稳定工作 261 天。异种移植正逐步从"概念验证"迈向"长期功能维持"。『免疫保护装置突破』
Sernova 开发的细胞袋血管化入口系统,通过在皮下构建高度集成的组织室,显着提升了移植胰岛细胞的重症监护与功能。最新的临床数据显示,在该装置配合免疫抑制治疗的支持下,已有 1 型糖尿病患者实现了超过 4 年的分离胰岛素自主状态,为糖尿病的功能性治愈提供了新的途径[11]。AI 赋能生物医药
『蛋白质设计突破』
AI 成功设计全球首例跨膜荧光激活蛋白,为药物靶点发现和分子工具开发打开新空间[12]。『染色体层级操控』
实现精准染色体编辑,显著加速疾病模型构建与基因治疗策略开发。『药物研发提速』
AI 在化合物活性预测、临床试验设计优化等方面,缩短研发周期 30%–50%,正在改变药物研发的底层逻辑。 图 3. tmFAP 结构模型艺术图[12]。
图 3. tmFAP 结构模型艺术图[12]。 Section.03
小结
2025,生物学再次证明:生命的边界,不是用来遵守,而是用来打破的。如今,我们迎来了 2026,值此十五五规划之年,生物医药的未来一定更加激动人心!产品推荐干扰素基因刺激物的激活剂 (STING),具有有效的抗肿瘤和免疫活性。
PD-1/PD-L1 免疫检查点抑制剂,拮抗 PD-1/PD-L1 免疫检查点对 T 细胞活化的抑制作用。
免疫检查点蛋白 VISTA 激动剂,可减少 VISTA 诱导的细胞因子的分泌,促进 VISTA 诱导的 T 细胞增殖,并表现出免疫调节活性。
GPR65 正向变构调节剂,可以诱导 GPR65 依赖性 cAMP 产生,具有用于自身免疫和炎症疾病研究的潜力。
口服活性的、选择性的、不可逆的共价 BTK 抑制剂,可用于癌症和自身免疫性疾病的研究。
收录了 1,781 个表观遗传相关的产品,可以用于表观遗传学及相关疾病研究。
参考文献[1] Nobel Prize in Physiology or Medicine 2025. NobelPrize.org. Nobel Prize Outreach 2026. Mon. 9 Feb 2026.
[2] Friedman JM. Cystic fibrosis: Correction of a fatal disease. Proc Natl Acad Sci U S A. 2025 Sep 16;122(37):e2519780122.
[3] Albert H. Tackling Autoimmune Disease with Cell and Gene Therapy. Inside Precision Medicine. 2025;12(2):36-41.
[4] Jessie Alexander, et al. Autologous Lentiviral Vector LVFOXP3 CD4 T Cells for IPEX Syndrome. J Hum Immun 25 April 2025; 1 (CIS2025): CIS2025abstract.27.
[5] Wang Y, et al. Synthetic rewriting technologies in mammalian cells. Nat Commun. 2026 Jan 13.
[6] Musunuru K, et al. Patient-Specific In Vivo Gene Editing to Treat a Rare Genetic Disease. N Engl J Med. 2025 Jun 12;392(22):2235-2243.
[7] China Daily Online. (2025, September 24). Breakthrough beyond 200 days! Xijing Hospital’s xenogeneic kidney transplant resets Asia survival record.
[8] Sethna Z, et al. RNA neoantigen vaccines prime long-lived CD8+ T cells in pancreatic cancer. Nature. 2025 Mar;639(8056):1042-1051.
[9] Sawamoto N, et al. Phase I/II trial of iPS-cell-derived dopaminergic cells for Parkinson's disease. Nature. 2025 May;641(8064):971-977.
[10] Weber RZ, et al. Neural xenografts contribute to long-term recovery in stroke via molecular graft-host crosstalk. Nat Commun. 2025 Sep 16;16(1):8224.
[11] Sernova Corp. A Safety, Tolerability and Efficacy Study of Sernova’s Cell Pouch? for Clinical Islet Transplantation. ClinicalTrials.gov. NCT03513939. Updated January 6, 2025. Accessed January 30, 2026.
[12] Zhu J, et al. De novo design of transmembrane fluorescence-activating proteins. Nature. 2025 Apr;640(8057):249-257.
https://wap.sciencenet.cn/blog-3536222-1529623.html
上一篇: Nature 子刊 | IsoNet:基于稳定同位素示踪代谢组学技术开发的新策略 _ MCE中国
下一篇:您的国自然申报 ai药物筛选「神助攻」已上线_MCE 中国