初稿 | 殷晓航 屈若颖
小编注 | 殷晓航 屈若颖
校对 | 张婷
排版 | 屈若颖
编辑 | 孟美瑶

背景介绍
生物体会根据环境变化寻找最优能量底物,并调整自身代谢需求。在食物供应有限的条件下,外周代谢器官的代谢方式会逐渐从利用葡萄糖和碳水化合物转变为燃烧脂肪(游离脂肪酸,FAO),同时储存葡萄糖供大脑使用,这一过程被称为能量底物转换。在慢性冷适应过程中,棕色脂肪会将能量底物从葡萄糖转换为脂肪酸,以维持机体温度。这一代谢过程对于机体抵御环境应激和维持长期代谢健康十分重要。反之,在病理条件下(如心力衰竭),心脏会更依赖于葡萄糖代谢。这些过程体现了能量底物选择在健康和疾病状态下的灵活性。目前,机体响应内外信号而发生能量转换的分子机制仍不明确。
左旋肉碱(L-肉碱)是一类关键代谢物,可介导长链脂肪酸进入线粒体发生脂肪酸氧化作用。机体中肉碱的来源主要有两种:一种是从食物中获取,另一种是内源性生物合成途径。肉类含有大量的肉碱,而大多数水果和蔬菜中肉碱含量非常少。除此之外,肝脏也可利用前体N6,N6,N6-三甲基赖氨酸(TML)合成肉碱。因此这一从头合成通路对严格素食者、纯素食者和食草动物而言十分重要。肉碱的生物合成始于将TML转运至线粒体基质中。TML是一种来源于膳食或蛋白质降解的前体物质。在线粒体基质中,ε-三甲基赖氨酸羟化酶(TMLHE)催化TML转化为3-羟基-6-N-三甲基赖氨酸(HTML),随后经历连续的酶促反应:3-羟基-6-N-三甲基赖氨酸醛缩酶(HTMLA)将其转化为4-N-三甲基氨基丁醛(TMABA),后者再经4-N-三甲基氨基丁醛脱氢酶(ALDH9A1)氧化生成γ-丁酰甜菜碱(γ-BB)。最终,γ-丁酰甜菜碱双加氧酶(BBOX1,又称γ-丁酰甜菜碱羟化酶)催化L-肉碱的合成(图1A)。该过程需要TML跨越线粒体内膜(IMM)进行转运,而该膜对代谢产物具有不通透性,说明这一步骤可能需要载体蛋白参与,但目前具体的载体蛋白转运机制仍不可知。
本研究中,研究人员确定SLC25A45蛋白为一种线粒体中的TML载体,它控制着肉碱的合成和能量转换。SLC25A45敲除会减少肉碱积累量,并损害线粒体脂肪酸氧化,使其对碳水化合物代谢的依赖增加。Slc25a45基因敲除小鼠对寒冷不耐受,并且对胰高血糖素样肽-1 受体激动剂(GLP-1RA)诱导的脂质动员具有抵抗性(即它们不会因这种治疗而出现脂肪组织流失)。综上所述,线粒体在能量转换的调节过程中起着关键作用,与代谢适应以及基于GLP-1RA的抗肥胖疗法的疗效有关。

敲黑板啦!
1.线粒体转运蛋白 SLC25A45 是介导三甲基赖氨酸(TML)进入线粒体、调控肉碱从头合成的关键分子
2.在冷适应等应激状态下,SLC25A45介导的肉碱合成途径是机体完成糖代谢向脂肪酸氧化转换的核心调控环节
3.肉碱合成能力是 GLP 1 受体激动剂介导脂肪动员所必需的
研究结果
1. SLC25A45是肉碱从头合成过程中的必需成分
通过对来自6136名芬兰志愿者的代谢物全基因组关联研究(GWAS-METSIM)分析显示,TML与SLC25A45基因位点之间存在高度显著的相关性(P = 1×1.9-80)(图S1A)。此外,公共代谢性疾病知识门户网站(https://hugeamp.org)中的数据显示SLC25A45基因的变异与血清肌酐浓度[人类遗传证据(HuGE)评分,121,800]以及基于肌酐的估算肾小球滤过率(eGFR)(小编注:血清肌酐是肌肉代谢终产物,主要通过肾脏滤过排出,是评价肾小球滤过功能的指标之一。反映估算肾小球滤过率(eGFR)是通过公式推算出,用于评估肾脏过滤血液能力的关键数值。肌酐水平升高和eGFR降低,均反映出肾功能受损。肾脏是能量消耗最为高的器官之一,肾近端管细胞拥有大量线粒体。在线粒体功能受损引起的多种病理机制中,缺陷脂肪酸氧化(FAO)可能是导致糖尿病肾病(DKD)发展的因素之一。而肉碱是脂肪酸氧化、能量代谢的关键分子。因此SLC25A45基因功能异常会影响体内代谢,而这种代谢紊乱很可能源于TML 转运受阻、L - 肉碱合成不足,进而通过能量代谢、肾脏血流等途径影响肾功能指标。)(图S1B)。这些数据提示SLC25A45可能参与了TML 的线粒体转运以及体内L-肉碱的合成过程。
SLC25A45在小鼠多种器官和组织中均有表达,如肾脏、肝脏、大脑以及肩胛区的棕色脂肪组织、脾脏和腹股沟的白色脂肪组织(WAT)等,其中在肾脏、大脑和肝脏中的表达量最高,并且这些器官的线粒体具备较强的肉碱合成能力(图1B)。研究人员发现SLC25A45表达量与肉碱代谢相关基因特征(图1C)以及包括 Tmlhe、Aldh9a1、Bbox1和Cpt1a在内的单个基因的表达(图S1C)之间存在显著的正相关(P = 0.0013),而与 SLC25A44(一种线粒体支链氨基酸载体)或 SLC25A47(一种肝脏特异性的线粒体载体)之间并未显示出相关性(图S1D)。
为了验证以上假设,研究人员构建Slc25a45flox/flox小鼠,之后将Slc25a45flox/flox小鼠与CMV-Cre小鼠杂交,得到全身性Slc25a45基因敲除小鼠 [CMV-Cre; Slc25a45flox/flox,即Slc25a45 KO小鼠](图1D-E)。此外,研究人员从Slc25a45flox/flox小鼠的腹股沟白色脂肪组织中获得并永生化了基质血管成分(SVF),通过逆转录病毒 Cre(pMSCV-Cre)或空载体对照病毒感染永生化的SVF细胞,从而构建了SLC25A45 KO细胞和对照细胞(图S1E)。为了探究线粒体对D9-TML (氘代标记的TML)的吸收情况,通过对这些细胞的线粒体进行液相色谱-质谱分析,发现在SLC25A45 KO细胞的线粒体中,D9-TML的摄取量显著低于对照组线粒体(P = 0.0006)(图1F),且肉碱含量减少,说明在缺乏SLC25A45的情况下,肉碱穿梭作用有所减弱(图1G)。同样,在Slc25a45 KO小鼠肝脏中分离出的线粒体中,D9-TML的摄取量也低于野生型对照小鼠(图S1F)。
肝细胞能够表达合成L-肉碱所需要的全部酶类,包括TMLHE、ALDH9A1和BBOX1等(图1A)。研究人员从对照小鼠和Slc25a45 KO小鼠中分离出原代肝细胞,并使用D9标记的TML进行全细胞追踪。代谢组学分析表明,对照小鼠的肝细胞能够以时间依赖的方式生成源自 D9-TML 的左旋肉碱前体——即HTML和γ-BB,以及D9-肉碱(图1H)。比较发现,SLC25A45 KO小鼠的肝细胞所生成的D9-HTML、γ-BB 和肉碱含量比对照组少。以上结果表明线粒体摄取TML和以TML为底物从头合成肉碱的过程,均需要SLC25A45蛋白。然而,虽然SLC25A45 KO细胞合成肉碱的含量下降,但也能产生一定量的肉碱,提示可能存在其他途径参与。结果显示Slc25a29(一种负责运输碱性氨基酸如赖氨酸等的线粒体载体)在SLC25A45 KO小鼠的肝脏中表达量高于对照小鼠。此外,以TML的下游代谢产物γ-BB作为示踪剂时,SLC25A45 KO小鼠的肝细胞能够生成肉碱,提示在SlC25A45 KO细胞中可能存在其他代偿途径产生肉碱。(图S2A-S2B)
为了研究SLC25A45 KO细胞中恢复SLC25A45表达是否能恢复TML转运通路,研究人员利用CRISPR系统在人类胚胎肾细胞293(HEK293)中敲除了SLC25A45基因,并重新插入人类SLC25A45的cDNA序列(即KO + SLC25A45)(图S2C)。随后,使用D9-TML对对照细胞、SLC25A45 KO细胞以及KO + SLC25A45细胞进行了全细胞代谢物追踪。代谢组学分析发现,由于HEK293细胞的内源性SLC25A45表达量较低,因此对照细胞和SLC25A45 KO细胞中差异不显著,而当SLC25A45 KO细胞中重新表达SLC25A45时,细胞中D9- HTML和γ-BB的含量高于KO细胞,且线粒体中的肉碱含量也显著升高(图1I-J),在SLC25A45过表达的HEK293细胞中也出现类似结果(图S2D)。先前研究表明,SLC25A45可能参与运输β-烟酰胺单核苷酸(NMN)。然而,在氚标记的 NMN 作为示踪剂的线粒体摄取实验中,对照细胞、SLC25A45 KO细胞以及KO + SLC25A45细胞的线粒体中NMN含量并无显著差异,这表明NMN可能不是SLC25A45的特定底物(图S2E)。以上结果表明,SLC25A45是细胞中线粒体摄取三甲胺(TML)所必需的,而且它还能促进TML合成L-肉碱的过程。这些结果与近期发表的研究成果相一致,该研究表明SLC25A45是甲基化氨基酸(如二甲基精氨酸和三甲基赖氨酸)进入线粒体以及肉碱合成所必需的。
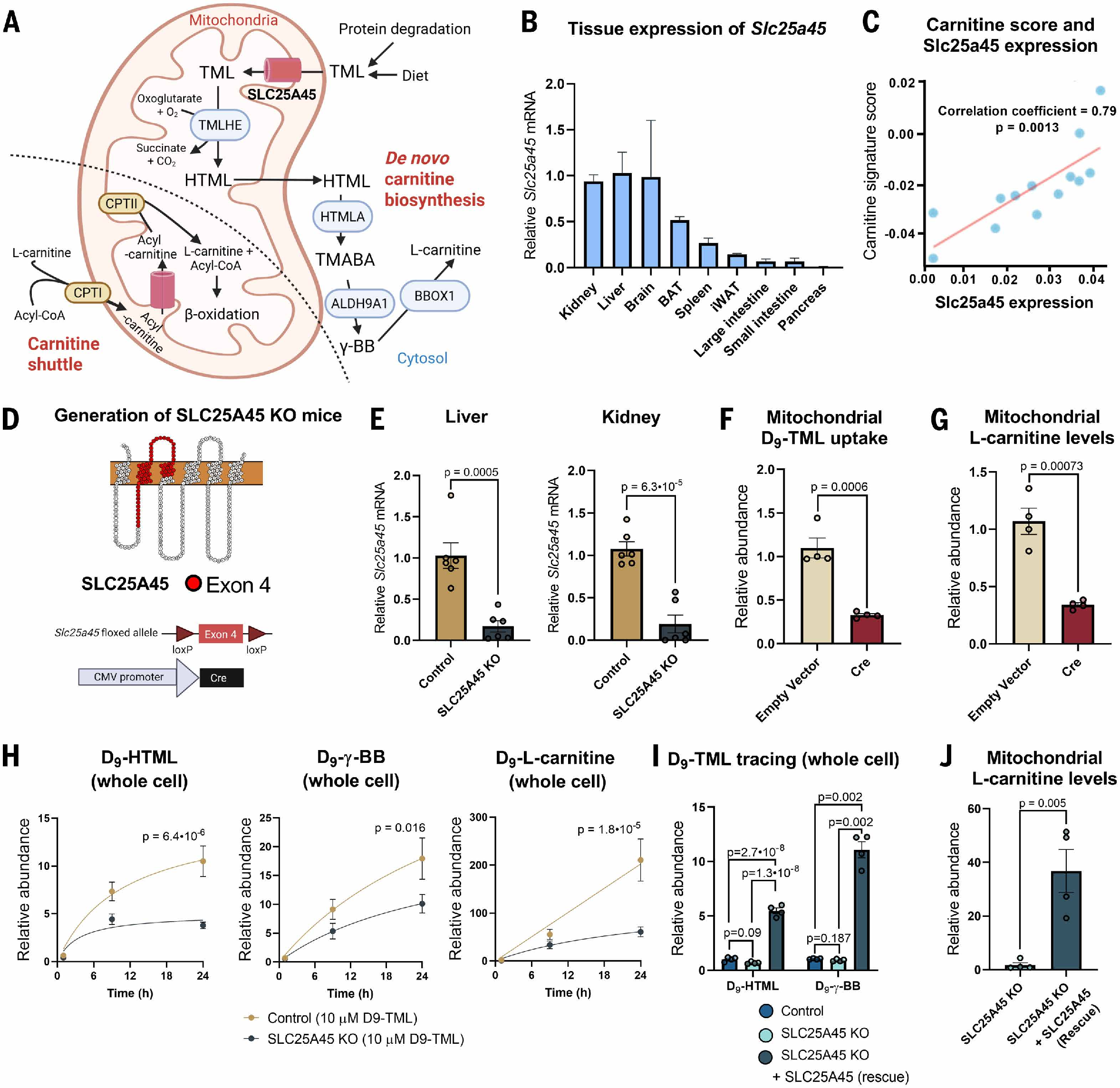
图1.SLC25A45是肉碱合成所必需的
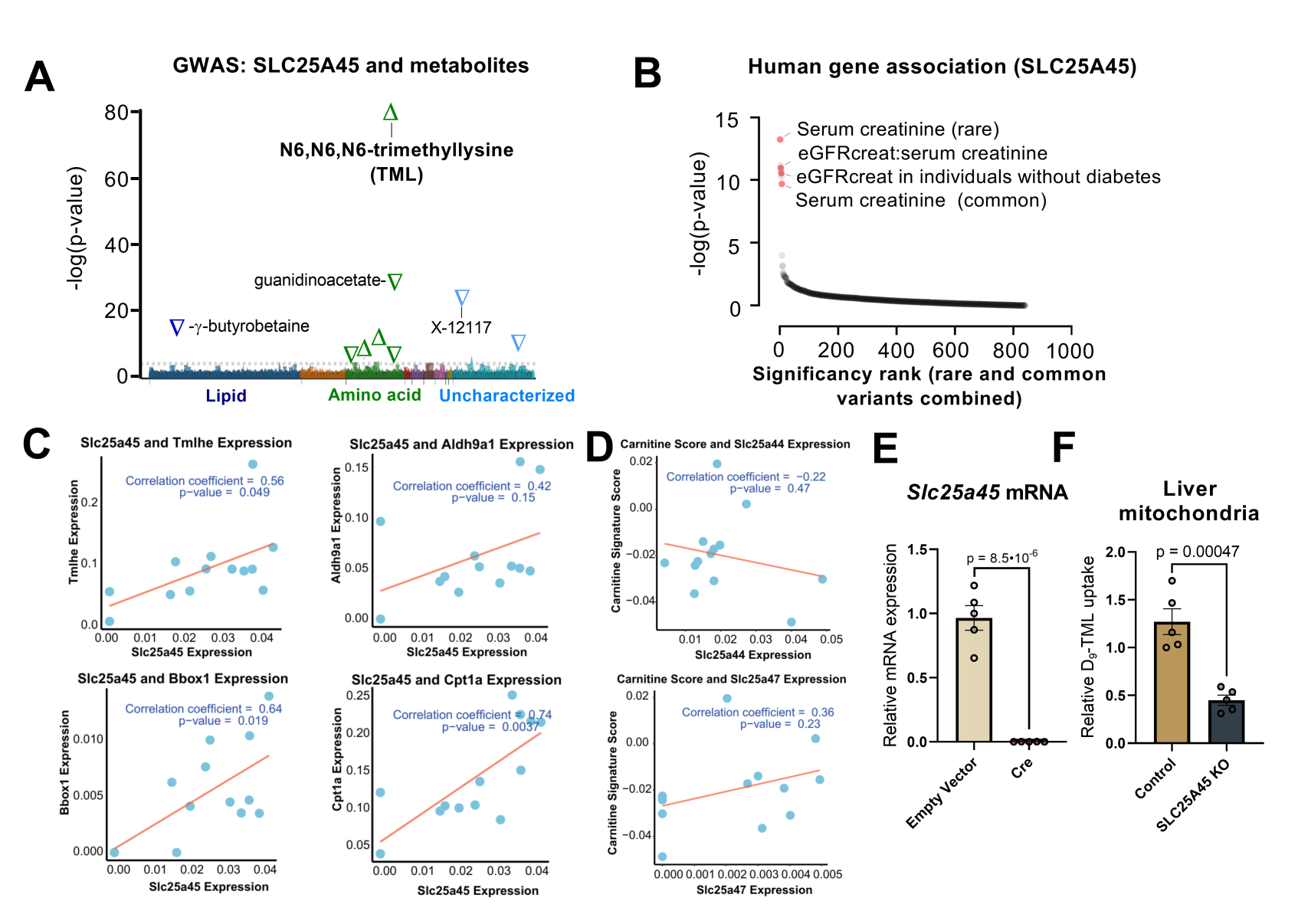
图S1.SLC25A45是三甲基赖氨酸(TML)合成L-肉碱的必需成分
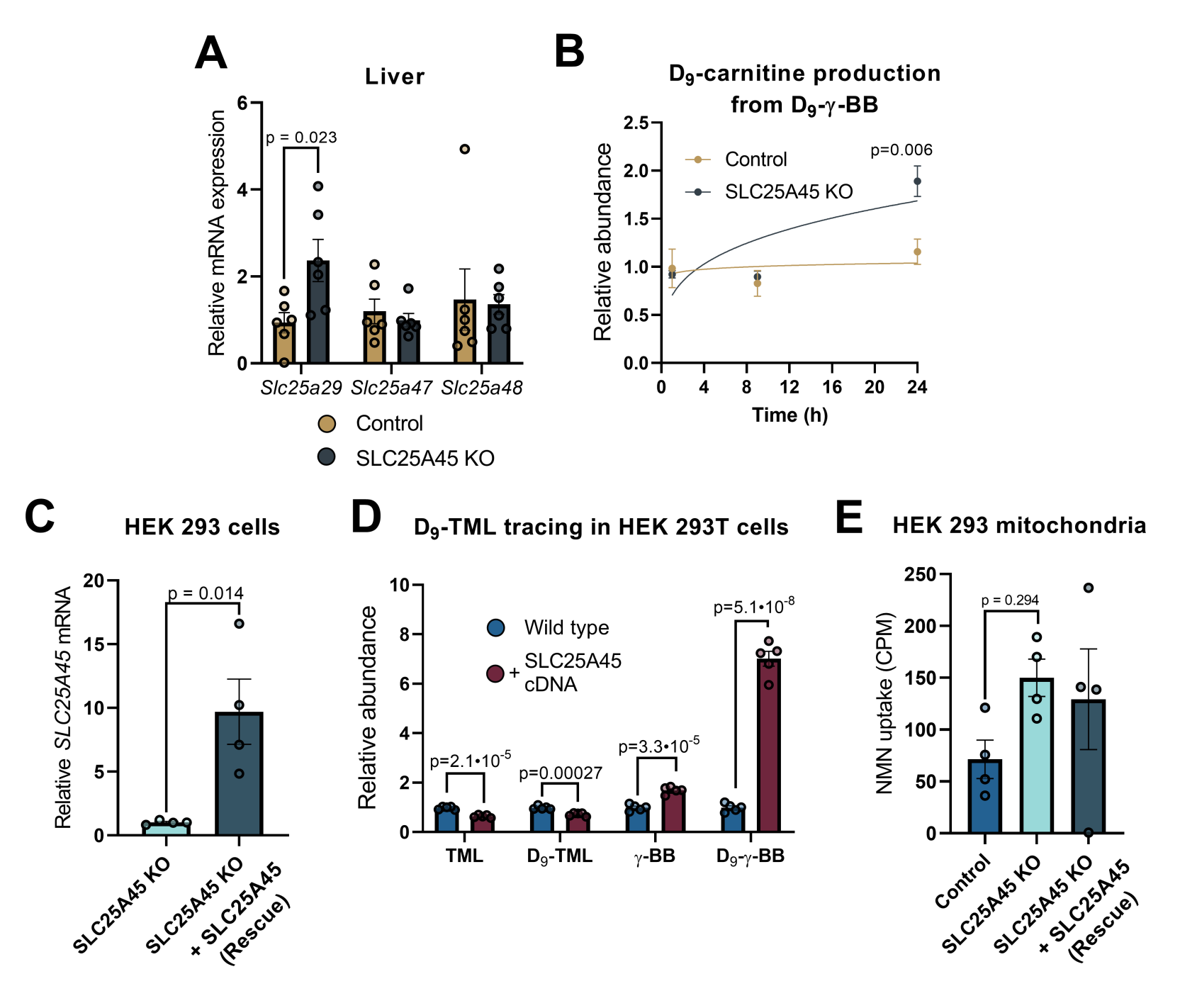
图S2.SLC25A45促进TML合成 L-肉碱
2、SLC25A45可重塑TML转运过程
为了通过SLC25A45重建TML在IMM上的转运过程,研究人员使用了一种大肠杆菌菌株(该菌株能够通过将 IMM 蛋白与麦芽糖结合蛋白(MBP)融合成一个框架的方式,在细菌内膜上有效地表达 IMM 蛋白(小编注:细菌的细胞膜有两层,外膜具有通透性屏障功能,内膜与线粒体内膜在结构和功能上类似,通透性较低,且是进行电子传递和能量转换的场所。)),分别构建了含有空载体和表达MBP-SLC25A45的E. coli(图S3A)。接下来,将这些细胞与D9-TML进行孵育,快速洗涤后通过LC-MS测定其转运活性(小编注:大肠杆菌属于典型的革兰氏阴性菌,其内膜在结构组成、脂质特性及进化起源上,均与线粒体内膜高度同源,契合线粒体载体蛋白的天然定位微环境,可保障目标蛋白实现正确的膜定向插入与生理折叠。其次,大肠杆菌不具备线粒体结构,也没有内源SLC25家族同源转运蛋白,实验背景干净无干扰,能够排除真核体系中其他转运蛋白的代偿作用,实现对SLC25A45独立转运活性的判定。)。研究发现,与对照组相比较,在SLC25A45表达的E. coli中D9-TML的摄取量呈现出时间依赖性的增加趋势,其峰值出现在培养60分钟时(图2A)。接下来,研究人员通过检验SLC25A45是否能够转运结构相似的底物(如γ-乙酰胆碱和胆碱)来评估其底物特异性,发现SLC25A45表达的E. coli中的TML转运量显著高于对照组(P = 0.00013),但γ-胆碱或胆碱摄取量无显著增加(图2B)。
之后,研究人员又探究了SLC25A45选择性地结合并运输TML的作用机制。由于目前SLC25A45蛋白的三维结构没有被解析,因此研究人员通过AlphaFold预测SLC25A45三维结构,并对该结构进行了严格的处理流程,以确保其适合后续的分析方法。该预测结构具有较高可信度评分,并且与其他已知的溶质载体具有相同的结构特征,其中包括由六条垂直于离子通道膜(IMM)方向的跨膜α螺旋所形成的中央通道状空洞(图S3B-C)。该结构展现了朝向细胞质面的构象,中心腔体朝向细胞质溶胶(或膜间隙)敞开,从而使潜在的底物能够进入其中(图2C)。在通道内部的表面存在一些残基:L17、I66、Q113、L117、F120、K124、R173、D174和R268(图2D)。研究人员依次采用共有对接(consensus docking)与诱导契合对接(induced-fit docking)策略,预测能量最优且结构稳定的TML-SLC25A45 复合物。结果显示TML可形成与SLC25A45通道空腔高度契合的构象(图2E)。该结合构象主要通过特异性相互作用得以维持的,如TML中的羧酸根与SLC25A45中的Q113、R173和D174位点的残基之间形成的氢键和/或盐桥;TML的N-三甲基部分与位于凹槽内侧的L17、I66、V69、N70、L73、L117、F120和 K124等残基的侧链之间的疏水相互作用。
随后,为了研究SLC25A45结构在线粒体内膜上的动态变化,研究人员进行了多次分子动力学(MD)模拟,结果表明TML与SLC25A45结合形成了稳定的复合物构象,SLC25A45-TML复合物的均方根偏差(RMSD)平均值为 2.74 Å,显著低于 apo状态(在无TML的基础构象)轨迹所观察到的 3.23 Å(图2G 和S4)。TML-SLC25A45复合物的平均结合自由能[ΔG]为-17.10±3.75kcal/mol,这表明TML与SLC25A45的结合在能量上是有利的(表S1)。同时,在MD模拟中发现TML的羧酸基团与SLC25A55的R268相互作用形成氢键,而TML的N-三甲基部分仍紧密靠近SLC25A55的疏水性残基(图2H和S5A),TML与SLC25A55紧密作用。基于MD的突变分析表明,其中SLC25A55蛋白中一个关键结合口袋的氨基酸(D174E)发生突变,可导致TML与SLC25A45的结合变得不稳定,提示SLC25A55的D174介导了SLC25A45对TML的高度特异性(图S5B)。SLC25A45与SLC25A48具有结构同源性,SLC25A48可将胆碱作为底物运输。胆碱也带有 N-三甲基基团。在SLC25A45-TML复合物中围绕N-三甲基部分的主要疏水残基中,I66和N70是保守的(在SLC25A48中为I69和N73);但是L17、V69、L73、L117和F120不是保守序列(在SLC25A48中为V20、Y72、V76、G121和V124)(图S5C),这可能是SLC25A45可以转运TML但无法转运胆碱的原因。
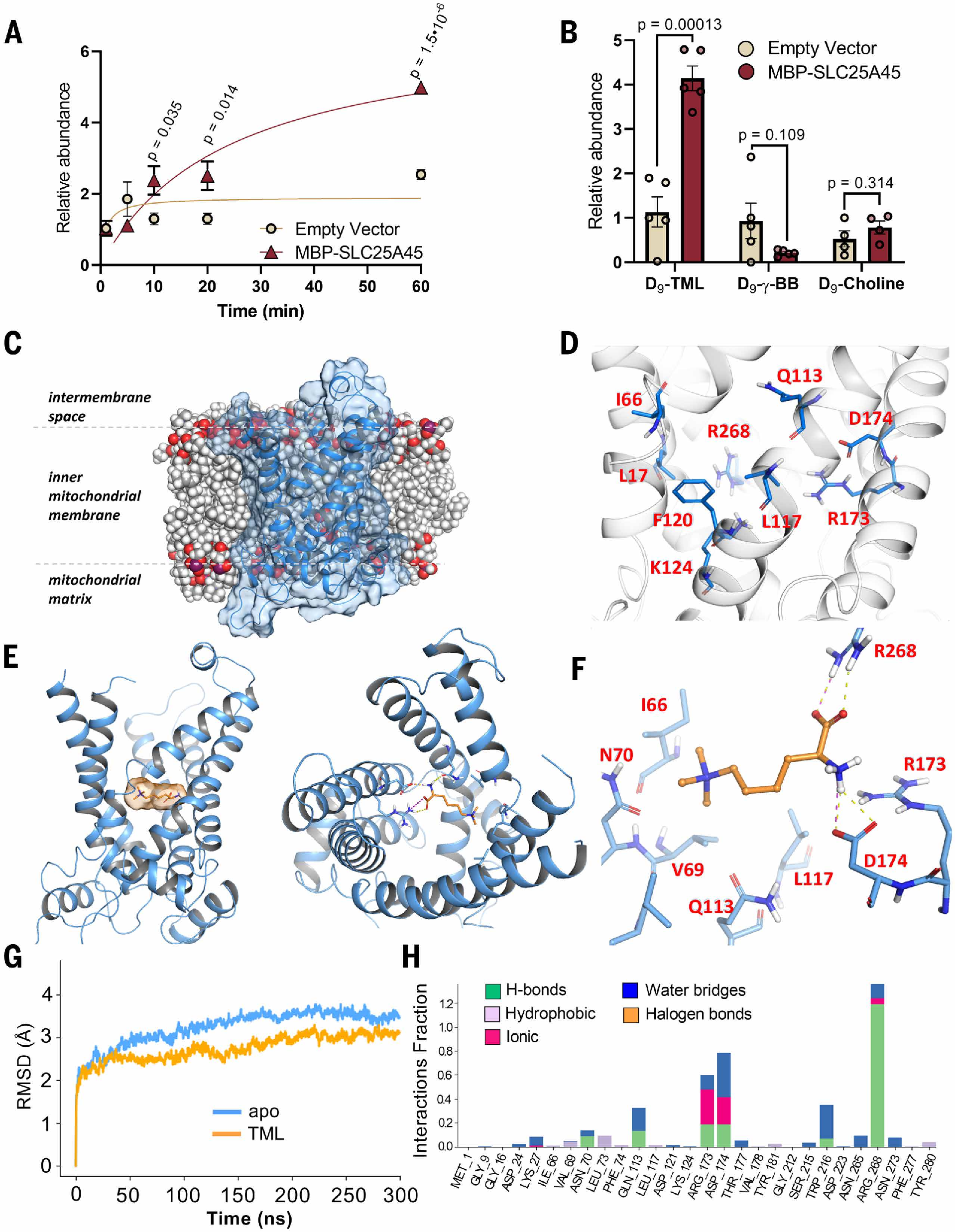
图2.SLC25A45可调控TML的转运
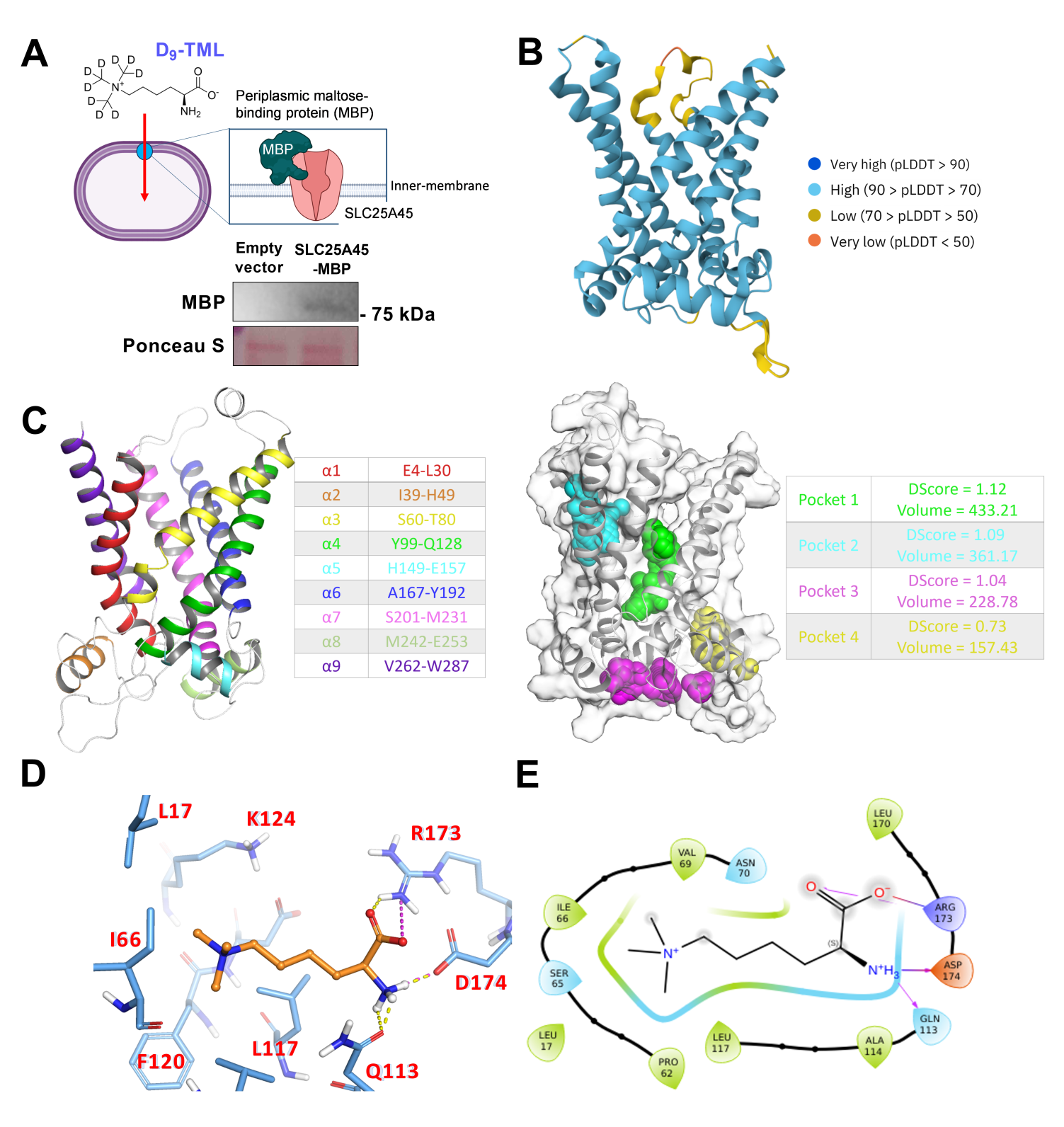
图S3. 线粒体SLC25A45 调控TML转运
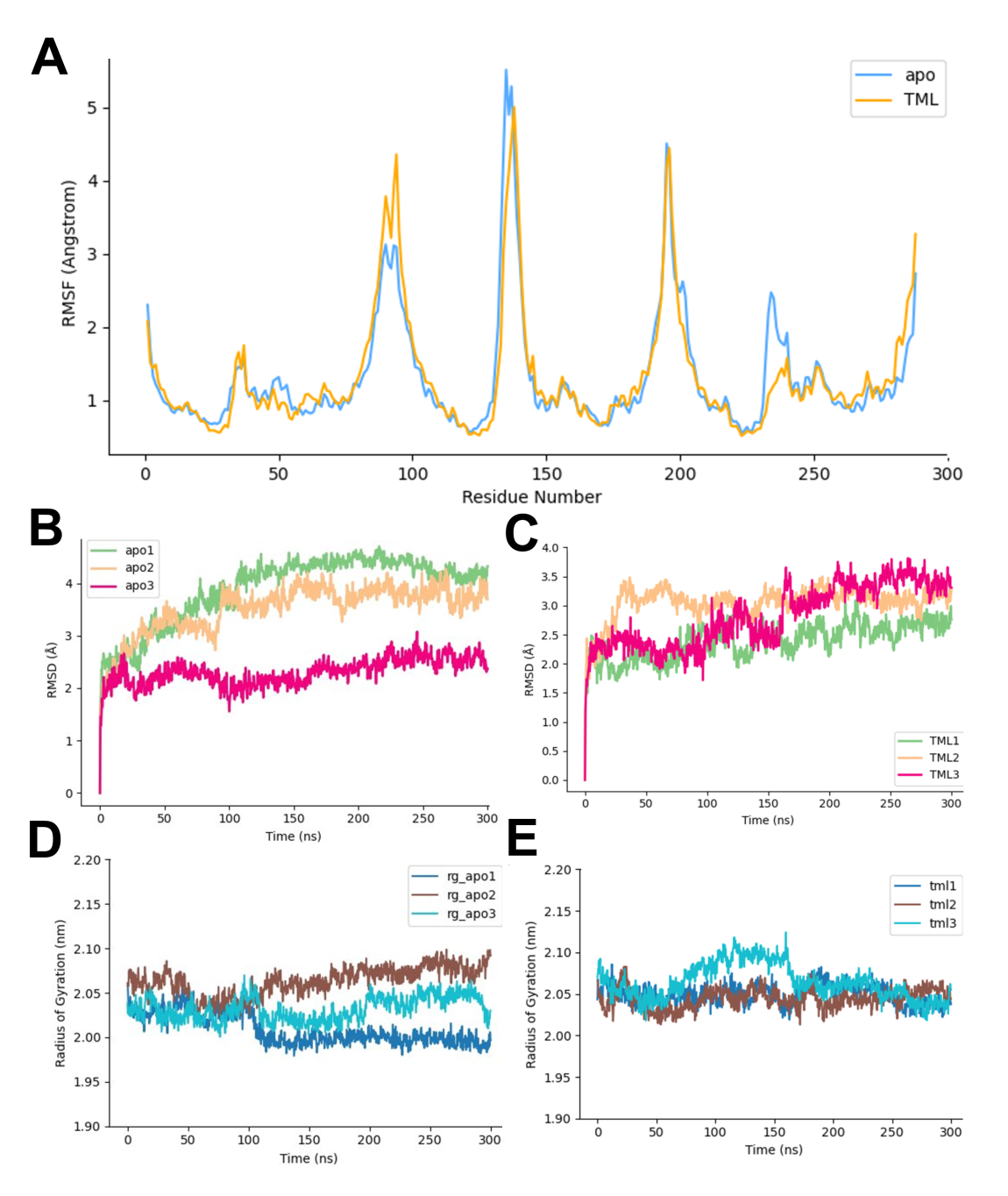
图S4.SLC25A45-TML的分子动力学(MD)模拟分析
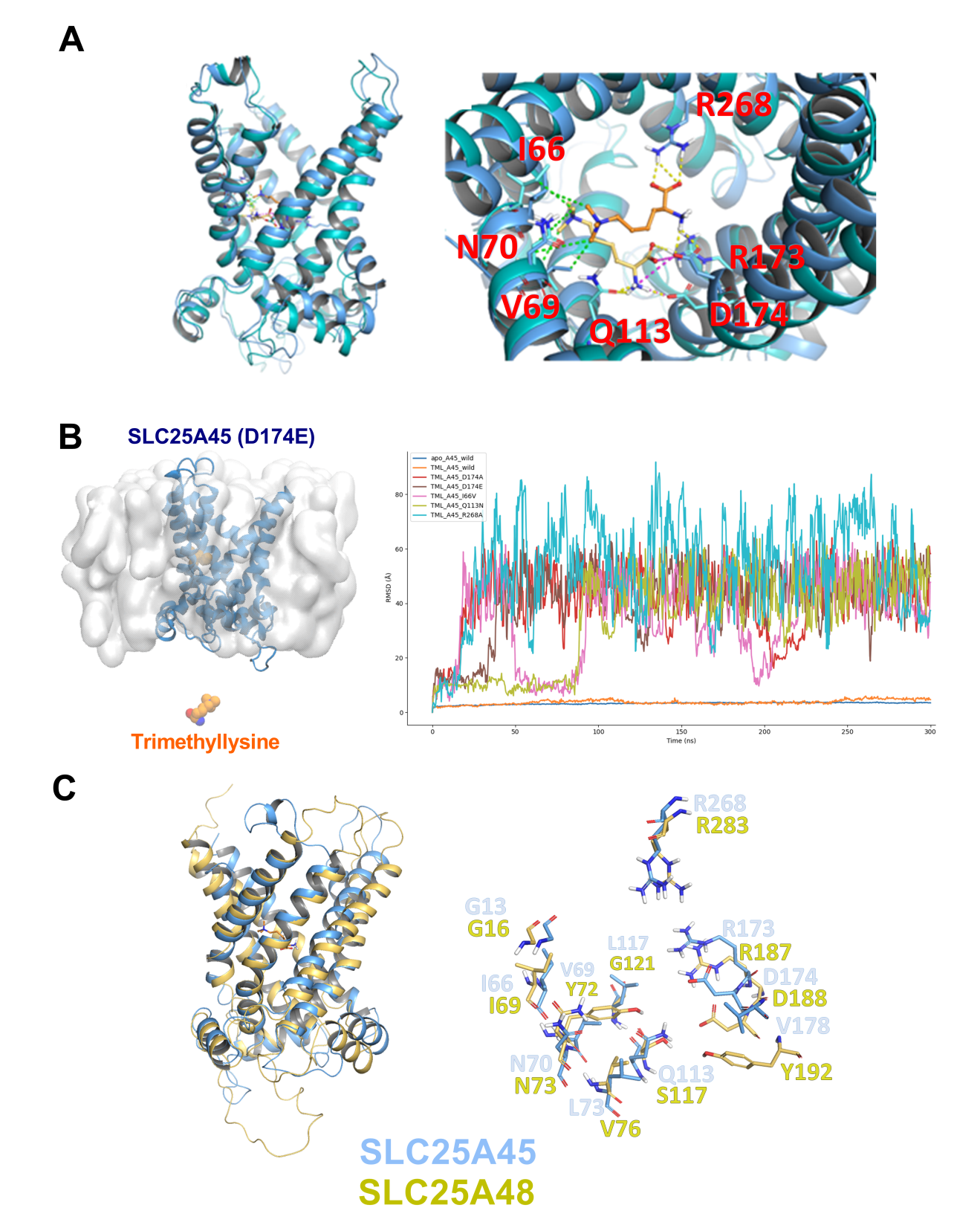
图S5.SLC25A45 底物特异性的结构机制解析

表S1.TML-SLC25A45复合物的平均结合自由能计算
3、SLC25A45的缺失会导致全身性肉碱缺乏,并诱导机体转向依赖碳水化合物代谢
接下来,研究人员在SLC25A45 KO小鼠中研究了SLC25A45对系统性肉碱代谢和脂肪酸氧化的调控程度。结果显示,在SLC25A45 KO小鼠中未观察到明显的发育缺陷,但血清代谢组学结果发现SLC25A45 KO小鼠血清中L-肉碱和γ-BB的含量降低,同时SLC25A45 KO小鼠血清中的L-肉碱前体、L-赖氨酸和TML水平显著升高,这与上文细胞实验结果TML转化为γ-BB和L-肉碱需要SLC25A45这一结果相一致(图3A)。据报道,骨骼肌以及心脏储存了机体超过95%的肉碱。与对照小鼠相比,SLC25A45 KO小鼠骨骼肌和心脏中的肉碱水平显著降低,BAT组织肉碱含量无差异(图3B和S6A)。与原发性肉碱缺乏(如质膜肉碱转运蛋白(如OCTN2)突变)小鼠相比,SLC25A45 KO小鼠肉碱缺乏没那么严重。这可能是由于SLC25A45 KO细胞通过其他来源(如Slc25a29)合成肉碱,因为本研究中使用的常规鼠粮中几乎检测不到肉碱(图S6B)。
全身性肉碱缺乏与多种致病性疾病相关如慢性肾病患者,其血液中肌酐和尿素氮浓度会异常升高。这可能与在人类遗传学研究中发现的SLC25A45基因与血清肌酐水平的相关性有关。与此一致的是,研究人员发现SLC25A45 KO小鼠的肾损伤标志物(包括血清肌酐浓度、血清半霉素C浓度和血尿氮浓度)均显著升高,同时肾脏中甲基二醛(MDA,氧化应激的标志物)水平也显著升高(图3C)。组织学水平检测发现,SLC25A45 KO小鼠肾脏近端小管表现出轻度的细胞质液泡化和细胞核的核固缩(细胞核体积减少、染色质凝聚)(图S7A)。值得注意的是,SLC25A45在小鼠肾脏中表达较高。单核RNA-seq数据发现肾近端小管和集合管的上皮细胞高表达Slc25a45和肉碱合成酶(包括Tmlhe和Aldh9a1)(图S7B)。因此,研究人员构建了肾脏特异性SLC25A45敲除小鼠(Slc25a45KSP KO小鼠)。与对照小鼠相比,Slc25a45KSP KO小鼠肾损伤标志物和循环肉碱水平无显著变化(图S7C-D)。同时,研究人员还构建了肝特异性SLC25A45 KO小鼠(Slc25a45ALB KO小鼠),结果显示Slc25a45ALB KO小鼠和Slc25a45KSP KO小鼠的肝肾组织中的肉碱及其前体的含量均无显著变化(图S7E)。这些数据表明组织特异性缺失SLC25A45不会导致全身性肉碱缺乏。基于此结论,研究人员使用了全身SLC25A45 KO小鼠进行后续研究。
拓展阅读:肉碱代谢和相关疾病
L-肉碱的核心功能是将长链脂肪酸转运进入线粒体内进行β-氧化,长链脂肪酸是心肌、骨骼肌等组织的主要能量来源。它们首先被活化成脂酰辅酶A,然后在肉碱脂酰转移酶1(CPT-1)的催化下,与肉碱结合形成脂酰肉碱,被转运至线粒体基质内,再由肉碱脂酰转移酶2(CPT-2)催化,重新释放出脂酰辅酶A,进入β-氧化,生成ATP。因此,肉碱缺乏时,依赖脂肪酸供能的组织(如心肌、骨骼肌)会出现能量供应不足的问题;肉碱缺乏可分为原发性肉碱缺乏和继发性肉碱缺乏。原发性肉碱缺乏为常染色体隐性遗传病,由SLC22A5基因突变导致OCTN2功能缺陷。患者肾脏重吸收肉碱的能力基本丧失,同时循环中游离肉碱水平极低。其症状为心力衰竭、肌无力、低酮性低血糖等;继发性肉碱缺乏主要存在于严重肝病患者、慢性肾病患者中(尤其是透析患者,肾脏损伤导致肉碱流失。
参考文献:
[1] Ito S, et al. JCI Insight. 2025;10(13):e179362.
[2] McCoin CS, et al. Nat Rev Endocrinol. 2015;11(10):617-625.
[3] Lahrouchi N, et al. Eur J Hum Genet. 2017;25(6):783-787.
接着,研究人员使用间接量热法评估SLC25A45缺失后机体的能量底物变化。结果显示,与对照小鼠相比,SLC25A45 KO小鼠的呼吸交换率(RER)显著升高,尤其是夜间,且SLC25A45 KO小鼠在夜间的耗氧量(VO₂)也显著降低,活动量无显著差异(图3D-F和S7F),这表明SLC25A45 KO小鼠中RER和VO₂的改变并非由活动量或行为改变所引起。相应地,与对照小鼠相比,SLC25A45 KO小鼠的体重和组织重量也没有显著差异(图3G和S7G)。
肉碱缺乏可损害脂肪酸氧化,迫使身体更多依赖碳水化合物代谢,进而导致机体低血糖。禁食状态下,SLC25A45 KO小鼠血糖和酮体β羟丁酸(BHB)浓度显著降低(图4A-B)。此外,与对照小鼠相比,SLC25A45 KO小鼠的葡萄糖清除率显著升高,而胰岛素敏感性无明显变化(图4C, S8A-B)。
为了研究Slc25a45调控机体糖脂代谢转换的分子机制,研究人员对对照小鼠和SLC25A45 KO小鼠的肝脏进行了RNA测序。结果显示,SLC25A45缺失后有1078个基因显著上调,597个基因显著下调。KEGG分析显示,下调基因主要富集在脂肪酸β氧化和肉碱合成,而上调基因主要参与糖酵解和线粒体氧化磷酸化途径(图4D)。此外,在SLC25A45 KO小鼠的肝脏中,参与甘油三酯合成和脂解作用的基因(例如Gpat3、Lpin1/2、Plin5和Ces1d/b)表达下调,而介导脂肪酸合成与延长的基因(例如Acacb、Elovl1、2、6)则表达上调(图4E))。这些结果表明,肝脏中SLC25A45缺失会诱导葡萄糖分解代谢和脂肪酸合成的代偿性激活,同时下调线粒体脂肪酸β-氧化。这些变化具有肝脏选择性,在SLC25A45 KO小鼠心脏中的糖酵解和β-氧化通路并无显著变化(图S8C-D)。
为了探究SLC25A45 KO小鼠中肉碱合成受损的后果,研究人员检测了心脏(长链脂肪酸氧化的主要部位)的线粒体呼吸。结果显示,在添加二磷酸腺苷(ADP)和棕榈酰辅酶A(palmitoyl-CoA)的状态(State 3)下,SLC25A45 KO小鼠的线粒体呼吸显著低于对照小鼠(图4F)。类似地,在利用棕榈酰辅酶A(State4)评估线粒体β-氧化时,来源于SLC25A45 KO小鼠腹股沟白色脂肪组织的脂肪细胞,其线粒体呼吸也低于对照细胞(小编注:State3是在ADP充足情况下,线粒体进行最大速率呼吸的状态,反映氧化磷酸化的能力;State4是在ADP缺乏的情况下线粒体的呼吸状态,反映线粒体的基础质子漏情况。在该结果中,研究人员发现,SLC25A45 KO小鼠心脏State4水平无差异,而State3水平显著下降,说明心脏作为高代谢组织,SLC25A45缺乏虽导致线粒体脂肪酸氧化水平受损,但线粒体功能没有发生损伤,可能切换了能量底物来维持基础能量水平;而SLC25A45 KO小鼠iWAT组织的脂肪细胞State3和State4水平均显著下降,提示iWAT组织作为储存脂质,氧化能力相对较低的组织,SLC25A45缺乏导致线粒体脂肪酸氧化水平受损,可能通过下调线粒体基础含量或基础呼吸(State4降低)等代谢重塑来应对这种代谢压力。)(图4G)。SLC25A45 KO小鼠线粒体脂肪酸氧化降低并非由普遍性线粒体功能障碍导致,原因如下:首先,在提供丙酮酸、谷氨酸和琥珀酸作为底物时,SLC25A45 KO小鼠线粒体的耗氧率(OCR)无明显差异(图4H,S8E);其次,当添加主要不依赖于CPT1/CPT2介导的肉碱穿梭机制即可进入肾和肝线粒体基质的中链脂肪酸(C8,辛酸)时,SLC25A45 KO小鼠的肝脏和肾脏耗氧率无显著变化,此外线粒体对辛酰基肉碱的呼吸反应也相似(小编注:辛酰基肉碱是辛酸与肉碱结合的形式。辛酸虽可直接穿过线粒体内膜,但也在较低程度上依赖肉碱穿梭系统,而辛酰基肉碱进入线粒体时完全不需要CPT1/2介导的肉碱穿梭系统和游离肉碱的参与,进一步证明了SLC25A45缺乏的线粒体脂肪酸氧化受损是由于肉碱转运过程受损,而非线粒体功能发生障碍。)(图S8F)。最后通过电子显微镜观察线粒体形态,未在SLC25A45 KO小鼠与对照组之间发现显著差异(图S8G)。综上所述,这些结果表明,SLC25A45缺失导致全身肉碱减少和长链脂肪酸氧化受损,从而促使能量底物选择向碳水化合物和葡萄糖分解代谢转变;而SLC25A45 KO小鼠的线粒体仍可利用替代能量底物,如丙酮酸和中链脂肪酸。
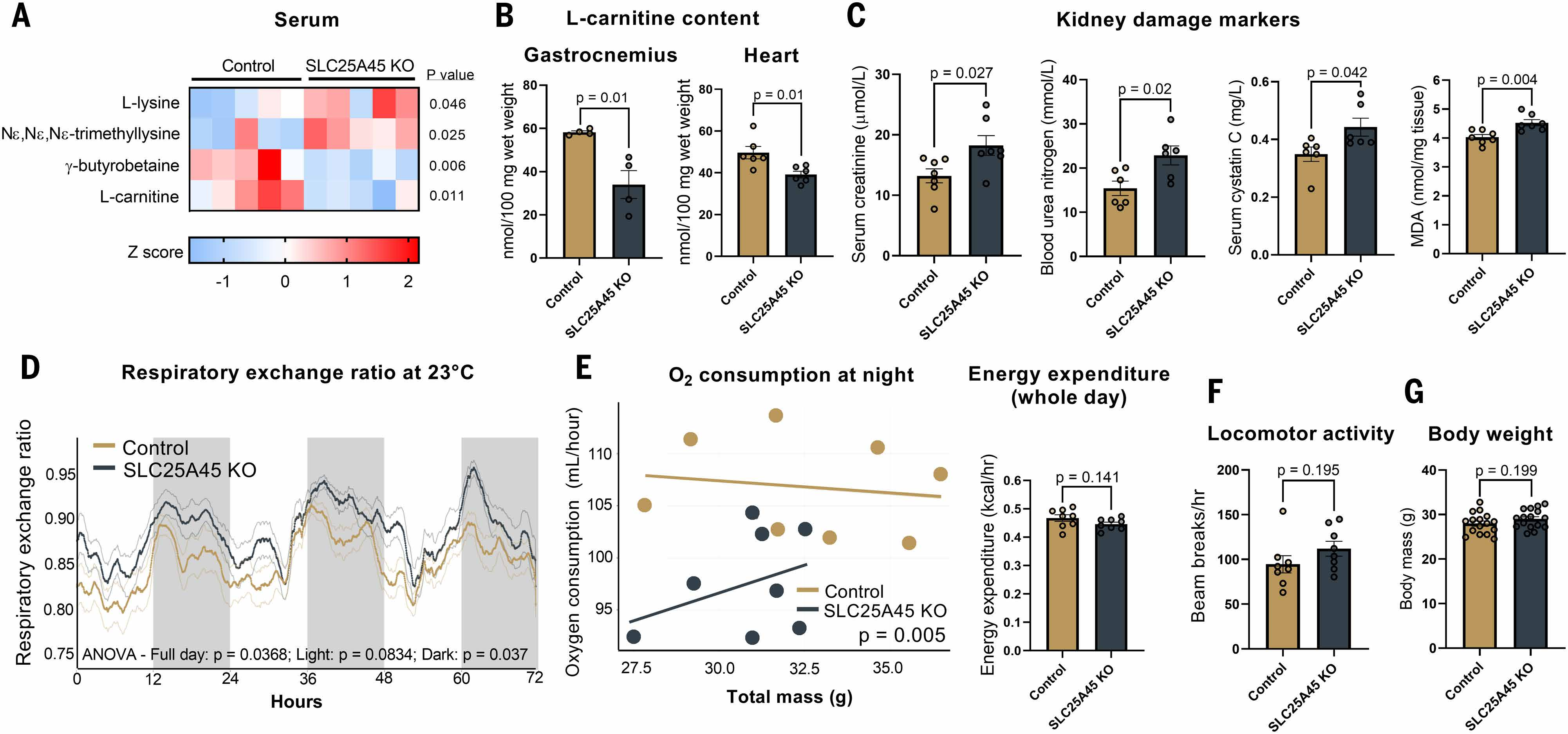
图3.SLC25A45的缺失会导致肉碱缺乏和能量底物选择改变
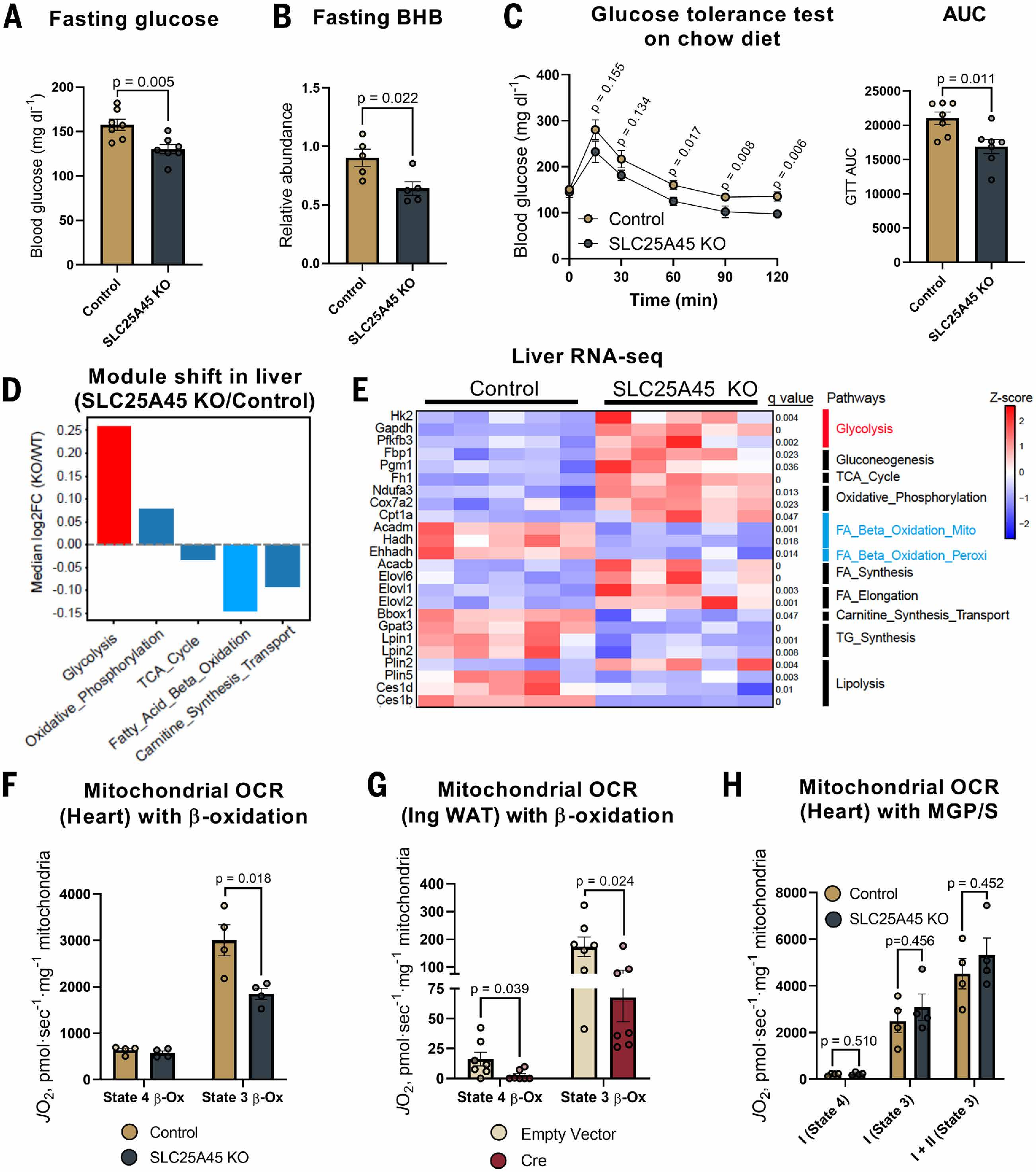
图4.SLC25A45缺失诱导机体从脂肪酸氧化转向碳水化合物和葡萄糖分解代谢
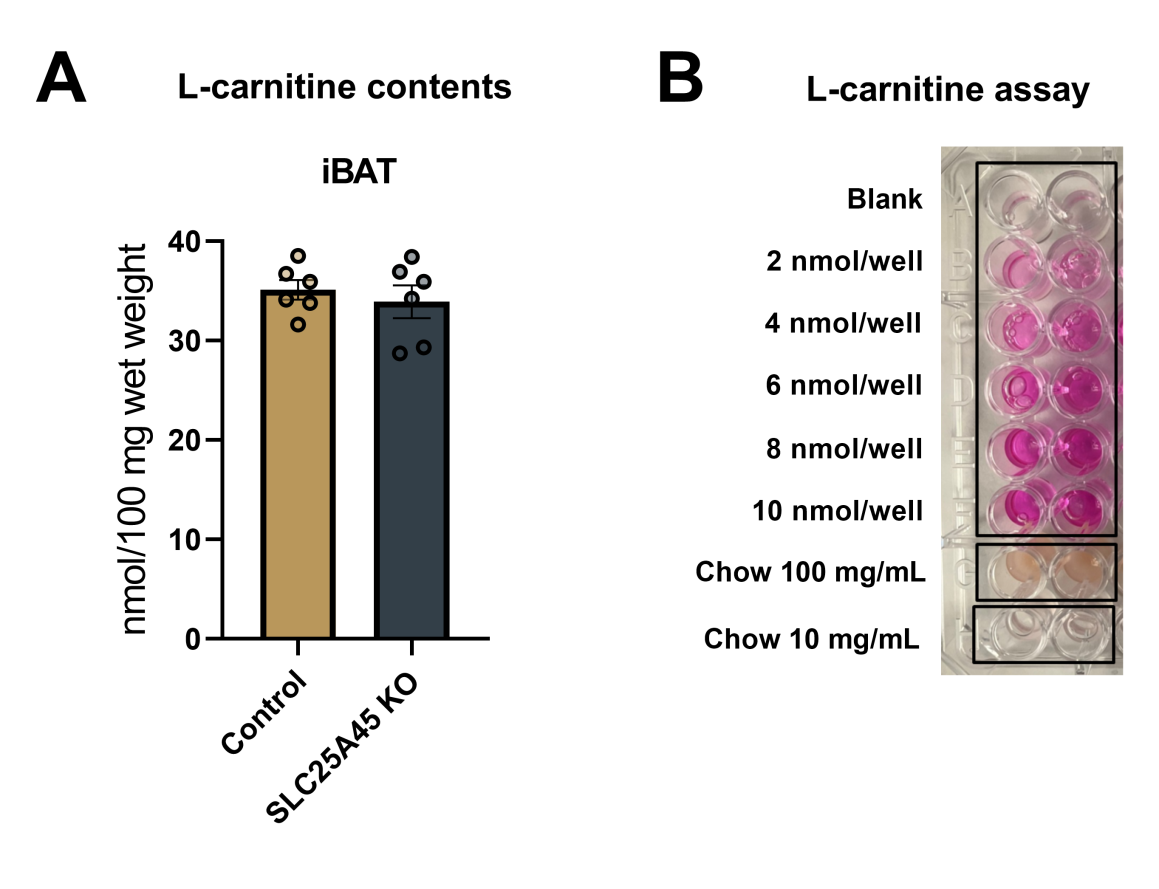
图S6 .组织和饮食中的 L-肉碱含量
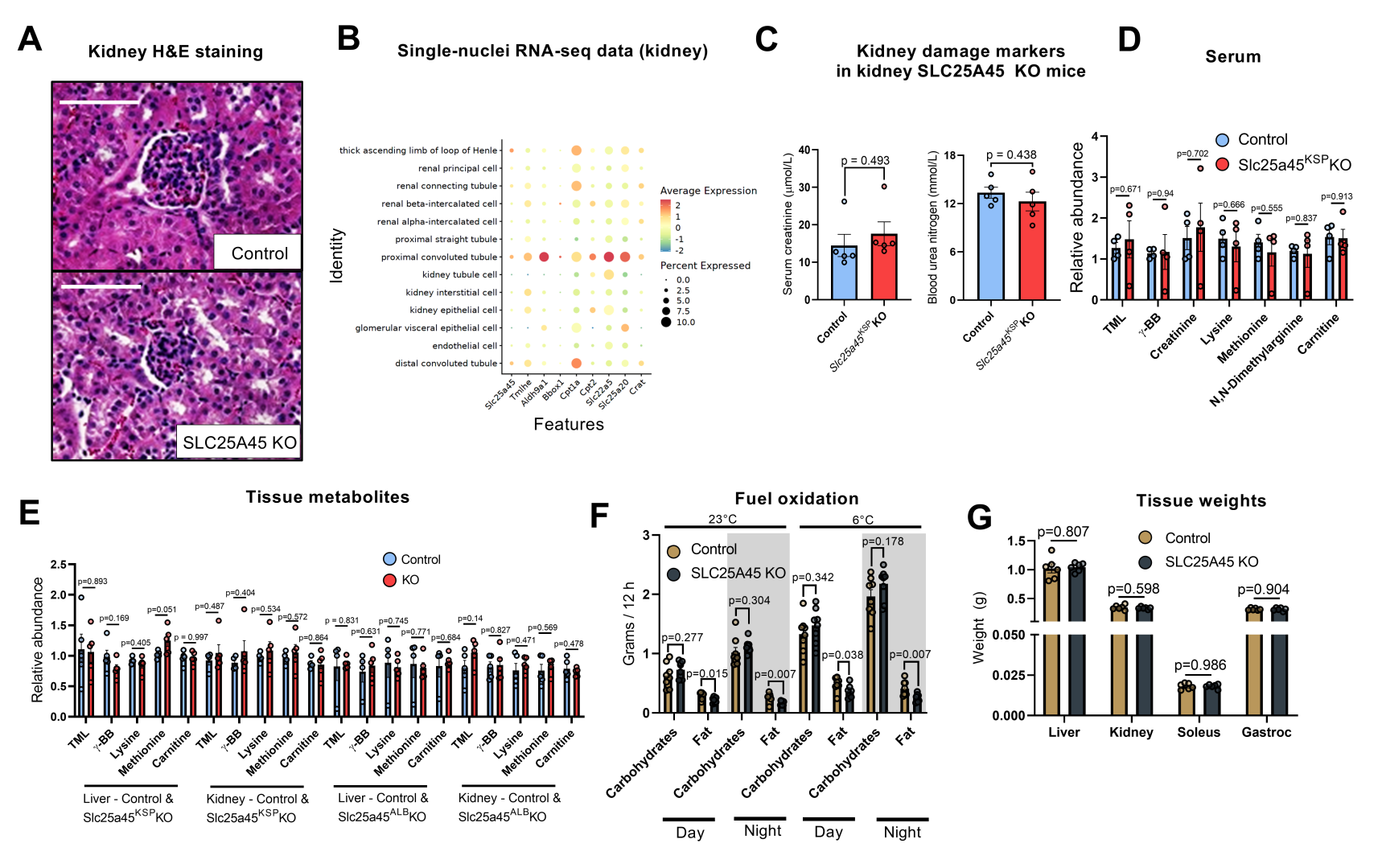
图 S7.全身及组织特异性 SLC25A45 KO小鼠的表征
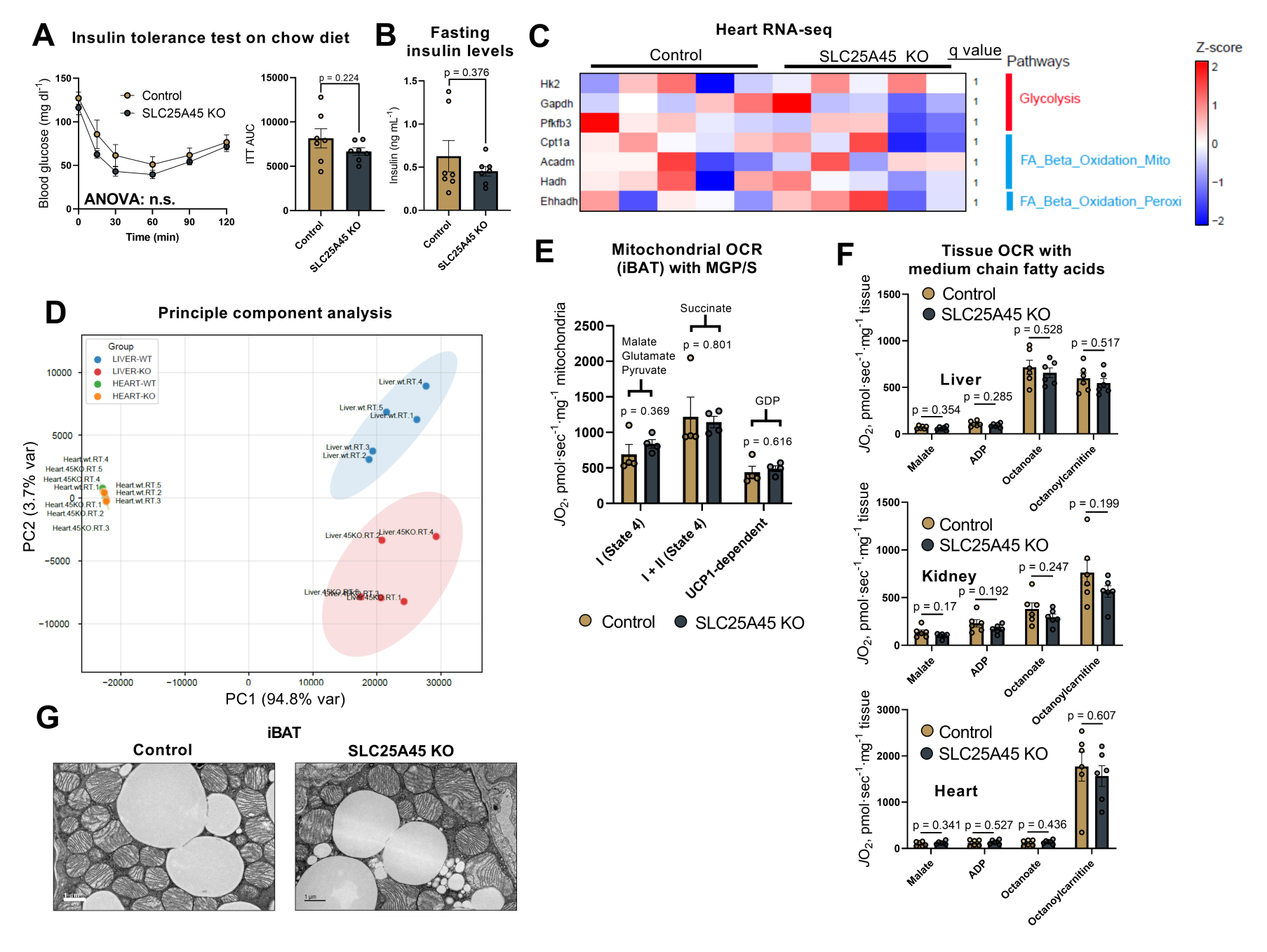
图S8. 全身 SLC25A45 KO小鼠的代偿性代谢途径
4、由SLC25A45介导的肉碱生物合成是机体冷适应的必要条件
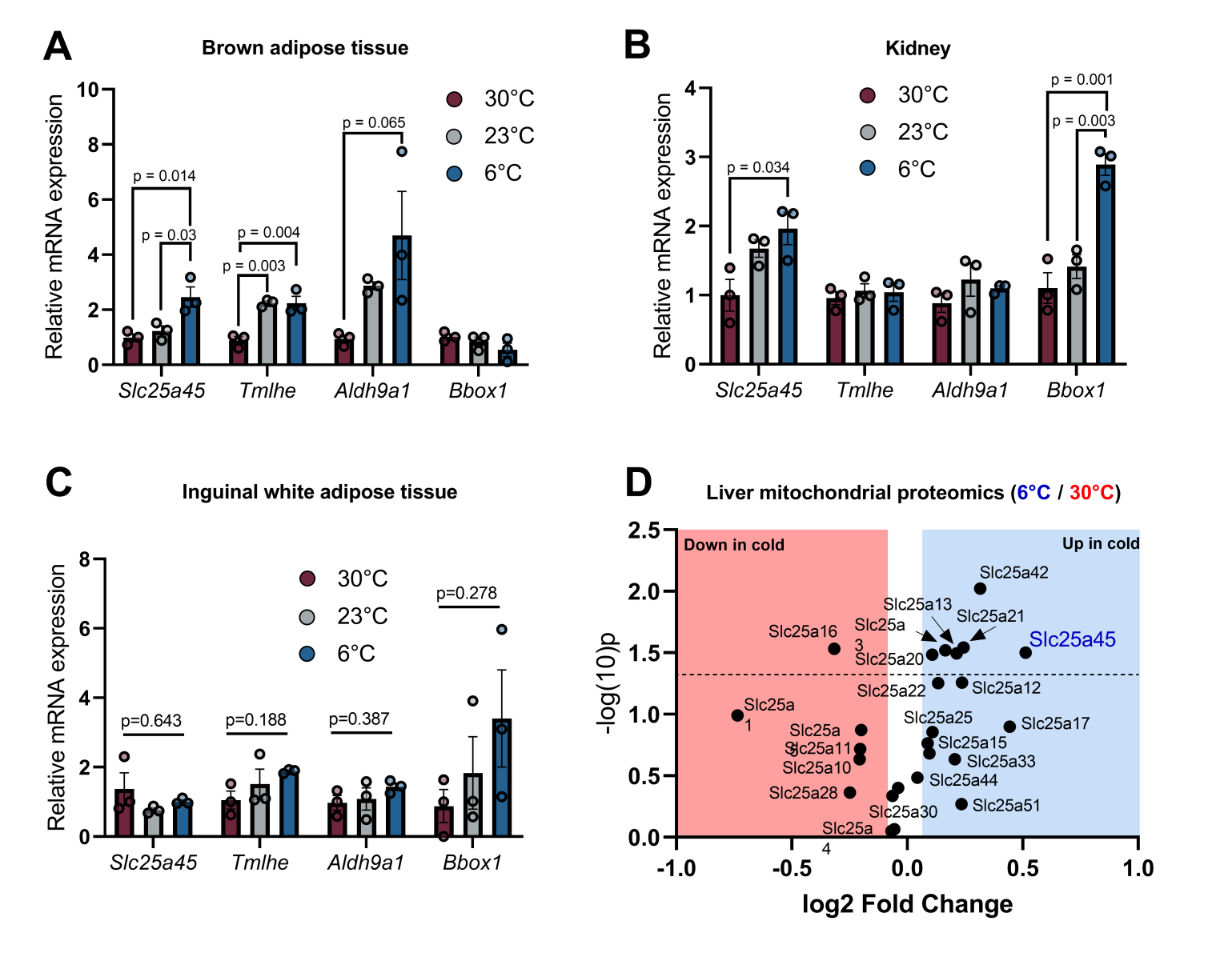
转向依赖脂肪酸代谢是机体在冷暴露过程中一个关键的适应性过程。研究人员发现冷暴露上调了肝脏、BAT和肾脏中包括Slc25a45、Tmlhe 和 Bbox1在内的肉碱合成基因的表达,但在腹股沟白色脂肪组织中则无此现象(小编注:冷刺激下iWAT组织中肉碱合成途径相关基因无差异变化的原因可能是:与BAT组织相比,iWAT组织棕色化是一个相对较慢的过程,且iWAT组织对肉碱的需求更依赖摄取而非自身合成,短期冷刺激可能不足以启动iWAT组织的肉碱合成途径。在冷暴露下,肝脏是肉碱合成的主要场所,通过血液循环将肉碱运送至其他依赖肉碱进行长链脂肪酸氧化的组织中;肾脏是肉碱重吸收和合成的场所,同样为其他组织提供肉碱;BAT是高度依赖脂肪酸氧化进行产热的组织,通过摄取和自身合成肉碱促进脂肪酸氧化。)(图5A,S9A-C)。此外,肝脏蛋白质组学进一步证实,冷暴露后SLC25A45蛋白表达水平升高(图S9D)。这些结果表明,SLC25A45是一种受寒冷诱导的线粒体溶质载体。
上述结果促使研究人员探究SLC25A45介导的肉碱合成是否为机体冷适应所必需。随后,研究人员将饲养于30°C的小鼠急性暴露于6°C寒冷环境后,发现SLC25A45 KO小鼠核心温度显著下降,并在冷暴露5小时后降至30°C以下,而在冷暴露前补充肉碱(100 mg/kg,连续5天)明显抑制SLC25A45 KO小鼠的体温下降(图5B)。在慢性冷暴露过程中,SLC25A45 KO小鼠的呼吸交换率均显著升高(图5C)。本研究所用小鼠饲料中肉碱含量极低(图S6B)。这些结果表明,SLC25A45 KO小鼠的冷不耐受主要源于系统性肉碱缺乏。为明确SLC25A45 KO小鼠冷不耐受表型是否由BAT产热受损引起,研究人员在冷暴露后分离了SLC25A45 KO小鼠与对照小鼠的BAT组织线粒体,并在添加或不添加GDP的条件下检测了线粒体耗氧量,结果发现在两种条件下SLC25A45 KO小鼠BAT来源的线粒体耗氧量均显著降低(图5D)。
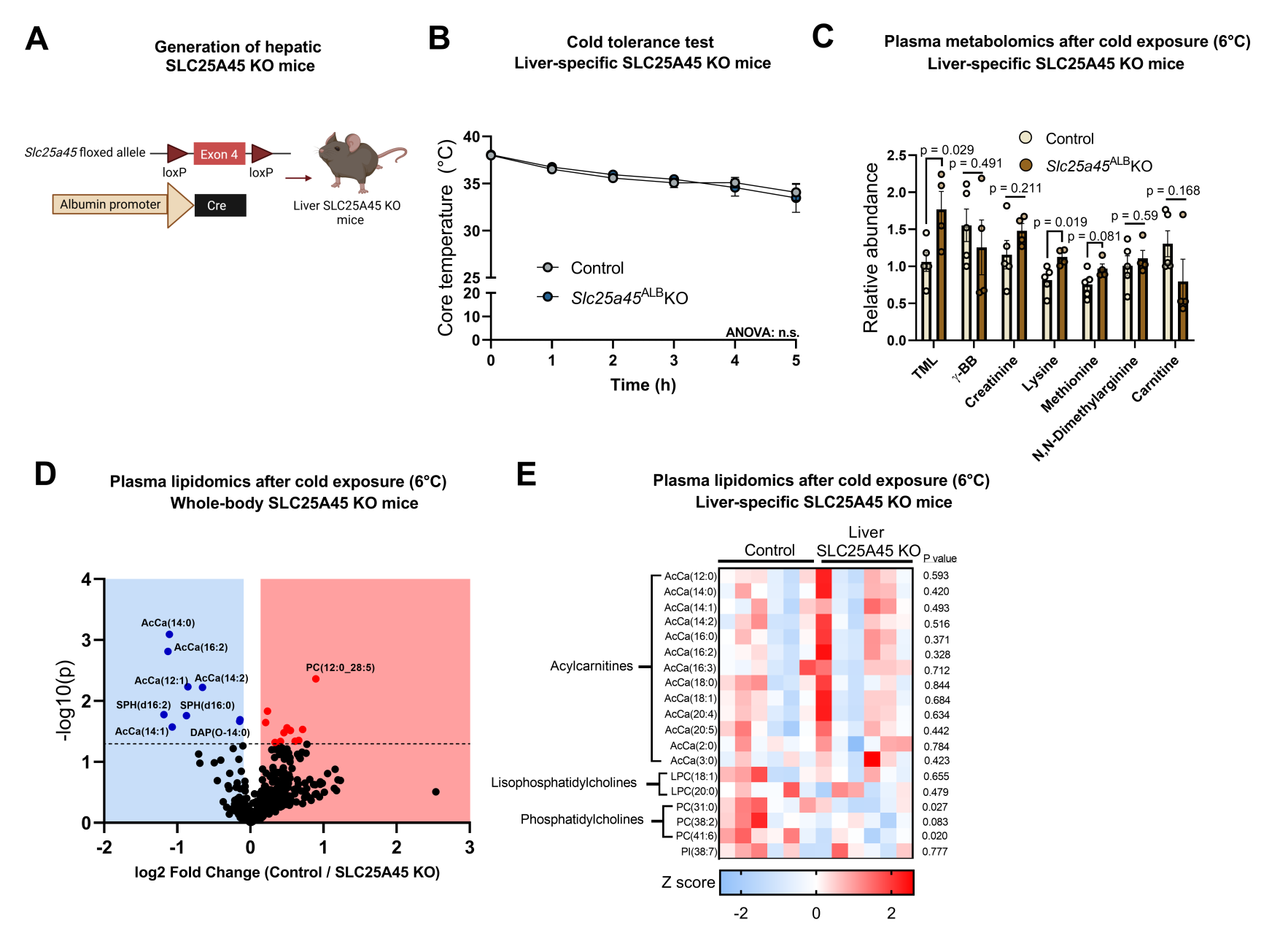
肝脏是内源性肉碱的主要合成部位,并高表达SLC25A45(图1B),与此同时,肾脏等其他组织也能产生肉碱。因此,研究人员构建了肝特异性SLC25A45 KO小鼠(图S10A)。然而,肝特异性SLC25A45 KO小鼠在寒冷暴露后核心体温与对照小鼠变化类似(图S10B)。这与全身SLC25A45 KO小鼠不同。此外,肝脏特异性敲除SLC25A45未改变小鼠血清中γ-BB和肉碱的浓度(图S10C)。进一步检测SLC25A45 KO小鼠和肝特异性SLC25A45 KO小鼠的循环代谢物,脂质组学分析表明,在6°C冷暴露后,全身性SLC25A45 KO小鼠血清中长链酰基肉碱(包括C12:1-、C14:0-、14:1-、14:2-、16:2-、18:0-肉碱)及若干鞘脂的浓度低于对照组小鼠(小编注:这里检测SLC25A45 KO小鼠血清中鞘脂水平,是为了说明全身性SLC25A45缺乏导致的肉碱缺乏和脂肪酸氧化障碍,不仅能导致机体能量代谢受损,还引起了广泛的脂质代谢网络重塑)(图5E和图S10D)。这一结果与之前研究一致,该研究表明小鼠血清酰基肉碱浓度在冷暴露3小时及之后升高,是BAT产热和冷耐受的关键能量底物。研究人员还发现与对照小鼠相比,SLC25A45 KO小鼠血清中溶血磷脂酰胆碱(LPC)、磷脂酰胆碱(PC)和鞘磷脂(SM)的浓度更高。此外,血清代谢组学显示,与对照小鼠相比,SLC25A45 KO小鼠左旋肉碱的前体代谢物(包括L-赖氨酸、蛋氨酸和TML)浓度明显升高(图5F)。相比之下,肝脏特异性SLC25A45 KO小鼠与对照小鼠血浆中的酰基肉碱、LPC和PC浓度无差异(图S10E)。这些结果强调了全身肉碱可用性在耐寒性和循环脂质谱中的重要性,这也解释了为什么肝脏特异性缺失SLC25A45不会改变机体的冷耐受能力。
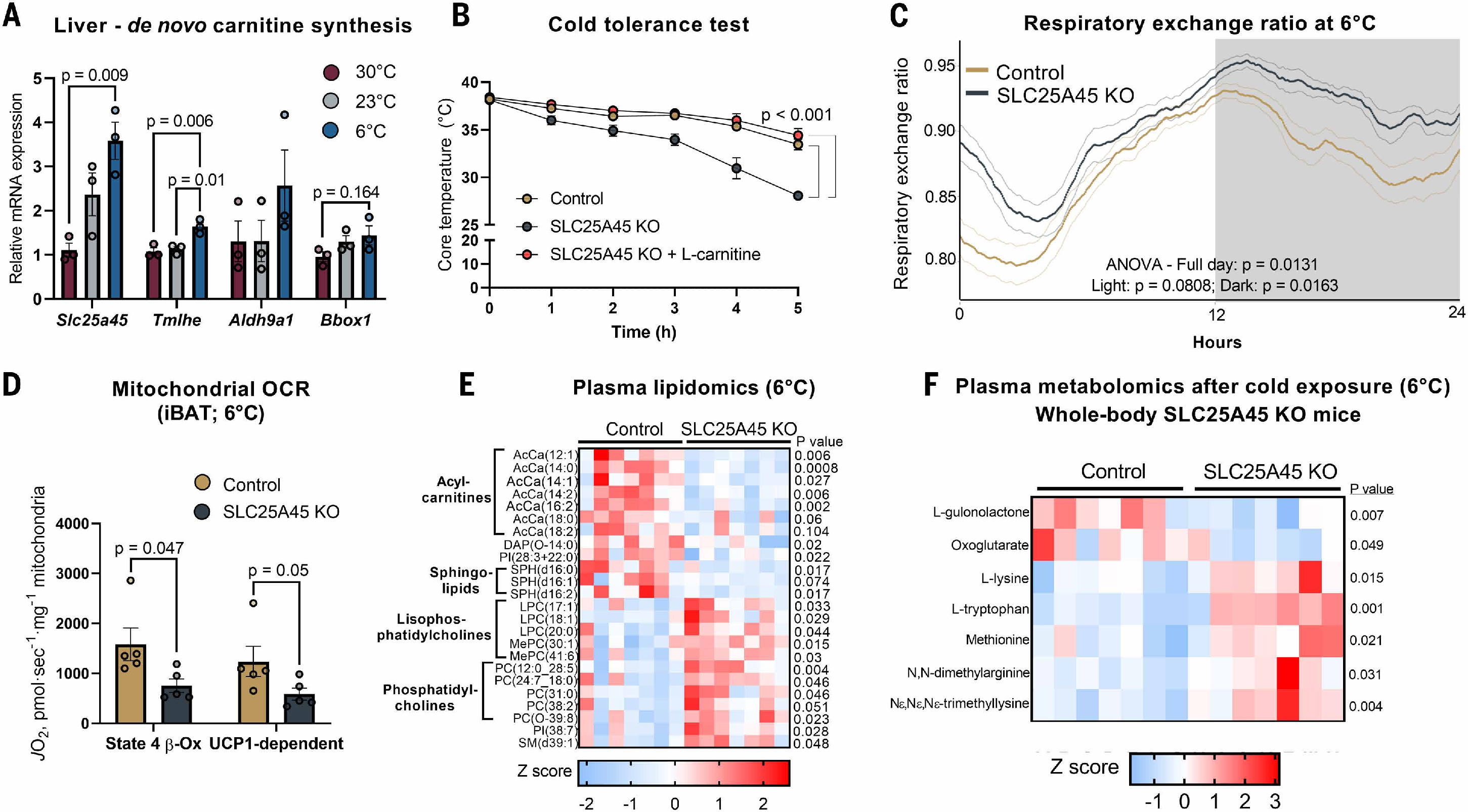
图5.SLC25A45介导的肉碱生物合成途径是冷适应所必需的
图S9.冷暴露可诱导SLC25A45 的表达
图S10.肝脏特异性 SLC25A45 KO小鼠的血清代谢物和脂质质谱
5、肉碱的生物合成是 GLP-1 受体激动剂达到最佳减重效果所必需的
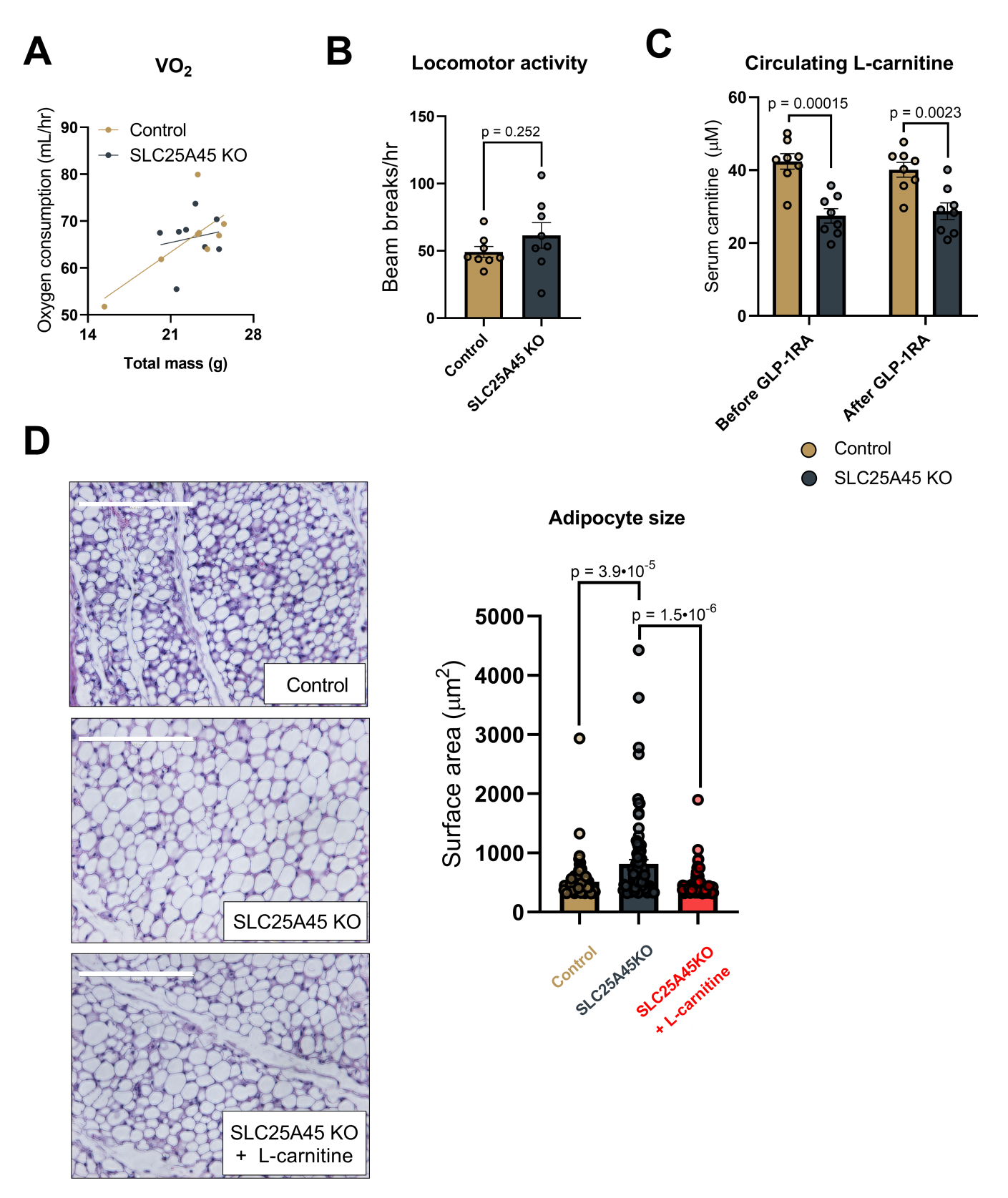
研究人员还研究了SLC25A45 介导的肉碱合成在多大程度上参与了除冷适应之外的其他适应性反应。在这方面,禁食是一个很好的例子,禁食能促使机体将能量底物转向脂肪酸,以确保三磷酸腺苷(ATP)的持续合成,同时将葡萄糖节省下来供给大脑。在自由进食的小鼠中,这种代谢反应可以通过胰高血糖素样肽-1(GLP-1)受体激动剂(GLP-1RAs)进行药理学诱导。GLP-1RA治疗可促进脂肪酸氧化,并降低啮齿动物和人类的呼吸交换率(RER)。因此,研究人员检测了SLC25A45缺失在多大程度上影响GLP-1RA对全身能量平衡的疗效。为此,研究人员给普通饲料喂养的SLC25A45 KO小鼠及对照小鼠注射GLP-1RA药物司美格鲁肽,剂量为30 nmol/kg,持续5天(图6A)。在治疗过程中,尽管对照组和SLC25A45 KO小鼠的RER水平暂时降低(很可能是因为肉碱通过其他途径合成),但SLC25A45 KO小鼠的RER水平显著高于对照组(图6B)。然而,与司美格鲁肽治疗的WT小鼠相比,SLC25A45 KO小鼠在耗氧量(VO₂)和活动量方面没有显著差异(图S11A和B)。此外,司美格鲁肽治疗导致对照小鼠血清中长链酰基肉碱(特别是C12:0、14:1、14:2和18:2)浓度升高;但在SLC25A45 KO小鼠中未观察到这种变化。司美格鲁肽还降低了对照小鼠的血清甘油三酯(TGs)和甘油二酯(DGs)水平,而在SLC25A45 KO小鼠中,这些脂质仍保持较高浓度。此外,两组小鼠之间某些溶血磷脂酰胆碱(LPCs)和磷脂酰胆碱(PCs)的浓度也存在差异(图6C)。与在冷暴露条件下观察到的现象一样,这些变化表明SLC25A45 KO小鼠调动脂质的能力存在缺陷。此外,SLC25A45 KO小鼠的血清肉碱浓度仍低于对照小鼠(图S11C)。这些结果进一步支持了这样一个观点:在应对GLP-1受体激动剂(GLP-1RA)处理模拟的禁食反应状态下,SLC25A45对于机体利用脂肪酸氧化进行供能是必需的。
司美格鲁肽在治疗第一天显著降低了对照组和SLC25A45 KO小鼠的食物摄入量(图6D)。然而,在为期5天的司美格鲁肽治疗期间,SLC25A45 KO小鼠的食欲逐渐恢复,进食量持续高于对照小鼠,尤其是在夜间时段(图6E)。此外,与对照小鼠相比,SLC25A45 KO小鼠对司美格鲁肽治疗引起的体重减轻和脂肪组织减少具有抵抗性(图6F)。相比之下,司美格鲁肽使对照组和SLC25A45 KO小鼠的血糖浓度均出现了相似程度的降低(图6G)。这些数据表明,SLC25A45介导的肉碱通路是司美格鲁肽发挥抗肥胖作用所必需的,但对于其降糖效果则不然(小编注:司美格鲁肽一方面作用于中枢,抑制食欲,另一方面作用于外周组织,促进脂肪酸氧化,这共同介导了减重作用。在司美格鲁肽治疗过程中,SLC25A45 KO小鼠RER显著高于对照小鼠,说明SLC25A45 KO小鼠脂肪酸氧化受损。然而在摄食量方面,在司美格鲁肽治疗的第一天,SLC25A45 KO小鼠与对照小鼠的摄食量均被显著抑制,说明SLC25A45缺失不影响司美格鲁肽的急性抑制食欲作用。但在司美格鲁肽持续治疗的阶段,SLC25A45 KO小鼠的摄食量逐渐恢复且显著高于对照小鼠,这可能是SLC25A45缺失介导脂肪酸氧化受损引起的代偿性反应。因此SLC25A45介导的脂肪酸氧化在司美格鲁肽的减肥作用中发挥着更重要的作用。)
考虑到禁食期间脂肪分解对于脂肪酸氧化的关键作用,研究人员随后测试了SLC25A45介导的肉碱生物合成通路是否是GLP-1RA治疗后脂肪组织分解所必需的。研究人员观察到,在GLP-1RA治疗后,SLC25A45 KO小鼠与对照小鼠的血浆甘油浓度没有显著差异,但补充肉碱恢复了SLC25A45 KO小鼠的脂肪组织脂解作用(图6H)。与这些变化一致的是,SLC25A45 KO小鼠对GLP-1RA诱导的脂肪组织减少具有抵抗性,而在GLP-1RA治疗期间补充肉碱,能有效恢复该作用(图6、I和J,图S11D)。此外,对SLC25A45 KO小鼠进行GLP-1RA治疗,同时给SLC25A45 KO小鼠补充肉碱,能有效降低SLC25A45 KO小鼠的RER,尽管这种效应是暂时的(图6K)。这些变化与能量摄入无关,因为在司美格鲁肽治疗期间补充肉碱并未改变食物摄入量(图6L)(小编注:图6L检测的是急性司美格鲁肽治疗后对照小鼠、SLC25A45 KO小鼠和SLC25A45 KO+肉碱补充小鼠的摄食量,结果显示三组小鼠间摄食量无明显差异,且在司美格鲁肽急性治疗后均出现了摄食下降的现象。这与图6D-E结果一致,即在司美格鲁肽治疗第一天均显著抑制了对照小鼠和SLC25A45 KO小鼠的摄食,且对照小鼠和SLC25A45 KO小鼠间摄食量无显著差异,在司美格鲁肽的持续治疗过程中,SLC25A45 KO小鼠的摄食恢复且高于对照小鼠)。最后,研究人员发现GLP-1RA治疗后,SLC25A45 KO小鼠Lean mass水平显著高于对照小鼠,而补充肉碱后SLC25A45 KO小鼠的Lean mass仍明显高于对照小鼠(图6M)。综上所述,这些结果表明机体在应对冷暴露以及GLP-1RA诱导的体重减轻时,由SLC25A45介导的肉碱生物合成在从碳水化合物向脂肪酸的能量底物切换中所起的关键作用。

图6.肉碱合成途径对于GLP-1RA的抗肥胖作用是必需的
图S11.SLC25A45 对 GLP-1RA 诱导的脂肪组织减少是必需的
总结
本研究揭示了线粒体代谢物运输作为能量底物选择调控检查点,在机体适应寒冷和禁食条件下的脂肪酸代谢中所起的作用。SLC25A45作为一种定位于线粒体的TML转运蛋白,在调控肉碱合成及能量底物转换中发挥关键作用。SLC25A45缺失可导致肉碱减少,进而损害线粒体脂肪酸氧化功能,迫使能量代谢向碳水化合物依赖模式转变。Slc25a45基因敲除小鼠不仅表现出冷耐受缺陷,同时对GLP-1受体激动剂(GLP-1RA)介导的脂质动员反应减弱,从而对药物诱导的脂肪组织减少产生抵抗。

原文链接:https://www.science.org/doi/10.1126/science.ady5532
转载本文请联系原作者获取授权,同时请注明本文来自徐凌燕科学网博客。
链接地址:https://wap.sciencenet.cn/blog-3483272-1527508.html?mobile=1
收藏

