 精选
精选
研究背景
全球能源需求的不断增长以及向脱碳经济转型的紧迫性,为电化学能量存储与转换装置开辟了新趋势,这些装置涵盖超级电容器、燃料电池、水电解槽和电池等,它们在构建绿色、清洁且可持续的能源经济中发挥着关键作用。
电化学能量存储的主要支柱是电池,电池能够存储化学能,并在必要时应用于固定站点或便携式设备,这使得电池成为满足日常需求的关键装置。尽管电池技术已取得显著进展,例如锂离子电池(LIBs)为电动汽车(EVs)提供动力,但由于对这些设备的需求日益增长,仍面临巨大挑战。锂离子电池所依赖的关键金属元素(如钴和锂等稀缺且有限的资源)的原材料长期供应情况及地理分布状况,是限制锂离子电池未来应用的制约因素。
为使电池技术获得社会经济认可,我们需要展示兼具高功率密度和高能量密度且成本效益显著的优势。为此,可充电金属-空气电池(MABs)因其成本低于锂离子电池而被广泛应用于众多领域。金属-空气电池还具备诸多优良特性与实用性,包括相对较高的能量密度以及不易燃的电解质,可确保其具有较高的安全性。
Engineering Bifunctional Catalytic Microenvironments for Durable and High〦nergy〥ensity Metal–Air Batteries
Jean Marie Vianney Nsanzimana*, Lebin Cai, Zhongqing Jiang, Bao Yu Xia*, Thandavarayan Maiyalagan*
Nano-Micro Letters (2025)17: 294
https://doi.org/10.1007/s40820-025-01799-w
本文亮点
1. 概述了金属-空气电池结构、反应机制以及开发双功能空气呼吸电极的挑战。
2. 综合讨论了无贵金属双功能氧电催化剂微环境化学工程化。
3. 洞察具有增强性能和耐用性的富含地球的双功能催化剂的未来研究方向,旨在指导未来开发可扩展应用的先进双功能催化剂。
内容简介
可充电金属-空气电池因其高能量密度和环境友好性而备受关注。然而,这类电池面临着重大挑战,特别是与吸空气电极相关的问题,这些问题会导致电池循环寿命短、效率低以及催化剂降解。由于氧电催化反应动力学迟缓,且遵循不同的反应路径,往往需要不同的活性位点,因此开发一种性能优良的双功能电催化剂仍困难重重。由此,在催化剂微环境(如原子调控、纳米/微米尺度以及表面界面)中,机制尚不明确且表面重构不可逆,这会导致电池在充放电循环过程中加速降解。要克服这些障碍,就需要在双功能电催化剂的开发和理解方面取得进展。印度SRM科技学院Maiyalagan等人讨论了金属-空气电池的关键组成部分、相关挑战以及当前解决这些问题的工程方法。此外,还研究了空气电极上氧电催化的机制,以及材料化学特性如何影响这些机制的见解。此外,重点介绍了双功能电催化剂的最新进展,着重阐述了合成策略、微环境调控以及展现高效性能的稳定体系,特别是在锌-空气电池和锂-空气电池中的应用。最后,针对金属-空气电池高效且耐用的双功能电催化剂的设计,提出了展望和未来研究方向。
图文导读
I 金属-空气电池的配置、工作原理和挑战
金属-空气电池配置、工作原理和挑战如图1a中示意性所示,MAB由几个关键部件组成,每个部件都具有特定的功能,并有助于设备的性能和耐用性。通常,MAB电池由四个主要部件组成:金属阳极、呼吸空气阴极、膜分离器和电解质。除了这些主要部件之外,其他部件(例如集电器和允许装置中的空气的燃料接入端口)一起工作以使得电池能够在放电期间经由阳极处的金属的化学氧化和在多孔阴极处的氧的还原来产生能量,同时电解质允许离子在它们之间流动。本节主要介绍各种组件的关键作用及其应对当前挑战的优化策略。
1.1 金属阳极
金属阳极是在放电过程中发生氧化的金属,MAB的名称来源于金属阳极。放电时,金属阳极因氧化反应释放电子,流经外电路,提供电能。然而,MAB的能量密度可能与用作阳极的金属有关,这使得金属阳极成为MAB中的关键组分。考虑到纯金属阳极,其中金属阳极是镁的镁-空气电池表现出更高的开路电压(OCV)(图1b),而铁-空气电池提供1.28 V(298 K)的降低的OCV,并且它是作为阳极最常用的金属元素中最便宜的金属元素。尽管镁空气电池表现出3.09 V的最高OCV和高比能量密度,但与其他阳极金属不同,它们的高腐蚀特性仍然是一个主要挑战,在其他阳极金属中,阴极电流的增加意外地加速了氢的析出。此外,由于氧化镁(MgO)和过氧化镁(MgO₂)作为放电钝化电极期间的副产物,它们的可逆性差,表现出缓慢的电荷传输和差的导电性。这些阻碍了电池的可充电性和性能,这是MABs实际商业化的关键参数。
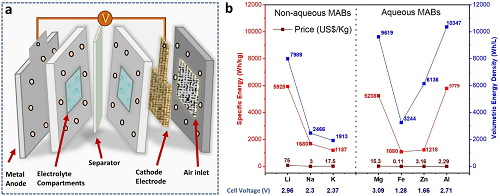
图1. a. MABs的示意图。b金属-空气电池(MABs)中锂(Li)、钠(Na)、钾(K)、镁(Mg)、铁(Fe)、锌(Zn)和铝(Al)金属阳极的开路电压、比能量密度、体积能量密度以及价格对比图。
1.2 电解质和隔膜
MABs中的电解质在促进电化学反应以及金属阳极和空气阴极的稳定性方面起着关键作用。根据MABs的类型,电解质可以是锂、钠和K-O₂电池中的非水非质子电解质,也可以是锌、铝、镁和铁空气电池中的水性液体电解质。在非水电池中,使用非水的非质子有机醚,但它们对外部环境条件高度敏感。因此,组件必须在惰性环境中制备,并且通常使用纯氧进行测试。非水电解质,如有机溶剂或离子液体,在其更宽的电化学窗口中提供了显著的优势,这允许在更高的电压下操作(对于水,为3-4 V,相对于约1.23 V),同时最大限度地减少寄生反应,如析氢,腐蚀水性电解质中的金属阳极。
1.3 空气阴极
氧作为MABs的燃料供应在正电极(空气阴极,图1a)上,其中催化活性层进行两个关键的电化学反应:OER和ORR。为了促进氧气从空气扩散到层催化剂,阴极通常被制造为多孔气体扩散层(GDL)或在多孔材料(如金属泡沫)上,以提供优异的导电性,暴露大的表面积,并增强传输。在该氧电极上,ORR发生在放电期间,而OER发生在充电期间。两种氧反应都是多步反应,表现出缓慢的动力学,因此限制了MABs的性能。双功能催化剂必须同时驱动充电期间的OER和放电期间的ORR;然而,很少有材料能持久地满足苛刻的要求。对于可切换的双功能活性和氧化还原稳定性,整体材料创新是迫切的。除了催化剂之外,装置的连续运行也面临着重大挑战。例如,湿气和二氧化碳等环境污染物的渗透会在电解质中形成碳酸盐,从而损害性能。此外,在放电期间,反应产物可能积聚在阴极孔中,导致堵塞并限制氧气扩散,从而随着时间的推移降低容量。所有这些问题都应通过系统的材料设计和工程来解决,以协同增强MABs的性能(图2)。
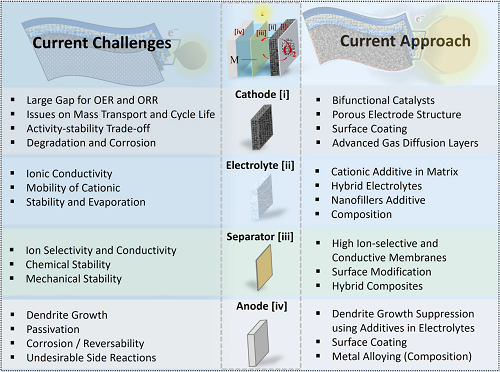
图2. MABs的主要部分、相关挑战和解决这些问题的当前方案。
II MABs的基础化学反应和挑战
在MABs中,化学反应的主要类型可以根据不同的电解质系统以及金属阳极进行分类。电解质是能够设计各种类型的MABs(水性、非水性和固态)的必要关键组分,包括那些需要机械稳定性的MABs,例如柔性MABs (图3)。在阴极,来自空气的氧气与金属离子反应,导致金属超氧化物或过氧化物在空气电极上放电。在水性电解质中,阴极空气中的氧气通过接受电子发生化学还原反应,形成OH⁻。之后,形成的OH⁻与来自阳极的金属离子相互作用。
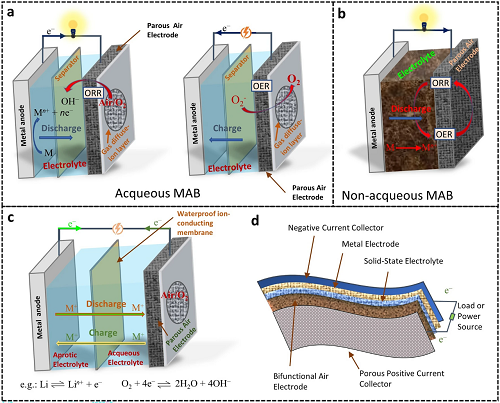
图3. MABs工作原理示意图。a水性、b非水性、c固态/水性混合电池和d柔性MABs。
在含水电解质中,氧还原反应(ORR)可能通过二电子或四电子反应路径进行。四电子反应路径,其标准电极电势E⁰ =+0.401 V,会生成水(图4a);而二电子反应机制,其标准电极电势E⁰ =−0.076 V,会导致过氧化氢的生成。由于过氧化氢可能会腐蚀金属-空气电池(MABs)或燃料电池中的某些材料,因此该反应路径并非理想途径。
符号*表示催化剂的活性位点,OOH*、O*和OH*表示吸附在这些活性位点上的中间体,其可以分别表现为去质子化物质,例如O₂⁻和O⁻。不希望的分子氧是MABs的燃料,可以在两个2e⁻途径中电化学还原,形成OOH*的中间体,并导致H₂O₂作为产物物质的形成(图4b)。
尽管该机制涉及四电子过程,这可能看起来像ORR和OER之间的可逆反应(图4c),但图4d中标度关系的火山图揭示了这两个反应显示出氧吸附能的不匹配,因此使催化剂难以在两个反应中都表现良好。因此,通过合理的结构设计打破线性尺度关系是实现高活性双功能催化剂的关键,这些催化剂可以弥合不同反应中大多数优化的中间体吸附的这种不匹配。
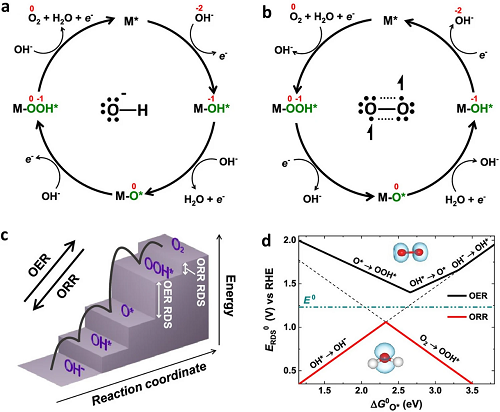
图4. 氧电催化机理和示意图;示出了在碱性条件下对应于OER和ORR循环期间的化学步骤的a、b基元化学反应。c图描绘了电位E=0 V时催化剂的势能与RHE的关系。d ORR和OER速率确定步骤的活动火山图示意图。
III MABs电催化剂的合成方法
功能材料合成的最新进展为开发具有原子、纳米/微米尺度和界面微调微环境的多样化纳米结构系统开辟了新的途径,从而增强了它们的催化性能,包括OER和ORR的双功能活性。例如,为了最大限度地减少金属的使用,合成策略的创新使得能够制造在碳或金属载体上具有高分散性的单原子催化剂(SACs),确保活性位点的最佳利用。它们是合成SACs和双原子催化剂(DACs)的各种策略,包括(1)干法合成路线(原子层沉积(ALD)法、热解合成、原子俘获法和两步掺杂法);以及(2)有利于原子在基底上的吸附(易吸附法、湿浸渍法和强静电吸附法)或SAC与基底的光化学和电化学性质的湿合成路线(例如:光还原法)。金属有机骨架(MOFs)由于其明确的结构和可调的孔隙率,是合成相对可扩展的囊的理想前体。热解时,包括MOFs、金属-菲咯啉配合物和金属酞菁-二氧化硅胶体复合材料在内的有机前体热化学分解,产生金属-氮-碳囊和DACs。此外,MOF热解可用于合成负载在氮掺杂碳上的金属合金。尽管这些技术对SAC催化剂的合成很有前途,但经济高效的合成阻碍了大规模工业化。因此,需要研究这些方法对于实际MABs的成本效益,并努力使用可重复和可扩展的方法。
IV 双功能氧电催化剂
尽管MABs的操作原理相似,但双功能电催化剂应适合电解氧,但也应在氧氧化和还原的可逆反应中稳定。因此,寻找氧化还原耐受材料应该定制长期充电/放电开关的能力。虽然PGMs是最好的ORR和OER电催化剂,但它们缺乏氧电催化的双功能催化活性。过渡金属具有更宽的可调d轨道电子结构空间,能够在氧化还原过程中实现自适应价态转变,导致多种含氧中间体的双功能吸附能。在这篇综述中,将从七个方面总结最近开发的用于空气呼吸电极的无PGM双功能催化剂:(i)单原子催化剂,(ii)尖晶石,(iii)钙钛矿,(iv)无金属催化剂,(v)金属-氮-碳,(vi)金属-有机骨架衍生催化剂,(vii)合金和高熵合金。
4.1 单原子催化剂
通过生物质水凝胶的直接热解合成了具有相邻铁纳米团簇的铁囊,生物质水凝胶用作铁前体和氮掺杂碳(图5a)。研究表明,Fe纳米团簇的存在增加了Fe原子中心的3d电子密度并降低了Fe原子中心的磁矩(图5b,c),与没有纳米团簇的样品相比,这提高了双功能催化性质和抗氧化性(图5d,e)。双功能阴极催化剂的性能优异,OCV为1.47 V,功率密度为49 mW cm⁻2(图5f,g),以及出色的长期性能,持续2300次连续充电/放电循环。此外,在环境条件下,表现其出增强的催化活性,强调了调整SACs的电子结构以定制性能和寿命的重要性。
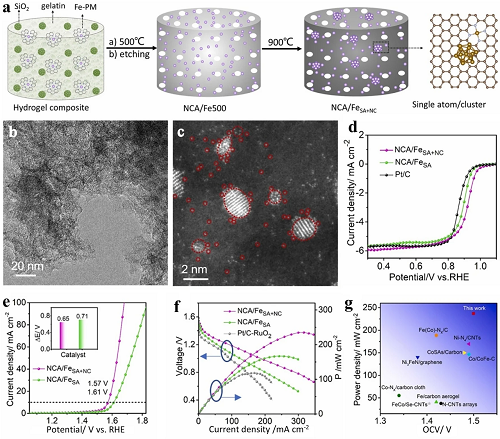
图5. 总结了电催化剂的合成过程。b、c TEM图像和相应的HRTEM图像显示了Fe囊和Fe簇。d在0.1 M KOH中的ORR性能。OER在1.0 M KOH中的e极化曲线。锌准固态电池恒流放电的f曲线。g图比较了优化的电催化剂与选定的ZABs。
以金属-有机框架(MOF)为前驱体,通过多步合成策略(图6a),成功在氮掺杂碳纳米材料(Fe/I-NCR)上制备了铁(Fe)与碘(I)共掺杂的双原子催化剂(Fe/I SAC)。研究发现,碘的引入可通过长程电子离域效应调控Fe-Nₓ活性位点的电子结构(图6b-d)。得益于Fe/I双原子协同效应及一维纳米棒的结构优势,Fe/I-N-CR电催化剂展现出优异的氧还原反应(ORR)性能,其活性显著优于商用Pt/C催化剂及单一Fe或I单原子催化剂。基于该催化剂组装的准固态锌-空气电池(ZABs)实现了197.9 mW cm⁻2的功率密度,并在20 mA cm⁻2恒电流下稳定运行280 h,性能远超商用Pt/C + IrO₂体系(119.1 mW cm⁻2,47 h)(图6e-g)。
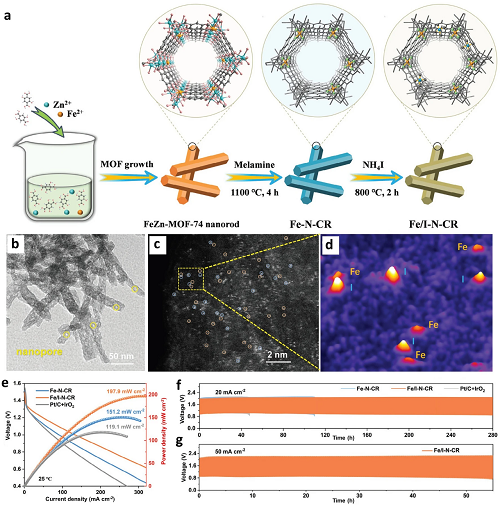
图6. Fe/I-N-CR的微观分析:a. Fe/I-N-CR制备过程的示意图;b、c. 透射电子显微镜(TEM)图像;d. Fe/I-N-CR对应的像差校正高角度环形暗场扫描透射电子显微镜(HAADF-STEM)图像,其中橙色圆圈代表Fe原子,蓝色圆圈代表I原子。性能评估:e. 组装准固态锌-空气电池(ZABs)的放电极化曲线和功率密度曲线;f、g. 分别在20 mA·cm⁻2和50 mA·cm⁻2电流密度下对应的充放电性能。
Li等人设计并构建了用于锂-氧电池(LOB)催化剂层的CuN₂C₂单原子催化剂(SACs)电催化剂(图7a)。如图7b所示,通过受限自引发分散策略,这些CuN₂C₂单原子催化剂成功分散于碳纳米管(CNT)基质中。为探究采用所制备CuN₂C₂单原子催化剂时锂-氧电池的运行反应机理,研究发现Li₂O₂的结构演变与放电/充电的I - IV阶段相关(图7c-h)。当CuN₂C₂电催化剂作为阴极双功能材料使用时,锂-氧电池展现出优异性能,在200 mA·g⁻1电流密度下,放电比容量达7122 mAh·g⁻1,显著优于采用CNT(3782 mAh·g⁻1)和氮掺杂碳纳米管(NCNT,3109 mAh·g⁻1)催化剂的电池(图7g、h)。
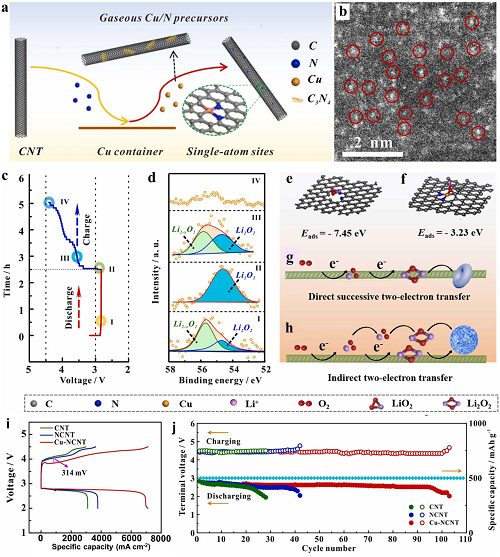
图7. a. Cu-NCNT制备过程的示意图。b. 球差校正高角度环形暗场扫描透射电子显微镜(HAAFD-STEM)图像。c. LiO₂中间体在电极表面各阶段演变的示意图,以及在200 mA·g⁻1电流密度下的充放电曲线;d. 与图7c中所示I、II、III和IV阶段相关的Li 1s的X射线光电子能谱(XPS)图谱。e、f. 中间体LiO₂在e氮掺杂碳纳米管(NCNT)和f Cu-NCNT上结构及结合能的示意图。g、h. 在g NCNT和h Cu-NCNT电催化剂上Li₂O₂形成路径的示意图。i. 在2.0 V至4.5 V电压范围内,以200 mA·g⁻1电流密度进行的恒电流充放电对比曲线。j. 锂-空气电池(LAB)的稳定性性能。
4.2 尖晶石
采用简便、可重复且可规模化的一步水热法(无需煅烧)合成的锰钴氧化物/氧化锰(MnCo₂O₄/Mn₂O₃)纳米棒(NR)材料,在析氧反应(OER)和氧还原反应(ORR)中展现出显著提升的电催化性能(图8a、b)。该方法成功构建了由纳米棒与纳米球组成的混合结构,该结构对增大电催化反应的表面积及优化电子与电解液离子的扩散路径至关重要。如图8b-d所示,相较于纯Mn₂O₃,MnCo₂O₄/Mn₂O₃纳米棒的氧电催化双功能性能显著提升,这归因于钴氧化物的引入改善了两种反应的动力学过程。尽管该催化剂基于电位差(ΔE)评估表现出更优的双功能活性,但其OER与ORR性能仍分别劣于IrO₂和Pt/C,需进一步优化。然而,采用MnCo₂O₄/Mn₂O₃纳米棒与Pt/C//IrO₂分别作为阴极电催化剂的锌-空气电池(ZAB)的电压间隙分别为1.16 V和1.52 V(图8e)。采用该优化催化剂组装的锌-空气电池在高电流密度下表现出更低的极化电压,且在68次循环(约20.3 h)内展现出优于Pt/C//IrO₂基电池的耐久性(图8e、f)。
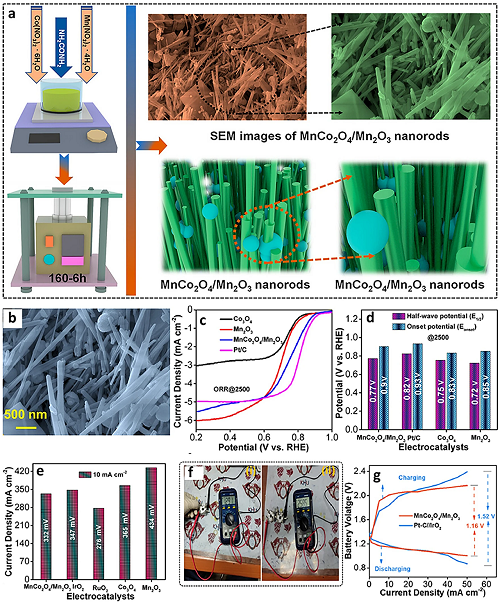
图8. a. MnCo₂O₄/Mn₂O₃纳米棒(NR)催化剂制备方法示意图。b. MnCo₂O₄/Mn₂O₃纳米棒的高倍场发射扫描电子显微镜(FE-SEM)图像。c. 在2500 rpm转速下,MnCo₂O₄/Mn₂O₃纳米棒、Mn₂O₃、Co₃O₄及Pt/C催化剂的氧还原反应(ORR)曲线。d. 对应起始电位与半波电位对比图。e. 图8c中各材料的析氧反应(OER)曲线。f. 锌-空气电池(ZAB)开路电位(OCP):(i)单电池及(ii)两节串联电池的测试结果。g. 基于MnCo₂O₄/Mn₂O₃纳米棒与Pt/C//IrO₂的锌 - 空气电池充放电曲线对比。
近期有研究报道,通过可重复的水热(HT)法,在表面分级结构碳球负载的自支撑α-MnO₂纳米棒阵列中掺杂钴(Co)或镍(Ni),成功制备了Func CSCs-2 M/Co₀.₂₅(或Ni₀.₂₅)MnOₓ系列催化剂(合成过程通过Func CSCs-2 M/NiᵧMnOₓ的制备得以验证,见图9a、b)。相较于原始Func CSCs-2 M/MnO₂电催化剂,该催化剂在金属-空气电池(MAB)及电解水反应中展现出卓越的三功能电催化性能(图9c)。采用电化学功能化阴极组装的两节串联锌-空气电池,可持续驱动红色发光二极管工作超过200小时(图9d、e),表现出优异的稳定性。
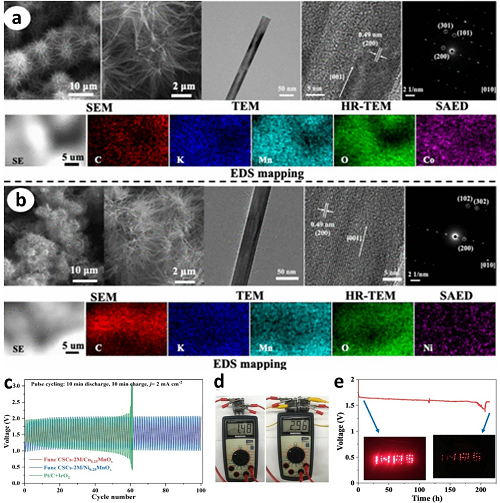
图9. a、b Func CSCs-2 M/Co₀.₂₅MnOₓ(图a)与Func CSCs-2 M/Ni₀.₂₅MnOₓ(图b)的物理化学表征结果。c 采用Func CSCs-2 M/Co₀.₂₅MnOₓ阴极构建锌 - 空气电池(ZAB)时,在2 mA·cm⁻2电流密度下的恒电流充放电(GCD)循环曲线。d 单节及两节串联锌-空气电池的开路电压(OCV)测试结果。e 两节串联锌-空气电池驱动带有加拿大国立科学研究院(INRS)标志的发光装置时,电压随时间变化的图示。
4.3 钙钛矿
Deng等人报道了一种钙钛矿/二氧化铈(CeO₂)/碳异质结材料(CeO₂-Pr₃Sr(Ni₀.₅Co₀.₅)₃O₁₀⁻δ纳米纤维,简称CeO₂-C/PSNC),该材料通过多步工程策略制备,包括静电纺丝、微波原位生长及煅烧处理(图10a)。微观结构分析表明,CeO₂紧密嵌入PSNC纳米纤维的孔隙中,有效调控了其微环境特性(图10b、c)。图10d显示元素组成分布均匀,证实了合成方法的有效性。该Ruddlesden-Popper型钙钛矿复合材料在氧还原反应(ORR)中的半波电位为0.78 V,达到10 mA·cm⁻2电流密度所需的过电位(η)为370 mV(图10e、f)。其优异的碱性溶液中双功能ORR/OER性能归因于分级纳米结构、强电子相互作用、氧空位及丰富活性位点的协同作用。当该电催化剂作为空气阴极的双功能ORR/OER活性材料时,组装的锌-空气电池展现出卓越性能,功率密度达161 mW·cm⁻2(图10g),循环寿命超过219小时(图10h)。
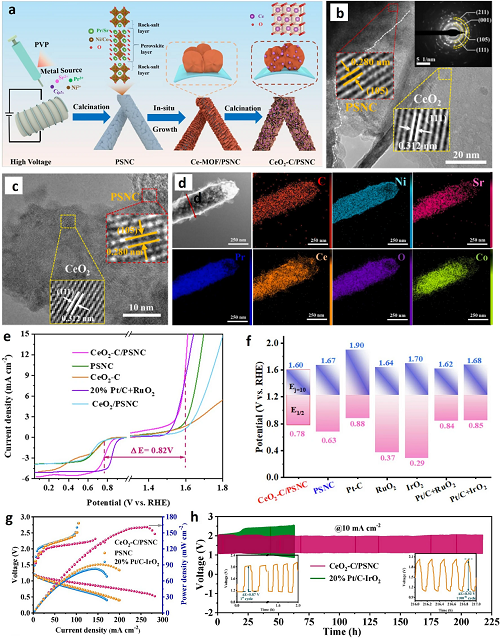
图10. a CeO₂-C/PSNC催化剂合成示意图。b, c 高分辨透射电镜(HRTEM)图像。d 透射电镜-能量色散X射线谱(TEM-EDS)元素分布图。e 双功能电催化性能的线性扫描伏安(LSV)曲线,误差估计为±2 mV。f 以20% Pt/C-IrO₂、CeO₂-C/PSNC和PSNC为阴极催化剂构建的锌-空气电池(ZABs)的充放电极化曲线及功率密度图。g 选定高效催化剂的氧还原反应(ORR)半波电位(E₁/₂)与析氧反应(OER)10 mA cm⁻2电流密度对应电位(Eⱼ=10)的电压间隙柱状图。h 稳定性研究循环曲线。
4.4 无金属碳基双功能催化剂
碳基材料因其优异的电导率、高比表面积及可调控的化学性质,在众多催化应用领域(无论是作为催化剂载体还是直接作为活性材料,如无金属碳材料)备受关注。此外,碳纳米材料的合成原料(如生物质)储量丰富、成本低廉,使其成为大规模应用的经济可行材料。除成本优势外,其化学稳定性及可与杂原子或金属功能化的特性,使其在水电解槽、燃料电池、电池和超级电容器等应用中表现出多功能性和高效性。鉴于金属-空气电池(MABs)对双功能材料的迫切需求,通过在商用碳纳米材料及生物质衍生碳材料中引入杂原子掺杂,可调控其电子结构与表面化学性质,从而赋予其双功能析氧反应(OER)和氧还原反应(ORR)所需的特性。非金属元素(如氮、硫或磷)的掺杂可引入活性位点、促进电荷转移并调节中间产物的吸附能,进而在不添加金属元素的情况下提升ORR和OER等反应的催化活性与选择性。
4.5 金属氮掺杂碳基材料
定制化双功能催化活性材料通过一种简便的一步退火法制备:在Ar/NH₃气氛下,将钴和铁前驱体与碳纳米角进行退火处理(图11a)。所得钴铁氧体@氮掺杂碳纳米角(CoFe₂O₄@N-CNHs)表现出与标准Pt/C催化剂相当的氧还原反应(ORR)电位,且在析氧反应(OER)效率方面优于RuO₂催化剂(图11b)。此外,采用该纳米杂化催化剂的锌-空气电池(ZABs)相较于传统Pt/C-RuO₂体系,展现出更高的循环稳定性和能量密度(图11c、d)。除优异性能外,CoFe₂O₄@N-CNHs-30%杂化催化剂相较于原始N-CNHs和CoFe₂O₄,表现出更佳的稳定性。
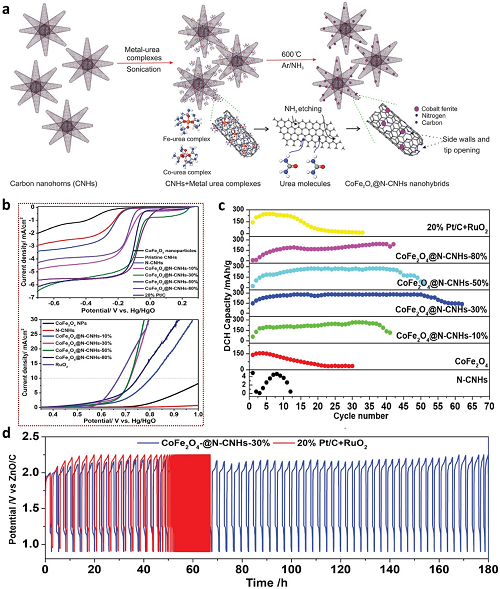
图11. a CoFe₂O₄@N-CNHs制备工艺简化示意图。b 氧还原反应(ORR)与析氧反应(OER)的线性扫描伏安(LSV)曲线。c 比放电容量随循环次数的变化曲线。d 在0.55 mA cm⁻2电流密度(j)下、每循环3 h的充放电循环曲线。
4.6 过渡金属衍生MOF材料
将金属合金衍生催化剂锚定于碳纳米材料(如以金属有机框架材料(MOF)为模板),用于调控双功能催化活性。采用乙酸亚铁辅助法,制备了锚定于氮化碳(NC)基质的铁钴合金催化剂(Co₃Fe₇-NC-OAc)(图12a(i))。Fe与Co的合金化形成了作为氧还原反应(ORR)/析氧反应(OER)活性中心的Co₃Fe₇纳米颗粒。除因乙酸亚铁引入导致孔径扩大(作为气体传输通道)而提升活性外,氮化碳基质与Co₃Fe₇纳米颗粒间的协同电子耦合效应,是进一步增强OER和ORR催化活性的另一关键特征(图12a(ii))。以该MOF衍生合金催化剂作为双功能催化剂时,固态和水系锌-空气电池(ZABs)分别实现了587 mW cm⁻2和193 mW cm⁻2的优异峰值功率密度(图12b-f)。
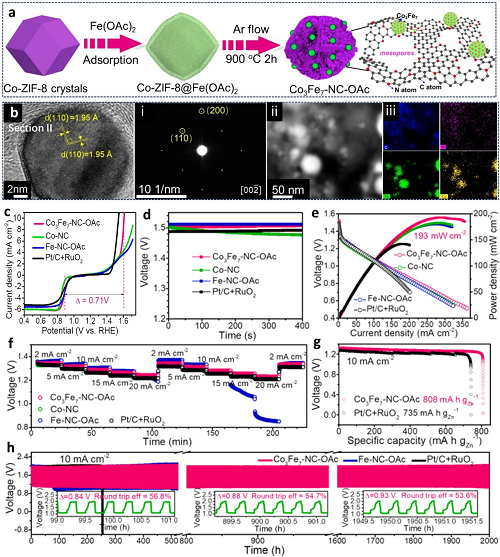
图12. a Co₃Fe₇-NC-OAc合成过程示意图。b 高分辨透射电镜(HRTEM)图像。i) 选区电子衍射(SAED)。ii, iii) 高角环形暗场扫描透射电子显微镜(HAADF-STEM)图像及对应元素分布图。c 双功能催化性能表征。d 开路电压(OCV)曲线。e 放电极化曲线及功率密度图。f 锌-空气电池(ZAB)对比放电曲线。g 比容量。h 恒电流充放电循环测试。
4.7 金属合金和高熵合金
Du等人设计了一种双金属钴-镍合金与氮掺杂碳纳米管(CoNi-NCNT)的杂化材料。其合成采用三步法:首先通过自组装制备催化剂前驱体溶液,随后进行原位生长,最后经煅烧形成杂化结构(图13a)。该催化剂中双金属钴-镍分布均匀,其界面结构微环境通过与碳氮化物的相互作用得以调控,促进了协同效应并提升了导电性(图13b)。详细理论计算表明,CoNi-NCNT界面因CoN₃位点对CoNi合金3d轨道的调制作用,展现出电子导电性增强特性。得益于上述电子结构调控及高比表面积(图13c-f),CoNi-NCNT在析氧反应(OER)和氧还原反应(ORR)中表现出双功能活性,电压间隙(ΔE)仅为0.63 V(图13g)。以该催化剂制备的空气电极锌-空气电池(ZAB)显示出780 mAh g⁻1的优异比容量,且具备800 h的长循环稳定性,而采用RuO₂和Pt/C制备的锌-空气电池循环寿命不足300 h(图13h)。
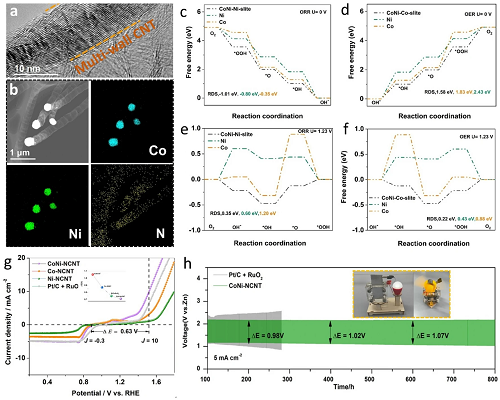
图13. a 碳纳米管(CNT)的高分辨透射电镜(HRTEM)图像。b 钴-镍氮掺杂碳纳米管(CoNi-NCNT)的高角环形暗场扫描透射电子显微镜(HAADF-STEM)图像及钴(Co)、镍(Ni)、氮(N)的对应元素分布图。c, e 电极电位U = 0 V和U = -1.23 V时的氧还原反应(ORR)自由能图。d, f 对应析氧反应(OER)的自由能图。g 氧还原反应(ORR)/析氧反应(OER)的极化曲线。h 5 mA cm⁻2电流密度下的恒电流充放电循环曲线。
V 结论和未来方向
在开发实用型金属-空气电池(MABs)的过程中,研发兼具氧还原反应(ORR)和析氧反应(OER)双功能的电催化剂(ECs),有助于实现更高效的电池设计并减少对稀有原材料的依赖。本综述系统阐述了金属-空气电池的工作原理,重点介绍了基于地球丰产元素的双功能电催化剂的最新研究进展。如前文所述,通过协同优化两类氧反应过程,地球丰产型双功能电催化剂可使金属-空气电池实现更高效率、更长寿命及更优综合性能,甚至超越基于贵金属的电催化剂。尽管双功能电催化剂在金属-空气电池领域已取得显著进展,但其大规模应用仍面临诸多挑战,包括规模化生产技术、原材料与试剂的环境可持续性,以及面向工业应用的成本效益平衡。未来金属-空气电池中电催化剂的实用化关键,在于其长期循环稳定性、与现有阴极设计的兼容性,以及与电池制造工艺的无缝集成能力。
作者简介

Thandavarayan Maiyalagan
本文通讯作者
印度SRM科技学院 副教授
▍主要研究领域
新型材料及其在能源转换与存储设备、电催化剂、燃料电池和生物传感器中的电化学性能。
▍主要研究成果
Thandavarayan Maiyalagan获得印度理工学院马德拉斯分校物理化学博士学位,并在英国纽卡斯尔大学和美国德克萨斯大学奥斯汀分校完成了博士后研究。在Nature Communications、ACS Catalysis、Nanoscale等知名期刊上发表了大量关于能源转换与存储材料创新设计的工作。
▍Email:maiyalat@srmist.edu.in
撰稿:原文作者
编辑:《纳微快报(英文)》编辑部
关于我们

Nano-Micro Letters《纳微快报(英文)》是上海交通大学主办、在Springer Nature开放获取(open-access)出版的学术期刊,主要报道纳米/微米尺度相关的高水平文章(research article, review, communication, perspective, highlight, etc),包括微纳米材料与结构的合成表征与性能及其在能源、催化、环境、传感、电磁波吸收与屏蔽、生物医学等领域的应用研究。已被SCI、EI、PubMed、SCOPUS等数据库收录,2024 JCR IF=36.3,学科排名Q1区前2%,中国科学院期刊分区1区TOP期刊。多次荣获“中国最具国际影响力学术期刊”、“中国高校杰出科技期刊”、“上海市精品科技期刊”等荣誉,2021年荣获“中国出版政府奖期刊奖提名奖”。欢迎关注和投稿。
Web: https://springer.com/40820
E-mail: editor@nmlett.org
Tel: 021-34207624
转载本文请联系原作者获取授权,同时请注明本文来自纳微快报科学网博客。
链接地址:https://wap.sciencenet.cn/blog-3411509-1494625.html?mobile=1
收藏

