今天给大家分享一篇发表在Advanced Science上,题目为 Scutellarin Rescued Mitochondrial Damage through Ameliorating Mitochondrial Glucose Oxidation via the Pdk-Pdc Axis的文章。本文的通讯作者为中国医学科学院药物研究所蒋建东院士和张金兰研究员。
大量研究表明,线粒体在神经退行性疾病中扮演着核心角色。近年来对神经疾病中线粒体异常的研究越来越多,线粒体功能障碍被认为是衰老、阿尔茨海默病(AD)和血管性痴呆(VaD)等神经退行性疾病的最终共同病理机制。这些不同的神经退行性疾病有两个重要特征:运动、感觉和认知系统中的系统性神经元丧失导致认知障碍,如痴呆和运动能力下降;其次,能量代谢变化与神经退行性有关。鉴于神经元组织的有限再生能力,限制神经元损伤和死亡至关重要。由于葡萄糖可用性和线粒体功能缺陷是许多神经退行性疾病的众所周知的标志,因此大脑对能量燃料供应和线粒体功能的变化非常敏感。从代谢变化的角度解释神经损伤,并寻找能够改善线粒体能量供应的治疗方法具有首要意义。
丙酮酸脱氢酶(PDH)复合物(PDC)是线粒体葡萄糖氧化的关键调控酶,可被丙酮酸脱氢酶激酶(PDK)磷酸化。灯盏乙素(Scutellarin,SG)是一种黄酮类葡萄糖醛酸,在心脑血管疾病表现出广泛的药理活性和应用价值。作者前期发现,SG可以调节神经元中的神经递质代谢。而神经递质代谢与神经细胞的能量代谢密切相关。由于神经细胞和脑组织的功能极其依赖于线粒体功能,因此作者深入研究SG在生物能量缺乏模型下对细胞能量代谢的作用。
作者首先在水迷宫实验、氧化应激测试和组织病理分析评估了Scutellarin(SG)对慢性脑缺血模型大鼠海马CA1区域的影响。结果显示,SG处理组与模型组相比,在逃避潜伏期、效应停留时间和目标穿越次数等水迷宫实验指标上表现更好,表明SG能够减轻缺血脑组织中的认知障碍。HE染色显示SG能够改善模型组大鼠海马CA1和纹状体区域的典型神经病理变化。
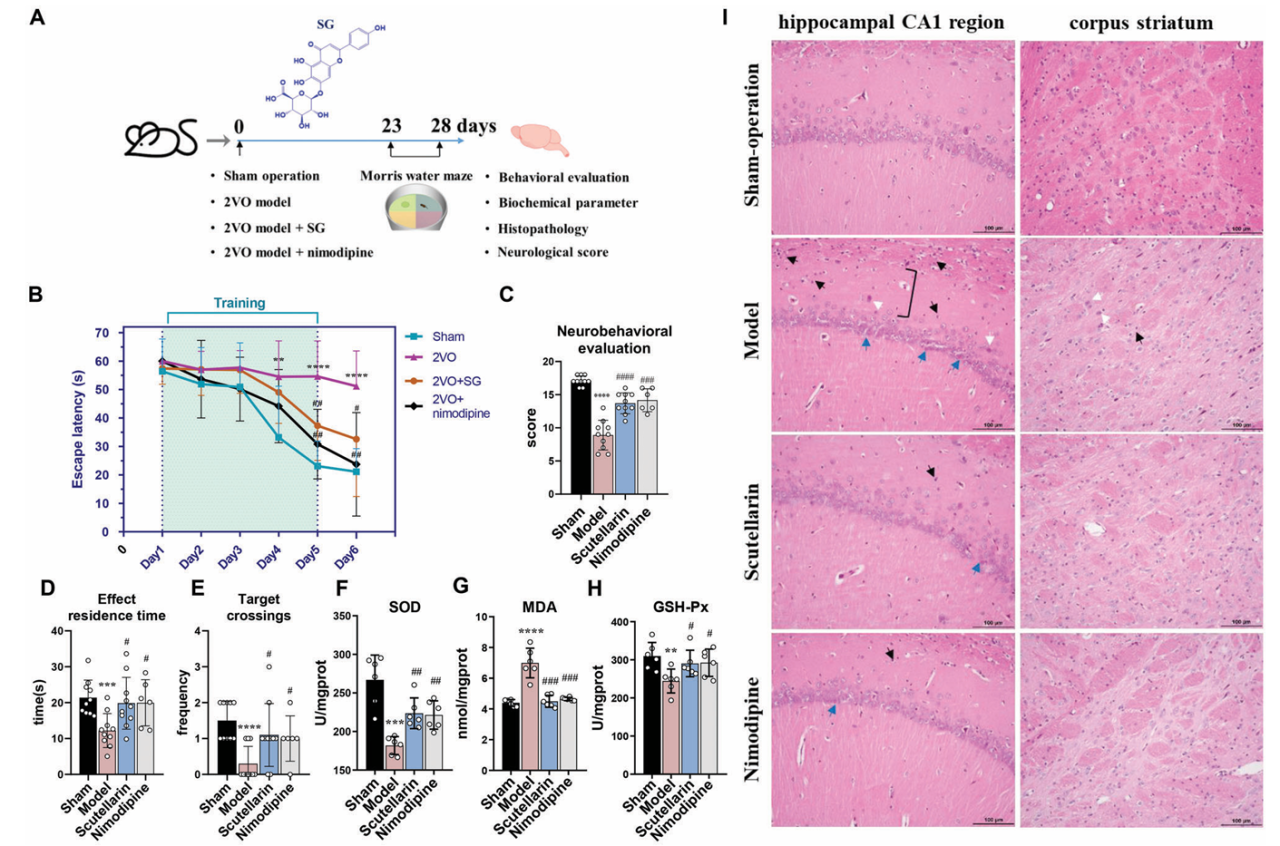
图1. SG可以缓解慢性脑缺血引起的病理变化,改善认知障碍,减轻氧化应激。
由于线粒体在神经能量代谢中发挥着重要作用,作者进一步评估了SG对线粒体ROS水平、Na+-K+ ATP酶和Ca2+-Mg2+ ATP酶活、线粒体通透性转换孔(mPTP)和线粒体内部结构的影响。发现SG处理能够显著降低ROS水平并提高ATP酶活性,恢复mPTP的变化,且改善线粒体肿胀,內嵴断裂等病理现象。
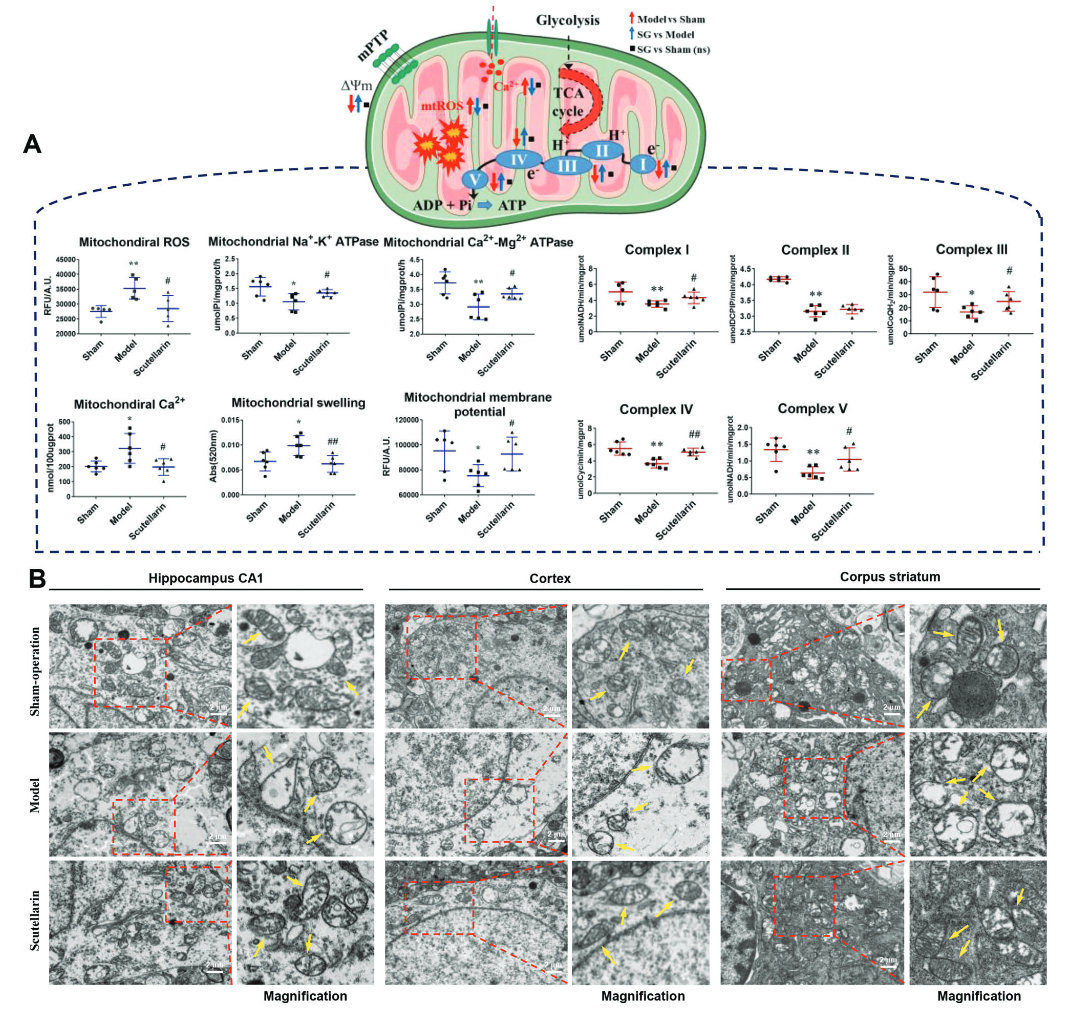
图2. SG改善CCH诱导的线粒体功能障碍
进一步,作者联合利用代谢组学和转录组分析,发现SG能够调节与能量代谢相关的代谢物,如TCA循环中的琥珀酸、苹果酸和草酰乙酸,以及糖酵解中的关键代谢物丙酮酸。线粒体富集纯化的无标记定量蛋白质组学分析显示,SG对线粒体氧化磷酸化(OXPHOS)和三羧酸(TCA)循环产生显著调控。
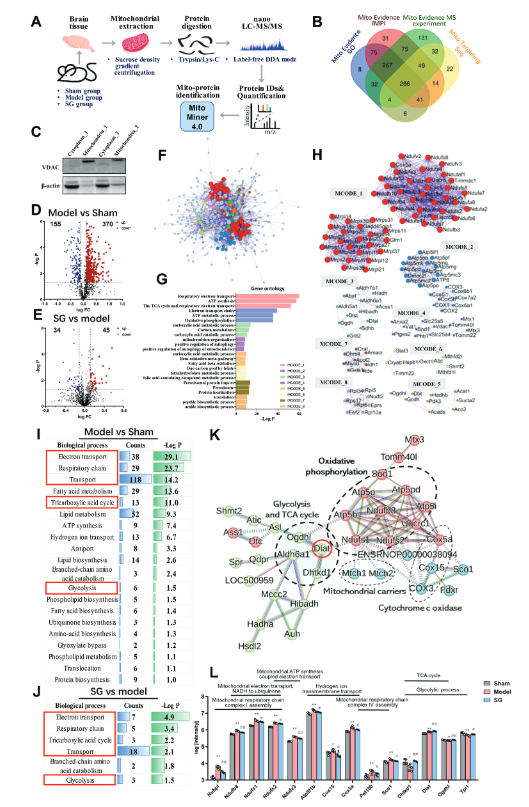
图3. 线粒体蛋白质组学揭示了SG对氧化磷酸化和能量代谢途径的调节作用。
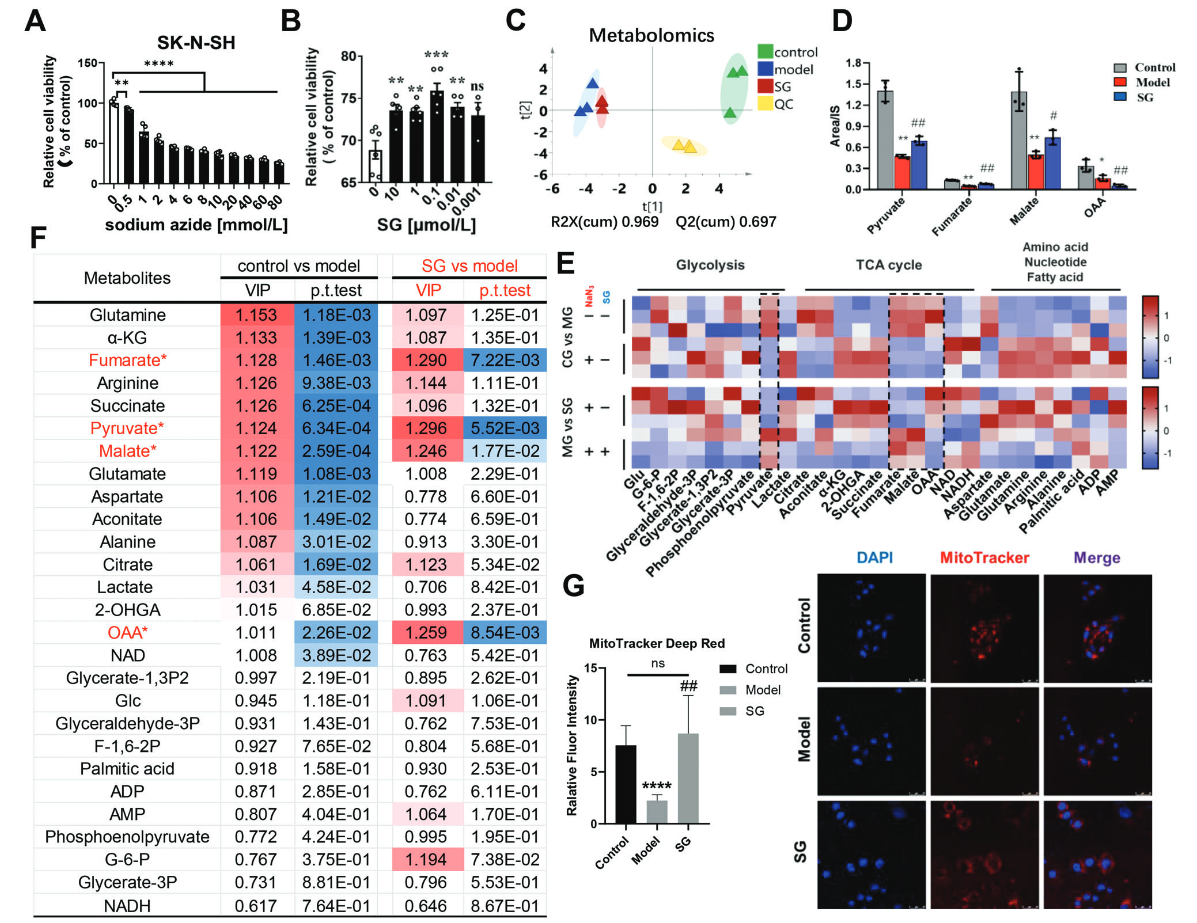
图4. 线粒体的代谢组学和形态学表明,SG在线粒体OXPHOS损伤期间调节丙酮酸代谢相关的糖酵解和TCA循环。
接下来,作者利用Seahorse实验实时测量细胞外酸化率(ECARs)和氧气消耗率(OCRs)评估SG对线粒体有氧呼吸的影响,结果显示SG能够增强基础糖酵解和线粒体呼吸能力。利用[13C6]标记的代谢流实验,证明了SG对糖酵解和TCA循环的影响,发现SG显著增强了[13C3]-丙酮酸代谢流向[13C2]-乙酰辅酶A的通量。
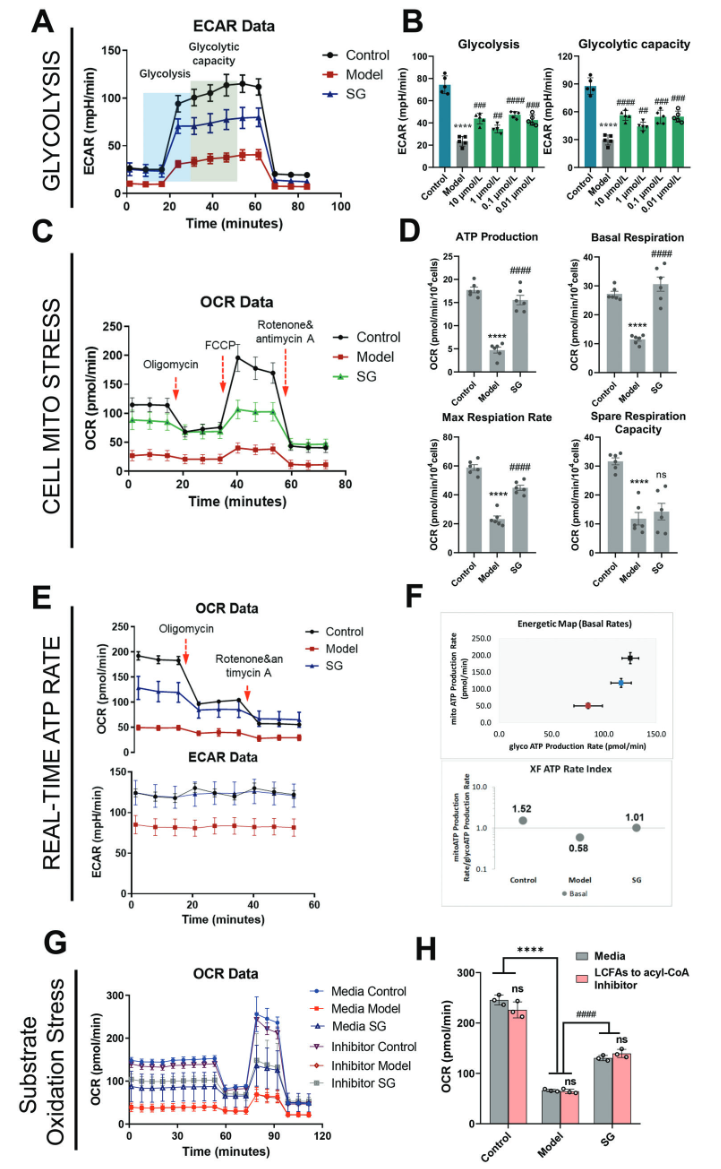
图5. NaN3诱导线粒体OXPHOS损伤和SG对细胞实时ECAR和OCR检测。
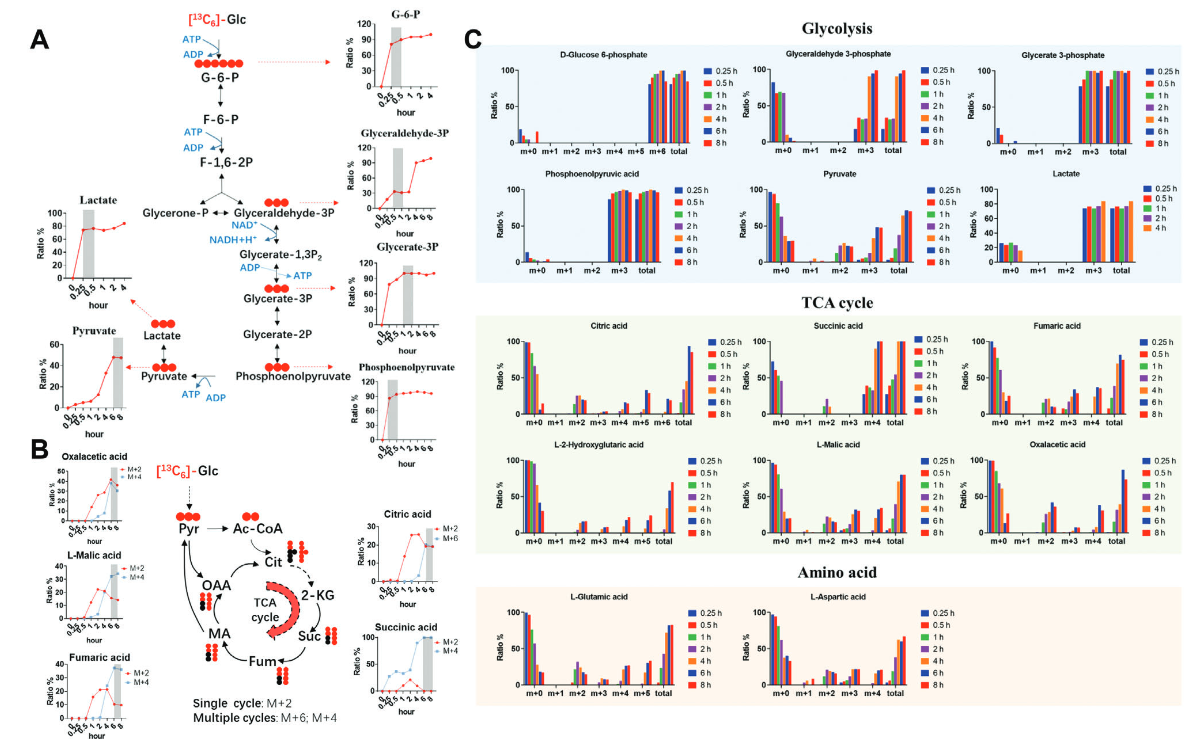
图6. [13C6]-标记的葡萄糖能量代谢途径稳态条件实验。
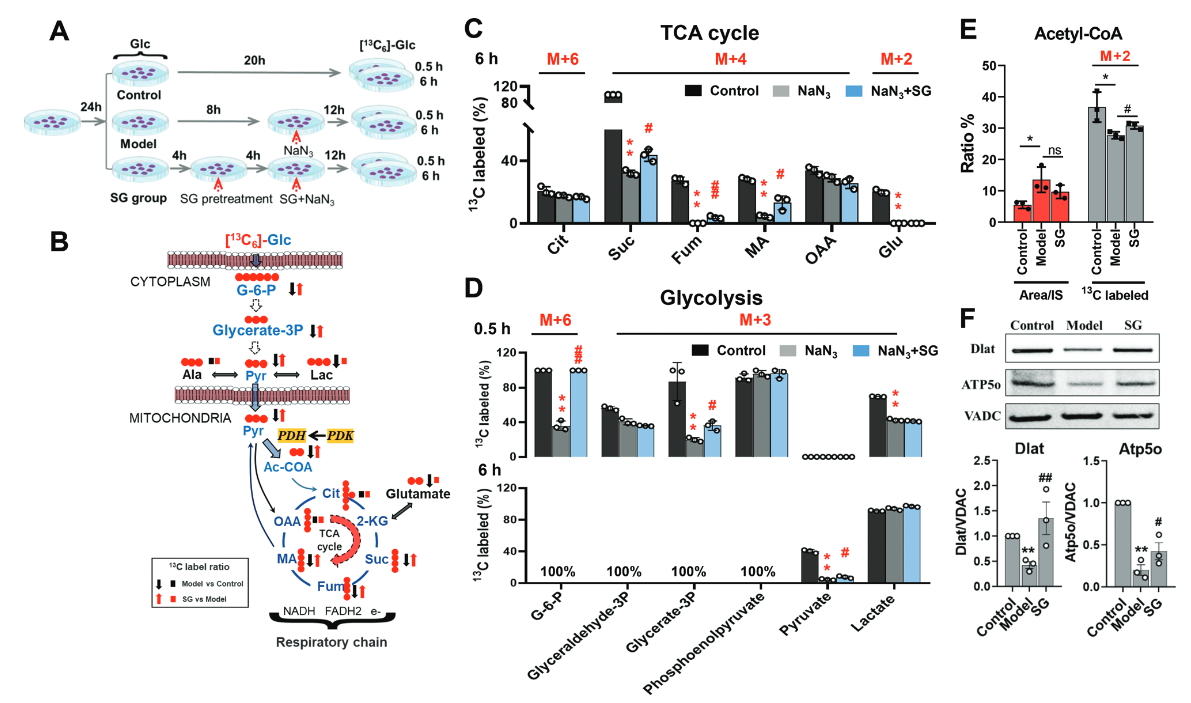
图7. [13C6]-标记的代谢流实验显示,SG可以调节葡萄糖-丙酮酸TCA循环轴相关的丙酮酸代谢。
为了证明SG通过PDK-PDC轴增强线粒体有氧代谢,作者通过激酶活性评估、Docking、co-IP、DARTS和CETSA等实验,证明SG与PDK2的相互作用,并通过抑制PDK2的活性来增强线粒体有氧呼吸。通过蛋白质组学分析和流式细胞术评估了SG对线粒体损伤诱导的细胞凋亡影响,发现SG能够通过靶向PDK2调节线粒体依赖性凋亡。
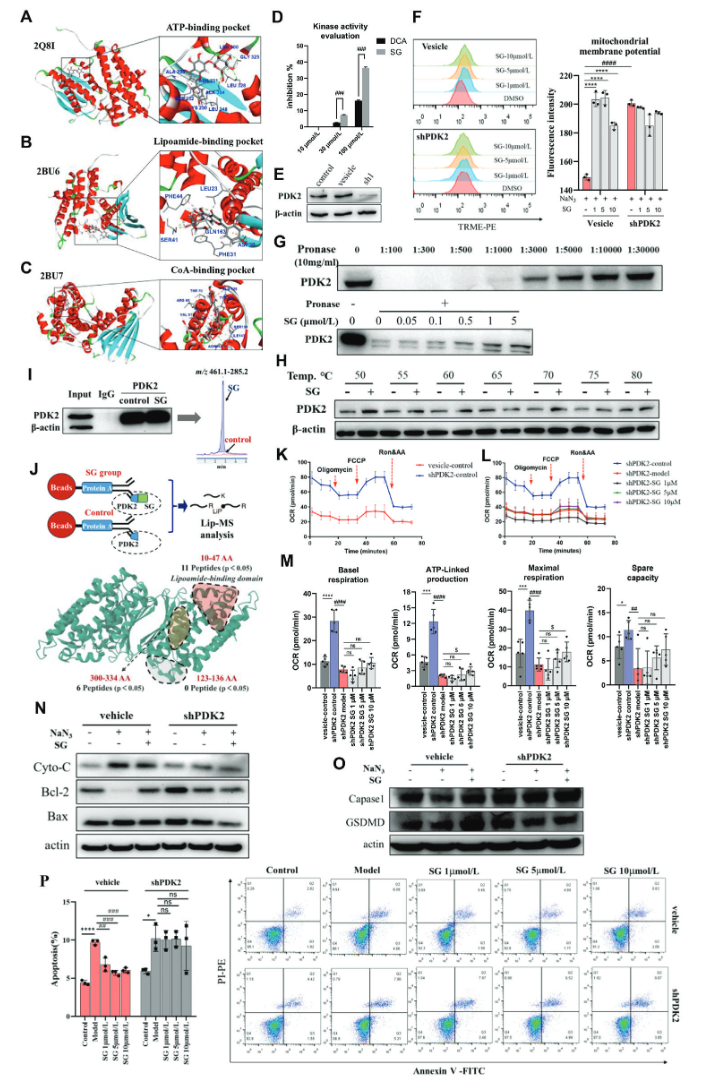
图8. SG通过抑制PDK2作为靶点,促进线粒体有氧呼吸,调节线粒体依赖性凋亡。
这些结果表明,SG通过调节线粒体功能和能量代谢,对慢性脑缺血引起的神经损伤和认知障碍具有保护作用,并且PDK-PDC轴可能是治疗神经系统损伤和认知障碍的潜在药物靶点/通路。
原文链接:
DOI: 10.1002/advs.202303584
转载本文请联系原作者获取授权,同时请注明本文来自Wiley开放科研科学网博客。
链接地址:https://wap.sciencenet.cn/blog-3411312-1469628.html?mobile=1
收藏

