2016年,上海交通大学教授赵立平接受了美国罗格斯大学的橄榄枝,任职该校讲席教授,并牵头组建中美合办的“微生物组与人体健康联合实验室”。
当时,赵立平的博士研究生吴国军很快就要毕业了,计划出国深造。不巧的是,他们开展的一项研究正处于关键时期。赵立平希望和吴国军继续合作,但又不想打乱后者的职业生涯发展规划。于是,赵立平就找吴国军商量,“如果我在美国组建实验室,你是否可以过去做博士后,继续深入目前的课题”,吴国军同意了。
8年后,他们找到了肠道菌群中维持人体健康必不可少的“核心菌群”。10月8日,这对师徒通力合作的又一项研究在Cell上线,这也是他们共事的第12年。
 Cell论文截图
Cell论文截图
中国科学院院士赵国屏评价此项研究:“成功将原本难以量化的微生态系统转化为可定量分析的网络结构,标志着从基于传统分类学的‘菌株代谢’鉴定分析到基于生态学的‘核心菌群’功能动态分析。这既是微生态理论的重大突破,也是微生物组研究方法上的重大创新。”
十余年来,越来越多证据表明,肠道菌群不仅参与人体消化系统的正常功能,还在维持健康中起着关键作用。
一方面,将健康人的肠道菌群通过粪菌移植(FMT)移植给患者,能够缓解多种疾病的症状;另一方面,将糖尿病等患者的肠道菌群移植给无菌的小鼠,小鼠很快就会得相应的病。这些结果表明,肠道菌群作为一个“器官”,与疾病的发生发展有因果关系。
然而,各类论文呈井喷式增长的同时,围绕肠道菌群的争议也时常出现。如2019年,美国一位血液疾病患者在经FMT治疗后,因为感染捐赠者粪便中的多重耐药大肠杆菌而死亡,美国食品药品监督管理局也因此紧急叫停了一系列相关临床试验。
究其原因,在于肠道菌群研究仍缺乏一块重要拼图——人体内存在的上千种细菌中,到底哪些细菌起到了核心作用,它们又是如何影响生命健康的?
维持人体健康必不可少的所有细菌被统称为“核心菌群”。“寻找核心菌群就是肠道菌群研究‘皇冠上的明珠’,是领域中所有人都在追寻的目标。”赵立平介绍。
此次,赵立平团队正是在核心菌群成员的鉴定上取得突破。他们将目光聚焦在经过各种环境变化的扰动后,仍能稳定地保持协作或竞争关系的细菌功能群上。
基于这个思路,赵立平团队利用吴国军牵头研发的高分辨率的菌群测序大数据分析技术,开始找寻“皇冠上的明珠”。这种技术的核心是把每一种细菌的高质量的基因组组装出来,简称HQMAGs。
值得一提的是,HQMAGs不依赖于现有数据库。即便是目前知之甚少的未知细菌,也可以通过追踪其基因组序列来研究它们的生态行为及其对人体健康的影响。同时,该方法分辨率极高,可以将细菌的识别精确到接近菌株的水平。
结果让赵立平惊喜但又不敢相信:“我们在各个环节反复验证了很多次,才最终确定,我们真的找到了核心菌群。”
 赵立平
赵立平
赵立平团队先是将营养干预作为一种环境扰动,对2型糖尿病患者进行高膳食纤维饮食的干预,并对干预前、干预后及一年后随访的3个时间点的粪便样本进行了菌群网络分析。团队筛选得到141株细菌,这些细菌构成了2个“相互竞争的功能群”。
其中一个功能群对健康有益,团队将之定义为“基石功能群”。这些细菌通过产生短链脂肪酸酸化肠道环境,从而抑制机会性致病菌的过度生长。赵立平将它们比喻为“大树菌”。只有“大树菌”占据主导地位,肠道的微生态系统才能像茂密的森林一样保持稳定。
另一个功能群则由机会性致病菌构成。它们携带几乎所有已知类型的抗药性基因和毒力因子基因,被命名为“病生功能群”。这类细菌在数量较低时对维持人体免疫系统的正常功能必不可少,其数量失控后则对人体有害。
而后,赵立平团队在不同疾病、不同地域、不同种族的人群中,都发现了同样的规律。在这两个功能群内部,细菌之间保持着稳定的协作关系,类似于“铁哥们儿”;而这两个功能群之间则维持着稳定的竞争关系,类似于“死对头”。
这是一个类似于“跷跷板”的网络结构模型,通过“你升我降”影响人体健康:在健康人群中,“基石功能群”占据绝对优势;而在患有某些疾病的人群中,“病生功能群”的数量变多了。
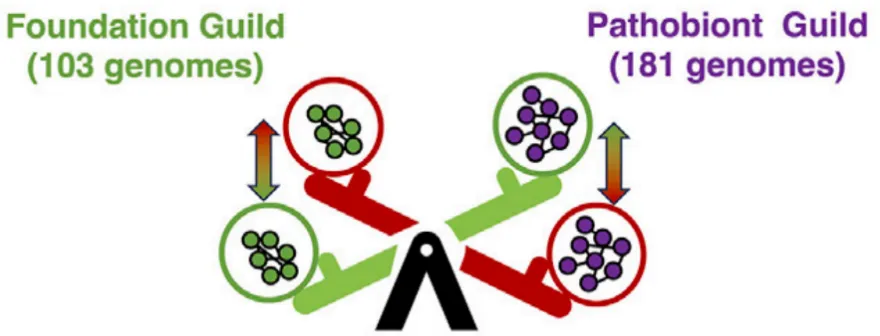 “跷跷板”模型图示
“跷跷板”模型图示
这套分析方法可以准确预测多种疾病的免疫疗法效果,并对每个人的菌群“跷跷板”进行精准的个性化检测,确保在FMT时“对症补菌”。
值得一提的是,以往肠道菌群领域无法达成共识的结论,也有了新的解释。“不同实验室研究同一种细菌和某个疾病的关系,能够分别得出正相关、不相关和负相关3种结论,原因是分辨率太低而且未考虑细菌和细菌之间的关系。将这些研究纳入‘跷跷板’模型的框架下,能够得到更为统一的结论。”赵立平表示。
“从2006年开始,我们实验室大概每五年左右能够完成一项重要研究。我认为论文的水平足够的,就会投给Nature,但每次都会卡在同行评议环节。”赵立平告诉《中国科学报》。
比如团队2018年上线的一项研究中发现,通过摄入多样化的膳食纤维,可使肠道内特定的有益生态功能菌群增多,促进胰岛素分泌、提高胰岛素敏感性,进而改善2型糖尿病。他们最初把论文投给Nature,但被审稿人“批糊涂”了,修改之后改投Science,半年后论文上线。
此次,故事还在重复。两年前,团队已经在糖尿病患者中找到2个稳定的功能群,并在十余种疾病的宏基因组原始测序数据中进行了验证。赵立平把论文发给Nature编辑部后,却再一次败兴而归。
“审稿人的意见中有一些不合理的地方。但我们都认为是自己没有把论文打磨得足够完美,才导致他们产生这些误解。”赵立平说道。
就这样,团队在原有实验基础上,构建了一个涵盖三大洲、涉及15种疾病的26项病例-对照研究的“超级数据集”。数据集中共包含1780名患者和1604名对照人群。他们最终得出结论:这个通用的“跷跷板”模型是一个不受地域、种族和病种限制的人类核心菌群模型。
“我们心里非常踏实,因为有扎实的实验和数据支撑我们的结论。”此时,整篇论文内容已经远超Nature的体量,赵立平考虑之后,把论文投给了Cell。
第一轮审稿后,团队又花费4个月时间,结合审稿人的意见修改论文,写了近50页的回复信。3名审稿人在收到邮件的第二天,都表示同意发表。最终论文顺利被Cell接收。
赵立平补充:“我们原来的题目是‘稳定的关系可以帮助找到核心菌群’。Cell的编辑认为我们已经找到了核心菌群,改成了现在的标题‘一种可作为健康指征的核心菌群特征’。”
为什么会想到将“稳定的关系”作为突破口?赵立平直言,他从二十年前就开始为这个问题做准备。
2004年,对赵立平而言是个特殊的年份。这一年,他第一篇关于肠道菌群的论文发表于Journal of Microbiological Methods。这项研究中开发了一个用基因组片段识别和追踪健康人类肠道中常见菌群的方法。
也是在2004年,我国最早开展系统生物学研究的科学家之一、中国工程院院士杨胜利提议,由中国科学院上海生命科学研究院和上海交通大学合作,组建系统生物学研究所。不久后,中国科学院院士陈竺提出了系统生物医学的概念。在陈竺的推动下,上海第二医科大学(上海交通大学医学院前身)和上海交通大学联合成立“上海系统生物医学研究中心”。
赵立平作为常务副主任主持了研究中心的筹备工作,在此过程中得以接触最前沿的系统生物学知识和研究进展,并与系统生物学的创始人之一Lee Hood、代谢组学创始人之一Jeremy Nicholson等专家有了密切接触和合作的机会。这段经历也使赵立平养成了从复杂系统的角度进行菌群研究的习惯。
此前,赵立平是国内微生物污水处理领域走在前列的科学家,但他以破釜沉舟的勇气,将方向完全转向彼时十分小众的肠道菌群研究。
由于赵立平完全放弃了申请原本优势的项目,最初的几年十分艰难,实验室一度因为经费短缺而面临关闭的危机。赵立平回忆:“因为有好几项指标都没有完成,学院年终总结汇报的时候,感觉像是被放在火上烤一样。”
但抱着“肠道菌群研究一定会大有可为”的信心,赵立平带领团队,咬牙挺过了最艰难的时光。
2005年底在巴黎举行的人类微生物组圆桌会议宣布:组织全球的力量开展“国际人类微生物组计划”。法国国家农业食品与环境研究院牵头的欧盟肠道菌群研究计划、美国国立卫生研究院(NIH)宣布启动的“人类微生物组计划”,以及中法肠道元基因组合作研究等项目都加入“国际人类微生物组研究联盟”,通过对人体内的微生物进行测序,解析菌群结构变化对人类健康的影响。
2010年之后,二代测序技术迅速发展普及,新技术和新方法的涌现使得肠道菌群研究迎来了春天,并迅速进入火热的夏天。
此时,赵立平已经完全将研究方向转到肠道菌群领域。更为重要的是,赵立平在上世纪90年代,就意识到测序技术以及生物信息学将是微生物研究的重要工具。转型的那几年,他们就在实验室搭建起高分辨率的测序和分析平台,并引入了机器学习等技术。
同时,赵立平注重将系统论、信息论、控制论等系统生物学的理念,同肠道菌群的研究相结合,他也因此形容自己是“被系统生物学思想武装起来的微生物学家”。
到2012年,赵立平实验室已经积累了大量肠道菌群宏基因组测序数据,他开始物色合适的学生从事数据分析等工作。本科为生物信息学专业的吴国军联系赵立平,希望在他实验室读博,这对师徒的缘分就此开启。
吴国军阅读了大量文献,综合国际上所有常规的数据分析方法,并创新性地引入高分辨率的方法,在实验室搭建起HQMAGs技术平台。不论是2018年的Science,还是今年的Cell,这套体系都发挥了重要作用。
 赵立平和吴国军在探讨高分辨率菌群分析技术
赵立平和吴国军在探讨高分辨率菌群分析技术
“要培养能够自主创新的科学家,必须首先让他在某一个方向深耕十年以上。”赵立平认为,对年轻科学家而言,在原有研究初步取得一定成绩的情况下,转换到一个新的方向从头开始,不利于个人的长期发展。因此,当吴国军考虑博士毕业后的去向时,为了满足他在国外做博士后的要求,赵立平欣然接受了罗格斯大学的职位。
现如今,吴国军已是罗格斯大学的一名研究助理教授。“如果不是把系统生物学的思想和原理用在寻找核心菌群上,如果不是我和吴国军密切合作了12年,很难会有今天的突破。”赵立平强调。
最近几年,赵立平的名字持续出现在“高被引学者”名单中。回顾过去二十年的科研生涯,赵立平感慨:“我们是从肠道菌群几乎无人问津的时候开始做的,然后看着它逐渐走向舞台中央。从我们实验室发展来说,也在不断取得阶段性的成果,就像爬楼梯一样,锚定了一个目标,然后一步一步慢慢向上,不断取得进步。”
他们依然在向着更高处攀登。接下来,赵立平团队将以“基石功能群”为靶点,开发一系列可以在临床上实际运用的检测和治疗方案,并在不同疾病中证明其效果,真正为患者带来福音。
“我们从来都不认为肠道菌群能够包治百病,而是在病人接受治疗的时候,把他们的肠道菌群调理好,让他们能够获得更好的治疗效果和生活质量。”赵立平的梦想是,通过恢复“大树菌”的生态优势地位,恢复肠道中的微生物的“森林”系统,至少让全世界1000万患者重获健康。
相关论文信息:
http://doi.org/10.1016/j.cell.2024.09.019
*本文图片均由受访者提供

