文 | 《中国科学报》见习记者 江庆龄
“目前由于没有已发表的文章,简历比较寒酸简洁,所以把我毕业答辩的PDF附上了,希望徐老师能给一次面试的机会。”2022年5月末,张衡给中国科学院上海药物研究所(以下简称上海药物所)研究员徐华强发了一封申请博后的邮件。摁下发送键的那一刻,张衡内心有些忐忑,因为他博士期间的工作还未整理成论文发表——尽管他为了这个课题,花了6年时间才毕业。
“Thank you for your interest in our lab. We should arrange a lab meeting for you to presentation Next Tuesday, 6:30PM.”(谢谢你对我们实验室感兴趣。我们安排下周二晚上6:30的实验室会议,请你做报告。)张衡很快收到了徐华强的答复。面试很顺利,张衡加入了徐华强课题组。
2024年5月15日,张衡作为共同一作,在《自然》发表了人生中的第一篇论文。这项由上海药物所徐华强课题组、杨德华课题组和临港实验室蒋轶课题组合作完成的工作,在研究去甲肾上腺素转运体(NET)的过程中,首次在近原子分辨率上发现了由胆固醇和脂质介导的膜蛋白同源二聚体形成机制,为细胞膜“脂筏模型”提供了眼见为实的依据。

《自然》论文截图
意外为27年前的假说提供了依据
人们很早以前就知道,细胞膜不仅为细胞提供了一个相对独立的空间,也是其同外界沟通联系的窗口。在由磷脂双分子层构成的细胞膜上,分布着多种多样的蛋白,这些蛋白起到了“邮递员”的作用,维持着细胞和外界环境之间的交流。
这些“邮递员”是如何在高度流动的细胞膜上工作的?1997年,芬兰学者Kai Simons和Elina Ikonen提出“脂筏模型”,即细胞膜上存在一些结构致密、流动性较低的区域,这些区域由特殊的脂质形成,就像漂浮在水面上的竹筏一样,其内聚集着一些可以传递物质的特殊蛋白质。
尽管有越来越多的证据证实了“脂筏模型”的准确性,但以往的研究手段均未能直接观察到这一结构,依然有人发出疑问:“脂筏”真的存在吗?
“90后”张衡在探索跨膜蛋白结构的药理学意义时,意外为这个问题提供了一些参考。
之前报道的真核神经递质-钠协同转运体(NSS)蛋白都为单体形式,张衡在冷冻电镜单颗粒数据处理过程中,发现NET大多“成双成对”,两两错位相依,一开始以为是人工(artificial)的结果,后来通过不同的样品制备方式发现,NET都呈现二聚体的形式。不同于常见的由蛋白-蛋白相互作用形成的多聚体膜蛋白,张衡观察到的二聚体结构呈现出由胆固醇和脂质分子介导的“汉堡模型”——两个NET单体组成了汉堡的“面包”,不同的脂质分子则构成了中间的“菜”和“肉”。
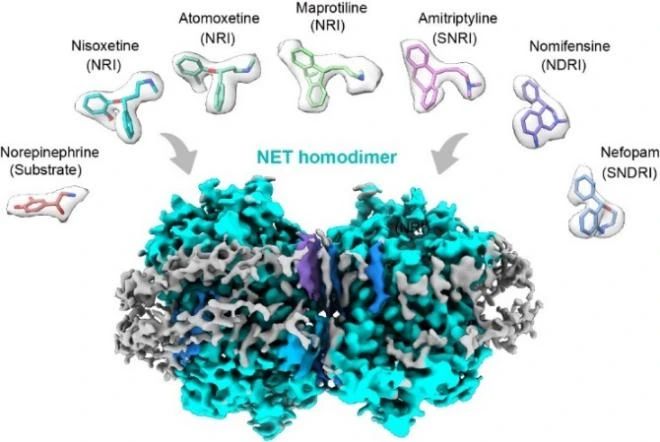
人源NET二聚体分别与底物和六种抗抑郁药物复合物的代表性结构
致密排列的脂质分子、依赖脂质的蛋白质,很好地契合了“脂筏模型”的定义。进一步,团队利用单颗粒冷冻电镜技术,获得了人源NET同源二聚体分别与底物结合、无底物结合,分别与6种抗抑郁药物结合共8个高分辨率结构。
生化细胞实验证实,较单体结构,NET二聚体结构能更为高效地转运神经递质。此外,与不同的抗抑郁药物结合时,NET展现出与其他转运体的明显差异,如马普替林对NET的亲和力是血清素转运体的520倍,而尼索西汀对NET的亲和力是多巴胺转运体的576倍。这些发现为抗抑郁药物研发提供了重要的结构基础和药物设计参考。
2023年教师节这天,他们完成了论文,投稿给《自然》编辑部。今年5月15日,论文正式上线。
“编辑和审稿人都对我们观察到的类似‘脂筏’的二聚体结构非常感兴趣。”张衡补充,“但是我们得到的类似‘脂筏’结构还不够大,偏向于人为模拟的状态,我们后面在尝试做更大的、更接近自然状态的‘脂筏’结构。”

提供给《自然》编辑部的候选科学插图,Zihao Li设计,蝴蝶意象由崔娜娜提供。(蝴蝶兰象征NET 同源二聚体,白色花瓣暗指 NET单体。中间的黄色唇瓣代替胆固醇和脂质分子。落在花朵上的蝴蝶象征选择性靶向药物,蝴蝶翅膀装饰着抗抑郁药物的化学结构。)
“转运”的转运体研究
NET属于单胺类转运体(MATs)家族,与同家族的血清素转运体(SERT)和多巴胺转运体(DAT)共同调控神经突触神经递质的浓度,维持体内神经递质的平衡。其中NET能够把过多的去甲肾上腺素和多巴胺进行回收,防止人们长期处于亢奋状态。
由于其在神经递质传递中的重要作用,MATs是精神刺激剂和抗抑郁药物的主要靶点。在过去的近70年,MATs与抑郁症病理学的关联从药理学、遗传学、分子生物学和临床研究等多个角度被证实,单胺假说也曾主导了近几十年抗抑郁药物的研发。
诸多研究表明,NET的功能异常同多种精神疾病相关,如抑郁症、焦虑症、注意缺陷多动障碍和帕金森病等。
“我博士期间的课题和转运体相关,做一个转运体的结构是我的个人愿望,蒋轶老师通过徐老师问我有没有意愿一起做神经递质相关的转运体,我们一拍即合。”张衡告诉《中国科学报》。
然而,徐华强团队以往并不关注转运体,这几乎是一个“从头开始”的项目。值得一提的是,从确定选题到论文上线,仅耗时15个月。当被问及实验何以如此迅速推进时,徐华强总结了3个原因。
首先是张衡“心灵手巧”。
NET是一类高度动态化的跨膜蛋白,一共有12个疏水跨膜结构域,包含了底物结合区域、外向通道和内向通道,在运输神经递质的过程中,涉及细胞膜内外通道的交替开放。同时,蛋白膜内外的区域都很少,难以利用以往的方法对其进行定位。再加上在前期样品处理的过程中,涉及把蛋白从细胞膜上分离的步骤,很容易丢失重要的信息。
为此,张衡引入了脂质纳米盘的方法。纳米盘是由磷脂和膜支架蛋白颗粒组装而成的盘状磷脂双分子层,可以模拟天然的磷脂双分子层膜环境。在纳米盘的环境中,NET的二聚体结构清晰可见。
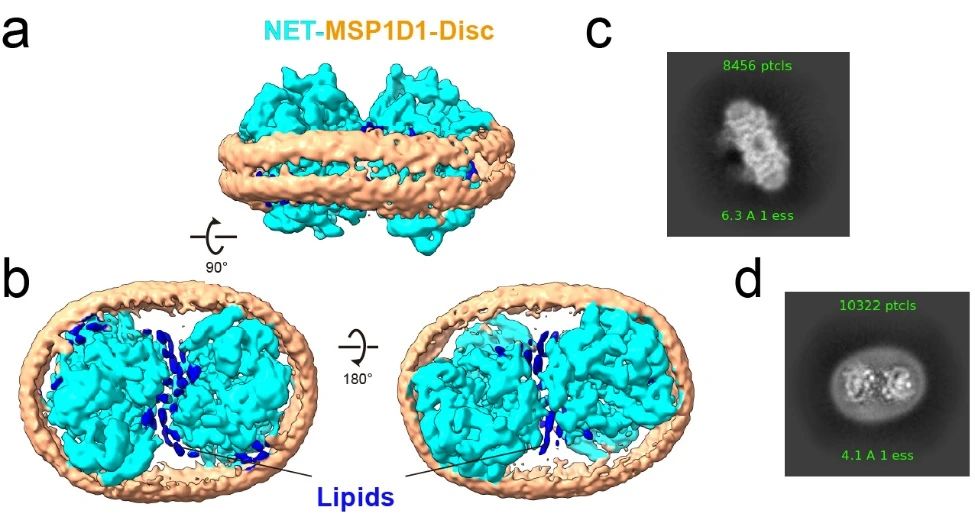
NET二聚体结构
其次是实验室前期在基础研究和技术方面的积累。
徐华强团队长期致力于神经递质受体的结构与功能研究。2013年以来,先后在5-羟色胺受体、多巴胺受体、阿片受体等系列受体的结构和识别机制等方面取得了系列进展。
实验室也相对应地发展了新技术。比如这项研究中,文章共同一作、蒋轶课题组在站博士后殷裕玲通过NanoBiT交联技术(俗称“纳米钩”),进一步验证了NET在细胞膜上倾向于形成同源二聚体结构。这项技术的发明者为徐华强的博士研究生——现已成为上海药物所研究员的段佳。
最后,有非常“给力”的合作伙伴。
第一次投稿之后,几位审稿人都建议团队补充转运体和药物之间结合力的实验,从而更直观地描述药物对不同转运体亲和力的差异。
“我们一开始采用了一种间接测量结合力的方法,但整整两个月时间没有拿到令人满意的数据。”张衡回忆,“后来我们联系了杨德华老师,他们利用放射性同位素标记技术,一个月时间我们就整理修回了。”
“结构生物学的竞争非常激烈,所以必须充分利用好实验室和研究所的平台。”徐华强补充,“我相信通过这段经历,张衡能够更为深刻地理解找寻能够‘强强联合’的合作者,也是科学研究的重要组成部分。”
开辟实验室新方向
目前徐华强团队围绕转运体,开展了一些与结构药理学相关的工作。
“我其实一开始没想到张衡可以把NET的结构做出来,可以说是超出了我的预期。”在徐华强看来,张衡是一个很有主见、能够自主开展选题的学生。“我们实验室原来主要做的是GPCR,张衡加入后也开始关注转运体。他给实验室开辟了一个很好的方向。”

参与工作的部分人员,从左到右分别为张超、代安涛、杨德华、徐华强、张衡、吴灿荣、胡雯。
徐华强团队的成员展现出一些共性——想要把事情做好的自我内驱力、不惧困难的自信。
“徐老师会给我们自由探索的空间,也会站在我们的角度帮我们克服科研中的困难。”张衡感慨,尽管加入课题组的时间不算很长,在实验室整体氛围的影响下,他能够更加专注于科研本身。同时徐华强极强的执行力,也带动着实验室的每个人前进。
潜移默化间,张衡的行动力也提高了。如今他正迎来阶段性的“收获期”,除了刚刚上线的《自然》论文,多个课题组合作的基于单胺类转运体结构设计的小分子化合物研究正在整理结果,另有一篇文章已经投稿。
“上海药物所在神经药理领域有非常好的积淀,我们实验室也做了系列中枢神经递质相关受体的工作。张衡以及其他的学生独立之后,如果对这些科学问题感兴趣,我也很期待他们开展下一代药物分子研究,把研究所在神经系统疾病领域的传统延续下去。”徐华强相信,互相尊重、自由探索的实验室文化,也可以同科学探索一样,继续传递下去。
相关论文信息:
https://www.nature.com/articles/s41586-024-07437-6

