博文
Nat Biotechnol前沿:个体化磷酸修饰组学,精准识别关键功能性磷酸化特征
|
蛋白质磷酸化是生物最普遍,也是最重要的蛋白翻译后修饰类型之一。在细胞中磷酸化动态地整合环境和细胞信息来调控生命过程。生物体受到干扰后,会有数千个磷酸化位点受到调节。在全局范围内识别出其中的关键功能性磷酸化位点及蛋白,是信号转导研究面临的最大挑战之一。
2021年12月2日,Nature系列顶尖刊物Nature Biotechnology发表了一项关于“个体化磷酸蛋白质组学研究”成果。澳大利亚科学院院士,悉尼大学查尔斯珀金斯中心生物学领域的领军人物David E. James、Sean J. Humphrey以及丹麦哥本哈根大学 Jørgen F. P. Wojtaszewski 研究团队共同合作开发出个体化磷酸蛋白质组学方案(Personalized phosphoproteomics),可用来鉴定复杂生物学背景下的功能性磷酸化信号。

该方案测量个体的磷酸化蛋白质组对干预措施的反应,同时测量相应的表型,利用人类表型差异将信号转导与生物功能联系起来,精确识别关键的功能性磷酸化信号。此方法成功应用于研究运动和胰岛素对肌肉葡萄糖代谢的相互作用,揭示了运动如何增强人类骨骼肌中的胰岛素信号传导及其过程中的关键机制。
研究理论框架与实验工作流程设计
研究人员基于个体间信号网络的差异或可确定对生物表型贡献最大的磷酸化的推测,首先建立了功能相关信号识别的理论框架。即通过在干预期间同时对个体进行纵向磷酸化修饰组分析和表型记录,从而将每个受试者的磷酸化动态变化与这些表型相关联(图1a)。如果表型类型反映了相关的生物学过程,如骨骼肌对葡萄糖的摄取,那么所观察到的表型差异的磷酸化位点即是与该生物学过程最密切相关的位点。

图1 磷酸蛋白质组保留独特的受试者特异性特征
基于以上理论框架,研究人员进行了精巧的实验工作流程的设计,以探讨运动如何在信号转导水平上影响胰岛素对晚期糖代谢的影响(图1b)。研究选取了未经训练的健康受试者(n=5),受试者都是年龄、体重指数和体质相似的年轻健康男性。首先进行2.5h的单腿膝伸肌运动,以增强肌肉胰岛素敏感性,运动后恢复4小时,对运动和休息的腿部进行肌肉活检。然后进行2小时高胰岛素-正葡萄糖钳夹技术处理来量化胰岛素敏感性。在钳夹期间,同时测量运动和休息腿部的动静脉血糖浓度差异,以量化活检肌肉的葡萄糖摄取量。钳夹后,再次对每条腿的肌肉进行活检。最后,对活检组织样本(n=20),采用基于质谱的磷酸化修饰组学技术进行定量分析,同时测量基态的匹配蛋白质组数据以作归一化分析。研究总共定量到2,776蛋白上的大于11000 个磷酸化修饰位点。
磷酸化修饰组的个体特异性差异
对磷酸化修饰组数据的层次聚类和主成分分析(PCA)表明,属于同一受试者的磷酸化修饰组组聚集得最紧密,即使在通过运动和胰岛素的组别中(图2a,b)。这表明从不同个体取样的相同组织的磷酸化蛋白质组具有独特的特征,其方式类似于大脑不同区域具有不同磷酸化组特征。磷酸化蛋白质组的这一受试者特异性部分反映了个体间信号结构的内在差异。
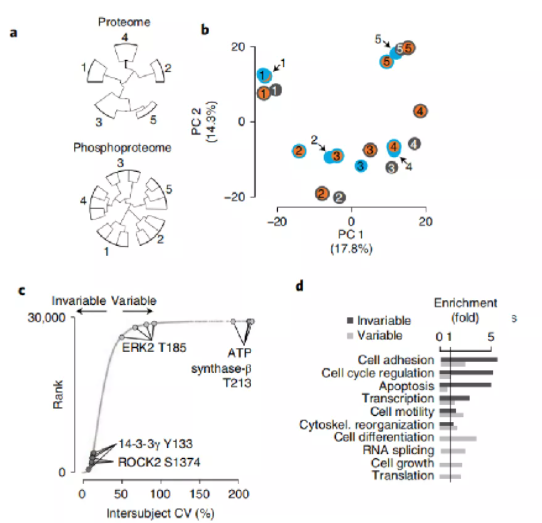
图2 磷酸化修饰组的个体特异性差异
研究人员将将“不变”磷酸化位点定义为受试者之间一致的磷位点(最大受试者间变异系数CV ≤ 15%),而“可变”磷位点则是受试者之间存在不同(任何受试者之间的CV >75%)。结果表明个体间恒定的磷酸化位点富含细胞周期和凋亡调节磷酸化位点 (图2c,d)。ROCK2蛋白磷酸化位点S1374的水平保持不变,表明激酶活性平衡蛋白表达受到严格调控。此外,在与所有受试者中位数相差>1.5倍的磷酸化位点中,只有13%的匹配蛋白质在同一方向上相差>1.5倍。表明磷酸化蛋白质组的受试者特异性与蛋白质丰度的变化无关。
运动与胰岛素信号的关联

为了精确定位与肌肉葡萄糖摄取有关的关键磷酸化修饰靶点,研究人员采用了严格的标准对磷酸化位点和表型之间的成对相关性进行分析。个体化磷酸修饰组学分析鉴定出与葡萄糖摄取显著相关的功能性磷酸位点,其功能富集度(18.6%)比所有差异磷酸位点(7.1%)高2.6倍(图4a)。功能性磷酸化位点的富集程度超过了单一的显著性截止值,也超过了许多潜在磷酸化位点功能的值(图4b)。
鉴定结果中包含许多已被报道与葡萄糖代谢有关的蛋白质上的磷酸化位点,及更多的未被报道的磷酸化位点,代表了适合进一步研究的候选位点。事实上,其中83%(>100)的葡萄糖摄取相关的磷酸化修饰还没有报道的上游激酶(图4c)。识别葡萄糖摄取相关磷酸位点的同源激酶可能指向剩余非特征磷酸位点的调节子。例如,在葡萄糖摄取相关磷酸位点中,研究人员观察到许多已知的激酶mTOR底物(图4d),并进一步揭示了 mTOR 和 AMPK 之间的合作关系,mTOR 能够直接磷酸化 AMPK 的 S377 位点来参与代谢调节。

总的来说,该研究报道了一种个体化磷酸化修饰组技术方法,能够精确定位与感兴趣的生物过程相关的磷酸化。通过将受试者的表型差异与个体动态磷酸化修饰组关联起来,研究报道了诸多新的未被报道的关键功能性磷酸化位点,并揭示了主要代谢调节激酶mTORC1和AMPK之间以前未被报道的相互作用。
重要的是,这种方法和思路,或可应用于与所关注的生物学问题相关的表型可与磷酸化蛋白质组同时测量的任何情况,尤其是可进行纵向取样的情况。在未来能够扩展到更大、更多样化的队列,以进一步加深我们对一系列生物学表型中特定磷酸化事件作用的认识,特别是在癌症生物学与肿瘤分子分型研究中将发挥更大的作用。
https://wap.sciencenet.cn/blog-3404471-1321023.html
上一篇:Cancer cell | 樊嘉/周虎/高大明/高强联合绘制肝内胆管癌的多组学分子图谱
下一篇:Nat Chem Biol | 天津医科大学张锴组发现赖氨酸2-羟基异丁酰化修饰酶TmcA及调控细菌耐酸新机制