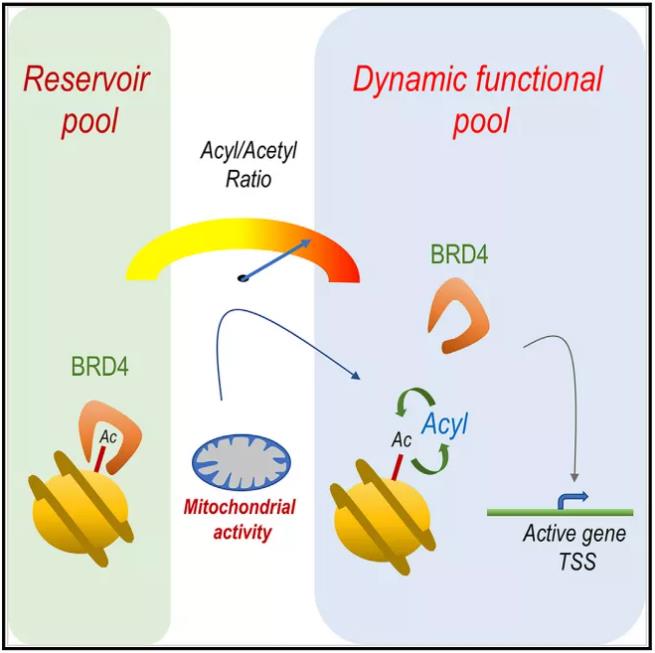
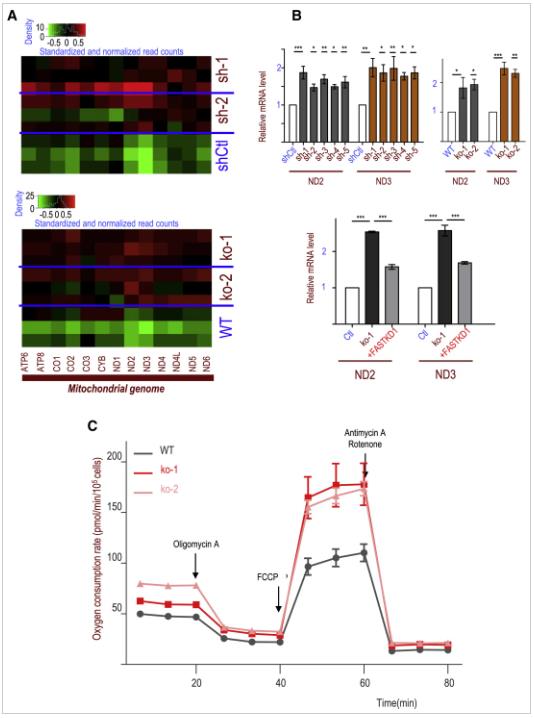
组蛋白翻译后修饰,被认为构成一类超越基因序列的“组蛋白密码”,控制着遗传信息的组织层次及其在染色质层面的解读。组蛋白赖氨酸乙酰化是研究最早的一类组蛋白修饰,与基因活化关系密切。除了组蛋白乙酰化外,近年来,丙酰化、丁酰化 [1] 等多种新型酰化修饰被相继报道,绝大多数新型酰化修饰发生在已知的乙酰化的位点上。这一系列研究极大地丰富了对组蛋白密码、表观遗传学和翻译后修饰领域研究的认识。 组蛋白乙酰化调控一个重要工作模型就是组蛋白乙酰化可以被特定阅读器结构域所识别,从而招募染色质调控因子到特定区域,协同完成基因表达调控。这种识别是调节蛋白和组蛋白的结合以及染色质结构重塑的先决条件。比较为人熟知的赖氨酸乙酰化阅读器是溴域 (Bromodomain, BRD) ,目前数个溴域靶向的一类新药已处于临床试验阶段。BRD4是BET溴结构域家族的成员,已被确定为许多癌症的治疗靶点,包括急性淋巴细胞白血病 (ALL) 、多发性骨髓瘤、结肠癌和乳腺癌等 [2] [3] 。 2021年7月27日,来自上海交通大学医学院附属瑞金医院的糜坚青研究员 Cell Reports Metabolically controlled histone H4K5 acylation/acetylation ratio drives BRD4 genomic distribution ”的研究成果。研究证明了 线粒体活性和β-氧化影响组蛋白H4K5酰化修饰/乙酰化的比率,从而调控BET家族成员BRD4与染色质的互作 。 表明代谢驱动的组蛋白乙酰化/酰化比率调节,可能是调节溴域因子功能及基因组分布的共同机制。景杰生物作为共同作者参与了该研究 ,且为该研究提供了一系列的高特异性蛋白修饰抗体,如抗H4K5bu (PTM-313/-310) 、抗H4K8bu (PTM-311) 、抗H4K5cr (PTM-521) 、抗H4K8cr (PTM-522) 、抗H4K5ac (PTM-119) 、抗H4K8ac (PTM-120) 、抗H4K5bhb (PTM-1205) 和抗H4K5ac (PTM-1407) 。 研究团队前期研究发现,FASTKD1 (Fas activated serine/threonine kinase domain 1) 在急性淋巴细胞白血病 (ALL) 中异位表达,且定位于线粒体上,因此可能在线粒体中发挥功能。因此研究人员首先在急性淋巴细胞白血病 (ALL) 细胞系中构建了FASTKD1 的稳定敲降/除细胞系,结果显示,FASTKD1 的缺失会导致线粒体相关基因的表达显著上调 (图1A) 。此外,qPCR结果显示线粒体相关基因如ND2 和DN3 在FASTKD1 缺失后会被显著激活,且这一现象在重新过表达FASTKD1 后消失 (图1B) 。这表明FASTKD1 能调节线粒体活性,下调线粒体相关基因的表达。
图1、FASTKD1 控制线粒体活性
接着,研究人员运用Label-Free 蛋白质组定量技术,对野生型REH和FASTKD1 KO细胞的组蛋白进行了鉴定。结果显示,H4K5/ K8位点丁酰化对FASTKD1 的缺失最为敏感 (图2A) 。WB结果显示FASTKD1 KO细胞系中H4K5/ K8的丁酰化和巴豆酰化修饰水平明显增加,而乙酰化修饰水平并未改变 (图2B) 。抑制细胞线粒体活性显著抑制组蛋白H4K5丁酰化和H4K5巴豆酰化在FASTKD1 KO细胞中的激活现象 (图2C) ,这表明线粒体活性参与调控H4K5酰化/乙酰化修饰水平的动态变化。 图2、FASTKD1 基因失活、线粒体激活导致H4K5K8酰化增加 03 脂肪酸合成/β-氧化是组蛋白酰化的主要驱动因素 脂肪酸合成和β-氧化涉及酰基辅酶A衍生物的产生,因此有可能促进组蛋白酰化发生。研究人员使用酰基辅酶a合成酶的竞争性抑制剂Triascin C、和乙酰辅酶A羧化酶 (ACC1) 抑制剂ND-630来阻止脂肪酸的合成,并监测对H4K5K8乙酰化和丁酰化的影响。结果显示,FASTKD1 KO细胞中在Triascin C或ND-630处理后,H4K5丁酰化的增加现象消失,但乙酰化未受影响 (图3D和E) 。促进和抑制β-氧化实验结果显示,脂肪酸氧化小分子octanoate的处理增加了细胞中H4K5丁酰化的水平,而消除了FASTKD1 KO细胞中H4K5丁酰化的增加 (图3F、G) 。这表明脂肪酸合成和β-氧化是组蛋白发生酰化修饰的主要驱动因素。 图3、脂肪酸合成/β-氧化是组蛋白酰化的主要驱动因素 04 H4K5酰化/乙酰化修饰动态调节BRD4-染色质相互作用 前期研究发现,在精子发生的晚期阶段,含有H4K5丁酰化的核小体会逃避乙酰化修饰,其组蛋白上Brdt (bromodomain testis-specific) 也随之减少。由此,研究人员猜测H4K5乙酰化/丁酰化-巴豆酰化修饰比率的变化也可能影响BRD4和染色质之间的相互作用。pull down实验证实,当H4K5发生丁酰化修饰时,BRD4无法结合H4 (图4A) ,表明H4K5丁酰化会影响BRD4与染色质相互作用的能力。 图4、H4K5酰化/乙酰化修饰动态调节BRD4-染色质相互作用 05 H4K5酰化/乙酰化修饰动态调控BRD4定位分布及功能 研究人员通过 ChIP实验,来观察各细胞系中H4K5cr和H4K5bu与H4K5ac之间的关系。结果发现,随着H4K5ac修饰水平的增加,H4K5cr-bu/H4K5ac比例也进一步升高 (图5A) 。这说明H4K5酰化的增加优先发生在高度乙酰化的染色质区域。抗BRD4 ChIP-seq实验结果显示,BRD4在高活性基因的TSS (transcriptional start site) 上积累,且在FASTKD1 KO细胞中更为明显 (图5B) 。这说明H4K5cr-bu/ac比率的变化促进了BRD4迁移,改变了BRD4的定位分布。 图5、H4K5酰化/乙酰化修饰动态调控BRD4定位分布及功能 本研究揭示了在染色质上组蛋白乙酰化和其他酰化的系统共存现象。 同时发现,线粒体活性增强会促使组蛋白H4K5酰化/乙酰化修饰比率整体增加,从而导致溴域因子BRD4与乙酰化核小体的结合减弱,BRD4可以被重新分配到特定和局部的基因组区域,包括在活性基因的TSS位点上。由此表明,线粒体代谢驱动的组蛋白乙酰化/酰化比率可能是调节溴域因子功能及基因组分布的常见机制。
[1] Chen, Y, et al., 2007, Lysine propionylation and butyrylation are novel post-translational modifications in histones. Mol Cell Proteomics [2] Flynn, et al., 2015, A Subset of Human Bromodomains Recognizes Butyryllysine and Crotonyllysine Histone Peptide Modifications. Structure [3] Olp, M.D, et al.,2017, Metabolically Derived Lysine Acylations and Neighboring Modifications Tune the Binding of the BET Bromodomains to Histone H4. Biochemistry [4] [1] Gao M , et al., 2021, Metabolically controlled histone H4K5 acylation/acetylation ratio drives BRD4 genomic distribution. Cell Reports
转载本文请联系原作者获取授权,同时请注明本文来自卜晨科学网博客。 https://wap.sciencenet.cn/blog-3404471-1298266.html
上一篇:
宏修饰蛋白组学,科学发现的又一扇大门! 下一篇:
Nat Comm | 中科院动物所张勇团队合作揭示动物中DNA转座子介导基因重复的机制