博文
Cell Reports最新:整合蛋白质组学研究揭示不同临床诊断分型HGSC的分子特征
|
卵巢癌的年发病率居女性生殖系统肿瘤的第3位,死亡率居妇科恶性肿瘤之首。高级别浆液性卵巢癌(HGSC)是卵巢上皮性癌中最常见的一种,大多数患者就诊时已属晚期,恶性程度较高,且表现出高度的肿瘤异质性和多样性。
近年来已有部分高质量的文章从蛋白质组学角度,对大队列卵巢癌患者进行蛋白水平或修饰水平进行整体研究,就其预后差,耐药性强等特点找到一些端倪。如:2016年在Cell主刊上报道的大规模卵巢癌蛋白基因组学与磷酸化修饰组学研究,发现卵巢癌在蛋白或磷酸化水平的分型规律,且蛋白磷酸化水平与病人预后生存期有显著相关性[1];2018年Cell主刊报道了晚期高级别浆液性卵巢癌(HGSC)肿瘤样本的蛋白质组学研究,发现了CT45的表达与卵巢癌患者化学耐药性存在明显相关[2];2019年Nature主刊报道了关于卵巢癌以及卵巢癌附近基质的大队列蛋白质组学研究工作,成功发现了NNMT作为基质细胞对肿瘤转移的关键调控靶点[3]。然而,对基于高度临床诊断样本的HGSC的分子和细胞异质性的理解依然知之甚少。
2020年4月14日,国际专业学术期刊Cell Reports上发表了卵巢癌蛋白质组学的最新研究文章。来自MD安德森癌症中心的卵巢癌治疗专家Anil K. Sood研究团队整合不同临床诊断分型HGSC的多维组学信息(基因组、转录组、蛋白质组和磷酸化组数据),对原发性和多发性转移灶的高度临床诊断注释的HGSC样品的分子和细胞特征差异进行了分析,为更好理解高级别浆液性卵巢癌的异质性提供了重要的依据。

研究者首先选取30例HGSC患者,通过临床诊断注释将其分为三组:R0组(手术后无明显复发,n=10);NACT-PR组(对新辅助治疗(NACT)反应不良,n=10);NACT-ER组(对NACT反应良好,n=10)(样本策略)。对患者的组织样品进行了整合组学的分析:1. 基于全基因组学的体细胞突变和拷贝数变异;2. 基于高通量测序的mRNA定量;3.基于质谱的蛋白质和蛋白质磷酸化的定量。
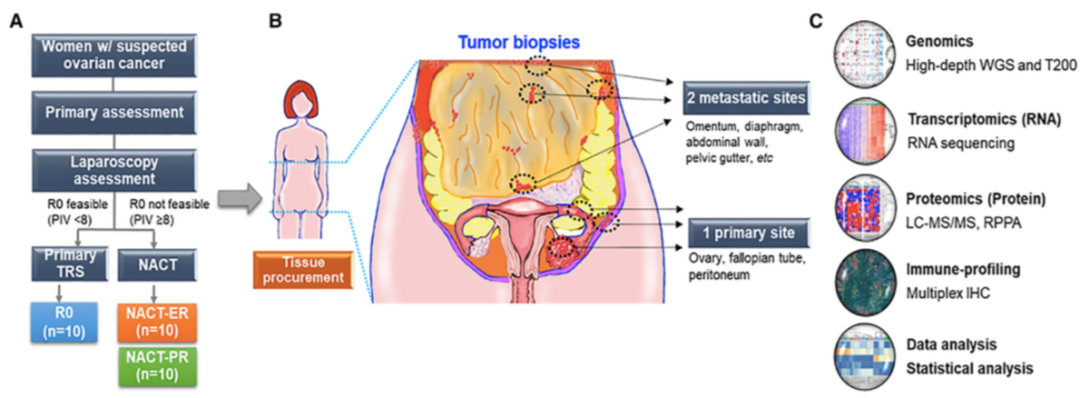
图1、HGSC患者的整合蛋白质组学研究示意图
研究者首先对以上三组的75个样本进行了全基因组学的体细胞突变分析,鉴定到每个样本约13653体细胞突变(图2)。结果表明三组的体细胞突变负荷并无统计学差异(P≥0.05),针对14个癌症相关基因的检测表明三组发生了不同程度的突变。例如:突变频率最高的TP53在三组样品的原发灶和转移灶中均被鉴定出来。此外,对各组的原发灶和转移灶的拷贝数变异(CNV)分析,发现与其他两组相比,在R0组中最常见的CNV是CSMD3(67%)、NF1(54%)、CDK1(50%)和CCND2(46%),其中NF1差异最显著。因此研究者聚焦到NF1后进行了深度靶向测序, 发现三组的NF1拷贝数缺失的比例分别为58.3%、20%、11.5%,与全基因组测序学结果一致。并在下文的转录组与蛋白质组学研究中,以NF1对结果进行了验证。即与NACT组相比,R0组中NF1 mRNA显著下调,NF1的蛋白表达水平显著降低,表明了结果的一致性和可靠性。
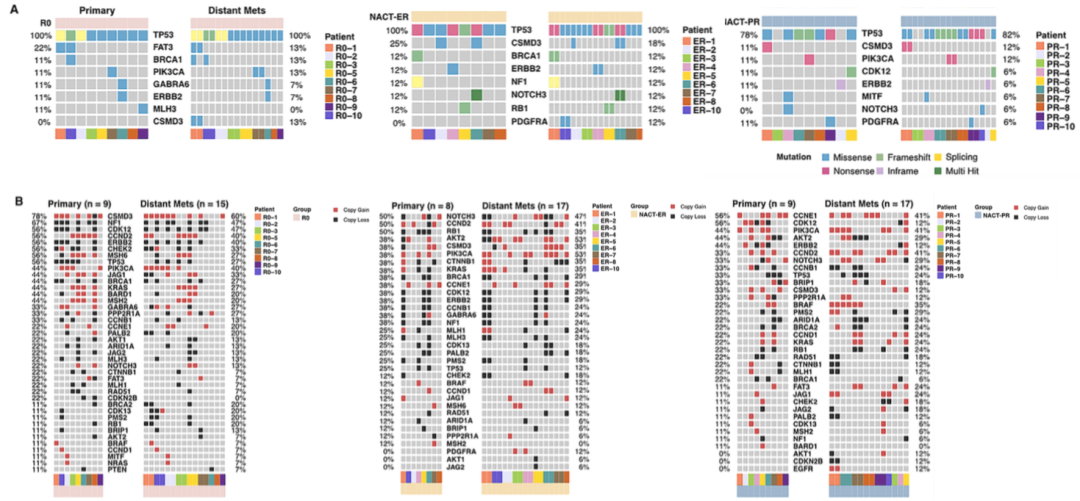
图2高级别浆液性卵巢癌患者的全基因组学测序
基于肿瘤特异性突变产生的新生抗原的数量与免疫活性呈正相关,研究者进一步确定并比较三组样本中新生抗原的数量,结果表明R0组和NACT-ER组均显著高于NACT-PR组。转录组学分析结果表明R0与NACT-ER/PR相比,鉴定到了206个差异表达基因(DEGs),包含67个蛋白编码基因,其中POU3F3, NKX6-1, 和PROK1明显被上调。
进一步研究者运用TMT标记蛋白质组学和磷酸化修饰组学定量技术(质谱策略),对HGSC样品的分子特征进行了分析,在87例卵巢癌样本鉴定到了7290个总蛋白;30例患者的66例样本中鉴定到12914个总磷酸位点。与R0组相比,NACT-ER/PR组有101个蛋白发生了显著变化。差异蛋白的功能分析显示NACT-ER/PR组的细胞内吞、细胞扩散以及抑制细胞死亡等信号通路显著改变。在药物和药物相关靶标中,研究者发现NACT-ER/PR组中钙转运ATP2C1和STAT3明显升高,HDAC6、MGMT和FDPS明显降低,为药物开发提供重要思路。

图3 高级别浆液性卵巢癌患者的整合组学分析
对磷酸化位点的通路分析表明, NACT-ER/PR组中结缔组织细胞的死亡信号通路被激活,而细胞骨架形成的信号通路却被抑制。在药物和药物相关靶标中,发现NACT-ER/PR组中SF3B1中的S129、FGA中的S594和CD44中的S706修饰水平明显升高。
最后,不同免疫细胞群体与肿瘤的临床特征密切相关,研究者通过免疫分析研究,发现肿瘤区域和所有区域(肿瘤/非肿瘤)的组间存在显著差异。然后,对T细胞浸润的百分比进行了分析,发现与NACT-ER/PR组(1.35%)相比,R0中浸润T细胞的数量显著增加(2.91%),从细胞构成上说明浸润T细胞的数量可能与预后的效果具有重要关系。
综上所述,研究者通过分析了HGSC的整合蛋白质组学信息,包括基因组、转录组、蛋白质组和磷酸化组数据,对原发性和多发性转移灶的HGSC样品的分子和细胞特征差异进行了分析,从分子特征解释手术后无明显复发与对新辅助治疗的效果差异,并揭示了与HGSC药物相关候选分子,为治疗HGSC的药物开发提供了新的靶标。
专家简介

Anil K.Sood 教授
Sood教授是国际知名的卵巢癌治疗专家,现任MD安德森癌症中心妇科肿瘤生殖医学外科教授,转化医学副主席,RNA干扰及非编码RNA中心主任,同时也是布兰顿-戴维斯卵巢癌多学科研究项目主任,“卵巢癌登月计划”的联合负责人之一。Sood教授是美国临床研究学会(ASCI)、美国科学进步协会(AAAS)和美国医师协会(AAP)的当选成员,于2017年被任命为美国癌症学会(ACS)教授。
Sood教授的研究主要集中在三个方面:1)卵巢癌血管生成和转移的机制;2)神经内分泌应激激素对卵巢癌生长和进展的影响;3)系统性体内siRNA传递新策略的开发。研究成果获得了重大的认可,包括Hunter奖、Margaret Greenfield/Carmel Cohen卵巢癌卓越研究奖、GCF/Claudia Cohen研究基金杰出妇科癌症研究奖等诸多奖项。
参考文献
1.Hui Zhang,et al., 2016, Integrated Proteogenomic Characterization of Human High-Grade Serous Ovarian Cancer. Cell.
2.Coscia, et al., 2018, Multi-level Proteomics Identifies CT45 as a Chemosensitivity Mediator and Immunotherapy Target in Ovarian Cancer. Cell.
3.Eckert MA, et al., 2019, Proteomics reveals NNMT as a master metabolic regulator of cancer-associated fibroblasts. Nature.
4.Sanghoon Lee, et al., 2020, Molecular Analysis of Clinically Defined Subsets of High-Grade Serous Ovarian Cancer. Cell Reports.
本文景杰学术团队原创,欢迎转发到朋友圈。如有转载、投稿、等其他合作需求,请文章下方留言,或添加微信ptm-market咨询。
https://wap.sciencenet.cn/blog-3404471-1230976.html
上一篇:Plant Journal | 蛋白组学揭示紫杉醇在红豆杉中的组织特异性及调控机制
下一篇:Nucleic Acids Research:赵国屏/赵维团队揭示乙酰化修饰对细菌染色体分离的调控机制