博文
Nat Commun: 表型研究发现SRC诱导转化的关键介质—SGK1
|
编者按:SRC蛋白是非受体酪氨酸激酶,可被多条信号转导途径所激活。今天解读的这篇文章最近发表在Nature Communications上。作者运用SILAC蛋白质组定量技术与siRNA筛选鉴定体系相结合,最终发现了SRC诱导转化中至关重要的SGK1-mTOR途径。研究思路典型,对于类似的研究有很高的可参考性,因此今天特地进行解读。

●研究疾病:癌症
●样本:MCF10A乳腺上皮细胞
●研究策略:SILAC定量蛋白质组
●发表期刊:Nature Communications(IF:12.353 )
●发表时间:2019.01.17
SRC蛋白属于SRC家族激酶(SFKs)成员,是其中目前研究最多,也是与人类疾病联系最为密切的蛋白。异常激活的SRC蛋白与许多肿瘤相关,包括乳腺癌、结肠癌和胰腺癌。
研究发现SRC蛋白活性的高低与肿瘤的发展密切相关,诱导癌症发展的具体机制包括促进癌细胞增殖、对癌细胞激动蛋白骨架的重组、引发生长机制侵袭转移以及诱导血管形成等。
SRC在癌症方面的研究已经取得了很大进展,绝大部分都集中在下游信号传导机制研究,如Ras/MAPK, PI3K/Akt, 和JAK/Stat途径。然而针对特定致癌基因如何诱导转换细胞的研究受到限制,其中一个原因是其下游信号的复杂性和功能性。
为了更好地理解这一过程,本文作者通过SILAC实验与siRNA筛选鉴定体系相结合,发现了该系统SRC转化中至关重要的SGK1-mTOR途径,提出了SRC诱导转化的主要机制,也为进一步改良癌症的治疗策略指明了方向。
1. 鉴定受酪氨酸调节的激酶
作者首先运用SILAC标记蛋白质组技术鉴定受酪氨酸调节的激酶。文章中选择了能够激活表达SRC(SRC Y527F)的MCF10A乳腺上皮细胞(样本)为研究对象,这些细胞在培养时就表现出转化表型,并可模拟三阴性乳腺癌(TNBC)的SRC家族性激酶信号转导网络特征。研究者对细胞对照组(MCF-10A_Ctrl)及细胞转化组(MCF-10A_SRC)进行了SILAC标记(质谱策略),经大规模的激酶纯化后,通过基于质谱的蛋白质组技术,进行激酶检测鉴定。
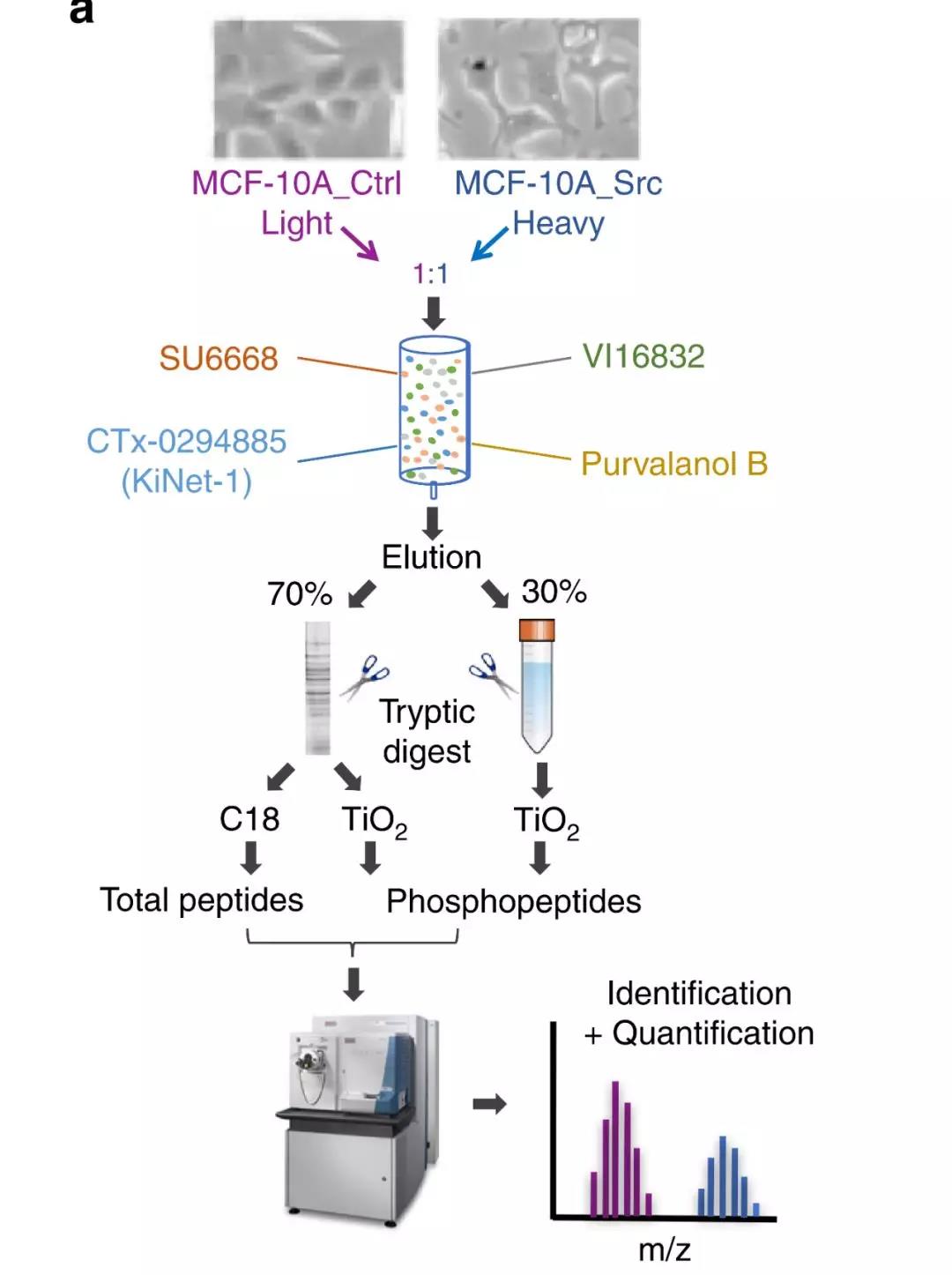
Fig1 SILAC标记定量的蛋白质组技术流程
结果表明,SRC激酶的活性几乎影响了所有主要激酶家族,也验证了SRC激酶下游信号的复杂性和全局性。研究者进一步对受激酶调节之间相互作用进行可视化分析中,揭示了SRC可作为酪氨酸激酶EPHA2,EPHA5,EPHB3,EPHB4,ABL1 / 2和PTK2(FAK)的细胞骨架组织调节网络的焦点。
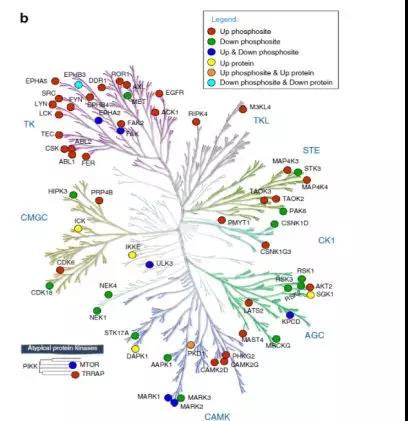
Fig2 SRC激酶组学鉴定分析
同时,研究还发现SRC的表达可导致多种非受体酪氨酸激酶(包括CSK和LCK)的磷酸化活性增加;同时SRC诱导的转化还扰乱了许多激酶的磷酸化活性。
2. SRC调节激酶的功能表征研究
为了进一步对SRC调节的激酶组进行功能表征研究,研究者首先确定了SRC激活表达前后,细胞之间的表型差异。如SRC转化的细胞在含有缺乏EGF的低血清的培养基中表现出更强的增殖能力;对照组细胞不能在缺乏EGF的培养基中形成腺泡,而SRC转化的细胞形成异常的大腺泡。这可能是因为该系统中活性SRC的表达克服了生长因子依赖性并破坏了正常的形态发生程序。
随后通过免疫荧光显微镜检测了剪切Caspase-3和Ki67的水平,其可看作是细胞凋亡和增殖的标志物。发现了该系统SRC转化中至关重要的SGK1-mTOR途径,即SGK1可通过TSC241的磷酸化调节mTOR。
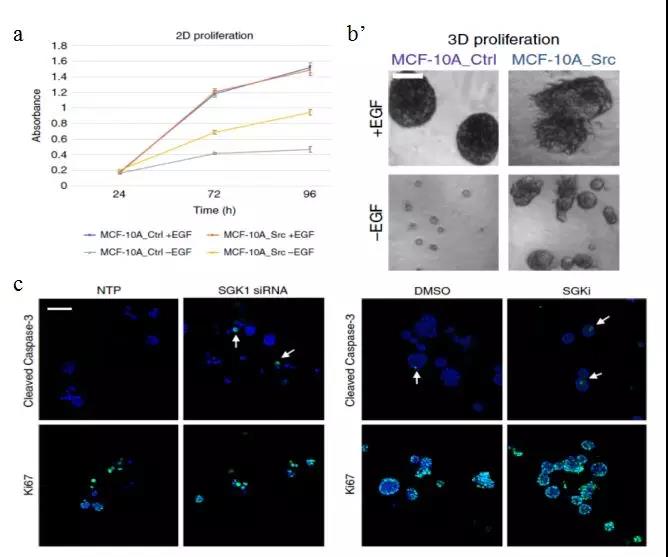
Fig3 SRC调节型激酶的功能表征分析
3. SRC下游SGK1的致癌作用研究
最后,作者通过分子机制研究与体外实验验证,详细阐述了SRC和SGK1联合靶向如何影响体内肿瘤生长的机制。研究发现:SRC和SGK1的组合能够更有效地抑制菌落形成和肿瘤生长。体外实验证明:用SRC抑制剂AZD0530治疗后,肿瘤生长缓慢且显着减少,而SGK1的作用更明显。
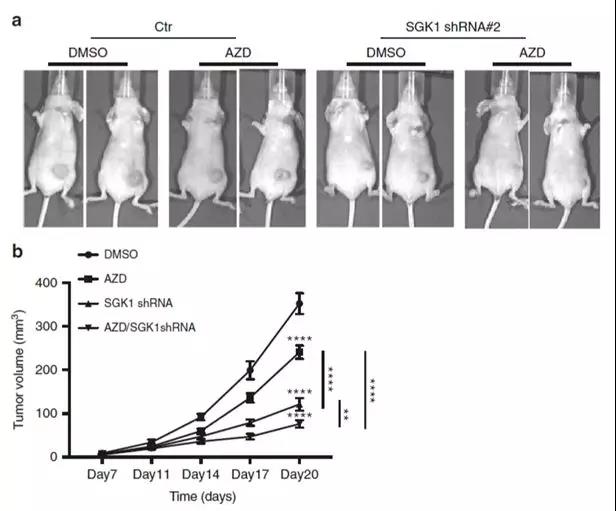
FIG4 敲除SGK1和SRC抑制剂治疗作用研究
本文中研究者首先运用蛋白质组技术鉴定出受酪氨酸调节的激酶网络,随后对SRC调节激酶的功能表征进行研究,发现对SRC转化中至关重要的SGK1-mTOR途径。最后加以分子机制研究,详细阐述了SRC和SGK1联合靶向如何影响体内肿瘤生长的机制。
研究层层深入,通过SILAC实验与siRNA筛选鉴定体系相结合,揭示了SRC诱导转化的主要机制,并为进一步改良癌症的治疗策略指明了方向。
参考文献:
Xiuquan M, et al., 2019, Characterization of the Src-regulated kinome identifies SGK1 as a key mediator of Src-induced Transformation. Nature Communications.
本文来自景杰生物学术团队补充编辑,欢迎转发到朋友圈。如有转载、投稿、等其他合作需求,请添加微信ptm-market或致电400-100-1145咨询。
https://wap.sciencenet.cn/blog-3404471-1163361.html
上一篇:Nat Commun | 蛋白质组学揭示癌症外泌体抑制抗肿瘤免疫反应
下一篇:国际罕见病日 | 蛋白质组学揭示罕见病面肩肱型肌营养不良症分子病理