博文
文献精读--GUOYU--第二篇
|||
第十章 多伴侣的演化:进化电容器的创新
分子伴侣和伴侣蛋白是大型和进化上保守的蛋白质家族的一部分,它们参与细胞中的多种功能。 这些功能中最主要的是它们能够帮助其他缓慢折叠的蛋白质获得其天然构象。
伴侣蛋白家族由于它们通过基因型调节表型的能力,伴侣蛋白是进化的有效电容,因为它们允许创新突变的存活,尽管它们对蛋白质结构具有不稳定作用。从这个意义上讲,伴侣蛋白通过使蛋白质更广泛地探索基因型网络,增加蛋白质对突变和燃料进化的抵抗力。
未来的研究将旨在了解这些蛋白质如何产生新功能,并使用这些电容作为定义细胞功能景观的手段。
合成蛋白质的一级氨基酸序列包含驱动折叠通过曲折的能量景观朝向最小能量和最稳定的天然构象所需的信息。
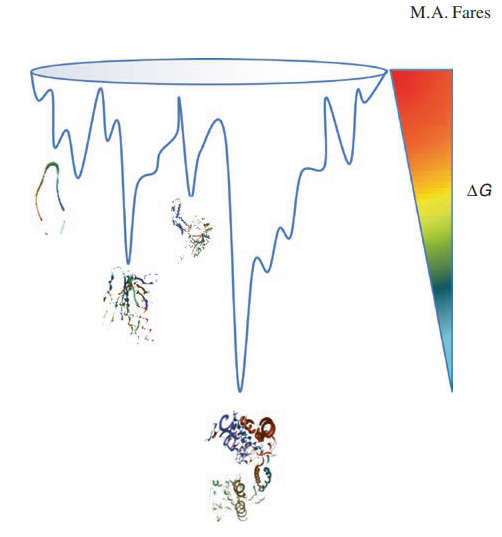
一个蛋白质被合成一个线性的多肽链,它启动了一个复杂的折叠途径,以达到最小能量(ΔG)状态。一开始该途径的ΔG较高(三角形的红色截面),蛋白质不稳定,当蛋白质接近景观的最低能量部分时,蛋白质的结构将稳定,在那里它获得天然的,功能性的构象。
在细胞或细胞器的胞浆中,一个100纳米立方体包含大约30,000小分子和50,000离子,非特异性聚集体是通常是通过部分未折叠蛋白质的疏水暴露表面之间的相互作用形成的。
大多数在蛋白质编码基因中发生的非同义核苷酸突变(即涉及密码子和编码氨基酸变化的突变)都是有害的。它们的随机性导致蛋白质结构不稳定,最终导致非特异性蛋白质聚集体的形成。伴侣结合暴露非天然蛋白质的疏水性表面以一种非特异性的方式,从而防止错误折叠和非特异性聚集,并允许本机折叠的新机会发生。
伴侣蛋白通常被组织为多个亚基,每个亚基包含许多不同的结构域(一般三个),它们交织成机械关系,每个亚基呈现两个主要结构域,包含底物结合区的顶端和包含ATP结合位点的赤道以及底物相互作用位点。这两个结构域通过由第三个灵活结构域,即中间结构域介导的复杂且实质的构象变化以相对的方式相互移动(Saibil和Ranson,2002)。
这些子单元被组织成一个或两个背靠背的环,每个环形成一个与其姐妹环一起工作的腔室有两个主要的伴侣蛋白家族占据了生命的三个领域,证明了它们对细胞功能的绝对必要性。 伴侣蛋白家族I或I组伴侣蛋白存在于细菌细胞质(也称为GroEL)或细菌内共生源的真核细胞器中,包括线粒体(Hsp60)或叶绿体和氢化体(Brocchieri和Karlin 2000)。 另一方面,II型伴侣蛋白存在于古细菌细胞质(通常称为热体)和真核细胞溶质(CCT / TRiC)中。
�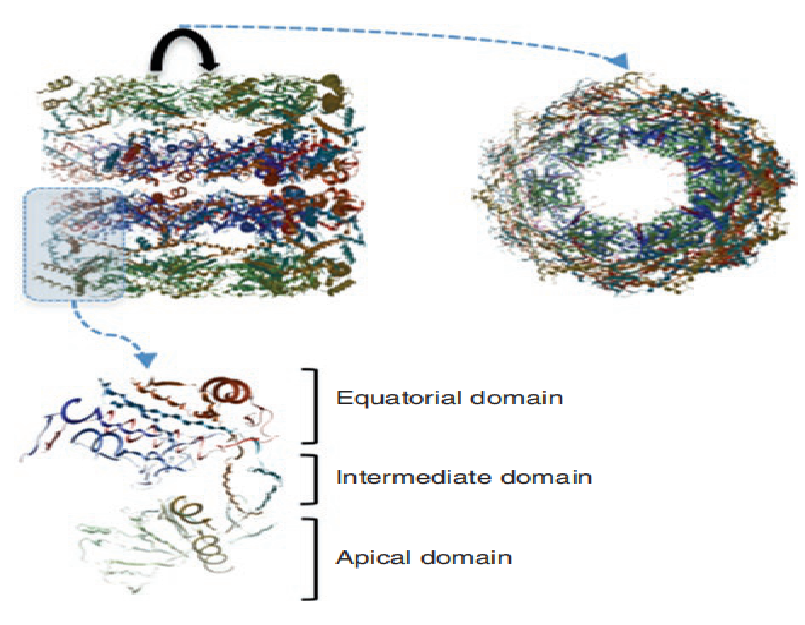
伴侣的一般结构。这个分子机器是组织在两个环背对背定向,有一个折叠室,每个组成的几个亚单位。亚单位包括三个区域:顶端,中间和赤道
伴侣是进化电容器
伴侣蛋白和伴侣蛋白协助慢折叠蛋白质到达其固有构象,防止蛋白质聚集,并重新折叠错误蛋白质。
遗传鲁棒性增加了生物系统进化的能力,增加了可以中立方式探索的基因型空间,并最终发现了新的表型。
大量证据支持伴侣和伴侣在提高生物体遗传稳健性方面的作用,因此它们具有进化能力。
大量证据支持伴侣和伴侣在提高生物体遗传稳健性方面的作用,因此它们具有进化能力。
伴随蛋白GroEL在进化的大肠杆菌细胞中的过度表达,使这些菌株的适应能力几乎完全恢复,有力地支持了GroEL的能力。以缓冲突变的有害影响(Fares等人)。2002年b)。GroEL在缓冲突变效应方面的作用也得到了GroEL中增强折叠突变的固定作用的支持
伴侣的缓减作用似乎并不是hsp 90和GroEL的唯一特性。最近,在一个类似于GroEL的进化实验中证明了这一点。Aperone DnaK(Hsp 70)也能消除有害突变的影响,使需要DnaK折叠的蛋白质快速进化。
基因复制与伴侣功能的扩展
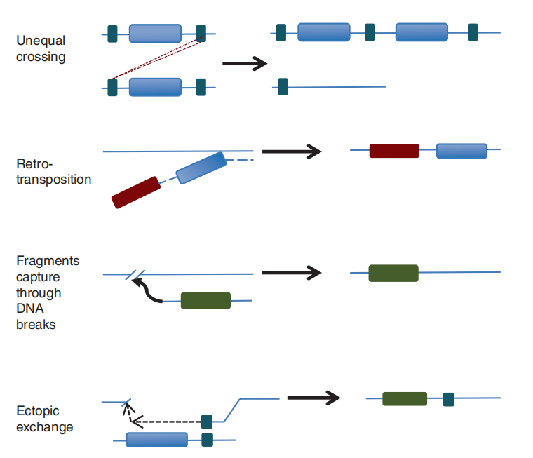
基因复制涉及基因加倍,产生两个相同的基因拷贝和编码功能。基因复制是作为副产品的随机起源的错误。f一些基本的细胞过程,包括同源基因组区域之间的不平等交叉、倒置、通过双螺旋断裂捕获DNA片段和c DNA片段交换。
在伴侣蛋白中兼职
除蛋白质最初已知的活性外,月光蛋白还具有一种或多种功能、独立的生物活性。
自从发现肠道细菌-鼠伤寒沙门氏菌的黏液结合蛋白为C以来,伴侣蛋白60(Cpn 60)已被证明具有大量的独立功能。这种有机体的Pn60 (En -sgraber和Loos 1992)。由于两个主要原因,这份报告令人吃惊。首先,Cpn 60是细胞内部分折叠蛋白的主要活性折叠物。第二,CPN60是一种明显的细胞内蛋白,因此发现它与细胞表面结合是令人惊讶的。
还报告了伴侣蛋白的许多其他职能,可归纳如下:
1.在真核生物中,Cpn 60被发现在细胞的胞浆中,在线粒体外,暗示着这种伴侣的功能可能与折叠无关。
2.Cpn 60已在su中找到。细胞表面,可能是受体
3.配体结合
4.胞内信号
陪伴素GroEL功能创新的分子基础
GroEL是一个操作程序Groe的一部分,在它中,辅助因子groes也被编码,而Groe和gros这两个基因的表达允许构造o。f由两个背对背的定向环构成的同型十四元环,每个环由GroEL和groes的七个相同的亚基组成,每个子单元由三个结构域组成。语言和功能上的不同:顶端结构域,包含与未折叠的蛋白质和肽以及辅助因子结合的氨基酸区;赤道区,包含ns是ATP结合位点,中间结构域允许根尖区的灵活移动,并促进顺式和反式构象之间的亚基的转换。为了证明GroEL结构域中氨基酸位点之间的功能和结构联系,作者在假定这类连接可能在选择下进行了共同进化分析。
这些结果揭示了GroEL在整个细菌系统发育过程中的巨大进化可塑性,揭示了其功能多样性的分子基础。
对伴侣进化理解的未来展望
分子进化的研究,包括基因型与表型的映射,蛋白质序列与功能之间的联系,以及隐藏在氨基酸中的功能可塑性。这种蛋白质的序列和结构密码。伴侣涉及到大量不同的功能,未来的一个挑战是确定所有可能的功能,即rema。
不同群体的伴侣之间,尽管进化距离很长,但氨基酸的替代作用很细微。打破伴侣密码识别其功能和进化可塑性在可预见的将来,它的驯化将成为现实。
https://wap.sciencenet.cn/blog-3404046-1150682.html
上一篇:文献精读--GUOYU--第一篇
下一篇:文献精读--GUOYU--第三篇 --2018.12.16