博文
电解液溶剂的几点花边知识
||
1.碳酸酯和羧酸酯的熔点(℃):
常温下为固态的是EC,熔点36.4℃。其实还有一个TMC,即1,3-丙二醇环碳酸酯,熔点在46~47℃,比EC还要高,但是它在电解液界很不常用,
冰点(0℃)以上为固态的,还有一个DMC,熔点4.6℃。
再往下冻,是MPC -43℃,PC也挺抗冻的,-48.8℃。 EMC -53℃, DEC虽然粘度高一点,但凝固点更低,-74.3℃,但早期有些资料说是-43℃,这个是不准确的。
羧酸酯GVL:-31℃, GBL:-43.5℃, EP -73℃,PP -75.9℃,BA -77.9℃,EA -83.5℃,MP -88℃,PA -92.5℃,EB -93.3℃,MB -95℃,所有的这些羧酸酯都是好样的:它们不会在冬季冻起来。
2.沸点
有几个的沸点是比较低的,主要是MA 58℃, EA 77℃,MP 79℃,DMC 90℃,EP 99℃,PA 101.6℃,MB 102℃, EMC 110℃。
MF 32℃,闪点-32℃,这个化合物一来有毒,二来分子中有醛基,酸性较强,也容易分解,因此甲酸酯在电解液中不能用的。
虽然不用作锂离子电池溶剂,乙腈ACN还是有必要一提:沸点82℃,也是很容易汽化的。
作为添加剂的FB沸点也低,仅85℃。
3.粘度(室温下,mPa.s)
乙腈很低,仅0.34, MA 0.37, EA 0.45, 碳酸酯中粘度最低的DMC 为0.59, EMC 0.65. 要想电导率高或者倍率性能好,挑低粘度的溶剂准没错---只要它能用。
4.自燃点,燃点与闪点
如果有空气助燃,溶剂温度升到多高(没有火花引燃,纯靠高温)就可以自燃呢? 这个自燃的温度叫做自燃点(AIT)。电解液溶剂的自燃点除了DEC查到过,其它没有报道。
"在规定的条件下,可燃物质产生自燃的最低温度称为自燃点。在这一温度时,物质与空气(氧)接触,不需要明火的作用就能发生燃烧。"--《消防安全技术实务》P10
为此我们测试了几种,数据如下:
EP 450℃
DMC 466℃
DEC 468℃ (文献值445℃)
EMC 477℃
PP 484℃
PC 497℃
EC 500℃
对比一下其它材料,乙醚160℃,汽油 530~685℃,乙醇 423℃。
可以看出,同一易燃溶剂,自燃点比闪点要高得多。所以多数情况下,我们考虑溶剂的安全性时,主要看它的闪点。"闪点是判断液体火灾危险性大小及对可燃性液体进行分类的主要依据"。
顺便说一下,消防上,可燃性液体的火灾危险性类别规定:闪点<28℃的定义为甲类,28≤F<60℃ 的定义为乙类, ≥60℃的为丙类。
再顺便说一下,燃点与自燃点的定义不一样。
燃点是"在规定的试验条件下,物质在外部引火源作用下表面起火并持续燃烧一定时间所需的最低温度。。。。通常,用燃点作为固体火灾危险性大小的主要依据之一"。(来源还是《消防安全技术实务》)
简单来讲,闪点→可燃液体, 燃点→ 可燃固体。 自燃点→ 都可以适用。
5. 溶解性
5.1 溶剂在水中的溶解性
这个很多溶剂都有在水中溶解性的数据报道,主要是出于消防安全的需要。以下查了几个:
EC:大约88.1 g/l 在 20 °C(这个值比较低,可能是因为20℃下EC为固态,溶解度不是特别高.)
PC: 175 g/l 在 25 °C 在 1,013 百帕 - 可溶
DMC: 水溶性 114.7 g/l at 20 °C
EMC: 水溶性 46.8 g/l 在 20 °C -
DEC: 水溶性 18.8 g/l 在 20 °C
之前我做过测试, 没有想到的是,EC在水中的溶解性如此之大,PC虽然小一些,其实也不算少。实测150g EC加入到100g水中可以完全互溶(但需要熔化EC再测定).但PC在100g水中约溶解22g左右. 22g PC溶于100g H2O中, 浓度就是22/122=18%, 与PC的文献值175g/l是大体符合的.
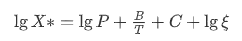
其中 X*为CO2在含水溶剂中的饱和溶解度,以摩尔分数计算。P为气相CO2的分压,单位为kg/cm2; 对溶剂PC而言,B=686.1, C=-4.245,ξ是溶剂含水量的修正系数,当含水量为2%时,ξ=0.9.
根据这个公式,我们就假定PC含水量为2%,常温(25℃)常压(1atm)下,lgP=0.005609, B/T=2.30119, lgξ=-0.04576, lgX为-1.9839, X转化为摩尔分数百分值即为1.037.
我们再进一步计算,假定CO2为理想气体按22.4L/mol计,不考虑CO2溶解后的溶液的密度变化以简化估算,1L PC为1200g,为11.75mol。按摩尔比CO2:PC(11.75mol)=1.037:98.963, 则溶解的CO2摩尔数为:0.123mol,对应CO2气体为22.4×0.123=2.75L。也就是CO2在常温常压下,1L PC大约可以溶解2.75L的二氧化碳。从公式看, 如果压力提高10倍,溶解度也大约提高10倍。
我还查到另一个数据,在DMC中,CO2的溶解度竟然比在PC中还要高。用数据说话如下:

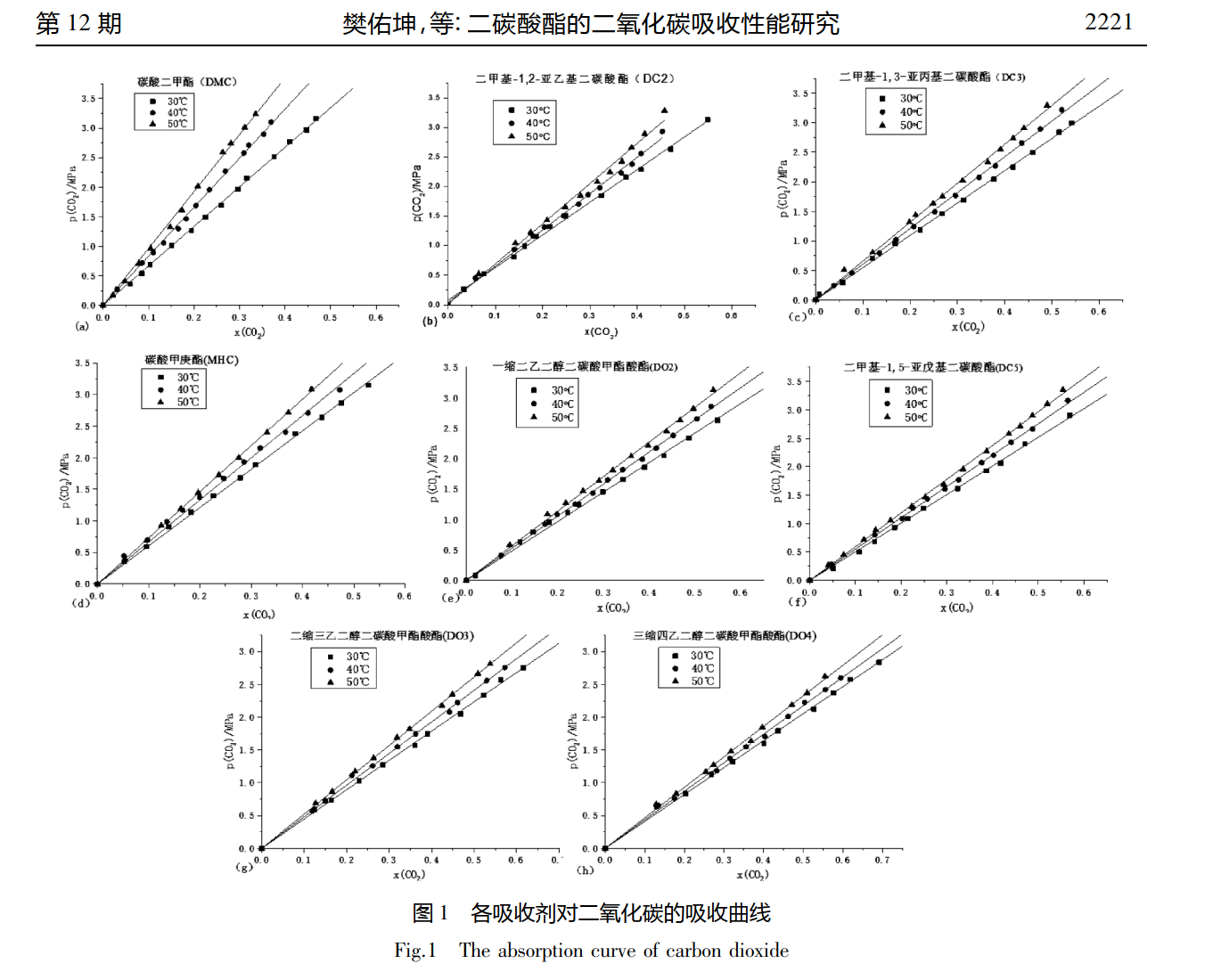
由于CO2的吸收与固定是一个碳平衡大背景下的热门话题,还有人研究了不同的二碳酸酯对CO2的吸收,这里面也提到了DMC在30℃,40℃,50℃下的吸收性,还有一个少见的碳酸甲庚酯(MHC)对CO2的吸收性数据。
6. 比热容(单位为 J/(g·℃) )
以下未注明为文献值的,结果为实测值
EC: 1)文献值1为1.93, 2)CRC手册的文献值2为 133.9J/(mol·K),折算为1.52
PC: 文献值218.6 J/mol·K),折算为2.14
DMC 1.7
EMC 1.7
DEC 1.73
比热容在CRC理化手册中,用Cp(l)表示,l表示liquid, 单位用J/(mol·K),与我们爱用的J/(g·K)不一样,要结合分子量一起换算一下。
https://wap.sciencenet.cn/blog-1213210-1272932.html
上一篇:MySQL安装笔记,及我的数据库学习平台
下一篇:中文字符的正则匹配 备忘