博文
手性 NHC 配体新突破:柔性结构适配多种催化反应 | 乐研试剂
|
不对称过渡金属催化是构建手性分子的关键技术,对现代有机合成产生了深远影响。过去几十年间,催化不对称合成取得了显著进展,这在很大程度上得益于精密手性配体的开发。尽管手性膦配体发展迅速且应用广泛,但手性 N-杂环卡宾(NHC)配体的研究仍相对滞后,主要原因是设计和合成合适的手性骨架面临固有挑战。鉴于 NHC 独特的拓扑结构和模块化空间环境,开发新型 NHC 配体具有重要前景。
中国科学院上海有机所施世良团队基于优势手性片段策略,开发了一系列诱导契合型手性 NHC 配体。这类配体具有结构易修饰、位阻大且柔性强的特点,在不对称金属催化中具有广泛适用性。值得一提的是它们可从廉价起始原料大规模合成,且无需柱层析纯化,其模块化、简便的制备方法为进一步探索其在不对称反应中的应用提供了便利。同时,研究发现该类配体可应用于一系列重要挑战性不对称催化反应中,包括不对称交叉偶联反应、烯烃不对称官能化反应、不对称氢转移反应、不对称 C−H 官能化反应及不对称亲核加成反应等,其位阻大且柔性强的特性使其能够在不同基元步骤和挑战性转化中实现自适应性立体控制。
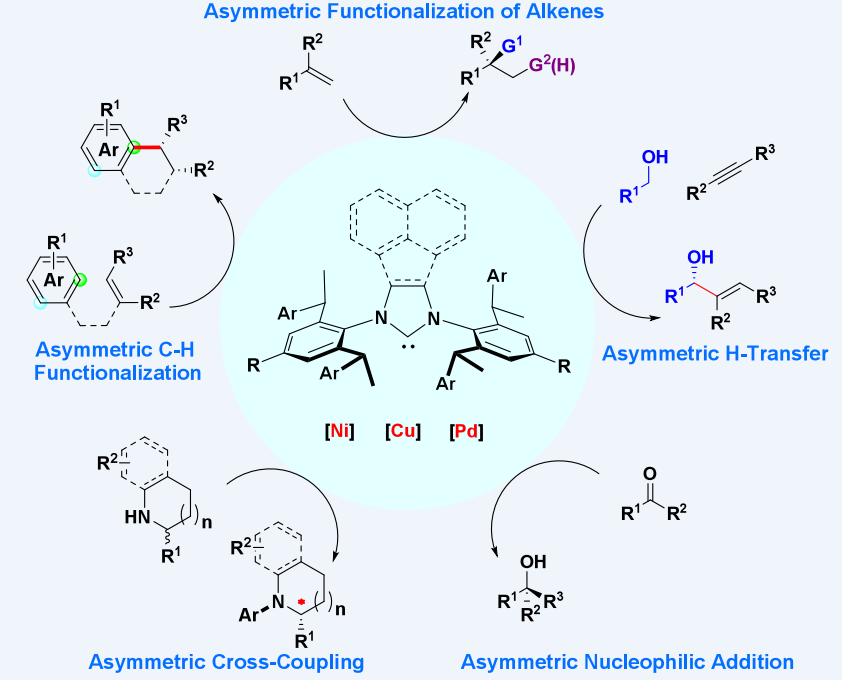
Acc. Chem. Res. 2025, 58, 2157−2177
Section.01
— Leyan.com —
核心逻辑:
为什么要开发这类配体?——
解决不对称催化的 “矛盾与挑战”
不对称过渡金属催化是合成手性药物、材料的核心技术,而手性配体是调控催化活性和对映选择性的关键。传统手性配体存在两大痛点:
1.NHC 配体因骨架设计难、合成复杂,发展滞后;
2.催化循环中,“氧化加成(需要小位阻配体)” 和 “还原消除(需要大位阻配体)” 对配体空间需求矛盾,传统刚性配体难以兼顾。
施世良团队的解决方案:借鉴酶的 “诱导契合模型”+ 优势手性片段(PCF)策略,设计 “大位阻但柔性” 的手性 NHC 配体 —— 既满足还原消除的大位阻需求,又能通过单键旋转调整构象,适应氧化加成、转金属化等步骤的空间需求,实现 “动态适配” 的立体控制。
Section.02
— Leyan.com —
关键内容:
配体设计、合成与核心应用
1. 配体设计:诱导契合 + 优势手性片段(PCF)
设计灵感:酶的活性中心具有柔性,结合底物后会调整构象优化结合(诱导契合);施世良团队将这一理念迁移到配体设计,让配体通过单键旋转实现构象自适应。
优势手性片段(PCF):以 C2对称的手性苯胺(DPEP)为核心片段 —— 相比传统刚性片段(如 BINAP 的联萘基),DPEP 的苯基可旋转,赋予配体柔性。
配体类型:SIPE(饱和咪唑啉型)、ANIPE(苊烯并咪唑型);
结构特点:强σ-给体(TEP 值~2047 cm-1)、大埋藏体积(ANIPE-CuCl 为 55.3%)、柔性手性口袋。
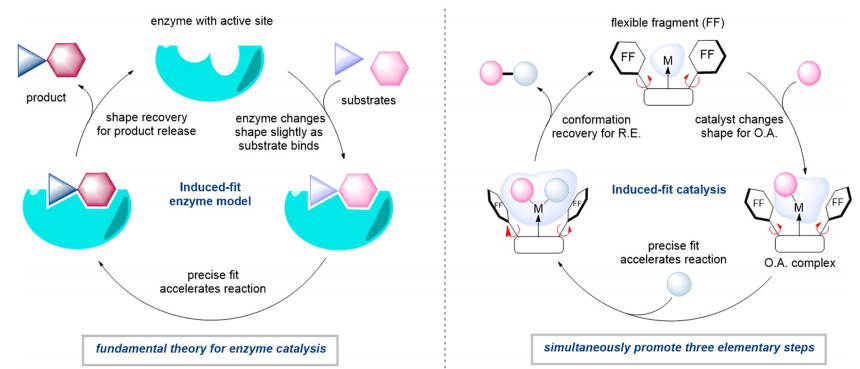
Acc. Chem. Res. 2025, 58, 2157−2177
2. 配体合成:简便、易放大(核心优势之一)
起始原料:廉价易得的苯胺,经 “双烯基化→不对称氢化→环化” 三步核心反应合成;
关键亮点:全程无需柱层析纯化,可 100g 级大规模制备,咪唑鎓盐前体空气稳定,室温可储存数月 —— 解决了传统手性配体 “合成复杂、难放大” 的痛点。
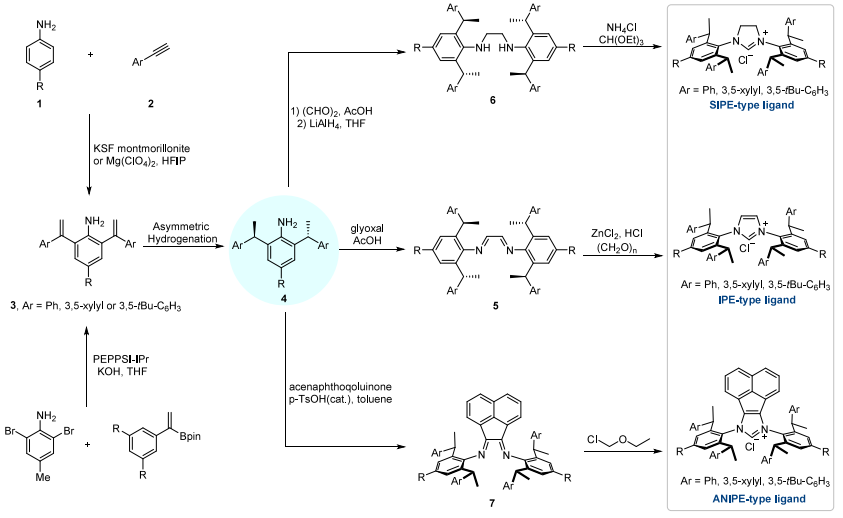
Acc. Chem. Res. 2025, 58, 2157−2177
3. 核心应用:覆盖 5 类关键不对称反应(解决多个长期挑战)
施世良团队将这类配体应用于 Pd、Ni、Cu等金属催化的不对称反应,均实现 “高活性 + 高对映选择性”,核心成果如下:
一、不对称交叉偶联
A.低温(-50℃)Ni 催化 C-N 偶联(动力学拆分):解决 α- 支链仲胺与芳基氯的对映选择性胺化;
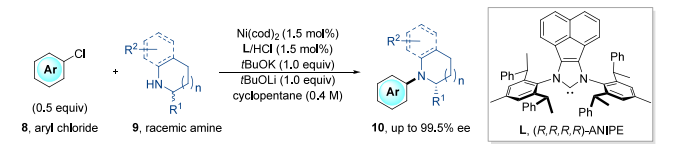
Angew. Chem., Int. Ed.2021, 133, 16213−16220.
B.Pd 催化 Suzuki-Miyaura 反应:构建轴手性联芳基(含杂环、多取代底物兼容);
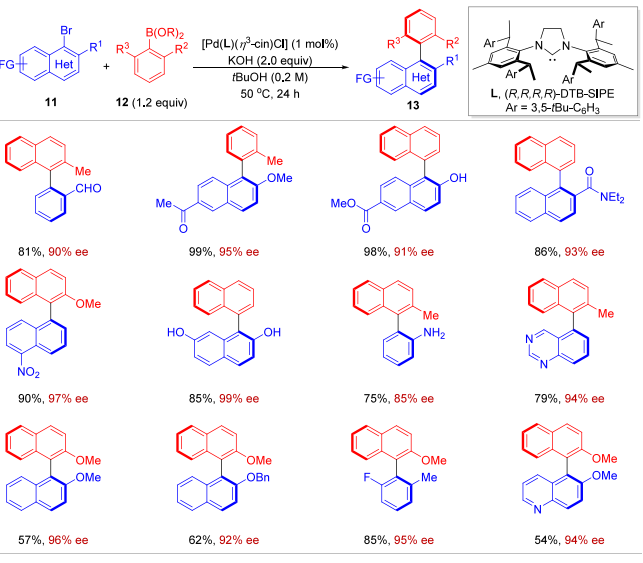
J. Am. Chem. Soc. 2019, 141, 14938−14945.
C.对映汇聚式 Negishi 偶联:消旋仲烷基锌与芳基卤合成 1,1-二芳基烷烃(ee 最高 91%)。
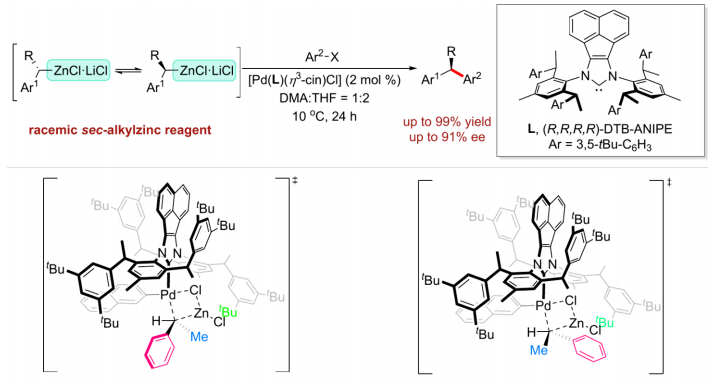
CCS Chem.2026, 8, 754–763.
二、烯烃不对称官能化
A.Cu 催化α-烯烃马氏规则氢硼化:首次实现未活化α-烯烃的高对映选择性氢硼化(ee>90%);
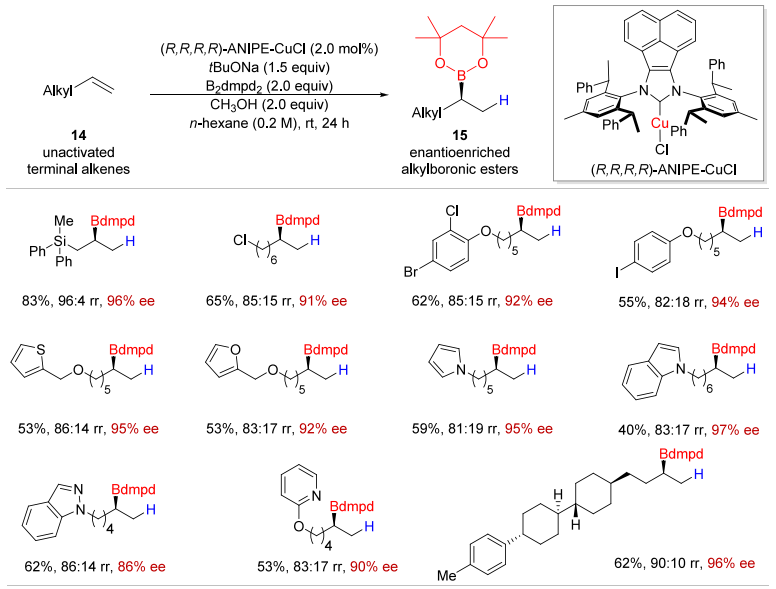
Angew. Chem., Int. Ed. 2018, 57, 1376−1380.
B. 烯烃氢芳基化/双碳官能化:构建三取代/四取代手性中心;
Nat. Catal. 2022, 5, 934−942.
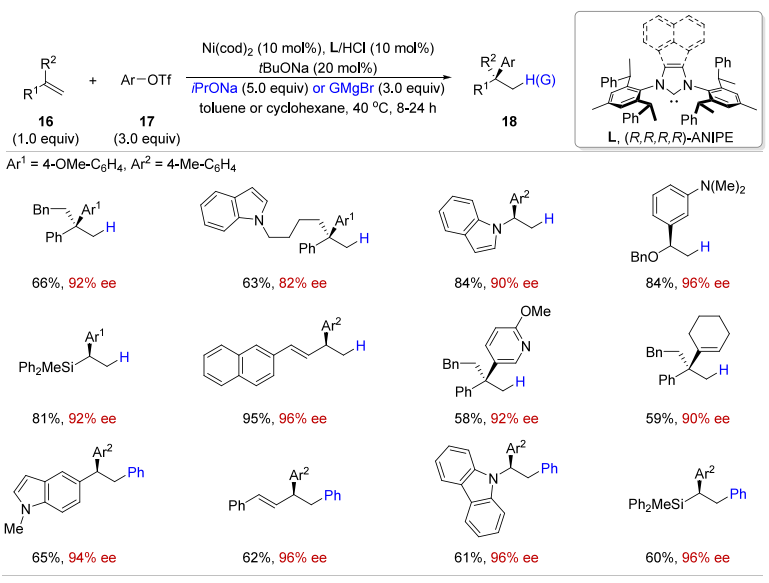
C. Ni 催化未活化烯烃的碳官能化:解决未活化烯烃 “结合弱、区域及立体选择性差” 的难题(85-98% ee);
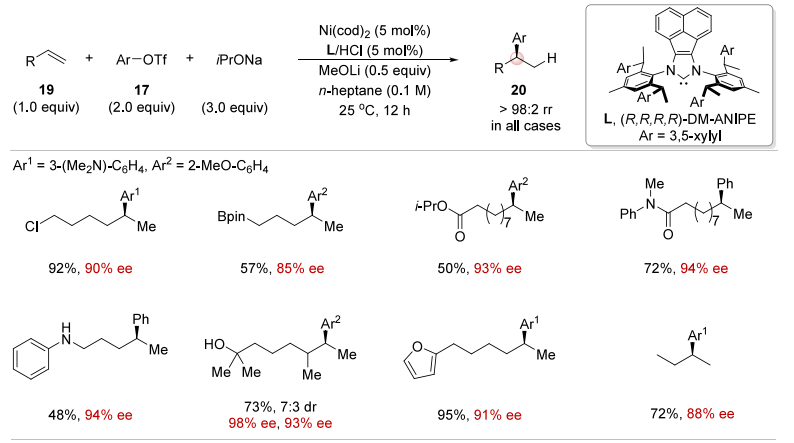
Nat. Catal. 2023, 6, 1087–1097
D.烯丙胺的不对称芳基化反应,高效合成手性苯乙胺片段。
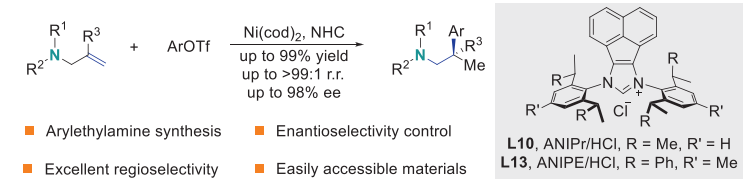
Angew. Chem. Int. Ed. 2025, e202503126
E.烯烃的不对称碳镁化反应,高效合成多类手性季碳。
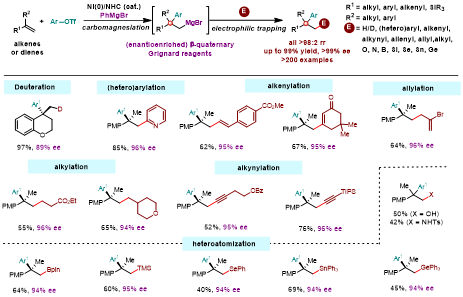
Nat. Chem., 2026, DOI: 10.1038/s41557-026-02073-1.
F.烯烃的不对称碳卤化反应,高效合成手性烷基溴或烷基碘类化合物。
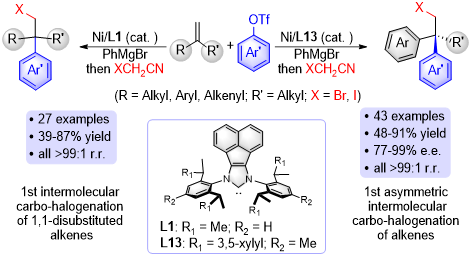
J. Am. Chem. Soc. 2026, DOI: 10.1021/jacs.5c20792.
三、不对称氢转移反应
A. Ni 催化醇与炔的 redox-neutral 偶联:合成手性烯丙醇(无需外加氢源/氧化剂);
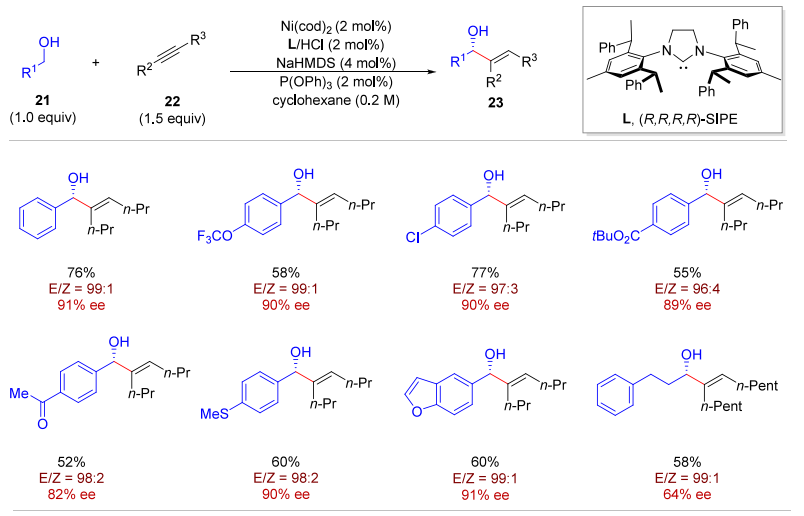
ACS Catal.2019, 9, 1−6.
B. 三组分(醛 + 炔 + 烯酮)反应:高效构建非环季碳手性中心(100% 原子经济性)。
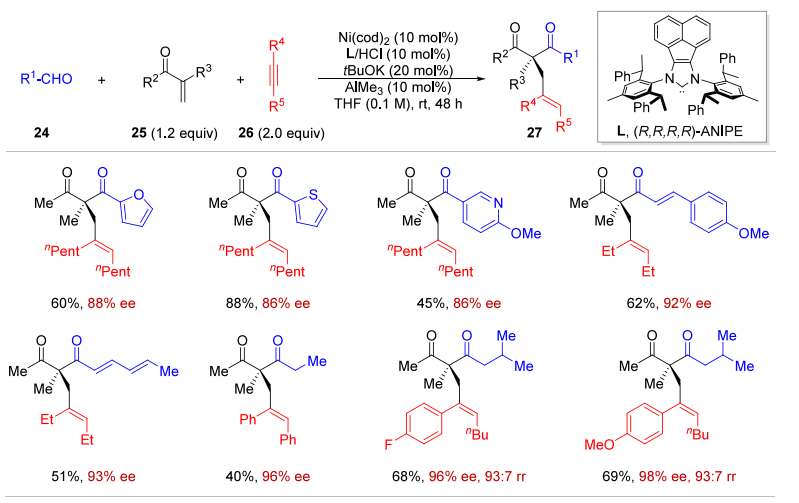
J. Am. Chem. Soc. 2022, 144, 130−136.
C. 炔烃、醛与硅烷的化学发散性、对映选择性与区域选择性偶联反应:发散性合成手性硅醚化合物。
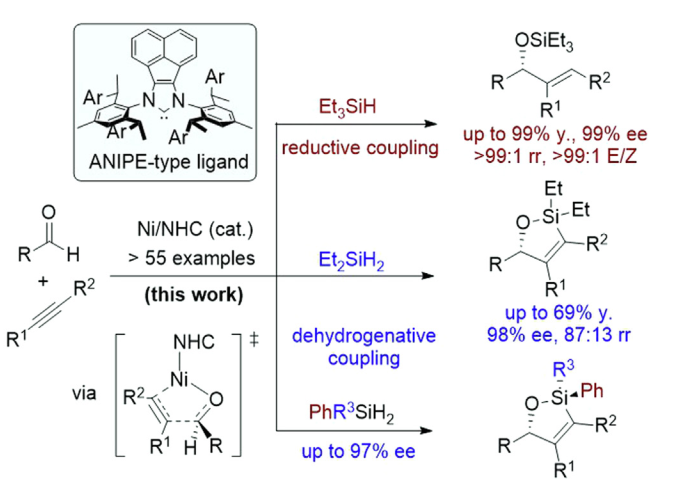
Sci. Bull.,2025, 70, 674–682
D. 选择性动态动力学不对称醛-炔还原偶联:高效构建含相邻手性中心烯丙醇。
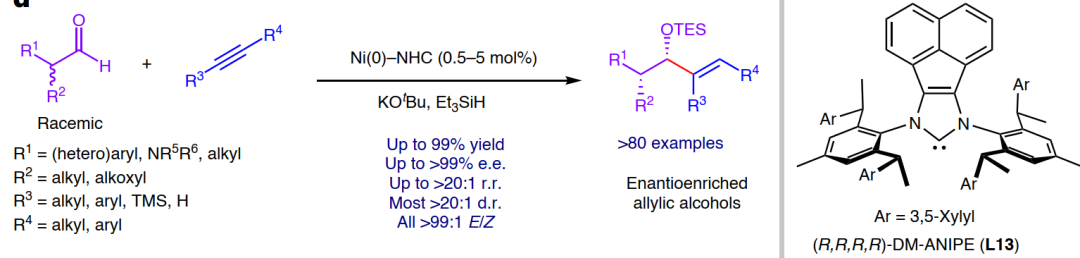
Nat. Synth.,2025, 4, 1630–1639
E. 选择性不对称醛-非活化烯烃还原偶联:高效构建手性1-茚醇。

Org. Lett., 2026, DOI: 10.1021/acs.orglett.6c00123.
四、不对称 C-H 官能化
A. Ni 催化吡啶C-H 烷基化:区域和对映选择性构建稠环吡啶(ee 最高 99%);
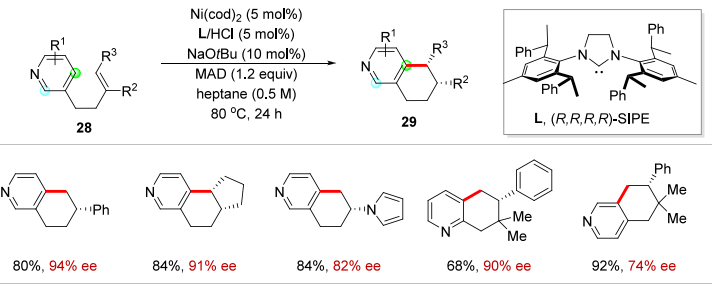
J. Am. Chem. Soc. 2019, 141, 5628−5634.
B. 吡啶对位 C-H 烷基化:通过分子间氢芳基化合成含吡啶的 1,1 - 二芳基烷烃;
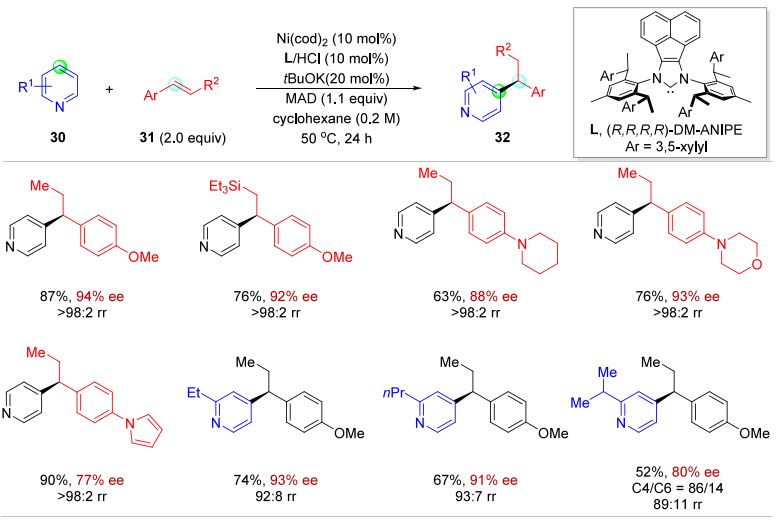
J. Am. Chem. Soc. 2022, 144, 13643−13651.
C.多氟芳烃 C-H 烷基化:选择性活化 C-H 键(而非 C-F 键),合成手性氟代四氢萘。
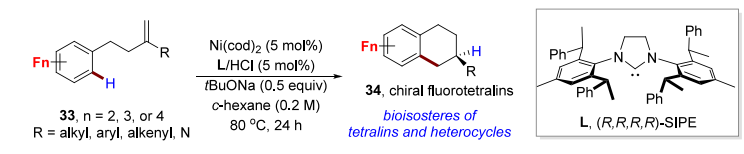
Angew. Chem., Int. Ed.2019, 131, 13567−13571.
D. Ni 催化吡啶C-H 烷基化:区域和对映选择性构建稠环吡啶酮和嘧啶酮(ee 最高 99%);
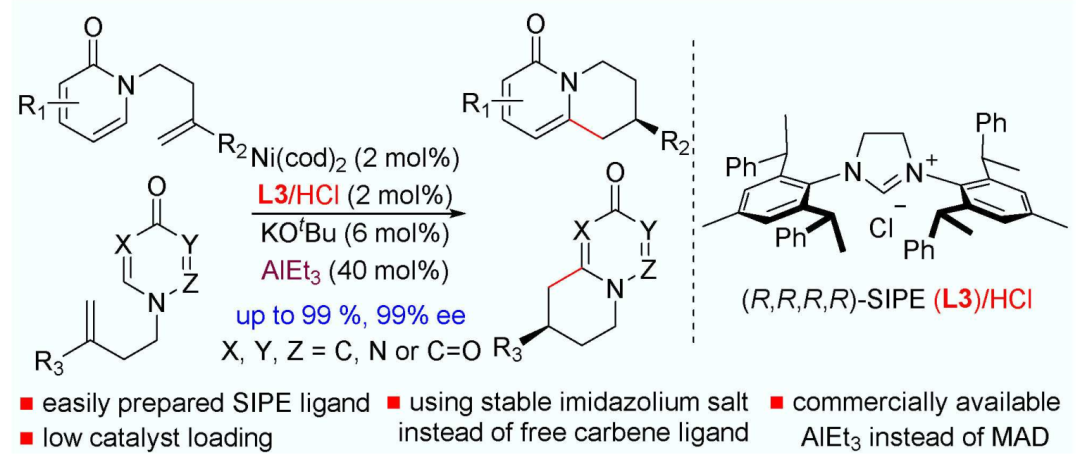
Adv. Synth. Catal. 2020, 362, 1125–1130
E. Ni 催化嘧啶C-H 烷基化:区域和对映选择性构建烷基嘧啶
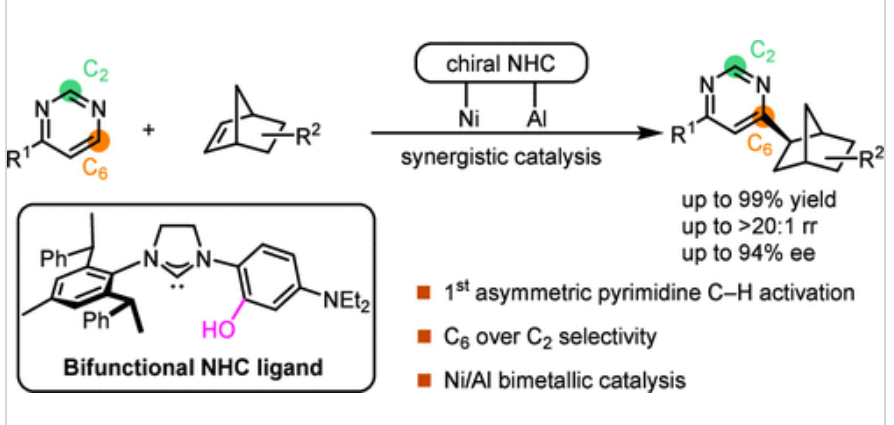
ACS Catal. 2025, 15, 18824−18833
五、不对称亲核加成
A. Ni 催化酮的芳基化/烯基化:10 分钟内完成反应,兼容杂环和多种官能团;
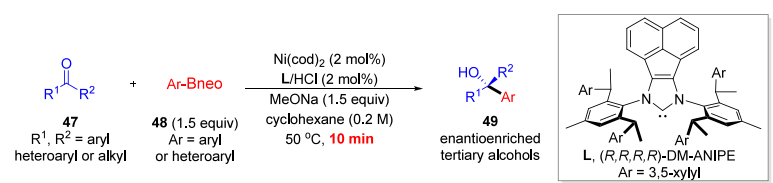
Angew. Chem., Int. Ed. 2021, 60, 5262−5267.
B.外消旋非活化酮的动态动力学不对称芳基化和烯基化,高立体选择性地制备一系列α,β-手性叔醇。
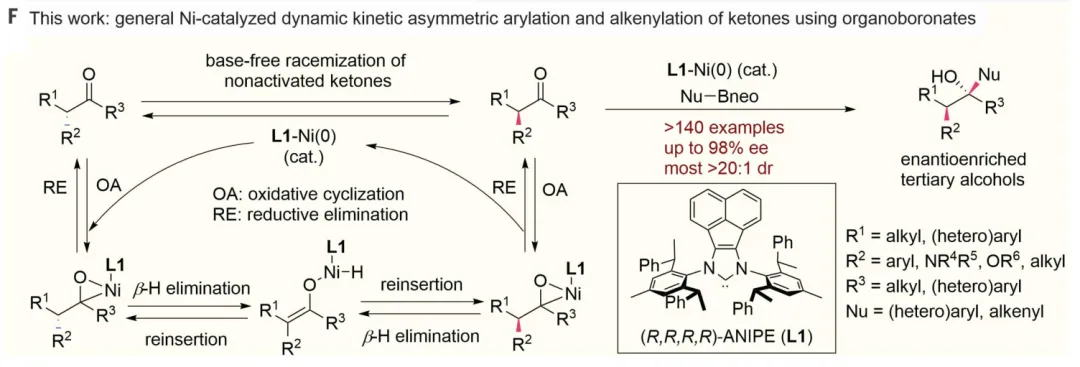
Science2023, 379, 662−670.
C. 醛的不对称芳基化及烯基化反应:高效高选择性构建手性仲醇结构。
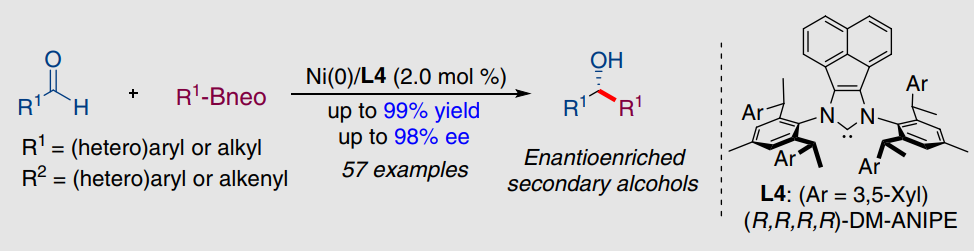
CCS Chem.2022, 4, 1169–1179
D. 醛的不对称烷基化反应。
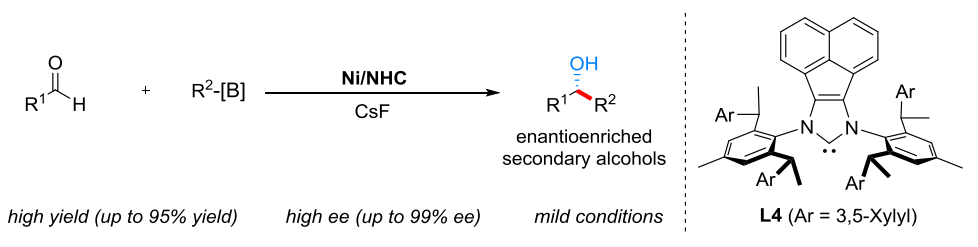
Chin. J. Chem.2024, 42, 2161—2165
E.亚胺的不对称加成。
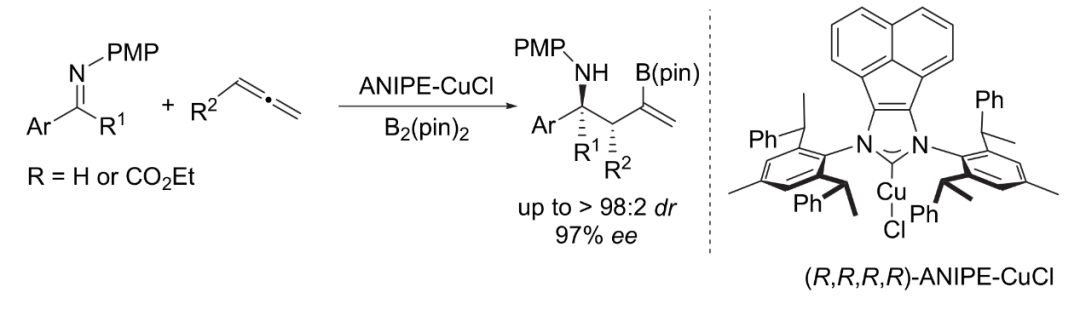
Chin. J. Org. Chem.2024, 44, 1884-1896
Section.03
— Leyan.com —
结构-性能关系:
为什么这类配体这么强?
通过 DFT 计算和实验验证,揭示了配体的 “动态适配” 机制:
催化循环中,配体的 C-C(Ph)键、C-N 键可发生显著旋转(苯基旋转角度达 60°),埋藏体积随反应步骤动态变化:氧化加成 / 转金属化时体积减小(提供空间),还原消除时体积增大(促进环化);强 σ-给体性质增强金属配位稳定性,抑制副反应;大位阻保证立体控制,柔性解决 “不同步骤空间需求矛盾”。

中国科学院上海有机所
施世良研究员
2011年获日本东京大学药学部博士学位(导师:Masakatsu Shibasaki和Motomu Kanai),2012-2016年在美国麻省理工学院从事博士后研究(合作导师:Stephen L. Buchwald)。2016年6月加入中国科学院上海有机化学研究所,现任金属有机化学国家重点实验室课题组长、博士生导师,兼任《科学通报》等期刊编委。获2025年中国化学会青年手性化学奖,2023年国家杰出青年科学基金,2022年上海市优秀学术带头人,2021年Bayer Investigator Award,2019年Thieme Chemistry Journals Award。累计在《Science》《Nature Chemistry》《Nature Catalysis》《Nature Synthesis》《JACS》《ACIE》等期刊发表论文60余篇。
施世良老师与乐研合作产品







https://wap.sciencenet.cn/blog-3543934-1524371.html
上一篇:浙大陆展团队突破铁催化难题,实现高效氢联硅化反应 | 乐研试剂