博文
连发两文 | 哈尔滨医科大学原慧萍团队蛋白组研究揭示青光眼发病机制新进展
|
青光眼是引起全球不可逆性致盲眼病的首要病因,其致病危险因素包括眼内压升高、基因突变和衰老。在临床上,降低眼压是青光眼最常用的治疗方法,但它不能逆转视力损害和防止失明的进展,并且对于正常眼压性青光眼(normal tension glaucoma,NTG)患者,它的疗效也不甚理想。因此,阐明青光眼分子变化和特异性生物标志物对于早期诊断和新的治疗靶点至关重要,明确该疾病的致病机制和建立有效的治疗方法刻不容缓。
近日,来自哈尔滨医科大学附属第二医院原慧萍教授研究团队在国际专业学术期刊Human Molecular Genetcs、Cell Death & Disease接连发表研究成果,运用蛋白质组学技术提供了NTG致病机制新的见解,并进一步指明了新的潜在治疗方法。

第一篇文章中,研究团队运用蛋白质组学技术首次报道了正常眼压性青光眼(NTG)进展中细胞代谢、分子通路等生物进程的改变,发现NTG疾病状态下视网膜出现的退行性改变与阿尔茨海默病具有相似的分子通路及病理改变 [1]。第二篇文章中,研究团队进一步探索了骨髓(BM)干细胞对年龄相关性视网膜变性的神经保护作用,体内补充年轻骨髓优质细胞可以修复NTG视网膜损伤及功能下降[2]。景杰生物为该研究的蛋白组学数据分析提供技术支持。

Proteomic analysis of aged and OPTN E50K retina in the development of normal tension glaucoma.
视网膜神经节细胞(RGCs)进行性凋亡是青光眼的一个主要特征,其潜在机制尚不清楚。OPTN基因的E50K突变与正常眼压性青光眼(NTG)的发病密切相关,并且带有该突变的患者多具有更严重的临床表型。对NTG小鼠模型的系统分析有助于更好地理解青光眼的潜在病理机制。
为了阐明NTG发病过程中蛋白质组学和生化途径的改变,研究者通过CRISPR/Cas9基因编辑技术构建OPTN E50K突变小鼠,并对不同年龄(选择3月、18月)OPTN E50K突变小鼠和野生型(WT)对照小鼠视网膜(样本策略)进行TMT标记蛋白质组学分析(质谱策略)。经鉴定发现7019种视网膜蛋白质,其中6364种可从所有视网膜样本中定量。
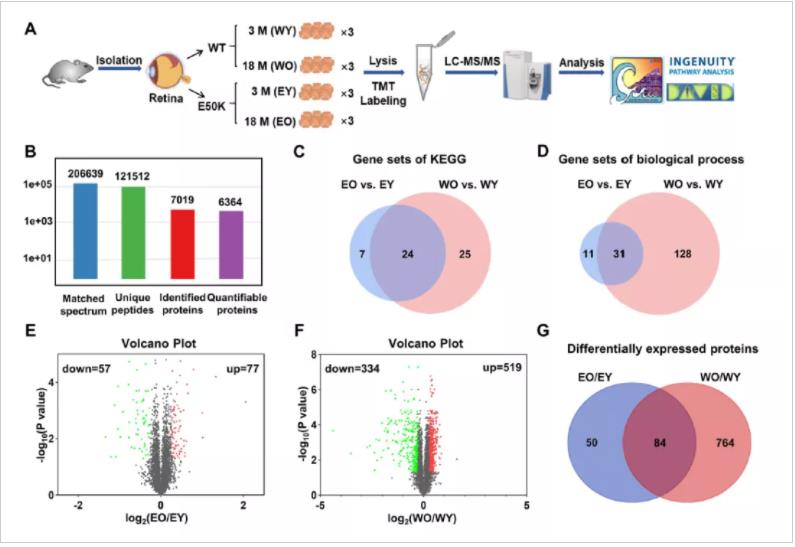
图、正常眼压性青光眼发展的蛋白质组学分析
进一步生信分析显示,OPTN E50K小鼠呈现蛋白质合成失调、年龄依赖性能量缺陷和自噬溶酶体途径功能障碍。值得注意的是,NTG小鼠中线粒体能量代谢以及神经退行性疾病阿尔茨海默病有关的途径上调,mRNA、蛋白等加工及降解途径下调,晶体蛋白、剪接体、自噬、胶质细胞异常,与阿尔茨海默病相似。进一步验证发现视网膜出现Aβ沉积、胶质细胞活化、晶体蛋白表达减低,表明NTG与阿尔茨海默病具有相似的分子通路。
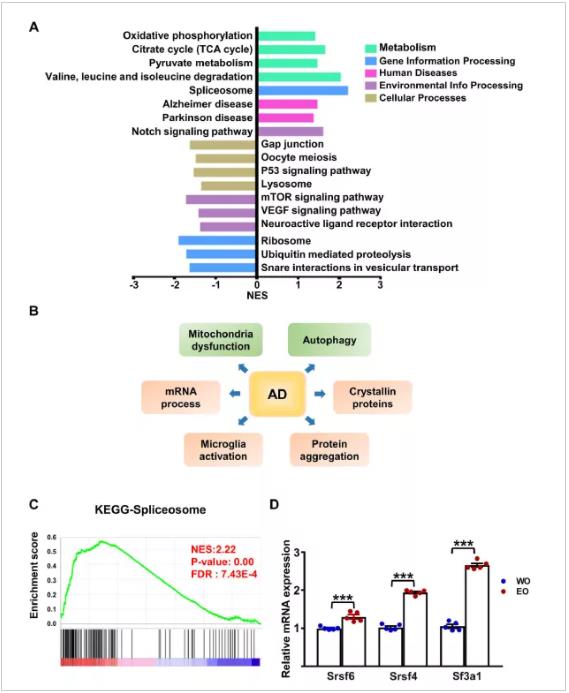
图、NTG与阿尔茨海默病具有相似的生化途径
Neuroprotective effects of bone marrow Sca-1+ cells against age-related retinal degeneration in OPTN E50K mice.
为了揭示年龄相关性的NTG疾病机理,研究人员对年老的OPTN E50K和WT对照小鼠视网膜(样本策略)进行了TMT标记蛋白质组学分析(质谱策略)。蛋白功能注释分析表明,差异蛋白通路显著富集于神经营养因子(NFs)通路,且各神经营养因子在GO显著富集的生物过程中处于核心位置,经分子实验验证视网膜神经营养因子表达减低。
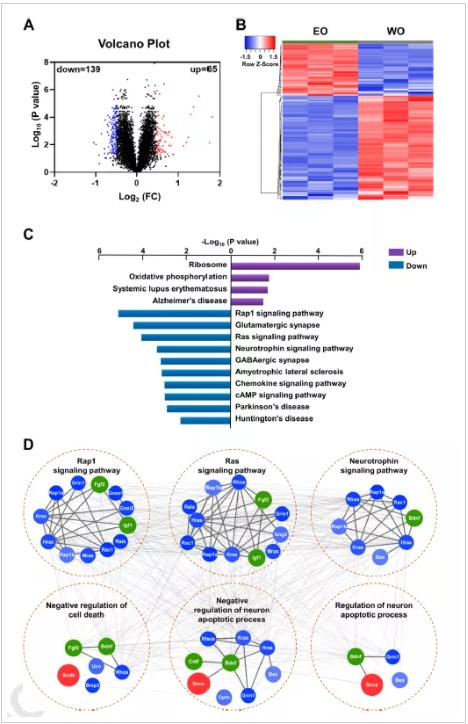
图、年老的OPTN E50K小鼠视网膜的蛋白质组学分析
骨髓(BM)干细胞通过其营养效应和归巢能力,在衰老和疾病过程中的受损组织再生中起着关键作用,也是治疗视网膜变性疾病的理想细胞。为进一步探索BM干细胞在NTG治疗中的作用,研究人员将BM干细胞分离成Sca-1+和Sca-1-细胞,并将它们移植到致死量照射的老年OPTN E50K小鼠中。结果表明来自年轻健康小鼠的Sca-1+细胞由于其出色的神经营养能力而表现出更强的修复NTG视网膜变性的能力。
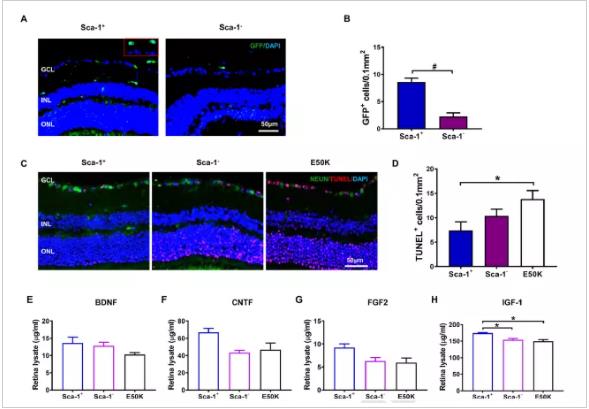
图、BM衍生的Sca-1+细胞具有增强的归巢和神经保护能力
总之,该研究揭示在NTG发育过程中,OPTN E50K突变加剧了视网膜和BM中神经营养因子的年龄相关性缺乏,导致视网膜变性和BM功能障碍。通过体内补充优质骨髓干细胞可以上调视网膜神经营养因子表达,修复NTG视网膜损伤。
神经营养因子参与OPTN E50K突变在老年期诱导发生正常眼压性青光眼关键分子途径,体内补充年轻骨髓优质细胞可以修复正常眼压性青光眼视网膜损伤及功能下降。
参考文献
https://wap.sciencenet.cn/blog-3404471-1304009.html
上一篇:NC | 柏林科学家开发微型TMT方法实现FFPE样本高深度
下一篇:CTM | 大连医科大学附属第二医院王琪团队报道肺癌脑转移化疗耐药新机制