博文
Cell最新播报:新冠病毒侵染的磷酸化蛋白质组全景图
|
今年以来,新冠肺炎的全球流行已经造成了超过四百万人的感染和近50万人的死亡。为应对疫情,针对新冠病毒的生命医学研究也成为当前的紧迫性工作。其中,蛋白质组学技术也发挥了重要作用,从寻找药物靶点到鉴定体液标志物,都有一系列的重要进展不断涌现。
2020年6月28日,Cell 主刊又刊登了题为“The Global Phosphorylation Landscape of SARS-CoV-2 Infection”的最新文章。该文章是加州大学旧金山分校等多家机构合作的最新研究成果,系统解析了新冠病毒侵染细胞后导致的系统性磷酸化修饰改变,并发现了新的针对异常磷酸化通路的潜在候选药物。

该研究使用新冠病毒SARS-CoV-2侵染Vero E6细胞为模型,选择了侵染的6个时间点,分别是0h、2h、4h、8h、12h和24h,鉴定到4,624个磷酸化修饰位点和3,036个蛋白质(图1左上)。结果显示,相比于蛋白质的丰度,蛋白质的磷酸化修饰水平在不同时间点之间呈现更为显著的改变,这体现了磷酸化修饰在迅速侵染过程中有更为重要的作用。
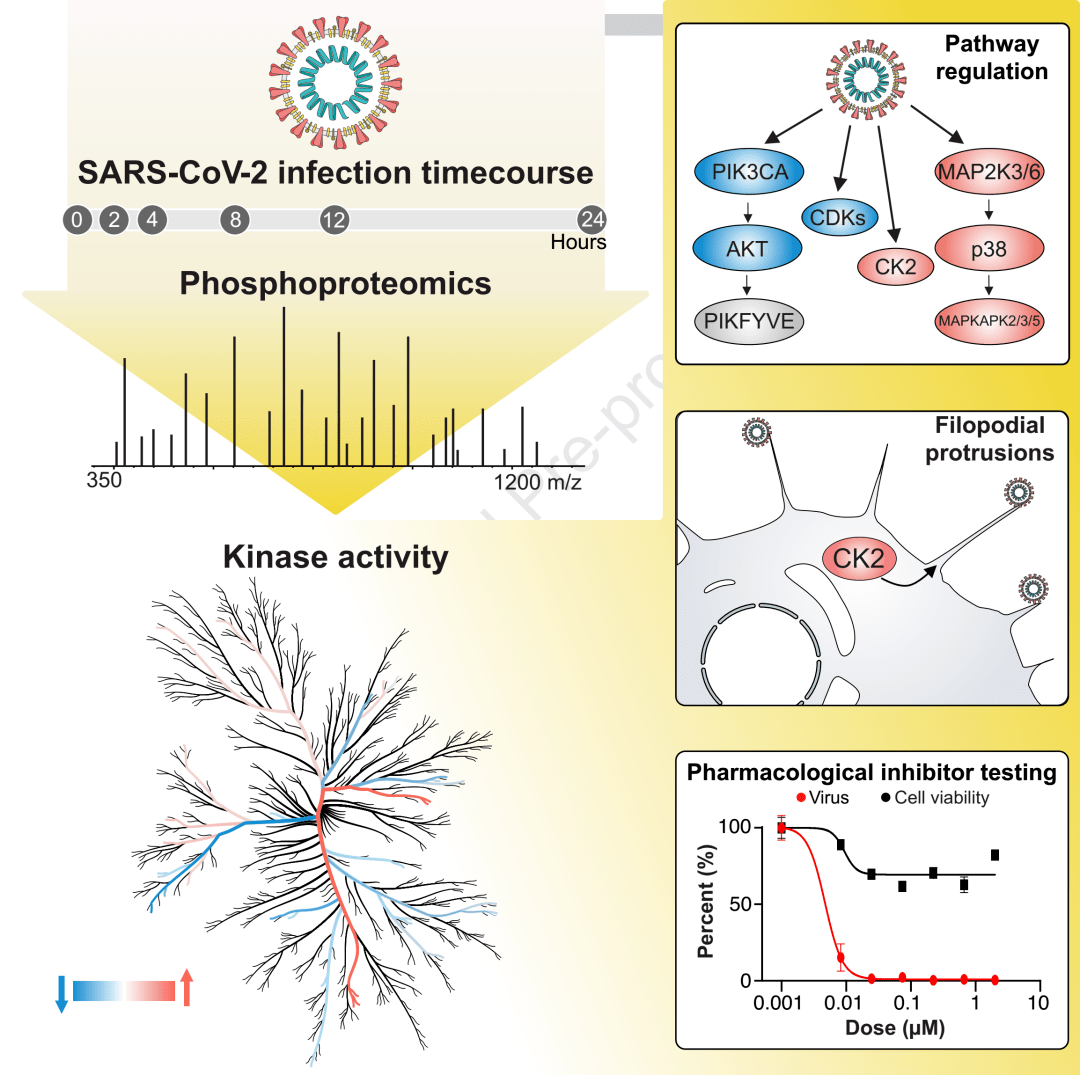
磷酸化组的结果首先显示了部分的病毒蛋白可以发生磷酸化,并且通过序列特征分析预测,发现宿主的CK2,CDK和PKC是导致这些病毒蛋白磷酸化的上游激酶,推测这些激酶可能在病毒侵染中扮演了“帮凶”的角色。在宿主的层面,通过对磷酸化位点的聚类分析和激酶预测,发现p38MAPK、CK2、CAMK2G等激酶活性出现上调,而CDK、AKT以及Rho家族的激酶活性出现下调(图1右上)。
为进一步研究这些激酶的功能,研究者通过细胞学和生物化学的实验证明,病毒N蛋白能够同CK2结合并进而调节了细胞骨架的组装,而病毒侵染会导致p38MAPK的升高并导致细胞周期中止。
那么,这些差异的激酶,能够成为潜在的药物治疗靶点呢?作者最后选择了68个潜在的药物或者化合物来测试其抗新冠病毒的能力,并最终发现CK2、p38MAPK、PIKFYVE以及CDKs家族的抑制剂有强效的抗新冠病毒作用,为未来的治疗提供了新的思路和依据。
参考文献:
1、Mehdi Bouhaddou, et al., 2020, The Global Phosphorylation Landscape of SARS-CoV-2 Infection. Cell.
https://wap.sciencenet.cn/blog-3404471-1239987.html
上一篇:Cell重磅 | 西湖大学郭天南团队发现新冠重症患者重要生物标志物
下一篇:“诱”敌深入,Nature Plants | 华中农大揭示植物抑制病原菌侵染的分子机制