博文
Sci Adv | 南开大学黄兴禄/孔德领组人造3D干细胞,解决缺血损伤难题
|
血管的狭窄或堵塞易引起缺血性组织坏死或病变,临床表现为心肌梗死、糖尿病足等疾病。缺血性疾病的治疗策略主要通过功能性血管网络的再生来灌注缺血组织。近年来,基于干细胞疗法的使用在缺血性疾病治疗方法的开发中受到了广泛关注。然而,一些关键问题限制了该方法在局部缺血治疗中的应用,例如极低的细胞滞留率和植入细胞的整合,因此递送干细胞治疗的功效受到了相当的限制。在再生医学中,发展仿生重建血管网络的新方法仍然是一个挑战。
近日,南开大学黄兴禄课题组和孔德领课题组合作在国际期刊Science Advances(IF=12.804)上发表最新论文,研究者创造性的通过诱导干细胞聚集成三维球体用于血管再生,蛋白质组学方法揭示了其作用机制:通过低氧诱导因子-1(HIF-1)信号通路调控促血管生成生物活性因子分泌。将SSP分泌因子整合到具有细胞膜衍生表面涂层的微/纳米颗粒中,人工重构了3D干细胞(ASSP),在局部缺血和全身性缺血的动物模型中均表现出良好的血管重建效果,为缺血组织再生的治疗选择提供了新的希望。景杰生物为该研究的蛋白质组学提供了检测和分析工作。


1、诱导生成3D SSPs,更能够促进促血管生成因子的分泌
研究者首先采用一种简便的方法(8-PEG-RGD)诱导促血管生成因子(CF)的脂肪组织骨髓间充质干细胞(aMSCs)聚集成三维球体(3D-SSPs)。分别比对2D培养和3D培养细胞条件下,发现在细胞数量无明显差异情况下,3D-SSPs更能够促进促血管生成因子(CF)的分泌(图1A)。

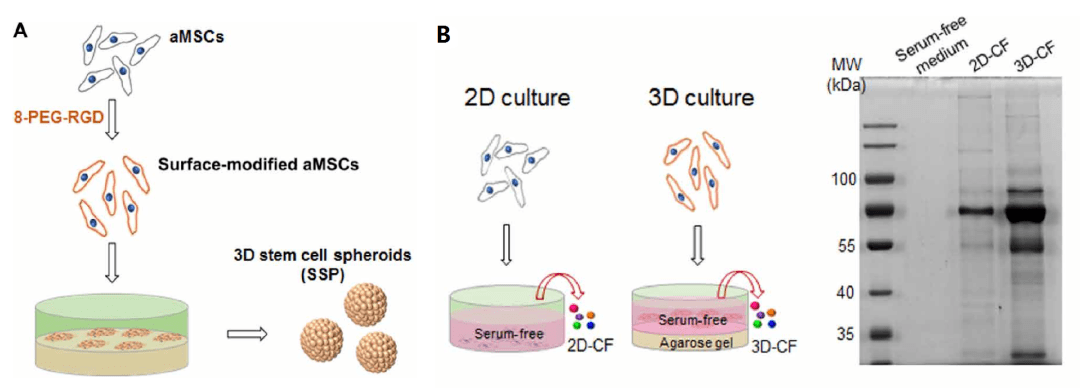
图1、3D-SSPs更能够促进CF分泌
2、蛋白质组学揭示3D-SSPs的机制特性
进一步评估不同细胞结构引起的蛋白组成变化,研究人员采用label-free蛋白质组学定量(LFQ)方法,对比分析2D-SSPs和3D-SSPs的蛋白质组差异。差异蛋白质的KEGG通路富集分析发现低氧诱导因子-1(HIF-1)信号通路被显著富集(图1B),对球体的中心细胞中绿色荧光的存在(吡莫尼唑染色的缺氧)证实了缺氧的发生,验证了该蛋白质组学的发现(图1C)。此外,蛋白质组学分析发现3D-SSPs的血管再生相关蛋白的表达被明显上调(图1D)。通过对比2D-CF和3D-CF处理人脐静脉内皮细胞,发现3D-CF可促进细胞的迁移和血管的形成(图1E和F)。以上结果表明3D SSPs的作用主要通过缺氧微环境的驱动和促血管生成因子分泌的增强实现血管的形成。

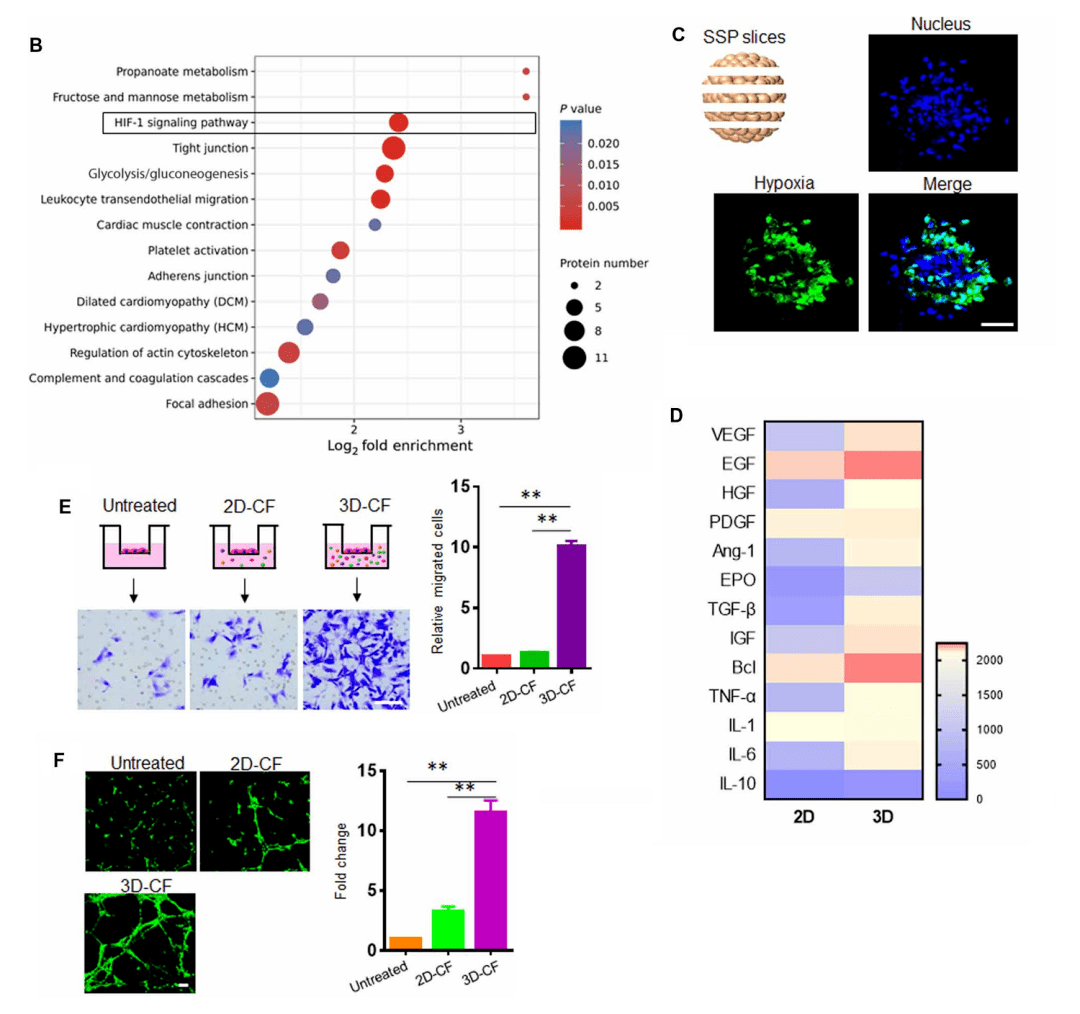
图2、蛋白质组学揭示3D-SSPs的机制特性
3、人工重构3D干细胞(ASSP)表现出良好的血管重建效果
接着,研究者通过将SSPs分泌因子整合到具有细胞膜衍生表面涂层的微米、纳米颗粒中,人工重建了三维球体(即ASSP-MPs和ASSP-NP)。分别在后肢缺血模型的小鼠缺血后肢局部注射ASSP-MPs微粒(图3A、B),和心肌梗死模型中全身注射ASSP-NP微粒(图3C、D),发现都能够为缺血组织提供了良好的血管重建效果。
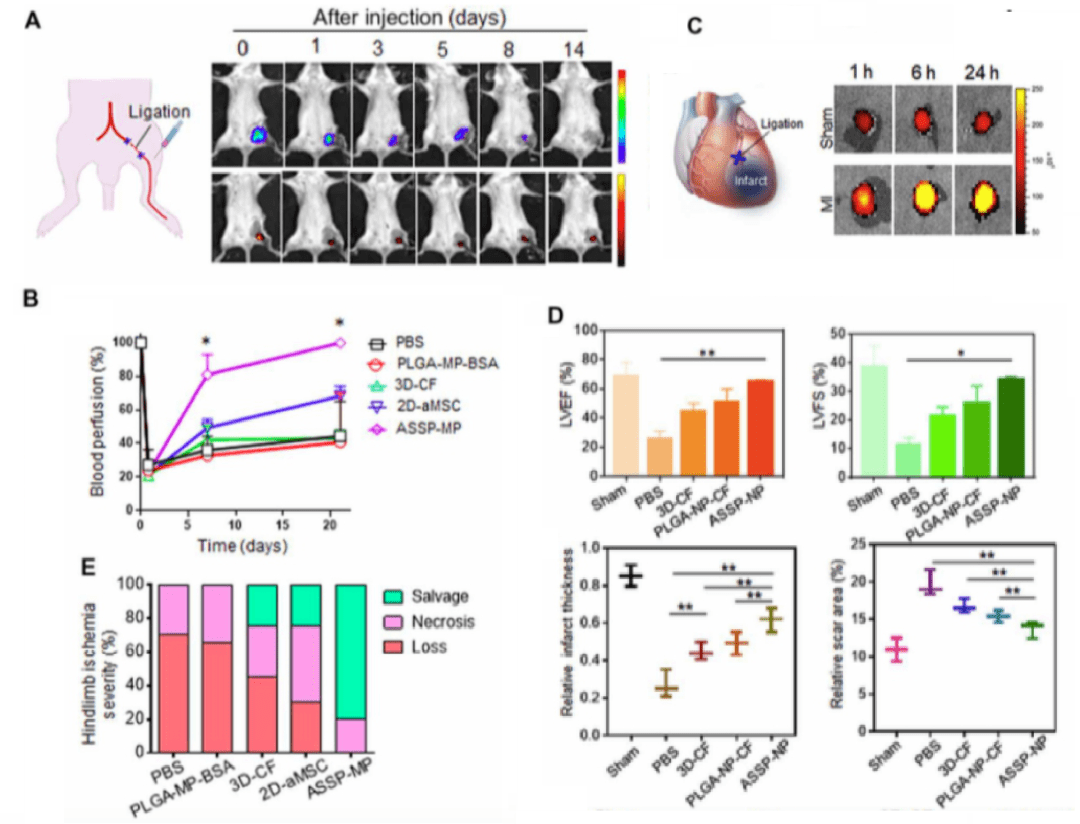
图3、局部注射ASSP微粒的缺血模型的血管重建效果
综上所述,通过将3D-SSPs分泌因子整合到具有细胞膜衍生表面涂层的微/纳米颗粒中,重建人工3D干细胞,在后肢缺血模型和心肌梗死模型中均提供了良好血管重建效果。定量蛋白质组学分析揭示可3D-SSPs通过低氧诱导因子-1(HIF-1)信号通路及促血管生成生物活性因子分泌的增强,来发挥其功能。该研究为缺血组织再生提供了一种新的治疗选择策略,还运用合成生物学思维为再生医学和材料科学架起了一座桥梁。
参考文献
1. Zhang R, et al., 2020, Particle-based artificial three-dimensional stem cell spheroids for revascularization of ischemic diseases. Science Advances.
https://wap.sciencenet.cn/blog-3404471-1235533.html
上一篇:专访高友鹤教授:为什么尿液是疾病早期标志物的来源?
下一篇:Cell重磅 | 西湖大学郭天南团队发现新冠重症患者重要生物标志物