博文
[转载]合理用药,科学施治——谈“上海共识”指导下的新型冠状病毒肺炎临床用药
|||
资料来源:张宇一,卢洪洲. 合理用药,科学施治——谈“上海共识”指导下的新型冠状病毒肺炎临床用药[J]. 中华临床感染病杂志,2021,14(1):7-12.
摘要:2020年1月起新型冠状病毒疫情暴发,目前仍在全球肆虐。面对疫情,上海市在2020年3月初发布了《上海2019冠状病毒病综合救治专家共识》。其对疾病救治,特别是临床用药进行了规范和指导,促进了新型冠状病毒肺炎治疗的合理用药。“四素一肽”等治疗方案是共识中的亮点,是成功阻断与救治危重症的关键。
自2020年1月起,由新型冠状病毒(2019-nCoV)导致的新型冠状病毒肺炎(COVID-19)疫情逐步在全球蔓延。COVID-19全球病死率(2.2%左右)看似低于严重急性呼吸窘迫综合征(SARS)的10%和中东呼吸综合征(MERS)的35%[1,2]。但研究表明COVID-19武汉疫情开始之初,病毒传播系数R0高达3.54[3],传播能力远超SARS和MERS,其危害毋庸置疑。截至2021年1月25日24时,我国(包括港澳台地区)已累计确诊COVID-19患者100 291例、死亡4 814例[4]。同时疫情也席卷全球200多个国家及地区,截至2021年1月26日,全球累计确诊98 925 221例、死亡2 127 294例[5]。此次疫情给包括中国在内的世界各国带来了巨大的健康危机,将在较长时间对全球社会生活、经济生产的正常秩序产生影响。上海作为国际化大都市,承受了本土病例暴发和持续境外输入的双重压力。截至2021年1月25日24时,上海市累计确诊COVID-19患者1 654例,其中1 290例为境外输入[6]。而上海市公共卫生临床中心(以下简称“公卫中心”)作为全市抗疫的堡垒,承担了全市95%以上确诊患者的救治任务,收治了全部重型、危重型病例。面对疫情肆虐,上海的临床救治秉承科学救治的原则,依据《上海2019冠状病毒病综合救治专家共识》[7](以下简称“上海共识”)展开治疗,避免盲目用药、不合理用药的情况发生。
回顾抗疫历程,我们发现上海本次临床救治用药是科学而理性的。公卫中心卢洪洲教授也将上海共识中的关键治疗用药概括为“四素一肽”的集束化方案,即糖皮质激素、肝素、大剂量维生素C、干扰素-κ和胸腺肽。本文将围绕“上海共识”总结上海市COVID-19治疗中的临床用药情况,以体现在突发重大疫情下合理用药、科学施治的重要性。
1 SARS不合理用药的经验教训
2002年至2003年SARS期间,一些不合理用药带来的医源性伤害让人记忆犹新,诸如每日1000~2000mg甲泼尼龙的使用、长达数周甚至数月的糖皮质激素维持、“阿奇霉素+氟喹诺酮”的常规运用在之后均被证实是无效且有害的[8]。任何药物都存在不良反应,关键是如何正确运用,大剂量糖皮质激素冲击治疗在SARS时挽救了很多重症患者的生命[9],可部分不合理用药却掩盖了其功劳。
纵观SARS期间的临床用药,对于在明确病原后的不合理抗菌和抗病毒药物使用,以及面对疫情的盲目用药是我们必须坚决反对和引以为戒的。但对于在早期面对未知疾病时进行的科学、谨慎的治疗探索,我们则应给予支持和理解,因为科学研究总是伴随着不确定性,但不代表可以随意用药,所有的治疗尝试和研究必须遵循“不伤害原则”这一底线,诊疗过程中不损伤患者的身心健康是医务工作者应遵循的基本原则。
2 “上海共识”与COVID-19合理用药
2.1 率先明确病原,科学探索治疗药物
在2020年疫情暴发之初,上海公卫中心在全球率先明确了病原[10],同时也对新冠肺炎的临床特点、危险因素进行了研究[11,12,13,14,15],这为之后的上海COVID-19救治的用药方案提供了方向,也避免了SARS之初的盲目和混乱重现。
为了发现潜在的抗病毒药物,我们在早期就采用了科学手段进行探索[16],包括对现有广谱抗病毒药物分析、筛选现有化合物数据库,以及基于冠状病毒的基因组和生物物理学重新开发新的特异性药物,从而发现如核苷类似物、阿比多尔、羟氯喹、糖皮质激素、干扰素-κ、疏风解毒胶囊和连花清瘟胶囊等可能是有效的治疗药物。但这些药物没有因为疫情的紧急而简单地用于临床,所有的探索均在严格遵循医学伦理的情况下进行研究。
2.2 早期制订共识,规范治疗用药
上海的抗疫工作吸取了SARS的经验教训,在面对2019-nCoV的持续肆虐时始终保持了科学理性的态度。基于提高疾病治愈率、降低病死率的目的,同时也为了规范医务人员的医疗救治行为,尽最大可能避免或降低医源性伤害的出现,上海专家组在2月中旬,基于国家卫健委《新型冠状病毒肺炎诊疗方案》(以下简称“诊疗方案”)着手制订定“上海共识”,并在2020年3月初发布。
“上海共识”并不是对国家诊疗方案的照抄,而是基于相关循证学依据和临床实践的动态变化对其进行的细化和完善,以便于临床一线抗疫工作更好地开展。与同时期发布的第三版“诊疗方案”相比,“上海共识”偏重于临床治疗,早期提出了“四素一肽”的理念。如制订了小剂量、短疗程的糖皮质激素使用方案与适宜人群,通过应用肝素、大剂量维生素C来防治“细胞因子风暴”,优先推荐干扰素-κ抗病毒治疗,使用胸腺肽调节免疫功能。此外,“上海共识”还较为重视中草药对于肠道功能的调节,以及诸如营养支持、内环境平衡。这些内容有些早于“诊疗方案”提出,另一些则是更为详尽且具操作性。
“上海共识”的制订秉持科学严谨的态度,通过后续研究与临床实践,其主要治疗方案被证实有效且在上海的抗疫救治中普遍应用,目前暂无修订更新,同时包括专家组在内的医务人员至今仍在严格遵循共识进行临床诊治工作。通过“上海共识”也将治疗方案标准化、规范化,避免因医务人员轮换而出现治疗措施的变化。在本次抗疫期间,特别是在面对输入性疫情冲击之时,共识不但显著降低了上海COVID-19患者的重症化率,也确保了临床用药安全。
2.3 “上海共识”对医务人员心理应激下医疗行为的规范
COVID-19疫情时医务人员承担了较大的压力。根据对既往和本次疫情期间医务人员的心理状态研究发现,在面对突发重大公共卫生事件时医务人员常会伴随着更强烈的心理应激反应,尤其是表现为消极应对倾向,更有部分人会存在强烈的不满情绪[17,18,19]。
上海在本次COVID-19疫情期间很重视医务人员的心理问题。通过包括专业心理疏导在内的各种方式,尽可能避免医务人员出现严重心理问题,从而使得一线人员在强烈的应激状态下保持心理健康,进行安全且科学的临床医疗工作。而“上海共识”在对治疗行为进行规范的同时,更使医务人员心理上有了一定的依托,从而避免因心理问题带来医疗行为、临床用药的偏差。所以说,“上海共识”是在医务人员可能存在心理应激的情况下,在制度上保证临床安全、有效用药和救治的重要手段。
3 “上海共识”中的药物治疗亮点
虽然共识成稿于2020年2月份,但其中的大部分内容在现今仍被证明是正确而有效的,具有前瞻性和科学性。包括“四素一肽”、营养支持在内的相关治疗措施在当时提出虽然有些超前,但共识中这些“集束化”治疗理念并不是专家组随性提出的。每一个治疗药物均通过对疾病病理生理特点进行严谨分析、对患者各个临床指标和数据严密观察科学分析后得出的,有着循证医学依据且陆续被进一步研究所证实。
3.1 “四素一肽”的使用
糖皮质激素一直以来被医学界认为是一把“双刃剑”,一方面可以抑制过度的免疫反应,阻断“细胞因子风暴”,预防肺纤维化;但另一方面则可能诱发感染,影响病毒清除,甚至引起股骨头坏死等情况。最初世界卫生组织发布的相关治疗指南中就表示不推荐COVID-19患者常规使用糖皮质激素[20]。但2020年5月发表的英国RECOVERY研究则改变了人们的看法,使用糖皮质激素可将机械通气患者病死率降低约三分之一[21]。
而“上海共识”并未武断地否定糖皮质激素,而是对于糖皮质激素的使用问题进行了客观而科学的规范。给糖皮质激素戴上了枷锁,将使用人群、使用时机、给药剂量和疗程均做了限定,建议对存在重症化危险因素的患者给予20~40 mg/d的甲泼尼龙治疗,且疗程不超过1周。这使得一线临床医师可以更规范且安全的使用糖皮质激素,从而在给患者带来益处的同时也避免了不良事件的出现。此外,上海的救治经验也发现,根据共识对于病情发生进展、重型/危重型的高危人群进行短时间、小剂量糖皮质激素治疗是安全的,且对阻断重症化有效。
COVID-19患者的凝血功能问题一开始并未被人们重视,而肝素作为抗凝药物也是在2020年4月以后逐步在一系列研究中被证实可以控制2019-nCoV感染后炎症诱发的凝血功能异常、微循环障碍以及“细胞因子风暴”[22]。上海专家组则在早期就通过对患者病情的研判,发现大部分COVID-19患者存在凝血功能异常,且在重症和危重症患者中更为显著[23]。根据既往对危重症救治的经验和相关尸体解剖的结果,专家组意识到肝素使用的重要性和必要性,并写入了共识。针对D二聚体等凝血功能异常患者,每日1~2支低分子肝素的使用,可预防血栓形成。
大剂量维生素C的运用也是“上海共识”的亮点,对存在重症化危险因素的患者给予50~100 mg/d的维生素C。专家组成员通过既往研究发现,静脉使用维生素C可以保护内皮细胞,从而降低细胞因子的表达[24,25],对于阻断重症COVID-19患者细胞因子风暴、改善凝血功能也可起到重要作用。后续研究也发现,危重症患者血清中的维生素C含量明显下降,而低维生素C含量和高龄是疾病的独立危险因素[26]。
公卫中心科研人员在早期的研究中发现,干扰素-κ能显著抑制2019-nCoV在Huh7细胞系中的复制,而三叶因子2(TFF2)在小鼠模型中可通过减轻炎症反应和改善肺功能来降低流感感染的发病率和病死率。因此在疫情之初,干扰素-κ+TTF2就被认为可能对2019-nCoV的治疗有效,并严格按药物临床试验步骤进行研究。结果发现,雾化吸入IFN-κ+TFF2无论是在肺部影像学、临床症状改善,还是病毒转阴和住院时间上均显著优于对照组,同时无严重不良事件出现[27]。根据研究结果,该药物在之后的临床治疗中被广泛使用。
胸腺肽作为免疫调节药物具有调节和增强人体细胞免疫功能的作用,能促使T淋巴细胞成熟。上海的前期研究发现[13,15],淋巴细胞和CD4+T细胞减少是COVID-19重症化的危险因素,因此“上海共识”中提出,针对以上细胞降低的患者每周2次皮下注射胸腺肽,对提高患者免疫功能、阻止病情重症化和缩短排毒时间有一定效果。
“四素一肽”及营养支持在共识中占据重要地位,是上海市COVID-19患者成功救治和输入性病例危重症阻断的关键。
3.2 抗病毒、抗菌药物合理使用
公卫中心在2020年1、2月份就开始对洛匹那韦利托那韦、阿比多尔和羟氯喹等药物治疗COVID-19进行研究,但“上海共识”对于抗病毒药物是谨慎的。
编写共识时,国际上对于诸如羟氯喹等抗病毒药物的呼声很大,甚至被美国食品药品监督管理局批准紧急用药。但专家没有受到外界干扰,考虑到研究仍在进行中,秉承客观的科学研究态度,共识中使用了“可试用”、“有待进一步研究”这些措辞。而在研究结束并得出阴性结果后,也率先发表了研究结果[28,29],最早否定了这些药物的有效性并对羟氯喹的安全性提出质疑。这些举措是严谨的,体现了“上海共识”的科学性,也表明上海在疫情期间对于合理用药的高度重视。
同样,在“上海共识”的规范和约束下,临床医师的抗生素不合理使用受到了控制。共识明确提出,对于抗生素的运用必须严格遵循病原学依据、各项实验室炎症指标和临床表现综合判断后谨慎选用,避免因在面对发热、“肺炎”时随意使用抗生素治疗或预防,而即便是对接受呼吸机治疗、中心静脉置管的危重症患者,抗生素的经验性使用也被严格控制。为了减少抗生素的使用及其引起的耐药发生,院内感染被提到了重要位置,同时也创新性地使用噬菌体治疗。通过对泛耐药鲍曼不动杆菌、铜绿假单胞菌感染患者进行相应噬菌体吸入雾化和环境处理,并配合药物治疗,相关病原菌均在3~7 d内得以清除。
根据对公卫中心的数据初步分析,我们发现2020年第2季度COVID-19患者的抗菌药物使用强度为20,远低于1季度的43。这也表明“上海共识”对抗生素合理使用的严格管控和医务人员对共识的执行力。
3.3 COVID-19治疗费用
根据对公卫中心COVID-19轻型和普通型患者住院费用、药费及药占比的统计和分析,我们发现住院总费用、住院药费支出和药占比均在2020年3、4月份开始显著下降,这与“上海共识”的发布在时间上是契合的(图1,图2,图3)。通过数据我们可以看出,3月份后在“上海共识”的规范下,临床救治行为均已规划化和标准化,住院药费下降至2 500元以下且药占比低于10%。
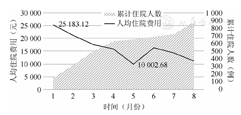
图1 2020年1月至8月上海市公共卫生临床中心新型冠状病毒肺炎轻型和普通型患者人均住院费用
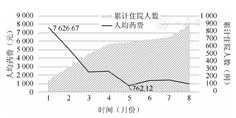
图2 2020年1月至8月上海市公共卫生临床中心新型冠状病毒肺炎轻型和普通型患者人均药费
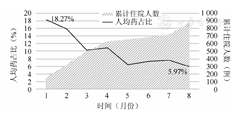
图3 2020年1月至8月上海市公共卫生临床中心新型冠状病毒肺炎轻型和普通型患者人均药占比
而即便是将重型和危重型患者包括在内,上海COVID-19患者的平均住院费用也仅为35 000元左右。如果考虑到我国每年人均医疗费用增长比例,该费用与2003年SARS患者18 000元左右的人均住院费用相比仍是较为合理的[30]。
此外,我们发现在各项费用降低的同时,上海整体治愈率也在稳步上升。截至2021年1月25日,病死率仅为0.4%,均优于全球(2.2%)和国内平均水平(4.8%)。这也证明合理用药、科学施治对于COVID-19患者救治的可行性、重要性和必要性。
3.4 中医药在COVID-19治疗中的使用
在上海的COVID-19患者救治中,特别突出祖国传统医学的作用。截止至2020年9月30日,市公卫中心收治的873例中国籍COVID-19患者中,有823例接受中药治疗(94.3%),而98例外籍患者中也有32例接受了中医药治疗(32.7%)。
中医从抗疫之初便介入,通过收集患者证候特征、舌象脉象等信息进行分析辨证。根据COVID-19以湿毒郁肺型为主、符合中医湿疫的特点,在临床治疗中遵循“一人一方”的原则(784例患者经由舌苔等辩证后使用草药),根据患者不同情况给予辨证施治,诸如通过大黄改善患者的肠道功能、使用石膏等进行体温调节和控制[31]。通过早期与单纯使用西药治疗的患者比较,中西医结合治疗住院时间缩短至12 d,同时临床症状积分小于对照组,可见中西医结合的方式取得了很好的临床效果[32]。此外,疏风解毒胶囊等中成药也被临床使用,研究发现其可缩短临床恢复时间并减少乏力、咳嗽症状,同时显著减少HCoV-229E小鼠肺组织病毒载量[33]。
4 总结
当然,“上海共识”也存在一些不足。如共识建议试用硫酸羟氯喹或磷酸氯喹、阿比多尔,而目前这些药物均已证实无效。此外,虽指出老年人及患有糖尿病、高血压、冠状动脉粥样硬化性心脏病、极度肥胖等基础疾病者感染后易发展为重症,但缺乏详细的重症化早期预警指标,且无量化预警模型或评分。为了做到早期发现、早期预警和早期阻断,可根据后续的进一步研究进行补充更新。
目前为止,上海在本次COVID-19疫情中的临床救治是成功的,而秉持理性、科学的态度,坚持合理用药、科学施治是其中的关键。通过对既往经验教训的吸取、早期制订科学的救治方案、严格执行和重视医务人员的心理干预,已建立起参与抗疫人员的标准化、规范化诊治流程,可对下一步的常态化抗疫工作带来帮助。也希望这种流程和经验可以得到保存并得以传承,从而在未来更好地应对可能出现的重大新发、突发传染病事件。
利益冲突 所有作者均声明不存在利益冲突
参考文献
[1]WHO. Summary of probable SARS cases with onset of illness from 1 November 2002 to 31 July 2003[EB/OL]. (2015-07-24) [2020-12-09]. https://www.who.int/csr/sars/country/table2004_04_21 /en/.
[2]WHO. MERS situation update september 2019[EB/OL]. (2019-09-01) [2020-12-09]. https://applications.emro.who.int/docs/EMROPub-MERS-SEP-2019-EN.pdf?ua=1&ua=1.
[3]HaoX, ChengS, WuD, et al. Reconstruction of the full transmission dynamics of COVID-19 in Wuhan[J]. Nature, 2020, 584(7821): 420-424.
[4]中华人民共和国国家卫生健康委员会. 截至1月25日24时新型冠状病毒肺炎疫情最新情况[EB/OL]. (2021-01-26)[2020-12-09]. http://www. nhc. gov. cn/xcs/yqtb/202001/ 9614b05a8cac4 ffabac10c4502fe517c.shtml. National Health Commission of the People's Republic of China. The latest situation of the epidemic situation of COVID-19 as of 24: 00 on January 25[EB/OL]. (2021-01-26) [2020-12-09]. http://www.nhc.gov.cn/xcs/yqtb/202001/9614b05a8cac4ffabac10c4502fe517c.shtml.
[5]WHO. WHO Coronavirus Disease (COVID-19) Dashboard (Data last updated: 2021/1/26, 9: 41am CET)[EB/OL]. (2021-01-26) [2020-12-09]. https://covid19.who.int/.
[6]上海市卫生健康委员会. 上海2021年1月25日,新增本地新冠肺炎确诊病例2例新增境外输入8例治愈出院1例[EB/OL]. (2021-01-26)[2020-12-09]. http://wsjkw.sh.gov.cn/xwfb/20210126 /6b928 fd430b8455591a0d54082129d51.html.Shanghai Municipal Health Commission. Two new confirmed COVID-19 cases in Shanghai were added,8 new cases were imported overseas, 1 case was cured and discharged on January 25,2021[EB/OL]. (2021-01-26)[2020-12-09]. http://wsjkw.sh.gov.cn/ xwfb/20210126/6b928fd430b8455591a0d54082129d51.html.
[7]上海市2019冠状病毒病临床救治专家组. 上海市2019冠状病毒病综合救治专家共识[J]. 中华传染病杂志,2020, 38(3):134-138.
Shanghai Clinical Treatment expert Group for Corona Virus Disease 2019. Comprehensive treatment and management of corona virus disease 2019: expert consensus statement from Shanghai City[J]. Chin J Infect Dis, 2020, 38(03): 134-138.
[8]缪晓辉,周先志. 对严重急性呼吸综合征药物治疗的几点看法[J]. 中华传染病杂志,2004, 22(1):66-68.
MiaoXH, ZhouXZ. Views on drug treatment of severe acute respiratory syndrome[J]. Chin J Infect Dis,2004,22(1): 66-68.
[9]李兴旺,蒋荣猛,郭嘉祯. 糖皮质激素治疗重症急性呼吸综合征初探[J]. 中华内科杂志,2003, 42(6):378-381.
LiXW, JiangRM,GuoJZ. Glucocorticoid in the treatment of severe acute respiratory syndrome patients: a preliminary report[J]. Chin J Intern Med,2003, 42(6):378-381.
[10]WuF,ZhaoS,YuB,et al. A new coronavirus associated with human respiratory disease in China[J]. Nature,2020,579(7798): 265-269.
[11]LiTS, LuHZ, ZhangWH. Clinical observation and management of COVID-19 patients[J]. Emerging Microbes and Infections, 2020, 9(1): 687-690.
[12]LingY, XuSB, LinYX, et al. Persistence and clearance of viral RNA in 2019 novel coronavirus disease rehabilitation patients[J]. Chin Med J (Engl), 2020, 133(9): 1039-1043.
[13]凌云,林逸骁,钱志平,等. 新型冠状病毒肺炎患者重症化危险因素的临床分析[J]. 中华传染病杂志,2020, 38(4):193-198.
LingY, LinYX, QianZP, et al. Clinical analysis of risk factors for severe patients with corona virus disease 2019[J]. Chin J Infect Dis, 2020, 38(4): 193-198.
[14]ShenYZ, ZhengF, SunDF, et al. Epidemiology and clinical course of COVID-19 in Shanghai, China[J]. Emerging Microbes and Infections, 2020, 9(1): 1537-1545.
[15]FengY, LingY, BaiT, et al. COVID-19 with different severity: A multi-center study of clinical features[J]. American Journal of Respiratory and Critical Care Medicine, 2020, 201(11): 1380-1388.
[16]LuHZ. Drug treatment options for the 2019-new coronavirus (2019-nCoV)[J]. Bioscience trends, 2020, 14(1): 69-71.
[17]TamCW, PangEP, LamLC, et al. Severe acute respiratory syndrome (SARS) in Hong Kong in 2003: stress and psychological impact among frontline healthcare workers[J]. Psychological Medicine, 2004, 34(7): 1197-1204.
[18]GouliaP, MantasC, DimitroulaD, et al. General hospital staff worries, perceived sufficiency of information and associated psychological distress during the A/H1N1 influenza pandemic[J]. Bmc Infectious Diseases, 2010, 9(10): 322.
[19]郭忠伟,王燕,祝睿晨,等. 130名抗新型冠状病毒肺炎一线救援医务人员焦虑抑郁状况调查及影响因素分析[J]. 中华精神科杂志,2020, 53(3):198-203.
GuoZW, WangY, ZhuRC, et al. Analytical report of anxiety and depression of 130 first-line medical staff against COVID-19[J]. Chin J Psychiatry, 2020, 53(3): 198-203.
[20]WHO. Clinical management of COVID-19:interim guidance[EB/OL].(2020-05-27) [2020-12-09]. https://www.who.int/publications/i/item/clinical-management-of- severe-acute- respiratory-infection-when-novel-coronavirus-(ncov)-infection-is-suspected.
[21]LedfordH. Coronavirus breakthrough: dexamethasone is first drug shown to save lives[J]. Nature,2020, 582(7813): 469.
[22]宋景春,王岗,张伟,等. 新型冠状病毒肺炎重症患者相关凝血功能障碍诊疗专家共识[J]. 解放军医学杂志,2020, 45(4):335-344.
SongJC, WangG, ZhangW, et al. Expert consensus for diagnosis and treatment of coagulation dysfunction in COVID-19[J]. Med J Chin PLA, 2020, 45(4): 335-344.
[23]ZouY, GuoHY, ZhangYY, et al. Analysis of coagulation parameters in patients with COVID-19 in Shanghai, China[J]. Bioscience trends, 2020, 14(4): 285-289.
[24]MaL, FeiJ, ChenY, et al. Vitamin C attenuates hemorrhagic shock-induced dendritic cell-specific intercellular adhesion molecule 3-grabbing nonintegrin expression in tubular epithelial cells and renal injury in rats[J]. Chin Med J (Engl), 2016, 129(14): 1731-1736.
[25]MaL,ChenY,SongXQ,et al. Vitamin C attenuates hemorrhagic hypotension induced epithelial-dendritic cell transformation in rat intestines by maintaining GSK-3β activity and E-cadherin expression[J]. Shock, 2016, 45(1): 55-64.
[26]ArvinteC, SinghM, MarikPE. Serum levels of vitamin C and vitamin D in a cohort of critically ill COVID-19 patients of a north American community hospital intensive care unit in may 2020. A pilot study[J]. Med Drug Discov, 2020, 8: 100064.
[27]FuWH, LiuY, XiaL, et al. A clinical pilot study on the safety and efficacy of aerosol inhalation treatment of IFN-κ plus TFF2 in patients with moderate OVID-19[J]. E Clinical Medicine, 2020, 25: 100478.
[28]陈军,张丹丹,钱志平,等. 硫酸羟氯喹治疗2019冠状病毒病(COVID-19)普通型患者的初步研究[J]. 浙江大学学报(医学版), 2020, 49(2):215-219.
ChenJ, ZhangDD, QianZP, et al.A pilot study of hydroxychloroquine in treatment of patients with moderate COVID-19[J]. J Zhejiang Univ(Med Sci), 2020, 49(2): 215-219.
[29]陈军,凌云,席秀红,等. 洛匹那韦利托那韦和阿比多尔用于治疗新型冠状病毒肺炎的有效性研究[J]. 中华传染病杂志,2020, 38(2):86-89.
ChenJ, LinY, XiXH, et al. Efficacies of lopinavir/ritonavir and abidol in the treatment of novel coronavirus pneumonia[J]. Chin J Infect Dis, 2020, 38(2): 86-89.
[30]肖峰,陈博文,武阳丰,等. 北京市SARS临床诊断病例住院费用及影响因素分析[J]. 中华流行病学杂志,2004, 25(4):312-316.
XiaoF, ChenBW, WuYF, et al. Analysis on the cost and its related factors of clinically confirmeds evere acute respiratory syndrome cases in Beijing[J]. Chin J Epidemic, 2004, 25(4): 312-316.
[31]陆云飞,杨宗国,王梅,等. 50例新型冠状病毒感染的肺炎患者中医临床特征分析[J]. 上海中医药大学学报,2020, 2:17-21.
LuYF, YangZG, WangM, et al. Analysis on Chinese medical clinical characteristics of 50 patients with novel coronavirus-infected pneumonia[J]. Journal of Shanghai University of Traditional Chinese Medicine, 2020, 2: 17-21.
[32]时佳,杨宗国,叶晨,等. 中西医结合治疗上海地区49例非危重型新型冠状病毒肺炎临床疗效观察[J]. 上海中医药杂志,2020, 54(4):30.
ShiJ, YangZG, YeC, et al. Clinical observation on 49 cases of non-critical COVID-19 in Shanghai treated by integrated traditional Chinese and western medicine[J]. Shanghai J Tradit Chin Med, 2020, 54(4): 30.
[33]XiaL, ShiYJ, SuJ, et al. Shufeng Jiedu, a promising herbal therapy for moderate COVID-19: Antiviral and anti-inflammatory properties, pathways of bioactive compounds, and a clinical real-world pragmatic study[J]. Phytomedicine, 2020: 153390.
https://wap.sciencenet.cn/blog-279293-1299607.html
上一篇:[转载]叶晓锜:概念的解读
下一篇:[转载]叶晓锜:概念意识探索